Удаление полностью безнадёжных зубов, а также таковых скомпрометированных пародонтальным или значительным кариозным поражением, является наиболее распространённой манипуляцией в повседневной практике врача-стоматолога. Поэтому число успешно экстрагированных зубных единиц среди некоторых клиницистов превышает тысячный рубеж, но, даже несмотря на тщательное планирование процедуры, данная манипуляция является одной из самых важных этапов данного ятрогенного вмешательства.
Особенности формирования и резорбции костной ткани
Одним из наиболее важных факторов морфологии костной ткани, как и процесса ее заживления, является именно клеточный компонент. Основными типами клеток, играющими определенную роль в ходе формирования костной массы, остаются остеопрогениторные клетки, остеокласты, остеобласты и остеоциты.
1. Остеопрогениторные клетки являются недифференцированными стволовыми клетками, которые выстилают эндостальную поверхности кости. В дальнейшем данные клетки дифференцируются в клетки пре-остеобластов, а затем и в зрелых остеобластов, находясь при этом в зоне эндоста.
2. Остеокласты являются клетками, ответственными за резорбтивные процессы, а также ремоделирование костной ткани.
3. Остеобласты отвечают за депозицию и кальцификацию новосформировашегося костного матрикса.
4. Остеоциты по своей природе являются остеобластами, которые выполнили свою функцию, и остались зацементированными в сформировавшемся костном матриксе, сохранив при этом межклеточную связь, значение которой крайне важно при адаптации к нагрузкам или нарушении целостности кости.
С целью общего описания всех динамических процессов в костной ткани, можно использовать всего два концептуальных понятия: моделирование и ремоделирование (фото 1).
Фото 1. Иллюстрация процесса формирования костной ткани.
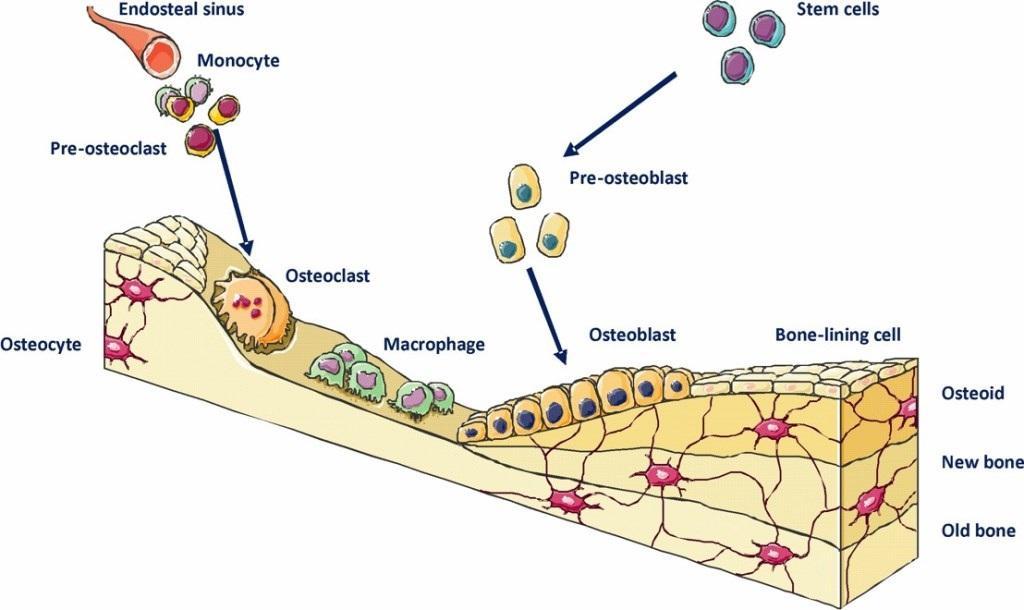
Моделирование представляет собой процесс внутрикостных изменений в ответ на некую стимуляцию или физическую силу. Ремоделирование относится же к более постоянному процессу внутренних изменений кости, при которых взаимодействие остеобластов и остеокластов является более гармоничным и сбалансированным, когда обеспечивается нормальное функционирование элементов человеческого скелета.
Виды трансплантационных материалов
Чаще всего фактором, определяющим необходимость проведения реконструкции лунки после удаления, является степень травмирования окружающих твердых и мягких тканей во время проведения процедуры экстракции. Степень целостности костных стенок лунки, в свою очередь, помогает адекватно подобрать вид трансплантационного материала с учетом будущих изменений в структуре альвеолярного гребня после выполнения твердотканной аугментации. В ходе выбора трансплантата важно учитывать три основных характеристики:
1. Остеокондуктивность: формирование площадки или каркаса, на которые в дальнейшем заселяются костеобразующие клетки, что приводит к восстановлению кости внутри дефекта, который в противном случае выполняется мягкими тканями.
2. Остеоиндуктивность: стимуляция роста костной ткани даже в тех областях, где она обычно не формируется: например, образование костной ткани внутри мышечной.
3. Остеогенные свойства: формирование новой кости активными клетками, пересаженными в структуре трансплантата.
В ходе реконструкции экстракционной лунки могут быть использованы разные типы костных трансплантатов: аутотрансплантаты, аллотрансплантаты, ксенотрансплантаты и аллопласты. Аутотрансплантаты, или аутогенные трансплантаты являются фрагментами костной ткани, собранной из донорской области у того же пациента, аллотрансплантаты – у другой особи, но обязательно того же вида. Ксенотрансплантаты, в свою очередь, являются костными заменителями, полученным из донорских участков других видов (животных), в то время как аллопласты есть ничем другим, как синтетическими, но обязательно биологически совместимыми, аналогами кости.
Идеальный костный трансплантат должен быть резорбируемым, остеокондуктивным, остеоиндуктивным и остеогенным материалом. Одновременно всем этим свойствам отвечают лишь аутотрансплантаты, но ввиду своего происхождения, врачу не всегда удается собрать достаточное количество данного материала у того же пациента. Следовательно, в большинстве случаев смежное использование других видов костных заменителей просто неизбежно, наиболее перспективными из которых остаются аллотраснплантаты. Во-первых, их использование является экономически обоснованным, не говоря уже о возможности использования данных материалов в разных формах:
1) Деминерализованная/минерализировання смесь – обладает остеоиндуктивными и остеокондуктивными свойствами, и, кроме того, обеспечивает структурную поддержку и объем пространства для выполнения его минерализованными частицами. Создает условия для быстрого формирования новой кости благодаря остеоиндуктивным свойствам деминерализованной составляющей. Показания: синус-лифт, реконструкция лунки зуба, горизонтальная и вертикальная аугментация костного гребня, восстановления пародонтальных дефектов.
2) Кортико-губчатая смесь – кортикальный компонент обеспечивает стабильность структуры трансплантата, в то время как губчатая составляющая облегчает процесс реваскуляризации области вмешательства. Показания: синус-лифт, реконструкция лунки зуба, вертикальная и горизонтальная аугментация резидуального гребня.
3) Минерализованный губчатый трансплантат – пористая структура, обеспечивающая условия для реваскуляризации, обладает остеокондуктивными и остеоиндуктивными свойствами. Показания: синус-лифт, реконструкция лунки зуба, горизонтальная и вертикальная аугментация резидуального гребня.
4) Минерализованный кортикальный трансплантат – благодаря большой плотности и прочности обеспечивает объем пространства для восстановления кости. Показания: синус-лифт, реконструкция лунки зуба, вертикальная и горизонтальная аугментация костного гребня, а также восстановления пародонтальных дефектов.
5) Деминерализованный кортикальный трансплантат – подходящий для тех случаев аугментации, где нет значительной потребности в структурной поддержке тканей. Показания: реконструкция лунки зуба и восстановление пародонтальных дефектов.
Конфигурации и показания к применению
Деминерализованный лиофилизированный костный аллотрансплантат (Demineralized freeze-dried bone allograft - DFDBA) формируют из человеческих трупов и, по мнению экспертов, благодаря наличию морфогенных белков он сохраняет свои остеоиндуктивные способности. Преимуществами использования данного материала является прогнозируемость процесса формирования кости, умеренная стоимость и доступность. Продолжительность его функционирования примерно такая же, как и у других аллотрнасплантатов: резорбция и замещение новосформировавшейся костной ткани происходит в период от 6 до 12 месяцев после аугментации.
Минерализованный лиофилизированный костный аллотрансплантат (Mineralized freeze-dried bone allograft – MFDBA) зачастую используется именно для аугментации лунки зуба после удаления с целью сохранения объема резидуального гребня под последующую установку дентального имплантата. MFDBA доступен в нескольких формах: кортикального или губчатого трансплантата, а также в виде костных блоков. При этом период его функционирования и ремоделирования более продолжительный, чем у DFDBA, и часто превышает 6-месячный срок, что и является его основным недостатком. Благодаря высоким показателям прочности и плотности MFDBA, а также более продолжительной резорбции, данный трансплантат целесообразно использовать при восстановлении больших костных дефектов с целью продолжительной поддержки объема пространства в области аугментации. При комбинации DFDBA и MFDBA клиницисту удается одновременно использовать преимущества остеокондуктивных свойств и короткого периода перестройки деминерализованного материала, сохраняя при этом пространство для аугментации на протяжении более длительного периода времени с помощью минерализованного плотного трансплантата. Подобный подход является наиболее оправданным в случаях планирования имплантации на месте недавно удалённых зубов.
Синтетические аналоги кости, аллопласты чаще всего используются при более традиционном подходе с последующей реабилитацией области адентии без применения трансплантатов. При их комбинации с аутотрансплантатом удается добиться лучшей плотности кости и более стабильного выполнения пространства полных или достаточно больших дефектов резидуального гребня. Данные материалы являются остеокондуктивными, а период их резорбции колеблется в диапазоне 6-24 месяцев, в зависимости от особенностей использованного материала и условий восстановления лунки зуба. Ксенотрансплантаты, как уже было указано выше, являются костными заменителями, полученными из особей другого вида. Наиболее распространенными представителями данного типа материалов являются бычья костная ткань и свиной коллаген. Ксенозаменители владеют остеокондуктивными свойствами, а их структура, химия и архитектура весьма схожи с аналогичными параметрами костной ткани человека.
Виды изолирующих мембран
В ходе физиологического процесса заживления клетки мягких тканей мигрируют в область дефекта гораздо быстрее, чем костнообразующие их аналоги. Следовательно, использование изолирующей мембраны вместе с костным трансплантатом является весьма важным биологическим аспектом при реконструкции пространства лунки удаленного зуба. Основная роль любой барьерной мембраны состоит в том, чтобы предупредить миграцию клеток мягких тканей в структуру трансплантационного материала во время периода заживления. Исследования показали, что использование барьерной мембраны после экстракции зуба уменьшает объем редукции костной массы, а также помогает минимизировать эффект горизонтальной резорбции резидуального гребня. Кроме того, данные мембраны являются биосовместимыми и биоинертными, достаточно легки в использовании, а также устойчивы к инфекционным агентам в полости рта. При этом для реконструкции лунки зуба могут быть использованы два вида подобных мембран: резорбируемые и нерезорбируемые. Наиболее часто резорбируемые мембраны изготавливают из коллагеновой матрицы, полученной из бычьего или свиного коллагена, человеческой дермы или тканей перикарда. Основными факторами, влияющими на выбор мембраны, являются именно плотность коллагеновой матрицы и ее способность противостоять воздействию факторов окружающей среды ротовой полости. Период резорбции данных структур достаточно вариабелен и может варьировать от пациента к пациенту. Кроме того, на процесс резорбции непосредственно влияют область хирургического вмешательства, возможность достижения первичного закрытия раны и фактор обнажения в полости рта. Другими вариантами изолирующих материалов являются коллагеновые губки или тампоны. Данные представители резорбируются значительно быстрее, чем истинные коллагеновые мембраны, поэтому использование таковых является целесообразным лишь в случаях реконструкции небольших лунок с ограниченным количеством трансплантата. При этом цена данных материалов довольно низка, а их применение с костным заменителем в любом случае способствует получению лучшего клинического результата.
Нерезорбируемые мембраны, как правило, изготавливаются из политетрафторэтилена (PTFE), также известного как Teflon, при этом данный материал может быть высокой плотности – d-PTFE или же иметь расширенные поры – е-PTFE. Использование нерезорбируемых мембран рекомендовано при восстановлении достаточно больших дефектов, или же в случаях, когда сложно добиться первичного закрытия раны для защиты низлежащего трансплантационного материала. В свою очередь, производственные характеристики d-PTFE мембран позволяют им оставаться обнажёнными в полости рта, не уменьшая при этом защиты области аугментации от бактериальной контаминации и миграции мягких тканей. Также мембраны из d-PTFE являются достаточно мягкими, гибкими и легкими в использовании, и могут быть легко удалены без необходимости проведения чрезмерно инвазивного хирургического вмешательства. В отличие от них, мембраны из е-PTFE характеризуются высокой пористостью, что, в свою очередь, увеличивает риск бактериального инфицирования и врастания мягких тканей в структуру трансплантата при их обнажении в полость рта, поэтому использование таковых при реконструкции лунки зуба не рекомендовано. Не говоря уже о том, что процесс удаления подобных изоляционных структур более манипуляционно сложный.
Дефекты лунки зуба
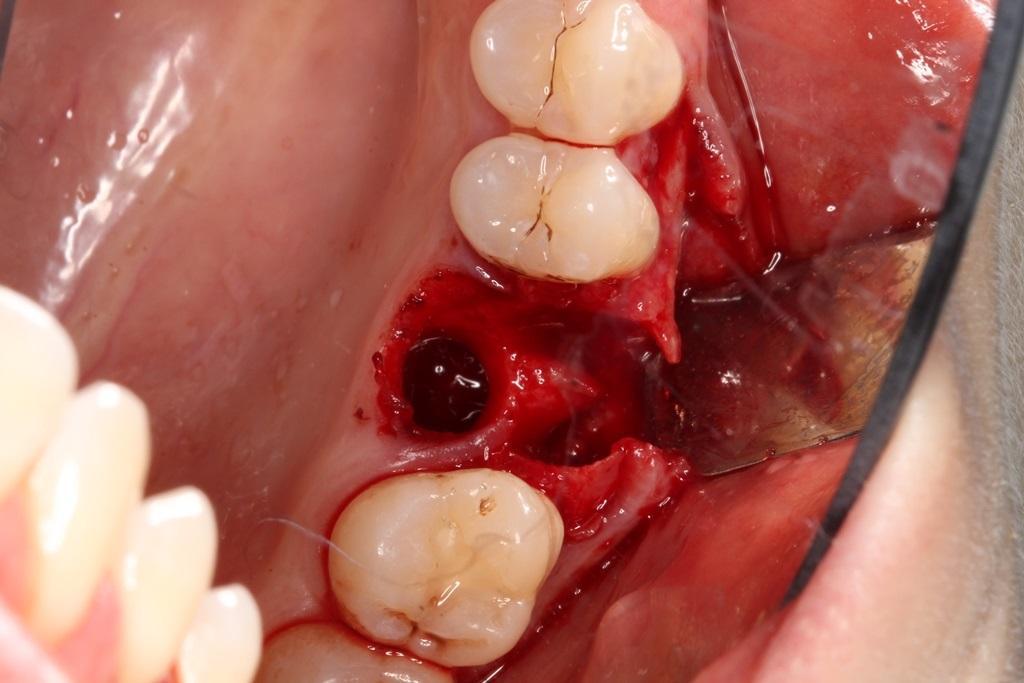
С целью обеспечения оптимального подхода к реконструкции лунки зуба сначала необходимо определить тип сформировавшегося дефекта в постэкстрационной области. Наиболее благоприятными являются дефекты лишь одной из стенок лунки, что формируются, как правило, в результате микроинвазивных хирургических манипуляций. Самый благоприятный вариант – это отсутствие самого зуба с дефектом одной из внутренних стенок с формированием так называемой интактной «чаши», которую впоследствии легко заполнить костным трансплантатом. Как правило, подобные дефекты характерны в ситуациях удаления одного зуба (фото 2). Дефекты одновременно двух стенок встречаются в результате повреждения щечной части лунки в ходе выполнения экстракции. В таких случаях стабилизировать трансплантат немного сложнее с учетом того, что также возрастает риск инвагинации мягких тканей с вестибулярной стороны (фото 3). При одновременном дефекте сразу трех или четырех стенок чаще всего рекомендуется комбинировать костные трансплантаты, по типу смеси DFDBA и MFDBA, или же кортикально/губчатого заменителя с частицами разного размера и обязательным использованием барьерных мембран. Дефекты всех пяти стенок являются редкостью, а объем реконструкции таковых значительно больше, следовательно, без специализированной хирургической помощи в данных случаях не обойтись.
Фото 2. Пример дефекта одной стенки лунки.
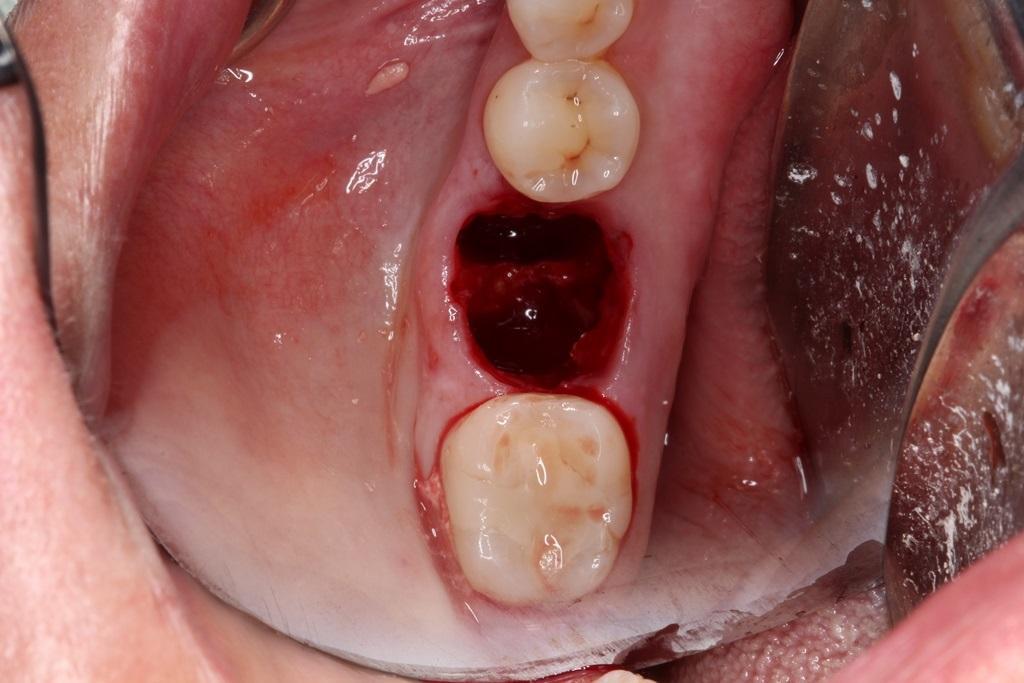
Фото 3. Пример обширного дефекта двух стенок одновременно.
Особенности выбора трансплантационных материалов
Сразу заметим, что идеального материала под все клинические случаи не существует, а выбор такового является частью планирования комплексного стоматологического вмешательства. Восстановление области адентии после выполнения экстракции может быть обеспечено посредством трех разных подходов: несъемными конструкциями, съемными протезами или супраконструкциями с опорой на имплантате. При этом для каждого из вышеперечисленных вариантов протезирования выбор костного заменителя значительно отличается. При замещении области адентии несъемной мостовидной конструкцией для аугментации лунки успешно могут быть использованы плотные нерезорбируемые синтетические аллопласты, обеспечивающие долгосрочную стабильность восстановленных параметров гребня без перспективы дальнейшего проведения имплантации. Данные материалы просты в использовании и относительно недорогие.
В случаях дальнейшей имплантации при относительно интактной лунке рекомендовано использовать резорбируемые трансплантаты, по типу минерализованного губчатого заменителя. При обширных дефектах, в случаях инфицирования или же неопределённости относительно проведения имплантации в будущем желательно комбинировать костные заменители, как это уже было описано выше, в сочетании с барьерной мембраной. Подобный подход поможет воссоздать достаточно плотную ткань в области имплантации и при этом обеспечить место для дальнейшей установки инфаконструкции через определенное время.
Алгоритм и техники реконструкции лунки
Использование адекватных методов удаления и техник аугментации постэкстракционной лунки позволяет клиницисту добиться более эффективных и прогнозированных результатов лечения:
1. Минимально инвазивное и атравматическое удаление резидуальных фрагметов зубов при помощи периотомов и других деликатных инструментов, как, например, секционирование зуба при соответствующей необходимости, помогает минимизировать травму тонкой кортикальной костной пластинки и окружающих мягких тканей (фото 4).
Фото 4. Атравматичное удаление зуба.
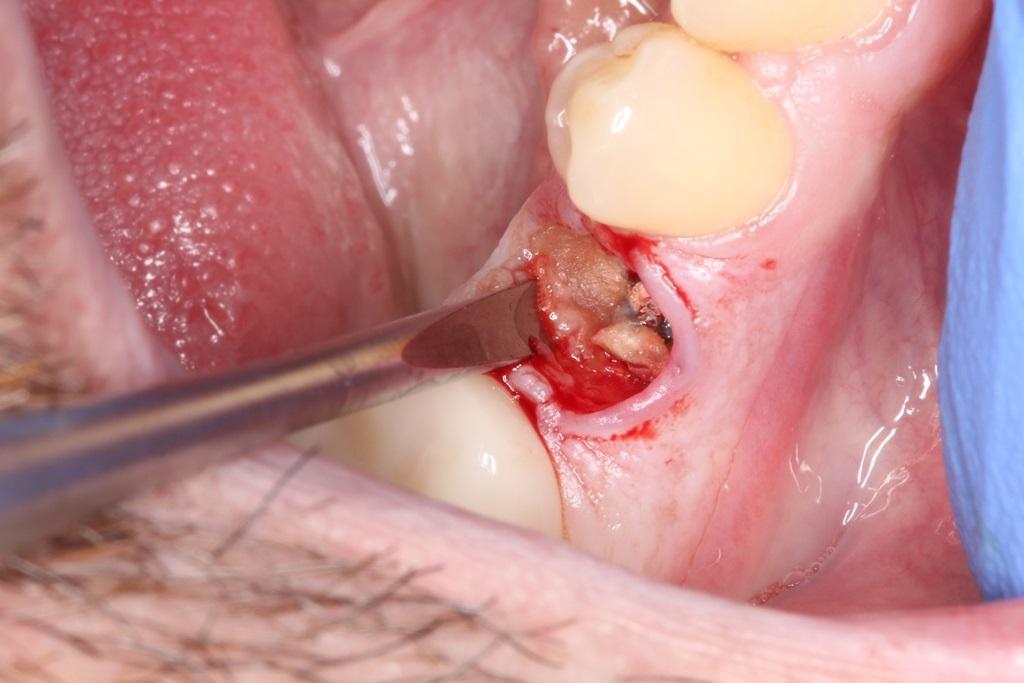
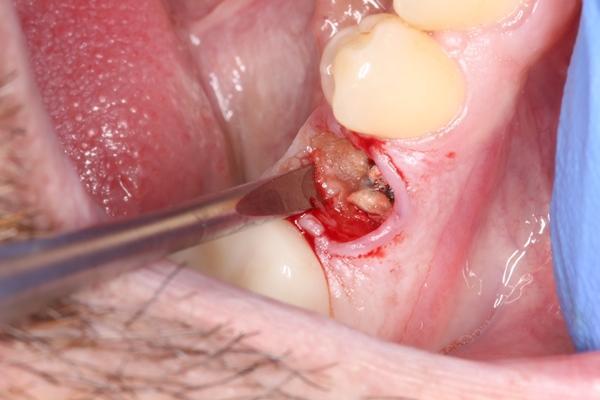
2. С целью удаления имеющихся грануляций и остаточных мягких тканей из области апекса после удаления обязательно нужно проводить кюретаж лунки, особенно в случаях экстракции эндодонтически пролеченных зубов (фото 5).
Фото 5. Очистка лунки зуба после экстракции.
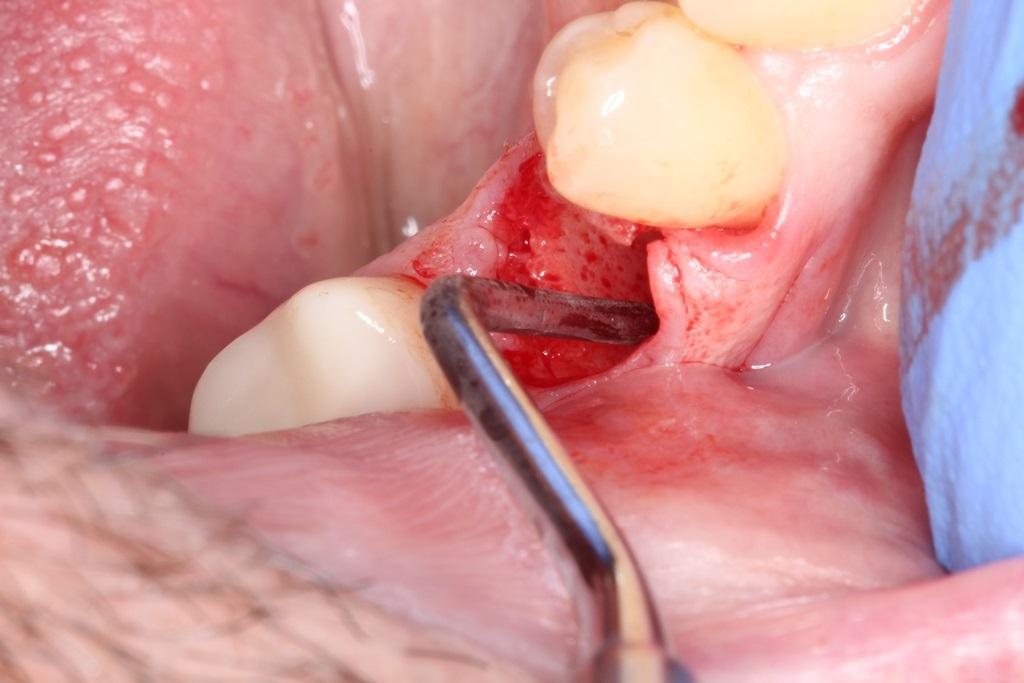
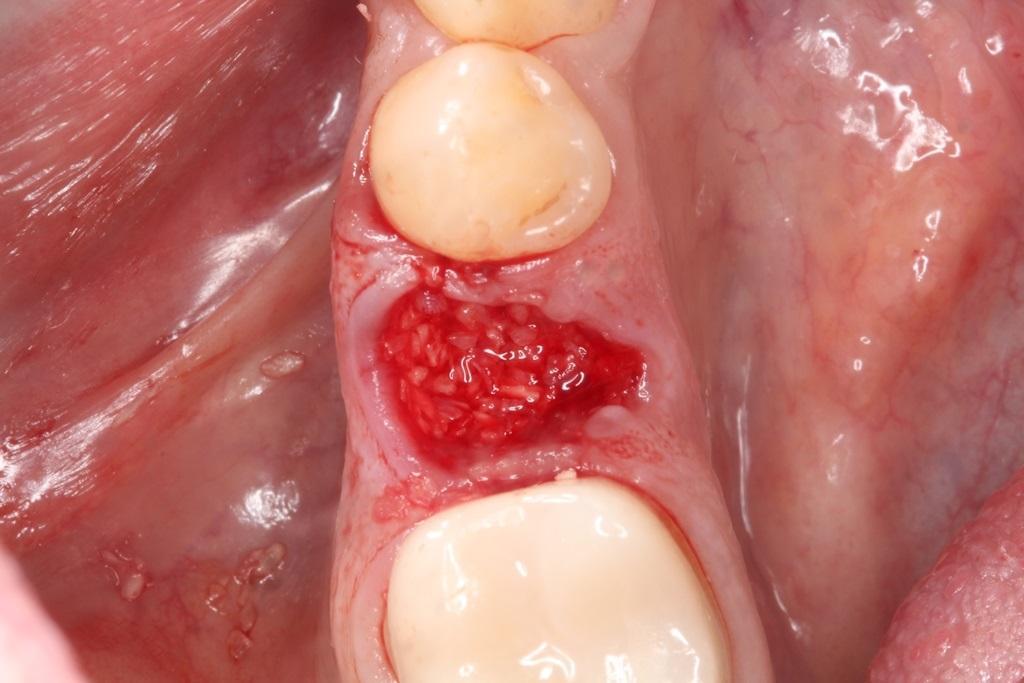
3. Убедитесь в том, что лунка зуба кровенаполняется (фото 6): при необходимости можно провести дополнительную декортикацию лунки хирургическим бором с целью обеспечения ее кровенаполнения, что в дальнейшем будет способствовать ранней васкуляризации и первичному заживлению области вмешательства.
Фото 6. Кровенаполнение лунки перед установкой костного трансплантата. Обеспечение адекватного кровенаполнения значительно увеличивает шансы достижения успешного результата аугментации постэкстракционной лунки.
4. Убедитесь в том, что выбранный трансплантационный материал достаточно увлажнен. Как правило, данную процедуру выполняют с использованием стерильного физиологического раствора за 15 до 20 минут перед установкой трансплантата в область лунки (фото 7).
Фото 7. Увлажнение гранулированного аллотрансплантата.

5. Независимо от выбора PTFE или коллагеновой мембраны, с помощью элеватора или кюреты сначала нужно сформировать поднадкостничный карман с вестибулярной и лингвальной сторон протяжностью в 3-5 мм мимо краев лунки или остаточного дефекта.
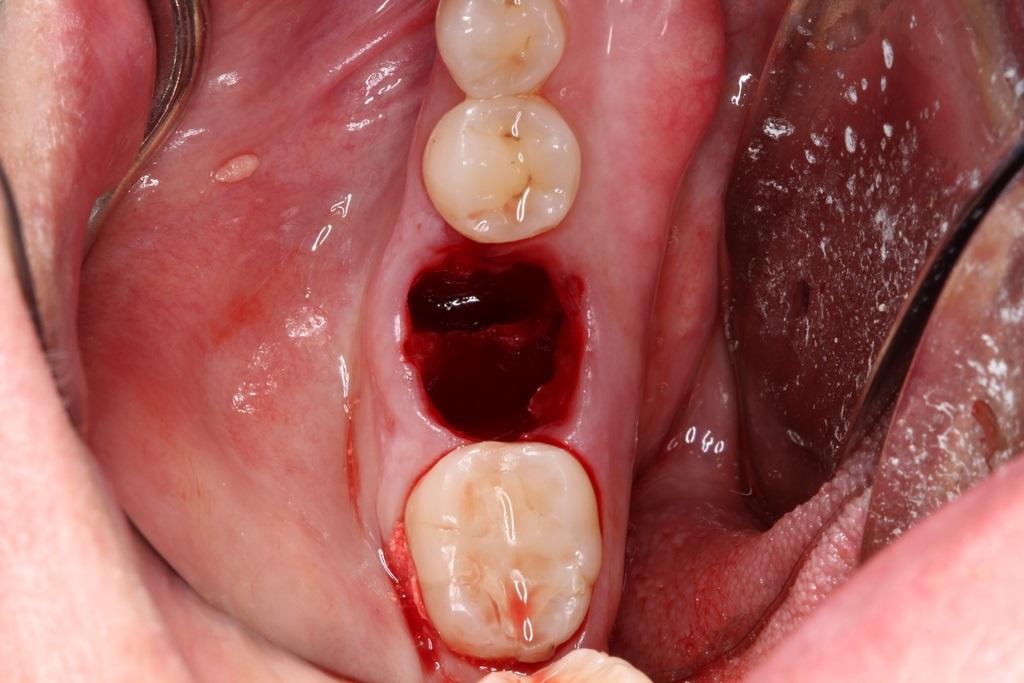
6. После установки трансплантата его нужно осторожно конденсировать и убедится в том, что материал равномерно распределен по пространству лунки без формирования пор и пустот. При этом конденсация материала должна быть умеренной с учетом необходимости васкуляризации области аугментации в будущем и прогноза срока заживления (фото 8).
Фото 8. Установка аллотрансплантата в лунку свежеудаленного зуба.
7. Мембрану нужно позиционировать в форме конверта заправляя ее аккуратно с вестибулярной и язычной стороны лунки, обеспечивая при этом ее плотное размещение над материалом трансплантата и стабильность после установки (фото 9).
Фото 9. Установка мембраны или коллагеновой губки перед ушиванием раны.
8. Обеспечить стабилизацию мембраны или коллагеновой губки с помощью крестообразных матрацных швов, следя за тем, чтобы не прошить саму мембрану. Для обеспечения адекватного закрытия раны дополнительно могут быть использованы узловые швы, при этом нужно обеспечить ушивание раны без чрезмерного натяжения, что в дальнейшем может спровоцировать возникновение соответствующих осложнений (фото 10).
Фото 10. Ушивание раны с целью стабилизации мембраны и костного заменителя.
9. Удаление швов должно проходить на 10-14 день после вмешательства.
10. При использовании d-PTFE мембраны, удаление таковой можно проводить на 21-28 день после вмешательства. Согласно данным исследований, в указанный срок успевает сформироваться плотная сосудистая матрица соединительной ткани, а в апикальных двух третях лунки уже прогрессирует процесс остеогенеза.
11. При восстановлении области адентии посредством несъемных ортопедических конструкций заживление раны должно проходить как минимум на протяжении 6 недель, а при планировании имплантации – на протяжении 4 месяцев (фото 11).
Фото 11. Рентгенограмма лунки зуба после установки костного заменителя.
Кроме того, при выполнении аугментации лунки дополнительно можно использовать плазму, обогащенную тромбоцитами (PRP), а также фибрин, обогащенный тромбоцитами (PRF). Но имплементация подобных подходов требует еще и умений забора крови у пациента, центрифугирования, сепарации частиц, а также формирования псевдо-мембран и заполнения ими лунки зуба. По мнению автора, все вышеперечисленные аспекты выходят за рамки данной статьи, адресатами которой являются врачи-клиницисты общей практики.
Выводы
Реконструкция лунки зуба является важным этапом комплексного лечения пациентов в разрезе подготовки области экстракции под будущую фиксацию несъемных ортопедических конструкций или установку дентальных имплантатов. Обеспечение атравматичности хирургической манипуляции с целью сохранения интактности окружающих твердых и мягких тканей, как и аргументированный выбор трансплантационных материалов с учетом специфики разных клинических ситуаций, поможет врачу-стоматологу добиться наиболее желаемого и прогнозированного результата лечения, не говоря уже о возможности сформировать наиболее эстетический и гигиенический профиль в области ятрогенного вмешательства. При разумном подходе и корректном выполнении, процедура аугментации постэкстракционной лунки является достаточно легкой в освоении и достаточно простой для использования в повседневной практике.
Автор: Scott Keys, DDS
Удаление полностью безнадёжных зубов, а также таковых скомпрометированных пародонтальным или значительным кариозным поражением, является наиболее распространённой манипуляцией в повседневной практике врача-стоматолога. Поэтому число успешно экстрагированных зубных единиц среди некоторых клиницистов превышает тысячный рубеж, но, даже несмотря на тщательное планирование процедуры, данная манипуляция является одной из самых важных этапов данного ятрогенного вмешательства.

Особенности формирования и резорбции костной ткани
Одним из наиболее важных факторов морфологии костной ткани, как и процесса ее заживления, является именно клеточный компонент. Основными типами клеток, играющими определенную роль в ходе формирования костной массы, остаются остеопрогениторные клетки, остеокласты, остеобласты и остеоциты.
1. Остеопрогениторные клетки являются недифференцированными стволовыми клетками, которые выстилают эндостальную поверхности кости. В дальнейшем данные клетки дифференцируются в клетки пре-остеобластов, а затем и в зрелых остеобластов, находясь при этом в зоне эндоста.
2. Остеокласты являются клетками, ответственными за резорбтивные процессы, а также ремоделирование костной ткани.
3. Остеобласты отвечают за депозицию и кальцификацию новосформировашегося костного матрикса.
4. Остеоциты по своей природе являются остеобластами, которые выполнили свою функцию, и остались зацементированными в сформировавшемся костном матриксе, сохранив при этом межклеточную связь, значение которой крайне важно при адаптации к нагрузкам или нарушении целостности кости.
С целью общего описания всех динамических процессов в костной ткани, можно использовать всего два концептуальных понятия: моделирование и ремоделирование (фото 1).
Фото 1. Иллюстрация процесса формирования костной ткани.

Моделирование представляет собой процесс внутрикостных изменений в ответ на некую стимуляцию или физическую силу. Ремоделирование относится же к более постоянному процессу внутренних изменений кости, при которых взаимодействие остеобластов и остеокластов является более гармоничным и сбалансированным, когда обеспечивается нормальное функционирование элементов человеческого скелета.
Виды трансплантационных материалов
Чаще всего фактором, определяющим необходимость проведения реконструкции лунки после удаления, является степень травмирования окружающих твердых и мягких тканей во время проведения процедуры экстракции. Степень целостности костных стенок лунки, в свою очередь, помогает адекватно подобрать вид трансплантационного материала с учетом будущих изменений в структуре альвеолярного гребня после выполнения твердотканной аугментации. В ходе выбора трансплантата важно учитывать три основных характеристики:
1. Остеокондуктивность: формирование площадки или каркаса, на которые в дальнейшем заселяются костеобразующие клетки, что приводит к восстановлению кости внутри дефекта, который в противном случае выполняется мягкими тканями.
2. Остеоиндуктивность: стимуляция роста костной ткани даже в тех областях, где она обычно не формируется: например, образование костной ткани внутри мышечной.
3. Остеогенные свойства: формирование новой кости активными клетками, пересаженными в структуре трансплантата.
В ходе реконструкции экстракционной лунки могут быть использованы разные типы костных трансплантатов: аутотрансплантаты, аллотрансплантаты, ксенотрансплантаты и аллопласты. Аутотрансплантаты, или аутогенные трансплантаты являются фрагментами костной ткани, собранной из донорской области у того же пациента, аллотрансплантаты – у другой особи, но обязательно того же вида. Ксенотрансплантаты, в свою очередь, являются костными заменителями, полученным из донорских участков других видов (животных), в то время как аллопласты есть ничем другим, как синтетическими, но обязательно биологически совместимыми, аналогами кости.
Идеальный костный трансплантат должен быть резорбируемым, остеокондуктивным, остеоиндуктивным и остеогенным материалом. Одновременно всем этим свойствам отвечают лишь аутотрансплантаты, но ввиду своего происхождения, врачу не всегда удается собрать достаточное количество данного материала у того же пациента. Следовательно, в большинстве случаев смежное использование других видов костных заменителей просто неизбежно, наиболее перспективными из которых остаются аллотраснплантаты. Во-первых, их использование является экономически обоснованным, не говоря уже о возможности использования данных материалов в разных формах:
1) Деминерализованная/минерализировання смесь – обладает остеоиндуктивными и остеокондуктивными свойствами, и, кроме того, обеспечивает структурную поддержку и объем пространства для выполнения его минерализованными частицами. Создает условия для быстрого формирования новой кости благодаря остеоиндуктивным свойствам деминерализованной составляющей. Показания: синус-лифт, реконструкция лунки зуба, горизонтальная и вертикальная аугментация костного гребня, восстановления пародонтальных дефектов.
2) Кортико-губчатая смесь – кортикальный компонент обеспечивает стабильность структуры трансплантата, в то время как губчатая составляющая облегчает процесс реваскуляризации области вмешательства. Показания: синус-лифт, реконструкция лунки зуба, вертикальная и горизонтальная аугментация резидуального гребня.
3) Минерализованный губчатый трансплантат – пористая структура, обеспечивающая условия для реваскуляризации, обладает остеокондуктивными и остеоиндуктивными свойствами. Показания: синус-лифт, реконструкция лунки зуба, горизонтальная и вертикальная аугментация резидуального гребня.
4) Минерализованный кортикальный трансплантат – благодаря большой плотности и прочности обеспечивает объем пространства для восстановления кости. Показания: синус-лифт, реконструкция лунки зуба, вертикальная и горизонтальная аугментация костного гребня, а также восстановления пародонтальных дефектов.
5) Деминерализованный кортикальный трансплантат – подходящий для тех случаев аугментации, где нет значительной потребности в структурной поддержке тканей. Показания: реконструкция лунки зуба и восстановление пародонтальных дефектов.
Конфигурации и показания к применению
Деминерализованный лиофилизированный костный аллотрансплантат (Demineralized freeze-dried bone allograft - DFDBA) формируют из человеческих трупов и, по мнению экспертов, благодаря наличию морфогенных белков он сохраняет свои остеоиндуктивные способности. Преимуществами использования данного материала является прогнозируемость процесса формирования кости, умеренная стоимость и доступность. Продолжительность его функционирования примерно такая же, как и у других аллотрнасплантатов: резорбция и замещение новосформировавшейся костной ткани происходит в период от 6 до 12 месяцев после аугментации.
Минерализованный лиофилизированный костный аллотрансплантат (Mineralized freeze-dried bone allograft – MFDBA) зачастую используется именно для аугментации лунки зуба после удаления с целью сохранения объема резидуального гребня под последующую установку дентального имплантата. MFDBA доступен в нескольких формах: кортикального или губчатого трансплантата, а также в виде костных блоков. При этом период его функционирования и ремоделирования более продолжительный, чем у DFDBA, и часто превышает 6-месячный срок, что и является его основным недостатком. Благодаря высоким показателям прочности и плотности MFDBA, а также более продолжительной резорбции, данный трансплантат целесообразно использовать при восстановлении больших костных дефектов с целью продолжительной поддержки объема пространства в области аугментации. При комбинации DFDBA и MFDBA клиницисту удается одновременно использовать преимущества остеокондуктивных свойств и короткого периода перестройки деминерализованного материала, сохраняя при этом пространство для аугментации на протяжении более длительного периода времени с помощью минерализованного плотного трансплантата. Подобный подход является наиболее оправданным в случаях планирования имплантации на месте недавно удалённых зубов.
Синтетические аналоги кости, аллопласты чаще всего используются при более традиционном подходе с последующей реабилитацией области адентии без применения трансплантатов. При их комбинации с аутотрансплантатом удается добиться лучшей плотности кости и более стабильного выполнения пространства полных или достаточно больших дефектов резидуального гребня. Данные материалы являются остеокондуктивными, а период их резорбции колеблется в диапазоне 6-24 месяцев, в зависимости от особенностей использованного материала и условий восстановления лунки зуба. Ксенотрансплантаты, как уже было указано выше, являются костными заменителями, полученными из особей другого вида. Наиболее распространенными представителями данного типа материалов являются бычья костная ткань и свиной коллаген. Ксенозаменители владеют остеокондуктивными свойствами, а их структура, химия и архитектура весьма схожи с аналогичными параметрами костной ткани человека.
Виды изолирующих мембран
В ходе физиологического процесса заживления клетки мягких тканей мигрируют в область дефекта гораздо быстрее, чем костнообразующие их аналоги. Следовательно, использование изолирующей мембраны вместе с костным трансплантатом является весьма важным биологическим аспектом при реконструкции пространства лунки удаленного зуба. Основная роль любой барьерной мембраны состоит в том, чтобы предупредить миграцию клеток мягких тканей в структуру трансплантационного материала во время периода заживления. Исследования показали, что использование барьерной мембраны после экстракции зуба уменьшает объем редукции костной массы, а также помогает минимизировать эффект горизонтальной резорбции резидуального гребня. Кроме того, данные мембраны являются биосовместимыми и биоинертными, достаточно легки в использовании, а также устойчивы к инфекционным агентам в полости рта. При этом для реконструкции лунки зуба могут быть использованы два вида подобных мембран: резорбируемые и нерезорбируемые. Наиболее часто резорбируемые мембраны изготавливают из коллагеновой матрицы, полученной из бычьего или свиного коллагена, человеческой дермы или тканей перикарда. Основными факторами, влияющими на выбор мембраны, являются именно плотность коллагеновой матрицы и ее способность противостоять воздействию факторов окружающей среды ротовой полости. Период резорбции данных структур достаточно вариабелен и может варьировать от пациента к пациенту. Кроме того, на процесс резорбции непосредственно влияют область хирургического вмешательства, возможность достижения первичного закрытия раны и фактор обнажения в полости рта. Другими вариантами изолирующих материалов являются коллагеновые губки или тампоны. Данные представители резорбируются значительно быстрее, чем истинные коллагеновые мембраны, поэтому использование таковых является целесообразным лишь в случаях реконструкции небольших лунок с ограниченным количеством трансплантата. При этом цена данных материалов довольно низка, а их применение с костным заменителем в любом случае способствует получению лучшего клинического результата.
Нерезорбируемые мембраны, как правило, изготавливаются из политетрафторэтилена (PTFE), также известного как Teflon, при этом данный материал может быть высокой плотности – d-PTFE или же иметь расширенные поры – е-PTFE. Использование нерезорбируемых мембран рекомендовано при восстановлении достаточно больших дефектов, или же в случаях, когда сложно добиться первичного закрытия раны для защиты низлежащего трансплантационного материала. В свою очередь, производственные характеристики d-PTFE мембран позволяют им оставаться обнажёнными в полости рта, не уменьшая при этом защиты области аугментации от бактериальной контаминации и миграции мягких тканей. Также мембраны из d-PTFE являются достаточно мягкими, гибкими и легкими в использовании, и могут быть легко удалены без необходимости проведения чрезмерно инвазивного хирургического вмешательства. В отличие от них, мембраны из е-PTFE характеризуются высокой пористостью, что, в свою очередь, увеличивает риск бактериального инфицирования и врастания мягких тканей в структуру трансплантата при их обнажении в полость рта, поэтому использование таковых при реконструкции лунки зуба не рекомендовано. Не говоря уже о том, что процесс удаления подобных изоляционных структур более манипуляционно сложный.
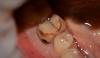
Дефекты лунки зуба
С целью обеспечения оптимального подхода к реконструкции лунки зуба сначала необходимо определить тип сформировавшегося дефекта в постэкстрационной области. Наиболее благоприятными являются дефекты лишь одной из стенок лунки, что формируются, как правило, в результате микроинвазивных хирургических манипуляций. Самый благоприятный вариант – это отсутствие самого зуба с дефектом одной из внутренних стенок с формированием так называемой интактной «чаши», которую впоследствии легко заполнить костным трансплантатом. Как правило, подобные дефекты характерны в ситуациях удаления одного зуба (фото 2). Дефекты одновременно двух стенок встречаются в результате повреждения щечной части лунки в ходе выполнения экстракции. В таких случаях стабилизировать трансплантат немного сложнее с учетом того, что также возрастает риск инвагинации мягких тканей с вестибулярной стороны (фото 3). При одновременном дефекте сразу трех или четырех стенок чаще всего рекомендуется комбинировать костные трансплантаты, по типу смеси DFDBA и MFDBA, или же кортикально/губчатого заменителя с частицами разного размера и обязательным использованием барьерных мембран. Дефекты всех пяти стенок являются редкостью, а объем реконструкции таковых значительно больше, следовательно, без специализированной хирургической помощи в данных случаях не обойтись.
Фото 2. Пример дефекта одной стенки лунки.

Фото 3. Пример обширного дефекта двух стенок одновременно.

Особенности выбора трансплантационных материалов
Сразу заметим, что идеального материала под все клинические случаи не существует, а выбор такового является частью планирования комплексного стоматологического вмешательства. Восстановление области адентии после выполнения экстракции может быть обеспечено посредством трех разных подходов: несъемными конструкциями, съемными протезами или супраконструкциями с опорой на имплантате. При этом для каждого из вышеперечисленных вариантов протезирования выбор костного заменителя значительно отличается. При замещении области адентии несъемной мостовидной конструкцией для аугментации лунки успешно могут быть использованы плотные нерезорбируемые синтетические аллопласты, обеспечивающие долгосрочную стабильность восстановленных параметров гребня без перспективы дальнейшего проведения имплантации. Данные материалы просты в использовании и относительно недорогие.
В случаях дальнейшей имплантации при относительно интактной лунке рекомендовано использовать резорбируемые трансплантаты, по типу минерализованного губчатого заменителя. При обширных дефектах, в случаях инфицирования или же неопределённости относительно проведения имплантации в будущем желательно комбинировать костные заменители, как это уже было описано выше, в сочетании с барьерной мембраной. Подобный подход поможет воссоздать достаточно плотную ткань в области имплантации и при этом обеспечить место для дальнейшей установки инфаконструкции через определенное время.
Алгоритм и техники реконструкции лунки
Использование адекватных методов удаления и техник аугментации постэкстракционной лунки позволяет клиницисту добиться более эффективных и прогнозированных результатов лечения:
1. Минимально инвазивное и атравматическое удаление резидуальных фрагметов зубов при помощи периотомов и других деликатных инструментов, как, например, секционирование зуба при соответствующей необходимости, помогает минимизировать травму тонкой кортикальной костной пластинки и окружающих мягких тканей (фото 4).
Фото 4. Атравматичное удаление зуба.

2. С целью удаления имеющихся грануляций и остаточных мягких тканей из области апекса после удаления обязательно нужно проводить кюретаж лунки, особенно в случаях экстракции эндодонтически пролеченных зубов (фото 5).
Фото 5. Очистка лунки зуба после экстракции.

3. Убедитесь в том, что лунка зуба кровенаполняется (фото 6): при необходимости можно провести дополнительную декортикацию лунки хирургическим бором с целью обеспечения ее кровенаполнения, что в дальнейшем будет способствовать ранней васкуляризации и первичному заживлению области вмешательства.
Фото 6. Кровенаполнение лунки перед установкой костного трансплантата. Обеспечение адекватного кровенаполнения значительно увеличивает шансы достижения успешного результата аугментации постэкстракционной лунки.

4. Убедитесь в том, что выбранный трансплантационный материал достаточно увлажнен. Как правило, данную процедуру выполняют с использованием стерильного физиологического раствора за 15 до 20 минут перед установкой трансплантата в область лунки (фото 7).
Фото 7. Увлажнение гранулированного аллотрансплантата.

5. Независимо от выбора PTFE или коллагеновой мембраны, с помощью элеватора или кюреты сначала нужно сформировать поднадкостничный карман с вестибулярной и лингвальной сторон протяжностью в 3-5 мм мимо краев лунки или остаточного дефекта.
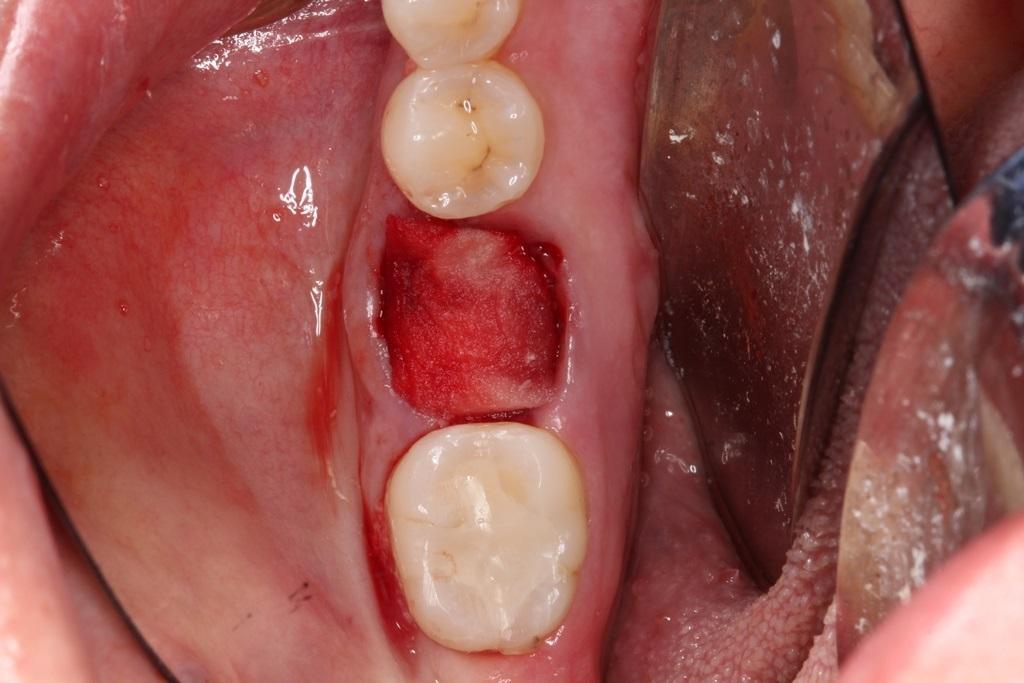
6. После установки трансплантата его нужно осторожно конденсировать и убедится в том, что материал равномерно распределен по пространству лунки без формирования пор и пустот. При этом конденсация материала должна быть умеренной с учетом необходимости васкуляризации области аугментации в будущем и прогноза срока заживления (фото 8).
Фото 8. Установка аллотрансплантата в лунку свежеудаленного зуба.

7. Мембрану нужно позиционировать в форме конверта заправляя ее аккуратно с вестибулярной и язычной стороны лунки, обеспечивая при этом ее плотное размещение над материалом трансплантата и стабильность после установки (фото 9).
Фото 9. Установка мембраны или коллагеновой губки перед ушиванием раны.

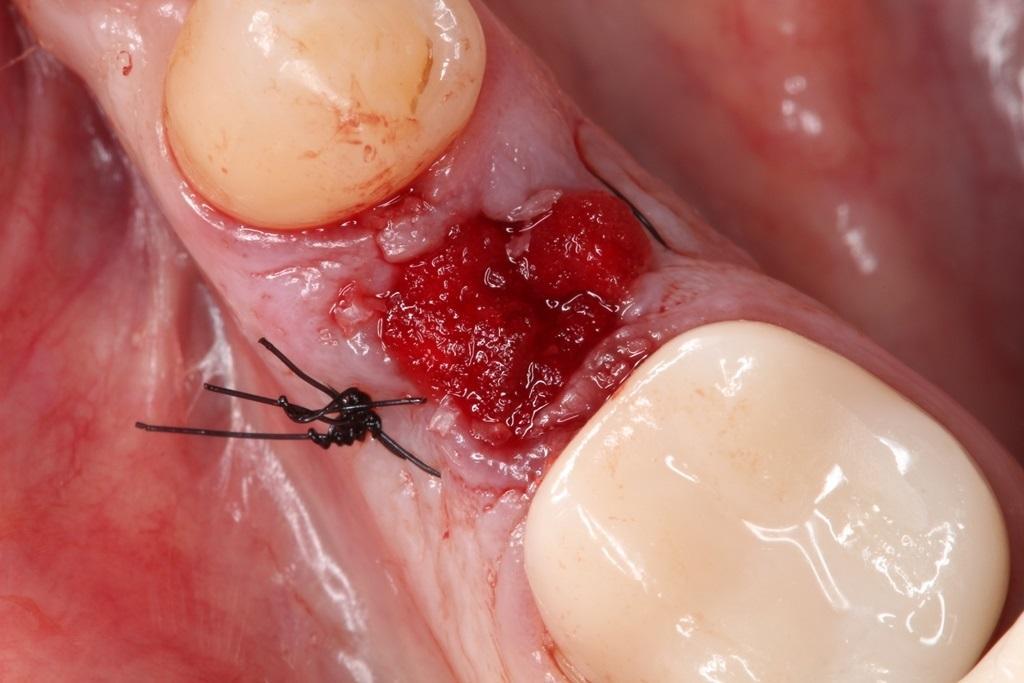
8. Обеспечить стабилизацию мембраны или коллагеновой губки с помощью крестообразных матрацных швов, следя за тем, чтобы не прошить саму мембрану. Для обеспечения адекватного закрытия раны дополнительно могут быть использованы узловые швы, при этом нужно обеспечить ушивание раны без чрезмерного натяжения, что в дальнейшем может спровоцировать возникновение соответствующих осложнений (фото 10).
Фото 10. Ушивание раны с целью стабилизации мембраны и костного заменителя.

9. Удаление швов должно проходить на 10-14 день после вмешательства.
10. При использовании d-PTFE мембраны, удаление таковой можно проводить на 21-28 день после вмешательства. Согласно данным исследований, в указанный срок успевает сформироваться плотная сосудистая матрица соединительной ткани, а в апикальных двух третях лунки уже прогрессирует процесс остеогенеза.
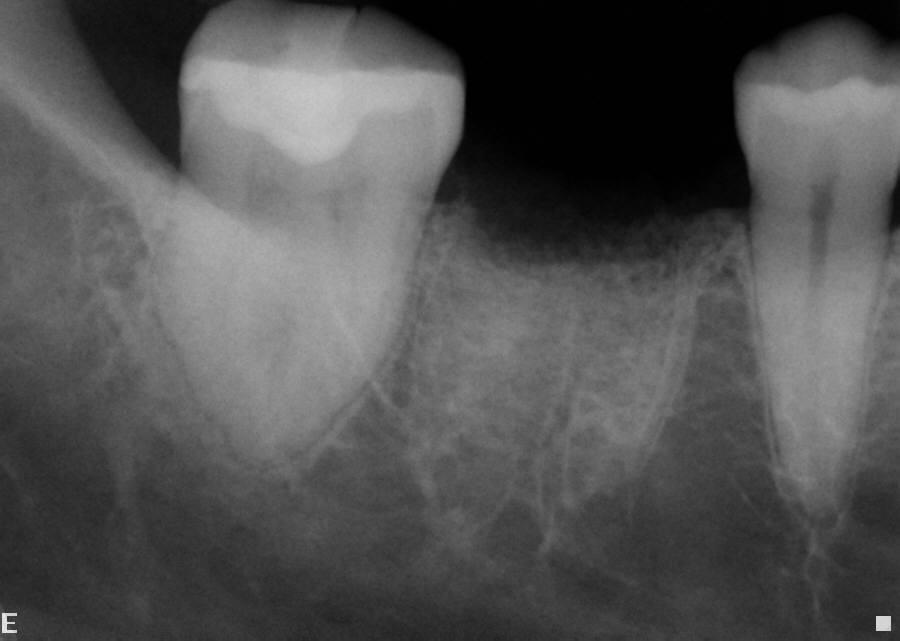
11. При восстановлении области адентии посредством несъемных ортопедических конструкций заживление раны должно проходить как минимум на протяжении 6 недель, а при планировании имплантации – на протяжении 4 месяцев (фото 11).
Фото 11. Рентгенограмма лунки зуба после установки костного заменителя.

Кроме того, при выполнении аугментации лунки дополнительно можно использовать плазму, обогащенную тромбоцитами (PRP), а также фибрин, обогащенный тромбоцитами (PRF). Но имплементация подобных подходов требует еще и умений забора крови у пациента, центрифугирования, сепарации частиц, а также формирования псевдо-мембран и заполнения ими лунки зуба. По мнению автора, все вышеперечисленные аспекты выходят за рамки данной статьи, адресатами которой являются врачи-клиницисты общей практики.
Выводы
Реконструкция лунки зуба является важным этапом комплексного лечения пациентов в разрезе подготовки области экстракции под будущую фиксацию несъемных ортопедических конструкций или установку дентальных имплантатов. Обеспечение атравматичности хирургической манипуляции с целью сохранения интактности окружающих твердых и мягких тканей, как и аргументированный выбор трансплантационных материалов с учетом специфики разных клинических ситуаций, поможет врачу-стоматологу добиться наиболее желаемого и прогнозированного результата лечения, не говоря уже о возможности сформировать наиболее эстетический и гигиенический профиль в области ятрогенного вмешательства. При разумном подходе и корректном выполнении, процедура аугментации постэкстракционной лунки является достаточно легкой в освоении и достаточно простой для использования в повседневной практике.
Автор: Scott Keys, DDS



























































































































































0 комментариев