При переломе дентальных имплантатов требуется дальнейшее их удаление из структуры кости челюстей.

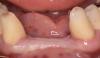
Фото 1. Перелом платформы имплантата. Из-за воспаления произошля потеря уровня костной ткани. В апикальной части отмечаются грануляции.
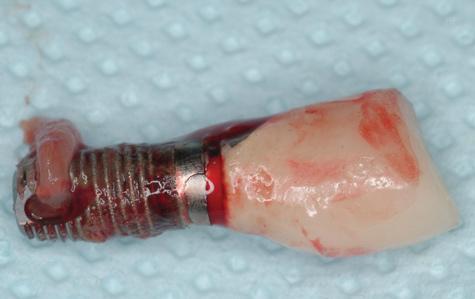
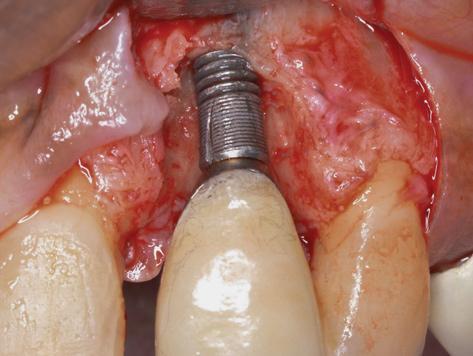
Фото 2. Пример перелома имплантата. Конструкция требует удаления, а область имплантации – аугментации для последующей процедуры имплантации.
Даже после очистки периимплантатной области в таких случаях, а также после приема антибиотиков системного действия, у пациента продолжает отмечаться потеря костной ткани, отек и дискомфорт в периимплантатной области. Удаление имплантатов с переломом корональной части области соединения является довольной сложной задачей при использовании лишь инструментов с возможностью развития обратного торка. Иногда подобный подход также может спровоцировать дальнейшее развитие перелома, что только усложняет возможность удаления дефектной конструкции. Обычно подобные конструкции удаляют при помощи пустотелого трепана. При этом диаметр трепана должен быть больше диаметра имплантата, чтобы режущий инструмент мог пройти параллельно поверхности титановой опоры при этом ее не задев. Если при сегментации имплантат разделился в самой широкой своей части, что, к сожалению, приводит к значительному распространению титанового дебриса, можно использовать более узкий трепан, чтобы сохранить дополнительную кость. После того, как тело имплантата больше не контактируют с окружающей костью, маленьким корневым элеватором проникают по окружности, чтобы разрушить апикальную часть конструкции в подлежащей кости.
Процедура удаления имплантата является довольно-таки деликатной, если речь идет об удалении апикальной части конструкции, при близком положении имплантата к соседним зубам, полости синуса или каналу нижнечелюстного нерва. Планирование подобной процедуры осуществляется с обязательным применением конусно-лучевой компьютерной томографии (КЛКТ), которая позволяет оценить состояние костной ткани во всех проекциях. На фото 3 изображен один имплантат, который был удален посредством обратного торка, и второй, который удаляли с применением трепана. Поскольку при выполнении остеотомии трепаном, сформировавшейся дефект костной ткани является больше размера первоначально установленного имплантата, таковые участки довольно сложно заимплантировать повторно, особенно если речь идет и немедленной имплантации. В отдельных случаях для компенсации подобного исхода применяют имплантаты более широкого диаметра. При этом необходимо помнить об обеспечении расстояния в 1,5-2 мм между двумя смежными имплантатом и зубом, и в 3 мм между двумя смежными имплантатами. На фото 3 изображен перелом имплантата, который сформировался смежно с переломом 13 зуба. После удаления дефектной конструкции и зуба на их место были установлены два новые имплантата (Astra Tech, Dentsply Sirona), для стабилизации которых использовали как имеющуюся, так и дополнительный объемы костной ткани (фото 5).
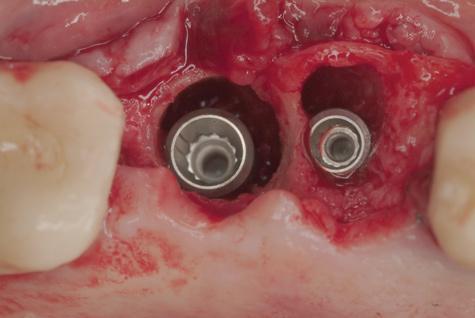
Фото 3. Два имплантата удалены двумя разными техниками. Узкий имплантат был удален инструментом с обратным торком, а широкий – посредством трепана.

Фото 4. Вид имплантата, который удалялся посредством трепана. После удаления на место дефектной конструкции был установлен имплантат с более широким диаметром. Вместе с имплантацией была проведена процедура аугментации.
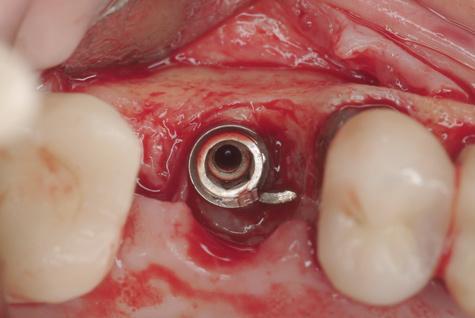
Фото 5. Вид имплантата, который удалялся посредством трепана. После удаления на место дефектной конструкции был установлен имплантат с более широким диаметром. Вместе с имплантацией была проведена процедура аугментации.
При невозможности проведения одномоментной имплантации, область удаления титановой опоры следует восстановить посредством костного аугментата, дождаться необходимого уровня организации кости на протяжении 4-6 месяцев, и только после этого приступить к повторной имплантации. В одиночных случаях в область удаления имплантата можно установить другой, более широкий, не нарушив при этом ни эстетических, ни функциональных критериев реабилитации (фото 6 - 10).
Фото 6. Вид после удаления 3,6 мм имплантата посредством 4,0 мм трепана.
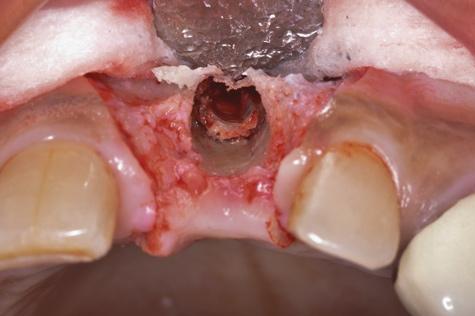
Фото 7. После удаления был установлен имплантат более широкого диаметра – 4,2 мм. Вместе с имплантацией была проведена процедура аугментации.
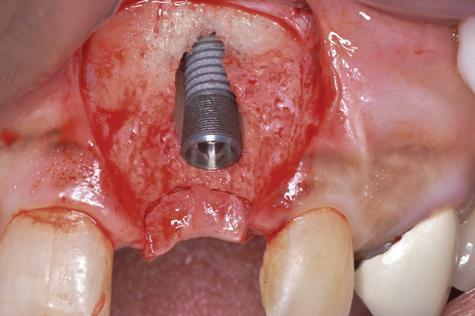
Фото 8. Аугментация в области имплантации посредством костного трансплантата и коллагенового матрикса.
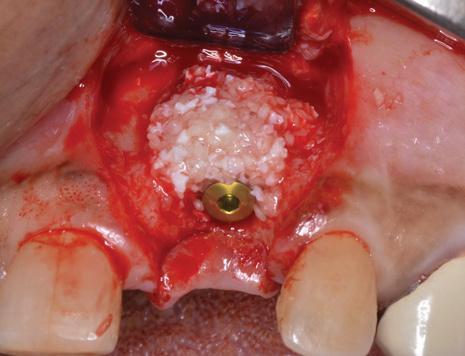
Фото 9. Аугментация в области имплантации посредством костного трансплантата и коллагенового матрикса.
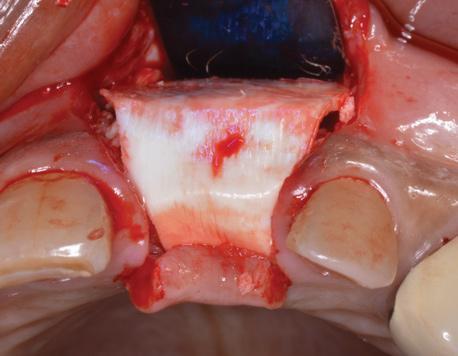
Фото 10. Вид после ушивания.
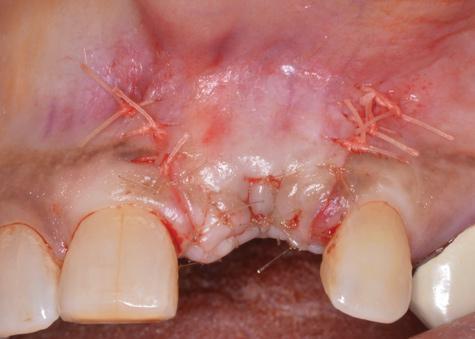
После эксплантации имплантата с диаметром 3,6 мм, который суживался до 2,5 мм апикально, был установлен конусный имплантат диаметром 4,2 мм с апикальным диаметром 2,5 мм (Astra Tech, Dentsply Sirona). В данном случае удалось добиться адекватной непосредственной стабильности интраоссальной конструкции. С вестибулярной стороны имплантата дополнительно был установлен аугментат, поскольку кость в данной области резорбировалась в результате развития перелома первичной конструкции.
Неправильно спозиционированные имплантаты
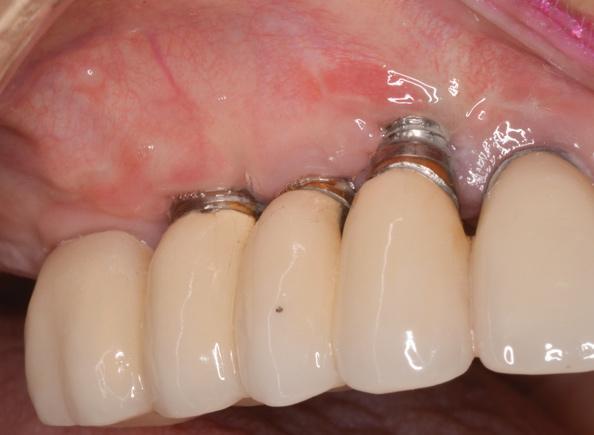
При неадекватном позиционировании имплантата ремоделирование окружающих его твердых и мягких тканей иногда приводит к обнажению абатмента и резьбы, таким образом, компрометируя эстетический результат лечения (фото 11 и 12).
Фото 11. Имплантаты были установлены слишком вестибулярно, что привело к потере костной ткани и рецессии мягких тканей.
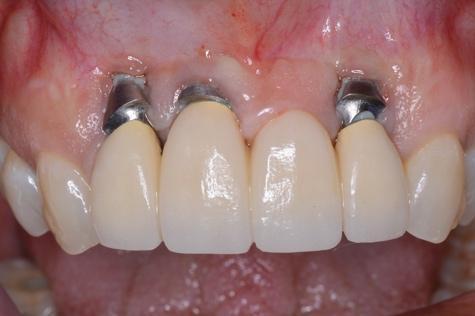
Фото 12. Имплантаты были установлены слишком вестибулярно, что привело к потере костной ткани и рецессии мягких тканей.
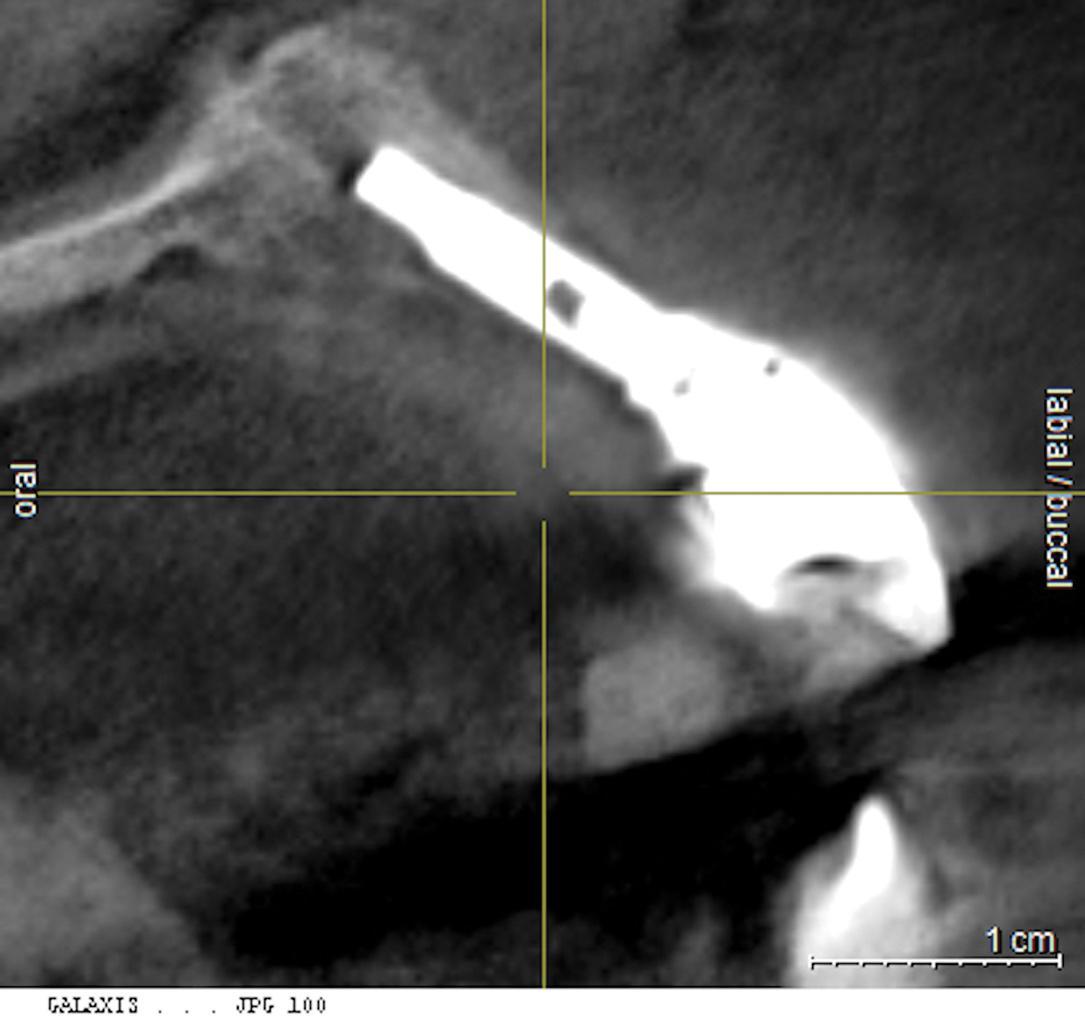
В таких случаях иногда лучше всего дефектный имплантат сначала удалить, потом провести аугментацию, и только после этого повторно установить опоры в необходимом трехмерном положении. При таком подходе количество удаленной при эксплантации костной ткани должно быть минимальным. Для подобных целей лучше всего применять инструменты с обратным торком. Kuhn и коллеги, удалявшие в своем исследовании ортодонтические имплантаты, установили, что уровень осложнений при эксплантации инструментами с обратным торком является минимальным, и точно более низким, нежели при использовании с этой же целью трепана. Для удаления имплантата уровень обратного торка может достигать значений в 200 Нсм, чтобы противостоять сформированному контакту между титановой поверхностью и костью челюстей (фото 13 и 14).
Фото 13. Удаление имплантатов посредством инструментов с обратным торком.
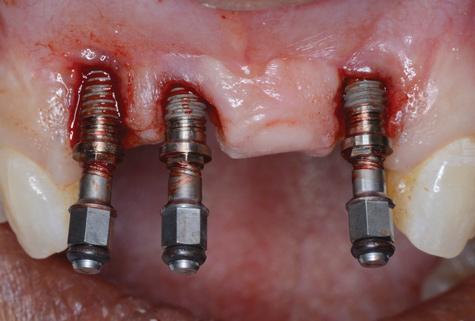
Фото 14. Вид удаленных имплантатов.

Важно отметить, что прочность остеоинтеграции может быть более высокой, чем возможности используемого инструмента с обратным торком, в таких случаях часто развивается вторичный перелом имплантата или же перелом самого инструмента. В таких случаях для завершения эксплантации применяют трепан. Данный инструмент часто входит в состав наборов для удаления широких, длинных или пустотелых конструкций имплантатов. В первую очередь они предназначены для отделения кортикальной кости на вершине гребня в периимплантатном участке для уменьшения силы, необходимой для реверсивного торка в ходе дальнейшего удаления имплантата. Дизайны трепанов, используемых в качестве дополнительных инструментов при реверсивной эксплантации, являются очень тонкими и не подходят для удаления кости по всей длине внутрикостной опоры. Попытки люксации имплантата, пока он находиться внутри трепана, чаще всего приводят к перелому самого трепана. Для объемного удаления окружающей костной ткани применяют широкие трепаны или специальные пьезоинструменты. При адекватном использовании реверсивного торка удается максимально сохранить объем окружающей периимплантатной костной ткани.
Противопоказания для удаления имплантата
Важно отметить, что не все имплантаты с компрометированным эстетическим профилем требуют эксплантации, особенно если таковые являются опорным для мульти-юнитных реставраций. Пример подобного случая представлен ниже. Имплантаты были установлены приблизительно 20 лет назад, и только сейчас у пациента на верхней челюсти начали проявляться признаки рецессии (фото 15). С правой стороны отмечался дефицит кератинизированной/прикрепленной слизистой и костной ткани в вестибулярном направлении. Однако зарегистрированная потеря кости не была патологической, а скорее являлась результатом физиологического ремоделирования (фото 16).
Фото 15. В результате физиологического ремоделирования отмечалась потеря костной ткани и развитие рецессий.
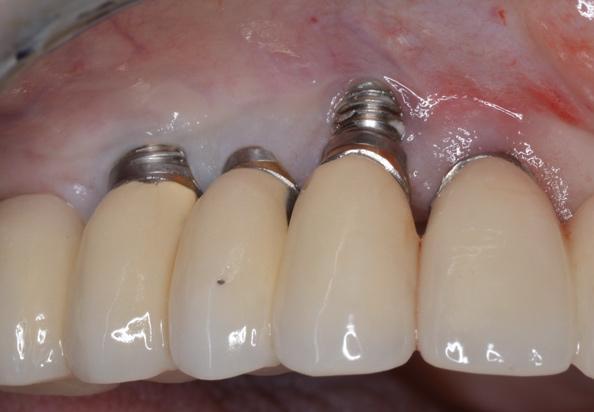
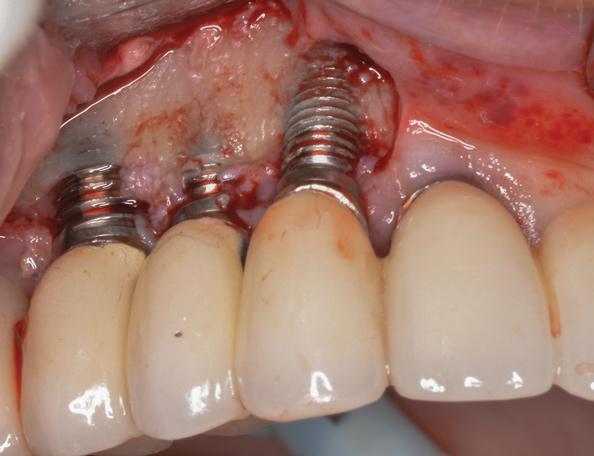
Фото 16. Визуализация уровня потери костной ткани после сепарации лоскута.
Аугментация костной ткани проводилась одновременно с установкой имплантатов. Очевидно, имеющаяся потеря уровня мягких тканей была ассоциирована с формированием соответствующей биологической ширины и наличием у пациента тонкого биотипа слизистой. Последние исследования Linkevicius и коллег доказали, что наличие достаточного исходного объема мягких тканей является важным критерием для прогнозирования успешности имплантации в будущем. В данном клиническим случае удаление имплантата потянуло бы за собой и необходимость удаления достаточно большой протетической конструкции, поэтому вместо эксплантация была проведена процедура коррекции слизистно-десневого профиля. После обработки поверхности имплантата глицином и стерильным физиологическим раствором, со щечной стороны всех трех проблемных имплантатов была зафиксирована коллагеново-костная матрица (OSSIX VOLUMAX; Datum Dental Ltd.) (фото 17). После забора субэпителиального соединительнотканного трансплантата из области твердого неба перекрыли участки костного аугментата, а также обнаженные области имплантатов и абатментов (фото 18). В конце вмешательства провели корональное смещение лоскута, который фиксировали уже в новом положении. Через 1 месяц после вмешательства можно отметить не полное, однако значительное восстановление уровня мягкотканого покрытия вокруг проблемных внутрикостных опор (фото 19).
Фото 17. Покрытие пораженных зубов трансплантатом и мембраной.
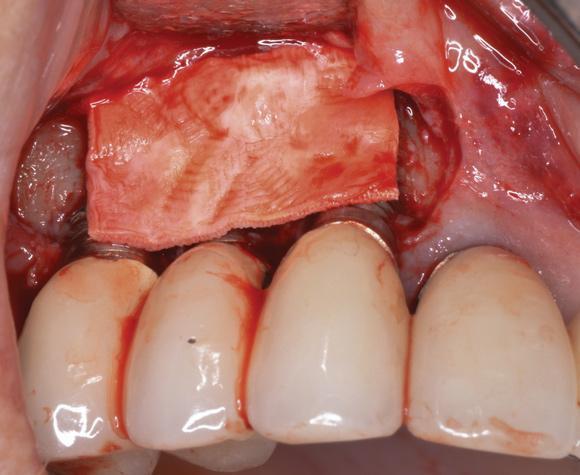
Фото 18. Установка субэпителиального соединительнотканного лоскута, собранного из области неба.
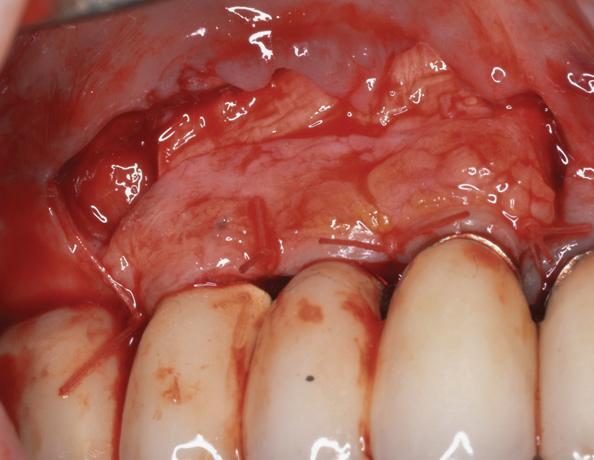
Фото 19. Через 1 месяц.
Учитывая круговую потерю костной ткани вокруг имплантатов, было практически невозможно достичь полного восстановления эстетического профиля в области титановых конструкций. Однако врачу удалось приостановить прогрессирование рецессии и добиться регенерации определённого объема костной ткани с вестибулярной стороны, а также увеличить зону кератинизированной слизистой.
Обсуждение
В начале внедрения имплантатов в стоматологическую практику приблизительно 30 лет назад, достижение остеоинтеграции считалось конечной точкой лечения. То есть оценка успешности лечения зависела от достижения определенных «костных» критериев. Пациент в таких условиях считался идеальным кандидатом на имплантацию при наличие достаточного объема костной ткани. Учитывая дефицит знаний о перспективной адаптации мягких и твердых тканей к установленному имплантату, становиться понятным, почему такое большое количество титановых опор было неправильно спозиционировано. В наше время клинические случаи со сложными пациентами решаются за счет индивидуализированных абатментов, цементируемых реставраций и розовой керамики. Кроме того, сейчас врачам более понятен процесс ремоделирования окружающих кости и десен на протяжении всего периода функционирования интраоссальной конструкции. Для замещения широких лунок зубов сразу же после их удаления было предложено использовать имплантаты широкого диаметра. Последние сразу, конечно, не увенчались заметным успехом, однако стало понятно, что даже при наличии зазора между стенкой лунки и поверхностью имплантата впоследствии заполняется костной тканью. В настоящее время подобные зазоры легко заполняются посредством аугментата, и подобные регенераторные методы вмешательств позволяют улучшить этетический исход реабилитации. Сегодня имплантация стала протетически-ориентированным видом лечения. То есть врач уже работает, планируя вмешательство «сверху-вниз», применяя на этапах диагностики новые технологии и форматы файлов от DICOM до STL. С подобными диагностическими возможностями врачу просто определить, какой пациент нуждается в аугментации в ходе имплантации, а какой нет. Кроме того, сейчас у врачей на вооружении имеется разное программное обеспечение, позволяющее им обсуждать с пациентами индивидуальные особенности лечения, балансируя уровень их ожиданий с прогнозированными результатами. Таким же актуальным является применение подобного программного обеспечения при удалении имплантатов и аргументации для пациента необходимости реализации подобной процедуры. Ведь, по сути, эксплантация – это не приговор, а еще один шанс для достижения успешных результатов реабилитации.
Выводы
В ходе реализации любого алгоритма лечения диагностика и планирование вмешательства являются ключевыми факторами для прогнозирования успешного исхода реабилитации. Даже если суть таковой состоит в удалении имплантата. При эксплантации врач должен четко понимать окончательный результат лечения, и каковы последующие цели стоят перед ним. Ведь пациенту после удаления имплантатов нужно обеспечить еще и адекватные условия социализации на период установки новых титановых опор и реставраций, на них опирающихся. Пациент должен быть ознакомлен со всеми рисками, ценой и возможностями лечения, чтобы ни в коем случае не завышать своих ожиданий. Доступность новых инструментальных методов удаления имплантатов способствует минимизации уровня инвазивности данной манипуляции и сокращению периода времени, требующегося на достижения полной реабилитации стоматологического пациента.
Автор: Barry P. Levin, DMD
При переломе дентальных имплантатов требуется дальнейшее их удаление из структуры кости челюстей.

Фото 1. Перелом платформы имплантата. Из-за воспаления произошля потеря уровня костной ткани. В апикальной части отмечаются грануляции.

Фото 2. Пример перелома имплантата. Конструкция требует удаления, а область имплантации – аугментации для последующей процедуры имплантации.

Даже после очистки периимплантатной области в таких случаях, а также после приема антибиотиков системного действия, у пациента продолжает отмечаться потеря костной ткани, отек и дискомфорт в периимплантатной области. Удаление имплантатов с переломом корональной части области соединения является довольной сложной задачей при использовании лишь инструментов с возможностью развития обратного торка. Иногда подобный подход также может спровоцировать дальнейшее развитие перелома, что только усложняет возможность удаления дефектной конструкции. Обычно подобные конструкции удаляют при помощи пустотелого трепана. При этом диаметр трепана должен быть больше диаметра имплантата, чтобы режущий инструмент мог пройти параллельно поверхности титановой опоры при этом ее не задев. Если при сегментации имплантат разделился в самой широкой своей части, что, к сожалению, приводит к значительному распространению титанового дебриса, можно использовать более узкий трепан, чтобы сохранить дополнительную кость. После того, как тело имплантата больше не контактируют с окружающей костью, маленьким корневым элеватором проникают по окружности, чтобы разрушить апикальную часть конструкции в подлежащей кости.
Процедура удаления имплантата является довольно-таки деликатной, если речь идет об удалении апикальной части конструкции, при близком положении имплантата к соседним зубам, полости синуса или каналу нижнечелюстного нерва. Планирование подобной процедуры осуществляется с обязательным применением конусно-лучевой компьютерной томографии (КЛКТ), которая позволяет оценить состояние костной ткани во всех проекциях. На фото 3 изображен один имплантат, который был удален посредством обратного торка, и второй, который удаляли с применением трепана. Поскольку при выполнении остеотомии трепаном, сформировавшейся дефект костной ткани является больше размера первоначально установленного имплантата, таковые участки довольно сложно заимплантировать повторно, особенно если речь идет и немедленной имплантации. В отдельных случаях для компенсации подобного исхода применяют имплантаты более широкого диаметра. При этом необходимо помнить об обеспечении расстояния в 1,5-2 мм между двумя смежными имплантатом и зубом, и в 3 мм между двумя смежными имплантатами. На фото 3 изображен перелом имплантата, который сформировался смежно с переломом 13 зуба. После удаления дефектной конструкции и зуба на их место были установлены два новые имплантата (Astra Tech, Dentsply Sirona), для стабилизации которых использовали как имеющуюся, так и дополнительный объемы костной ткани (фото 5).
Фото 3. Два имплантата удалены двумя разными техниками. Узкий имплантат был удален инструментом с обратным торком, а широкий – посредством трепана.

Фото 4. Вид имплантата, который удалялся посредством трепана. После удаления на место дефектной конструкции был установлен имплантат с более широким диаметром. Вместе с имплантацией была проведена процедура аугментации.

Фото 5. Вид имплантата, который удалялся посредством трепана. После удаления на место дефектной конструкции был установлен имплантат с более широким диаметром. Вместе с имплантацией была проведена процедура аугментации.

При невозможности проведения одномоментной имплантации, область удаления титановой опоры следует восстановить посредством костного аугментата, дождаться необходимого уровня организации кости на протяжении 4-6 месяцев, и только после этого приступить к повторной имплантации. В одиночных случаях в область удаления имплантата можно установить другой, более широкий, не нарушив при этом ни эстетических, ни функциональных критериев реабилитации (фото 6 - 10).
Фото 6. Вид после удаления 3,6 мм имплантата посредством 4,0 мм трепана.

Фото 7. После удаления был установлен имплантат более широкого диаметра – 4,2 мм. Вместе с имплантацией была проведена процедура аугментации.

Фото 8. Аугментация в области имплантации посредством костного трансплантата и коллагенового матрикса.

Фото 9. Аугментация в области имплантации посредством костного трансплантата и коллагенового матрикса.

Фото 10. Вид после ушивания.

После эксплантации имплантата с диаметром 3,6 мм, который суживался до 2,5 мм апикально, был установлен конусный имплантат диаметром 4,2 мм с апикальным диаметром 2,5 мм (Astra Tech, Dentsply Sirona). В данном случае удалось добиться адекватной непосредственной стабильности интраоссальной конструкции. С вестибулярной стороны имплантата дополнительно был установлен аугментат, поскольку кость в данной области резорбировалась в результате развития перелома первичной конструкции.
Неправильно спозиционированные имплантаты
При неадекватном позиционировании имплантата ремоделирование окружающих его твердых и мягких тканей иногда приводит к обнажению абатмента и резьбы, таким образом, компрометируя эстетический результат лечения (фото 11 и 12).
Фото 11. Имплантаты были установлены слишком вестибулярно, что привело к потере костной ткани и рецессии мягких тканей.

Фото 12. Имплантаты были установлены слишком вестибулярно, что привело к потере костной ткани и рецессии мягких тканей.

В таких случаях иногда лучше всего дефектный имплантат сначала удалить, потом провести аугментацию, и только после этого повторно установить опоры в необходимом трехмерном положении. При таком подходе количество удаленной при эксплантации костной ткани должно быть минимальным. Для подобных целей лучше всего применять инструменты с обратным торком. Kuhn и коллеги, удалявшие в своем исследовании ортодонтические имплантаты, установили, что уровень осложнений при эксплантации инструментами с обратным торком является минимальным, и точно более низким, нежели при использовании с этой же целью трепана. Для удаления имплантата уровень обратного торка может достигать значений в 200 Нсм, чтобы противостоять сформированному контакту между титановой поверхностью и костью челюстей (фото 13 и 14).
Фото 13. Удаление имплантатов посредством инструментов с обратным торком.

Фото 14. Вид удаленных имплантатов.

Важно отметить, что прочность остеоинтеграции может быть более высокой, чем возможности используемого инструмента с обратным торком, в таких случаях часто развивается вторичный перелом имплантата или же перелом самого инструмента. В таких случаях для завершения эксплантации применяют трепан. Данный инструмент часто входит в состав наборов для удаления широких, длинных или пустотелых конструкций имплантатов. В первую очередь они предназначены для отделения кортикальной кости на вершине гребня в периимплантатном участке для уменьшения силы, необходимой для реверсивного торка в ходе дальнейшего удаления имплантата. Дизайны трепанов, используемых в качестве дополнительных инструментов при реверсивной эксплантации, являются очень тонкими и не подходят для удаления кости по всей длине внутрикостной опоры. Попытки люксации имплантата, пока он находиться внутри трепана, чаще всего приводят к перелому самого трепана. Для объемного удаления окружающей костной ткани применяют широкие трепаны или специальные пьезоинструменты. При адекватном использовании реверсивного торка удается максимально сохранить объем окружающей периимплантатной костной ткани.
Противопоказания для удаления имплантата
Важно отметить, что не все имплантаты с компрометированным эстетическим профилем требуют эксплантации, особенно если таковые являются опорным для мульти-юнитных реставраций. Пример подобного случая представлен ниже. Имплантаты были установлены приблизительно 20 лет назад, и только сейчас у пациента на верхней челюсти начали проявляться признаки рецессии (фото 15). С правой стороны отмечался дефицит кератинизированной/прикрепленной слизистой и костной ткани в вестибулярном направлении. Однако зарегистрированная потеря кости не была патологической, а скорее являлась результатом физиологического ремоделирования (фото 16).
Фото 15. В результате физиологического ремоделирования отмечалась потеря костной ткани и развитие рецессий.

Фото 16. Визуализация уровня потери костной ткани после сепарации лоскута.

Аугментация костной ткани проводилась одновременно с установкой имплантатов. Очевидно, имеющаяся потеря уровня мягких тканей была ассоциирована с формированием соответствующей биологической ширины и наличием у пациента тонкого биотипа слизистой. Последние исследования Linkevicius и коллег доказали, что наличие достаточного исходного объема мягких тканей является важным критерием для прогнозирования успешности имплантации в будущем. В данном клиническим случае удаление имплантата потянуло бы за собой и необходимость удаления достаточно большой протетической конструкции, поэтому вместо эксплантация была проведена процедура коррекции слизистно-десневого профиля. После обработки поверхности имплантата глицином и стерильным физиологическим раствором, со щечной стороны всех трех проблемных имплантатов была зафиксирована коллагеново-костная матрица (OSSIX VOLUMAX; Datum Dental Ltd.) (фото 17). После забора субэпителиального соединительнотканного трансплантата из области твердого неба перекрыли участки костного аугментата, а также обнаженные области имплантатов и абатментов (фото 18). В конце вмешательства провели корональное смещение лоскута, который фиксировали уже в новом положении. Через 1 месяц после вмешательства можно отметить не полное, однако значительное восстановление уровня мягкотканого покрытия вокруг проблемных внутрикостных опор (фото 19).
Фото 17. Покрытие пораженных зубов трансплантатом и мембраной.

Фото 18. Установка субэпителиального соединительнотканного лоскута, собранного из области неба.

Фото 19. Через 1 месяц.

Учитывая круговую потерю костной ткани вокруг имплантатов, было практически невозможно достичь полного восстановления эстетического профиля в области титановых конструкций. Однако врачу удалось приостановить прогрессирование рецессии и добиться регенерации определённого объема костной ткани с вестибулярной стороны, а также увеличить зону кератинизированной слизистой.
Обсуждение
В начале внедрения имплантатов в стоматологическую практику приблизительно 30 лет назад, достижение остеоинтеграции считалось конечной точкой лечения. То есть оценка успешности лечения зависела от достижения определенных «костных» критериев. Пациент в таких условиях считался идеальным кандидатом на имплантацию при наличие достаточного объема костной ткани. Учитывая дефицит знаний о перспективной адаптации мягких и твердых тканей к установленному имплантату, становиться понятным, почему такое большое количество титановых опор было неправильно спозиционировано. В наше время клинические случаи со сложными пациентами решаются за счет индивидуализированных абатментов, цементируемых реставраций и розовой керамики. Кроме того, сейчас врачам более понятен процесс ремоделирования окружающих кости и десен на протяжении всего периода функционирования интраоссальной конструкции. Для замещения широких лунок зубов сразу же после их удаления было предложено использовать имплантаты широкого диаметра. Последние сразу, конечно, не увенчались заметным успехом, однако стало понятно, что даже при наличии зазора между стенкой лунки и поверхностью имплантата впоследствии заполняется костной тканью. В настоящее время подобные зазоры легко заполняются посредством аугментата, и подобные регенераторные методы вмешательств позволяют улучшить этетический исход реабилитации. Сегодня имплантация стала протетически-ориентированным видом лечения. То есть врач уже работает, планируя вмешательство «сверху-вниз», применяя на этапах диагностики новые технологии и форматы файлов от DICOM до STL. С подобными диагностическими возможностями врачу просто определить, какой пациент нуждается в аугментации в ходе имплантации, а какой нет. Кроме того, сейчас у врачей на вооружении имеется разное программное обеспечение, позволяющее им обсуждать с пациентами индивидуальные особенности лечения, балансируя уровень их ожиданий с прогнозированными результатами. Таким же актуальным является применение подобного программного обеспечения при удалении имплантатов и аргументации для пациента необходимости реализации подобной процедуры. Ведь, по сути, эксплантация – это не приговор, а еще один шанс для достижения успешных результатов реабилитации.
Выводы
В ходе реализации любого алгоритма лечения диагностика и планирование вмешательства являются ключевыми факторами для прогнозирования успешного исхода реабилитации. Даже если суть таковой состоит в удалении имплантата. При эксплантации врач должен четко понимать окончательный результат лечения, и каковы последующие цели стоят перед ним. Ведь пациенту после удаления имплантатов нужно обеспечить еще и адекватные условия социализации на период установки новых титановых опор и реставраций, на них опирающихся. Пациент должен быть ознакомлен со всеми рисками, ценой и возможностями лечения, чтобы ни в коем случае не завышать своих ожиданий. Доступность новых инструментальных методов удаления имплантатов способствует минимизации уровня инвазивности данной манипуляции и сокращению периода времени, требующегося на достижения полной реабилитации стоматологического пациента.
Автор: Barry P. Levin, DMD






























































































































































0 комментариев