В имплантологии уже более чем на протяжении 40 лет используются интраоссальные опоры, выполненные из сплава титана, но актуальный тренд применения неметаллических материалов и повышенная чувствительность отдельных пациентов к титану обосновывают необходимость разработки новых образцов имплантатов для повседневной стоматологической практики. Примером тому являются внутрикостные опоры из диоксида циркония, биосовместимость и специфические механические свойства которых делают их пригодными для использования во многих клинических ситуациях. Основное преимущество оксида циркония состоит в его улучшенной эластичности по сравнению с титаном и кортикальной частью альвеолярного гребня челюстей. Для профилактики переноса чрезмерной нагрузки на окружающую костную ткань был предложен также ряд материалов, адсорбирующих чрезмерное функциональное действие на границе имплантат/кость. К последним, кстати, и относится PEEK, реставрации из которого вместе с циркониевыми имплантатами позволяют добиться наиболее биосовместимого и механически выгодного результата лечения.
Клинический случай
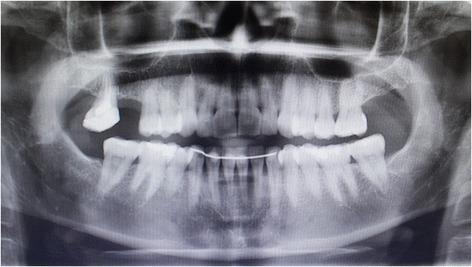
45-летняя пациентка без вредных привычек и с неотягощенным соматическим анамнезом обратилась за помощью с основной жалобой на боль в области правого второго моляра верхней челюсти. Боль усугублялась при жевании, что ограничивало возможности нормального функционирования зубочелюстного аппарата. Со слов пациентки стало известно, что 16 зуб был удален еще приблизительно 8 лет назад. В ходе клинического осмотра было обнаружено продольный перелом в небном корне 17 зуба, что было подтверждено в ходе рентгенографического исследования (фото 1). Зуб был удален в ходе этого же визита. Из-за отсутствия обоих моляров пациентка выразила желание восстановить область адентии при помощи имплантатов. Она также беспокоилась относительно наличия металлических конструкций во рту и настаивала на альтернативном методе лечения с перспективой замены утраченных зубов неметаллическими реставрациями. Через 4 месяца после заживления ей было предложено использовать в качестве опоры 2 белых имплантата SKY (Bredent) из оксида циркония (4,5 × 10 мм и 4,5 × 8 мм), а также PEEK-реставрации с композитным покрытием.
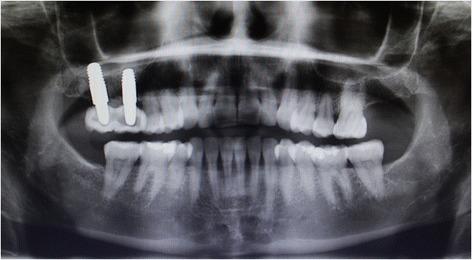
Фото 1. Ортопантомограмма пациентки до начала лечения.
Начальная оценка
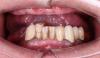
В области адентии было отмечено достаточное количество кератинизированных десен, позволяющее провести безлоскутное оперативное вмешательство с использованием кругового скальпеля. Таким образом удалось сохранить целостность периимплантатных структур и уменьшить послеоперационные болевые ощущения.
Хирургическое вмешательство
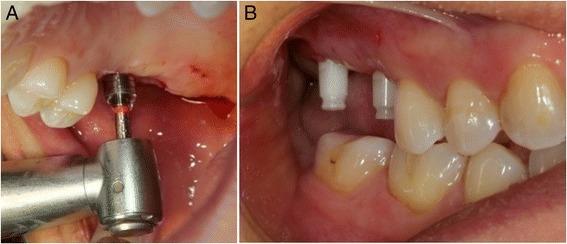
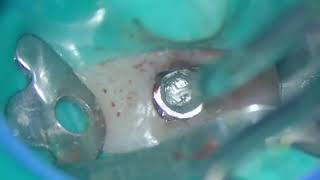
В ходе реализации безлоскутной техники вмешательства было проведено два круглых разреза с помощью кругового скальпеля, после чего фрагменты слизистой удалили посредством периотома, сохраняя целостность мягких тканей вокруг операционной области. Остеотомию проводили согласно протоколу производителя для дальнейшей установки двух белых SKY (Bredent) имплантатов из оксида циркония диаметром 10 мм × 4,5 мм в области 17 и 16 зубов (диаметр 8 мм × 4 мм) (фото 2).
Фото 2. Процедура безлоскутного вмешательства с использованием круглого скальпеля (a); чистый бескровный вид операционного поля (b).
Период заживления
Через 15 дней после операции внешний вид мягких тканей не демонстрировал никаких нарушений или признаков воспаления. Пациентка отметила отсутствие кровотечения и боли в ходе заживления области вмешательства. Параллельно провели клиническую и рентгенологическую оценку. Через три месяца после операции имплантаты были обнажены для проверки параллельности опор, после чего приступили к получению оттисков полиэфирным материалом (Impregum, 3M ESPE) для изготовления окончательных реставраций без использования ретракционных нитей. Окончательные конструкции были получены посредством применения системы CAD/CAM Juvora для PEEK-коронки с композитным покрытием (Anaxdent). Для фиксации использовали стеклоиономерный цемент, модифицированный композитом (GC FujiCEM, GC Europe N.V.) (фото 3 - 4).
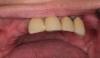
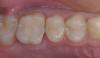
Фото 3. Вид окончательных реставраций. Достижение параллельности опорных элементов: окклюзионный и лингвальный вид.
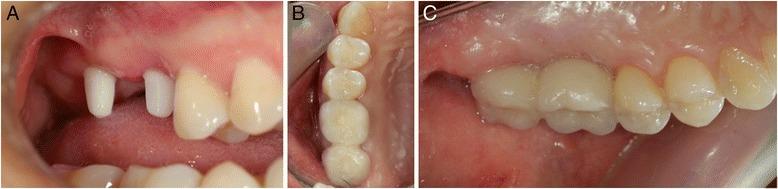
Фото 4. Ортопантомограма через 1 год после имплантации: визуализация осстеоинтеграции имплантатов.
Контроль пациента
Клинический и рентгенографический контроль, проведенный через 1 год после имплантации, продемонстрировал успешность интраоссальных конструкций, согласно критериям Albrektsson и с учетом состояния мягких тканей вокруг имплантатов (фото 5).
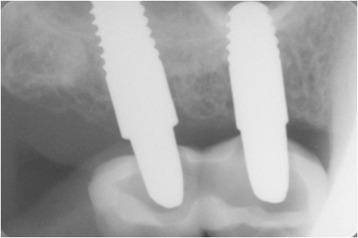
Фото 5. Периапикальная рентгенограмма через 1 год после имплантации: отмечается стабильность периимплантатных тканей.
Обсуждение
Факторы полости рта (рН слюны, кислотные напитки, бактериальные бляшки и т. д.) могут активно взаимодействовать с металлическими конструкциями, вызывая их коррозию. Данный феномен характерен и для титановых дентальных имплантатов. Поэтому так возрастает интерес к циркониевым интраоссальным элементам, которые могут служить отличной альтернативой классическим титановым имплантатам. Циркониевые имплантаты характеризируются успешными показателями осстеоинтеграции и взаимодействия с мягкими тканями полости рта. С другой стороны, у данных имплантатов отсутствует зазор между шейкой и телом, поскольку они изготовляются в форме одиночного блока (Bredent, Straumman). Вместе с тем, для достижения необходимой параллельности такие имплантаты часто приходиться модифицировать с использованием роторных инструментов. Несколько исследований показали, что имплантаты из оксида циркония характеризируются аналогичной схемой заживления и адаптацией краевой кости, что и их титановые аналоги. Тем не менее, дискуссия относительно долгосрочной стабильности интерфейса имплантат/кость, который зависит от действия таких факторов как поверхность, состав и дизайн имплантата, активно продолжается. Другими важными факторами, которые следует учитывать при планировании имплантации, являются особенности соединения между абатментом и коронкой, а также сам состав реставрационного материала и специфика передачи окклюзионной нагрузки через протетический супраэлемент. Частота использования PEEK-реставраций в качестве протезных структур с опорой на имплантатах значительно увеличилась. PEEK являет собой термопластичный полимер высокой плотности с линейной ароматической полукристаллической структурой, который обладает исключительными физическими и химическими свойствами в отношении прочности, твердости и эластичности. Кроме того, его низкая молекулярная масса в сочетании с отсутствием каких-либо металлических составляющих позволяет использовать его в качестве превосходного биосовместимого материала для разных типов супраконструкций. PEEK характеризируется модулем упругости (E-модуль 4 ГПa), значительно превышающим аналогичный показатель обычных материалов по типу титана (Е-модуль 110 ГПа) или диоксида циркония (Е-модуль 210 ГПа). Кроме того, сопротивление на изгиб среди металлокерамических реставраций составляет около 400-600 МПа, в то время как новые композитные покрытия, которые имеют твердость по Виккерсу приблизительно 400 Мпа, характеризуются сопротивлением на изгиб в 314 МПа. Диоксид циркония, с другой стороны, является в три раза тверже (1200 HВ), а показатели его сопротивления на изгиб достигают 1400 МПа.
В целом все эти показатели свидетельствуют о том, что использование материалов с высокой жесткостью приводит к прямой передаче жевательных нагрузок на структуру имплантата из диоксида циркония. Подобная потенциальная перегрузка может вызвать эффект резорбции костной ткани вокруг интраоссальной опоры. Некоторые авторы утверждают, что подобный эффект может наблюдаться только при наличие предшествующего воспалительного процесса (инфекционного происхождения), который ускоряет прогресс редукции костной ткани.
Чтобы избежать превышения адаптивных возможностей альвеолярной кости и для обеспечения поддержки надлежащего уровня механического напряжения, было предложено использовать в качестве супраструктур PEEK-реставрации, модуль упругости которых приближается к аналогичному показателю кортикальной костной ткани. Таким образом, врачу удается способствовать ремоделированию периимплантатной области без провоцирования ее перегрузки. PEEK обеспечивает первичную концентрацию нагрузок на себе, после чего проводит равномерное их распределение. Подобная способность материала побудила некоторых авторов рекомендовать его для применения у пациентов с тяжелой формой бруксизма. Анализ результатов использования метода конечных элементов показывает, что максимальное контактное давление на границе титанового имплантата с костью можно значительно уменьшить за счет использования коронок из PEEK материала вместо керамических супраконструкций. В дополнение к PEEK были разработаны новые материалы для покрытия из PMMA или композитов (Anaxblent Anaxdent, Nexco Ivoclar, Solidex Shofu, Novo.lign Bredent и др.), которые содержат керамические наполнители. Благодаря своей молекулярной структуре, эти материалы обладают отличной плотностью и гомогенностью. Микронаполнитель, помещенный в полимерную матрицу, повышает стойкость материала к истиранию, и в то же время обеспечивает оптимальную эластичность конструкции, которая максимально соответствует естественной структуре зуба. Однако, хоть данные реставрации и демонстрируют хорошую цветостойкость и долговременный блеск, стабильность параметров текстуры и яркости, они существенно отличаются от керамических покрытий, которые остаются золотым стандартом эстетических реставраций.
Выводы
Использование циркониевых имплантатов и PEEK-реставраций является хорошей альтернативой для восстановления участков адентии челюстей. Их биосовместимость и биостабильность аргументируют перспективу использования данных образцов у пациентов с аллергией или повышеной чувствительностью к металлическим сплавам. Использование реставрации из PEEK является реальной альтернативой для адекватного распределения жевательных нагрузок в области циркониевых интраоссальных опор, что, в свою очередь, способствует сохранению осстеоинтеграции на протяжении более длительного периода времени. В рамках данного исследования мы рекомендуем комбинированное использование имплантатов из оксида циркония и реставраций из PEEK-материала с PMMA покрытием у пациентов с непереносимостью к металлическим сплавам.
Авторы: Jose Maria Parmigiani-Izquierdo, Maria Eugenia Cabana-Munoz, Jose Joaquin Merino, Arturo Sanchez-Perez
В имплантологии уже более чем на протяжении 40 лет используются интраоссальные опоры, выполненные из сплава титана, но актуальный тренд применения неметаллических материалов и повышенная чувствительность отдельных пациентов к титану обосновывают необходимость разработки новых образцов имплантатов для повседневной стоматологической практики. Примером тому являются внутрикостные опоры из диоксида циркония, биосовместимость и специфические механические свойства которых делают их пригодными для использования во многих клинических ситуациях. Основное преимущество оксида циркония состоит в его улучшенной эластичности по сравнению с титаном и кортикальной частью альвеолярного гребня челюстей. Для профилактики переноса чрезмерной нагрузки на окружающую костную ткань был предложен также ряд материалов, адсорбирующих чрезмерное функциональное действие на границе имплантат/кость. К последним, кстати, и относится PEEK, реставрации из которого вместе с циркониевыми имплантатами позволяют добиться наиболее биосовместимого и механически выгодного результата лечения.

Клинический случай
45-летняя пациентка без вредных привычек и с неотягощенным соматическим анамнезом обратилась за помощью с основной жалобой на боль в области правого второго моляра верхней челюсти. Боль усугублялась при жевании, что ограничивало возможности нормального функционирования зубочелюстного аппарата. Со слов пациентки стало известно, что 16 зуб был удален еще приблизительно 8 лет назад. В ходе клинического осмотра было обнаружено продольный перелом в небном корне 17 зуба, что было подтверждено в ходе рентгенографического исследования (фото 1). Зуб был удален в ходе этого же визита. Из-за отсутствия обоих моляров пациентка выразила желание восстановить область адентии при помощи имплантатов. Она также беспокоилась относительно наличия металлических конструкций во рту и настаивала на альтернативном методе лечения с перспективой замены утраченных зубов неметаллическими реставрациями. Через 4 месяца после заживления ей было предложено использовать в качестве опоры 2 белых имплантата SKY (Bredent) из оксида циркония (4,5 × 10 мм и 4,5 × 8 мм), а также PEEK-реставрации с композитным покрытием.
Фото 1. Ортопантомограмма пациентки до начала лечения.

Начальная оценка
В области адентии было отмечено достаточное количество кератинизированных десен, позволяющее провести безлоскутное оперативное вмешательство с использованием кругового скальпеля. Таким образом удалось сохранить целостность периимплантатных структур и уменьшить послеоперационные болевые ощущения.
Хирургическое вмешательство
В ходе реализации безлоскутной техники вмешательства было проведено два круглых разреза с помощью кругового скальпеля, после чего фрагменты слизистой удалили посредством периотома, сохраняя целостность мягких тканей вокруг операционной области. Остеотомию проводили согласно протоколу производителя для дальнейшей установки двух белых SKY (Bredent) имплантатов из оксида циркония диаметром 10 мм × 4,5 мм в области 17 и 16 зубов (диаметр 8 мм × 4 мм) (фото 2).
Фото 2. Процедура безлоскутного вмешательства с использованием круглого скальпеля (a); чистый бескровный вид операционного поля (b).

Период заживления
Через 15 дней после операции внешний вид мягких тканей не демонстрировал никаких нарушений или признаков воспаления. Пациентка отметила отсутствие кровотечения и боли в ходе заживления области вмешательства. Параллельно провели клиническую и рентгенологическую оценку. Через три месяца после операции имплантаты были обнажены для проверки параллельности опор, после чего приступили к получению оттисков полиэфирным материалом (Impregum, 3M ESPE) для изготовления окончательных реставраций без использования ретракционных нитей. Окончательные конструкции были получены посредством применения системы CAD/CAM Juvora для PEEK-коронки с композитным покрытием (Anaxdent). Для фиксации использовали стеклоиономерный цемент, модифицированный композитом (GC FujiCEM, GC Europe N.V.) (фото 3 - 4).
Фото 3. Вид окончательных реставраций. Достижение параллельности опорных элементов: окклюзионный и лингвальный вид.

Фото 4. Ортопантомограма через 1 год после имплантации: визуализация осстеоинтеграции имплантатов.

Контроль пациента
Клинический и рентгенографический контроль, проведенный через 1 год после имплантации, продемонстрировал успешность интраоссальных конструкций, согласно критериям Albrektsson и с учетом состояния мягких тканей вокруг имплантатов (фото 5).
Фото 5. Периапикальная рентгенограмма через 1 год после имплантации: отмечается стабильность периимплантатных тканей.

Обсуждение
Факторы полости рта (рН слюны, кислотные напитки, бактериальные бляшки и т. д.) могут активно взаимодействовать с металлическими конструкциями, вызывая их коррозию. Данный феномен характерен и для титановых дентальных имплантатов. Поэтому так возрастает интерес к циркониевым интраоссальным элементам, которые могут служить отличной альтернативой классическим титановым имплантатам. Циркониевые имплантаты характеризируются успешными показателями осстеоинтеграции и взаимодействия с мягкими тканями полости рта. С другой стороны, у данных имплантатов отсутствует зазор между шейкой и телом, поскольку они изготовляются в форме одиночного блока (Bredent, Straumman). Вместе с тем, для достижения необходимой параллельности такие имплантаты часто приходиться модифицировать с использованием роторных инструментов. Несколько исследований показали, что имплантаты из оксида циркония характеризируются аналогичной схемой заживления и адаптацией краевой кости, что и их титановые аналоги. Тем не менее, дискуссия относительно долгосрочной стабильности интерфейса имплантат/кость, который зависит от действия таких факторов как поверхность, состав и дизайн имплантата, активно продолжается. Другими важными факторами, которые следует учитывать при планировании имплантации, являются особенности соединения между абатментом и коронкой, а также сам состав реставрационного материала и специфика передачи окклюзионной нагрузки через протетический супраэлемент. Частота использования PEEK-реставраций в качестве протезных структур с опорой на имплантатах значительно увеличилась. PEEK являет собой термопластичный полимер высокой плотности с линейной ароматической полукристаллической структурой, который обладает исключительными физическими и химическими свойствами в отношении прочности, твердости и эластичности. Кроме того, его низкая молекулярная масса в сочетании с отсутствием каких-либо металлических составляющих позволяет использовать его в качестве превосходного биосовместимого материала для разных типов супраконструкций. PEEK характеризируется модулем упругости (E-модуль 4 ГПa), значительно превышающим аналогичный показатель обычных материалов по типу титана (Е-модуль 110 ГПа) или диоксида циркония (Е-модуль 210 ГПа). Кроме того, сопротивление на изгиб среди металлокерамических реставраций составляет около 400-600 МПа, в то время как новые композитные покрытия, которые имеют твердость по Виккерсу приблизительно 400 Мпа, характеризуются сопротивлением на изгиб в 314 МПа. Диоксид циркония, с другой стороны, является в три раза тверже (1200 HВ), а показатели его сопротивления на изгиб достигают 1400 МПа.
В целом все эти показатели свидетельствуют о том, что использование материалов с высокой жесткостью приводит к прямой передаче жевательных нагрузок на структуру имплантата из диоксида циркония. Подобная потенциальная перегрузка может вызвать эффект резорбции костной ткани вокруг интраоссальной опоры. Некоторые авторы утверждают, что подобный эффект может наблюдаться только при наличие предшествующего воспалительного процесса (инфекционного происхождения), который ускоряет прогресс редукции костной ткани.
Чтобы избежать превышения адаптивных возможностей альвеолярной кости и для обеспечения поддержки надлежащего уровня механического напряжения, было предложено использовать в качестве супраструктур PEEK-реставрации, модуль упругости которых приближается к аналогичному показателю кортикальной костной ткани. Таким образом, врачу удается способствовать ремоделированию периимплантатной области без провоцирования ее перегрузки. PEEK обеспечивает первичную концентрацию нагрузок на себе, после чего проводит равномерное их распределение. Подобная способность материала побудила некоторых авторов рекомендовать его для применения у пациентов с тяжелой формой бруксизма. Анализ результатов использования метода конечных элементов показывает, что максимальное контактное давление на границе титанового имплантата с костью можно значительно уменьшить за счет использования коронок из PEEK материала вместо керамических супраконструкций. В дополнение к PEEK были разработаны новые материалы для покрытия из PMMA или композитов (Anaxblent Anaxdent, Nexco Ivoclar, Solidex Shofu, Novo.lign Bredent и др.), которые содержат керамические наполнители. Благодаря своей молекулярной структуре, эти материалы обладают отличной плотностью и гомогенностью. Микронаполнитель, помещенный в полимерную матрицу, повышает стойкость материала к истиранию, и в то же время обеспечивает оптимальную эластичность конструкции, которая максимально соответствует естественной структуре зуба. Однако, хоть данные реставрации и демонстрируют хорошую цветостойкость и долговременный блеск, стабильность параметров текстуры и яркости, они существенно отличаются от керамических покрытий, которые остаются золотым стандартом эстетических реставраций.
Выводы
Использование циркониевых имплантатов и PEEK-реставраций является хорошей альтернативой для восстановления участков адентии челюстей. Их биосовместимость и биостабильность аргументируют перспективу использования данных образцов у пациентов с аллергией или повышеной чувствительностью к металлическим сплавам. Использование реставрации из PEEK является реальной альтернативой для адекватного распределения жевательных нагрузок в области циркониевых интраоссальных опор, что, в свою очередь, способствует сохранению осстеоинтеграции на протяжении более длительного периода времени. В рамках данного исследования мы рекомендуем комбинированное использование имплантатов из оксида циркония и реставраций из PEEK-материала с PMMA покрытием у пациентов с непереносимостью к металлическим сплавам.
Авторы: Jose Maria Parmigiani-Izquierdo, Maria Eugenia Cabana-Munoz, Jose Joaquin Merino, Arturo Sanchez-Perez































































































































































0 комментариев