История костной аугментации материалами разного происхождения достигает почти столетней глубины. Существенные проблемы, связанные с трансплантационными материалами и усилителями роста, касаются их происхождения, обоснования использования, способа их забора с учетом объема так именуемых биологических «затрат». Еще одна ключевая проблема костных трансплантатов касается аспекта потенциальной «репарации» или регенерации области вмешательства. Репарация представляет собой процесс замены дефектного участка чем-то физически подобным по структуре, но отличающимся биологически и физиологически. Регенерация, напротив, предусматривает использование разных материалов и методов, которые позволяют восстановить биологическую структуру дефектной области полностью идентичной тканью. Хирургам, планирующим проведение аугментации, нужно четко понимать, какой результат они могут прогнозировать по окончании реабилитации, и насколько успешными окажутся применяемые ими техники. Четко понимая все аспекты, врач может достигнуть консенсуса в восстановлении витальной кости, выполненного объема аугментации, скорости заживления и оптимизации процедуры ятрогенного вмешательства.
Рекомендации относительно реконструкции костной ткани
Выбор, стоящий перед хирургом во время процедуры экстракции, выполнения аугментации или синус-лифтинга касается, главным образом, следующих аспектов:
- доступа к области дефекта. Доступ может быть сформирован без сепарации лоскута – миниинвазивно, или же классически – путем сепарации объема окружающих тканей.
- источник костного материала. Аутогенная кость, аллогенные аналоги, аллопласт, ксенотрансплантаты или другие материалы – все они подходят для реконструкции параметров резидуального гребня.
- тип используемого трансплантата. Трансплантат может быть представлен в форме частиц, пасты или блока, разного размера и зернистости, а также могут быть собраны из участков разного происхождения (кортикальной или губчатой части кости).
- специфические характеристики каждого трансплантата. Костные заменители характеризуются различными уровнями минерализации и различной тенденцией к резорбции. следует учитывать, является ли материал остеокондуктивным или остеоиндуктивным и как быстро или медленно, или если вообще подлежит ли он биодеградации.
- тип используемого биологического барьера. Используемые мембраны могут быть синтетическими или коллагеновыми: также они могут быть резорбируемыми или нерезорбируемыми, биологические активными или инертными.
Ранние исследования указывают на то, что в экстракционной лунке, даже без соответствующего использования трансплантата или мембраны, все равно наблюдается формирование витальной костной ткани. Однако полагаться лишь на такой исход не стоит. В 2008 году Fickl и соавторы исследовали различия между разными подходами к экстракции (с и без сепарации лоскута) с дальнейшим заполнением лунки аугментатом или же без выполнения процедуры реконструкции. Они обнаружили, что сепарация тканей слизистой и периоста приводит к большей потере ширины и высоты альвеолярного гребня, по сравнению с теми результатами, которые были получены после реализации миниинвазвиного подхода. Также они отметили факт сохранения первичных размеров кости при заполнении лунки неорганичным трансплантатом бычьего происхождения, чего не отмечалось без проведения процедуры аугментации. Iasella и коллеги, однако, отметили, что более витальная кость формировалась в области постэкстракционных лунок без использованного какого-либо типа графта, хотя потеря изначального объема твердых тканей при этом составляла около 30%. Аналогичных последствий удалось избежать при заполнении лунки минерализованным аллографтом, перекрытым резорбируемой коллагеновой мембраной.
В другом исследовании сравнивали два разных метода аугментации. В лунки устанавливали ксенотрансплантат, полученный из крупного рогатого скота, и перекрывали его резорбируемой мембраной – таким образом удавалось добиться незначительного приросла тканей по высоте, но объем сформированной витальной кости не превышал 26%. Когда же в качестве аналога применяли деминерализованный аллотрансплантат с сульфатом кальция, который перекрывали барьером из сульфата кальция, отмечали аналогичный результат изменения геометрических параметров костного гребня, однако количество витальной кости практически в два раза превышало то, что было отмечено при использовании аллотрансплантата.
Материала для аугментации и изоляции
Сульфат кальция
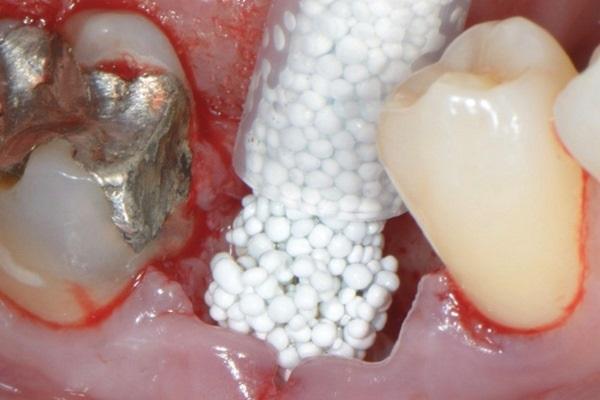
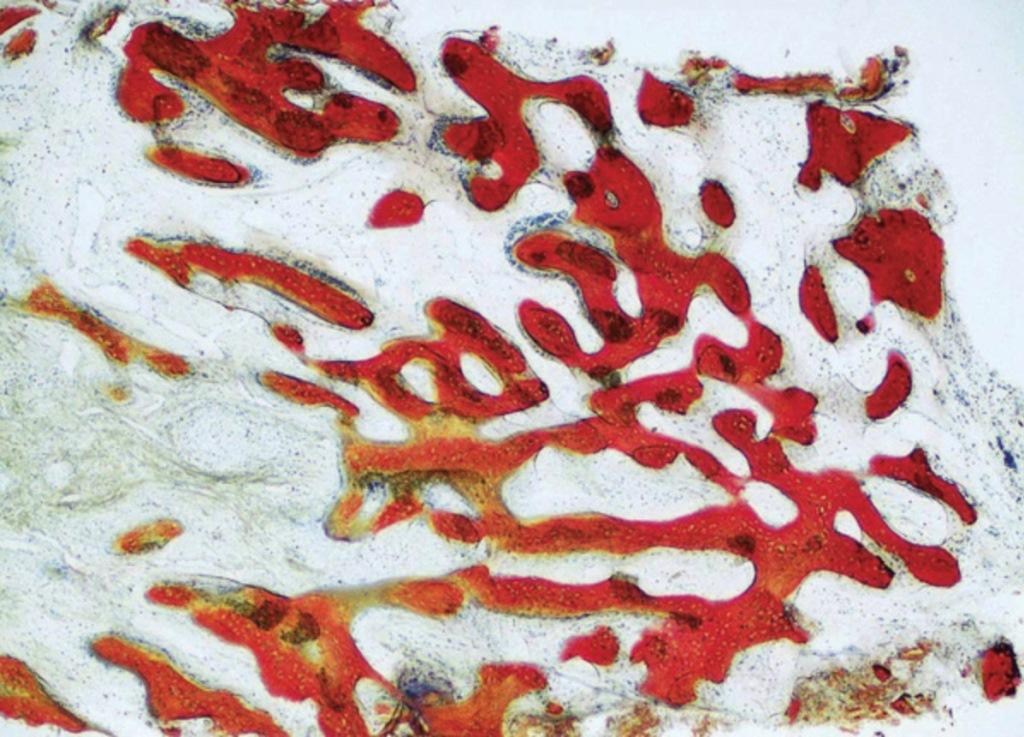
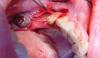
Сульфат кальция является синтетическим аналогом, который используется во многих конфигурациях в качестве как трансплантата, так и стимулятора роста (фото 1). Исследование, проведенное в 2004 году, продемонстрировало, что данный материал в полугидратной форме без мембраны позволяет отлично сохранить объем тканей, и при этом отмечается приблизительно 60% формирование витальной кости. Новый материал для трансплантации костной ткани, описанный в отчете за 2012 год, является двухфазным и содержит как геми- так и дигидрат кальция сульфата. Этот материал является самоосаждаемым в присутствии крови или слюны, и может использоваться с или без барьерной мембраны. В докладе были представлены гистологические результаты его использования при нескольких типах дефектов, которые свидетельствуют о приросте костной ткани. Кроме того, также удавалось добиться ретенции и увеличения геометрических параметром альвеолярного гребня. Пациентка, изображена на фото 1, обратилась за помощью после значительного абсцесса эндодонтической этиологии, который спровоцировал убыль как вестибулярной, так и язычной костной пластинок. Покрытие двухфазного кальциевого сульфата плотной политетрафторэтиленовой (PTFE) мембраной в течение 3 недель способствовало заживлению участка дефекта. Клинически было очевидно, что объем резиудального гребня удалось сохранить на протяжении более 5 лет, который в свою очередь поддерживал поверх лежащую кератинизированную мягкую ткань (фото 2). Самое главное, что при гистологической оценке было обнаружено 58% витальной костной без остатков гранул костного трансплантата (фото 3).
Фото 1. Процедура аугментации с использованием BPCS и покрытием ПТФЭ-мембраной.
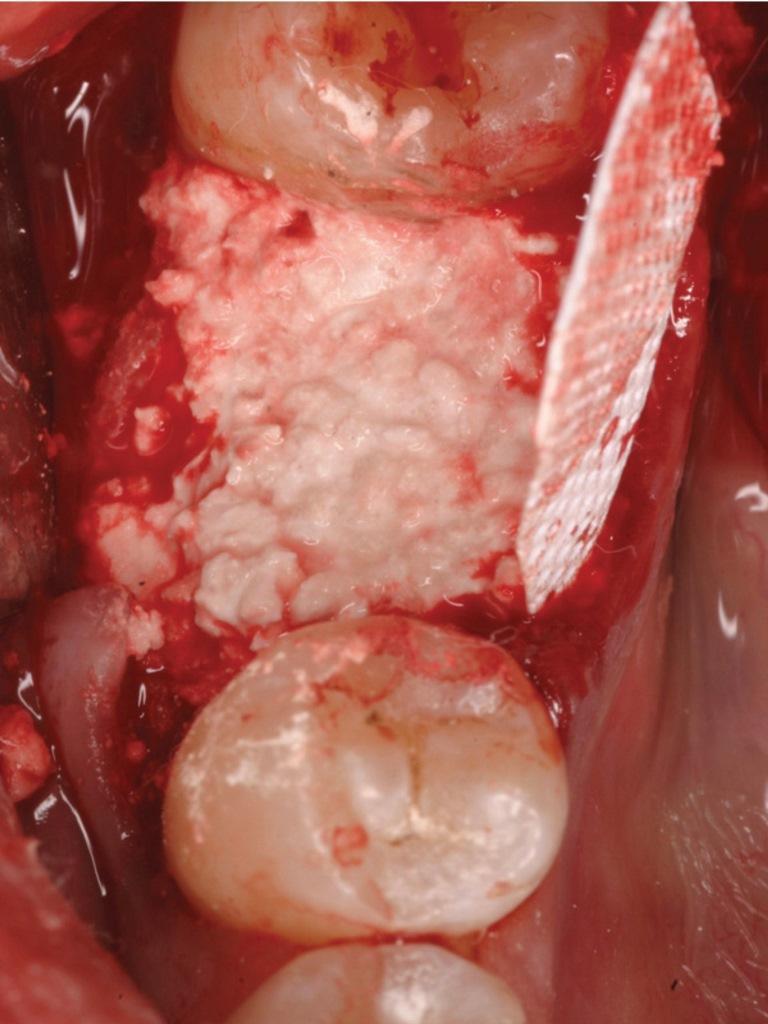
Фото 2. Вид пациента через 5 лет после лечения.
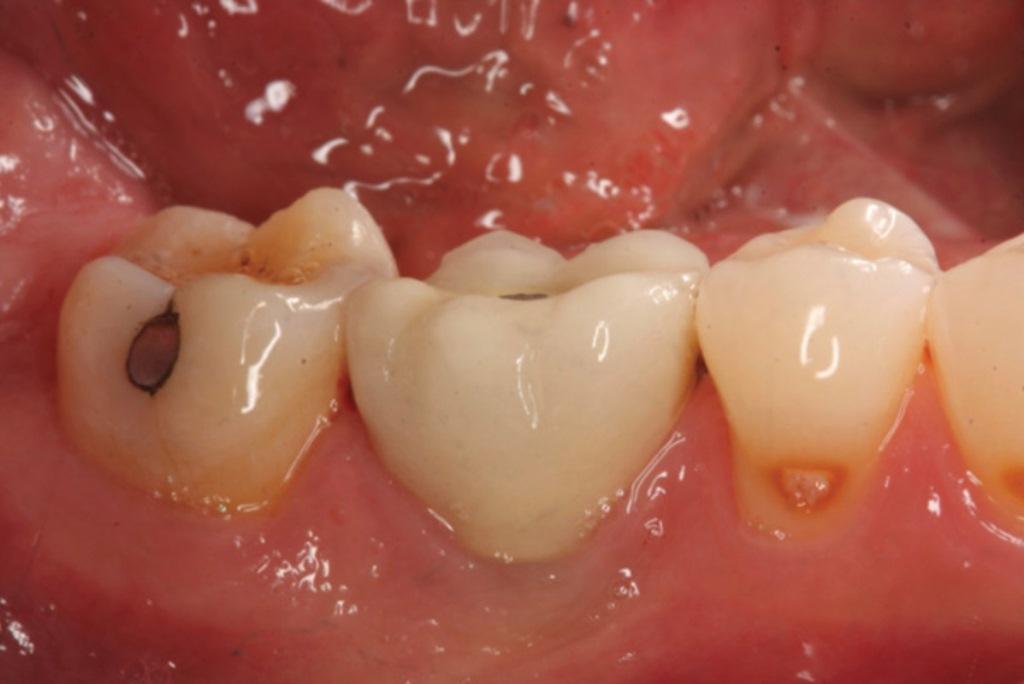
Фото 3. Результаты гистологического исследования демонстрируют 58% витальной кости через 4 месяца после аугментации.
Бета-трикальцийфосфат
Ранее существовали опасения, что трансплантационные материалы, которые полностью резервируются в короткий промежуток времени, могут провоцировать коллапс области проведенной аугментации. Чистый бета-трикальцийфосфат (ß-TCP) (фото 4) был одним из материалов, разработанных для решения этой проблемы. В ходе клинических и гистологических исследований удалось установить, что с его помощью можно обеспечить ретенцию 91% ширины костного гребня, заполняя область дефекта Cerasorb (Curasan, Inc.), и перекрывая участок вмешательства коллагеновыми, либо плотными мембранами из PTFE. Через 4-6 месяцев после аугментации, в область реконструкции были установлены дентальные имплантаты, которые также характеризовали высоким уровнем успешности. У пациента на фото 4, осталось только три зуба на верхней челюсти, которые поддерживали съемный протез. Учитывая специфические условия клинической ситуации было принято решение провести реконструкции резиудального гребня для формирования условий под установку дентальных имплантатов. Через 7 месяцев после заживления участка аугментации, провели сепарацию лоскута (фото 5), и установку имплантата. Было установлено, что аугментат позволил восстановить значительную часть предварительно зарегистрированного дефекта. Анализ полученного образца показал, что тот состоит на 85% из витальной кости в апикальной части, и на 90% в срединном участке, а β-TCP присутствовал только форме тонкой полоски на корональном участке (фото 6).
Фото 4. Бета-трикальцийфофат покрытый коллагеновой мембраной.
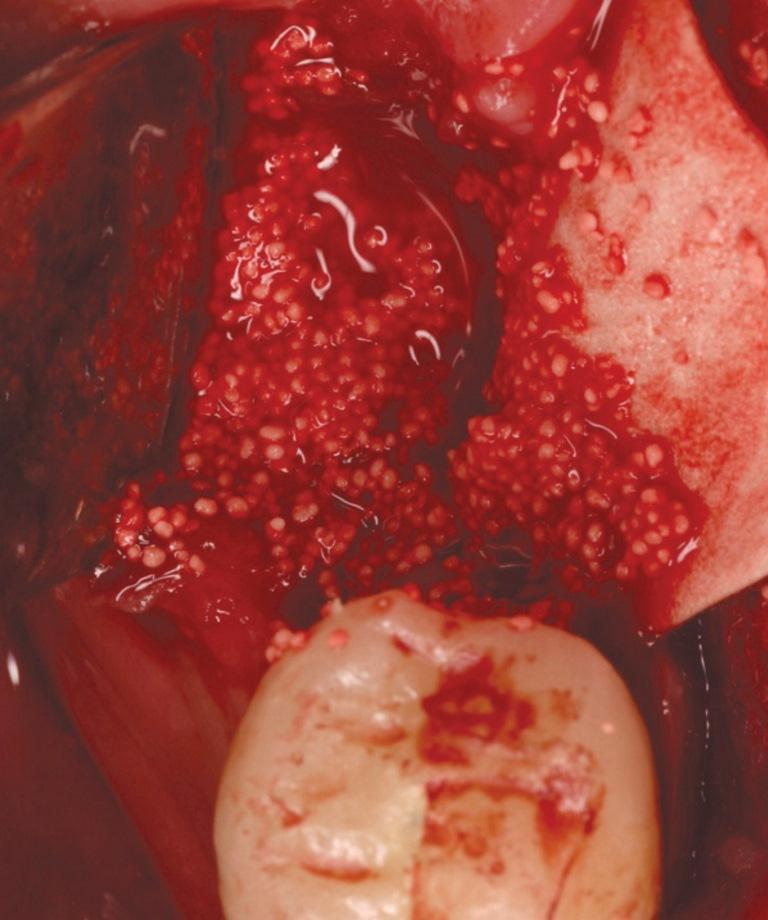
Фото 5. Вид через 7 месяцев после лечения в ходе повторного обнажения гребня.
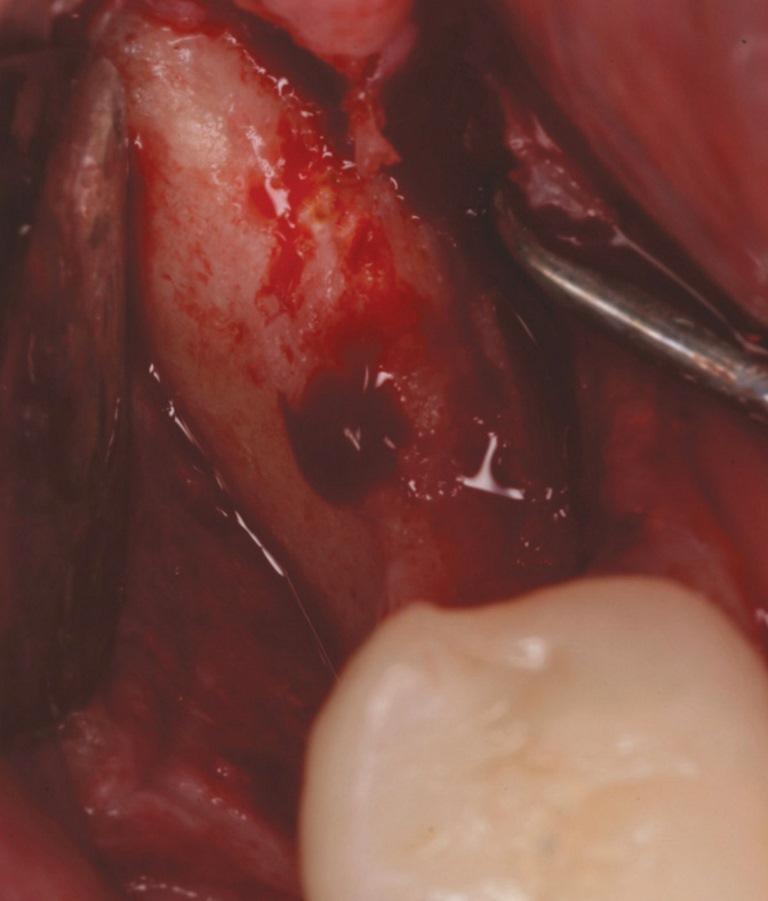
Фото 6. Результаты гистологического исследования демонстрируют значительный объем витальной кости.
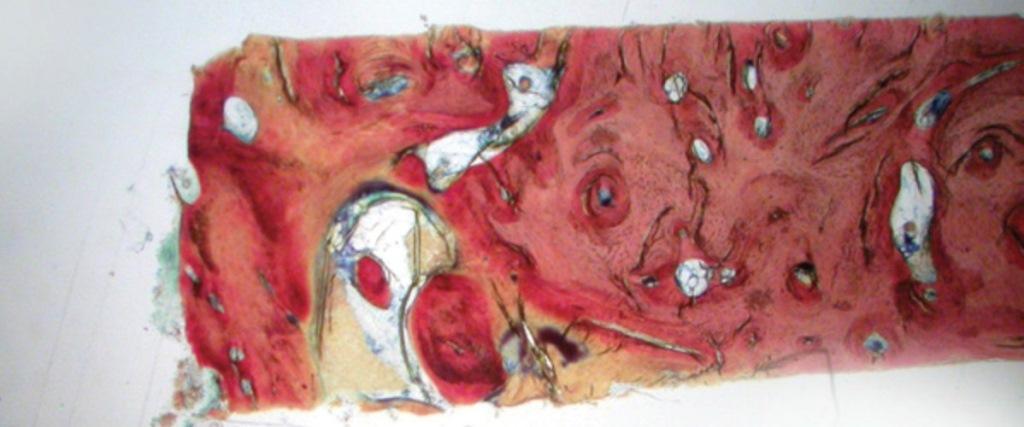
TCP (трикальцийфосфат) с покрытием PLGA
Для облегчения использования была разработана упаковка трикальцийфосфата в форме шприцов, материал которых непосредственно может быть использован для аугментации. Подобная система состоит из одного шприца, содержащего 99% β-TCP гранул, покрытых поли лактид-со-гликолидом (PLGA). Содержащие этого шприца смешивают с ампулой, содержащей BioLinker (N-метил-2-пирролидон и воду) (GUIDOR easy-graft, Sunstar) (фото 7). Исследование продемонстрировало биосовместимость и подходящую резорбции этого материала на примерах реконструкции лунок зубов после их удаления. Такой аугментат медленно резорбировался и длительно поддерживал необходимую форму, таким образом на данный момент являясь подходящей альтернативой для костной реконструкции с или без использования мембран. На фото 7 изображено процесс использования данного материала с целью аугментации лунки в области нижнего моляра. Область вмешательства перекрывали коллагеновой мембраной без первичного ушивания раны. Через 8 месяцев в данную область был установлен дентальный имплантата (фото 8). По фото 8 можно заметить, что значительное количество используемого материала резорбировалось и заместилось витальной костной тканью, в то же время удалось сохранить исходные параметры ширины костного гребня.
Фото 7. Упаковка PLGA-TCP в лунку удаленного зуба.
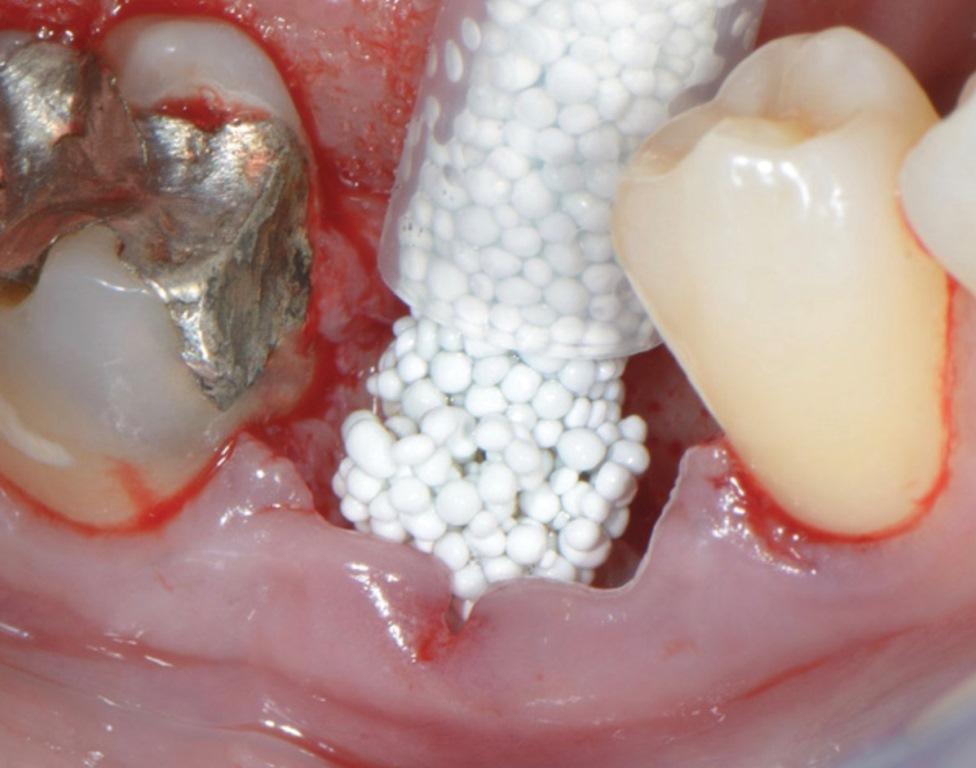
Фото 8. Вид через 8 месяцев после аугментации лунки.
Мембраны
Хотя вопрос об инфицировании и обнажении ПТФЭ-мембран с широкими порами остается еще недостаточно изучен, плотные безпористые аналоги таковых уже многие годы подтверждают свою клиническую эффективность. Использование плотных видов ПТФЭ-мембран (Cytoplast TXT, Osteogenics) для защиты кровяного сгустка по данным многочисленных работ позволяет в значительной степени сохранить исходную ширину альвеолярного хребта. При этом замещение пространства лунок витальной костной тканью по данным рентгенографических и гистологических исследований отмечалось уже через 3 месяца после покрытия областей вмешательства посредством мембран. Аналогично эффективно мембраны могут быть использованы и для покрытия аугментата (фото 1-3). Резорбируемые виды мембран были разработаны для поддержки необходимого объема пространства, учитывая параметры их жесткости и расстояние между внутренним и внешним слоями (GUIDOR Matrix Barrier, Sunstar). Пористый характер поверхностей, состоящих из комбинации эфира лимонной кислоты и полимолочной кислоты, позволяет тканям несколько врасти в мембрану, таким образом обеспечивая более высокий уровень ее стабилизации. При этом частота инфицирования или воспаления тканей вокруг мембран отмечается довольно редко, что аргументирует целесообразность их использования в регенеративной стоматологии, особенно в случаях восстановления дефектов кости вокруг имплантатов или еще до момента их установки. В случае, представленном на фото 9-11 синтетическая мембрана была установлена сразу же после экстракции зуба с дефицитом костной ткани с нёбной стороны. Жесткость мембраны обеспечила формирования такого объема пространства, который являлся необходимым для восстановления определённой конфигурации костного гребня. Через шесть недель участок вмешательства демонстрировал признаки полного заживления без каких-либо следов воспаления или инфицирования. Таким образом также удалось добиться формирования более широкой зоны кератинизировнаных тканей.
Фото 9. Субпериостальная установка мембраны при значительной потере костной ткани со щечной стороны лунки.
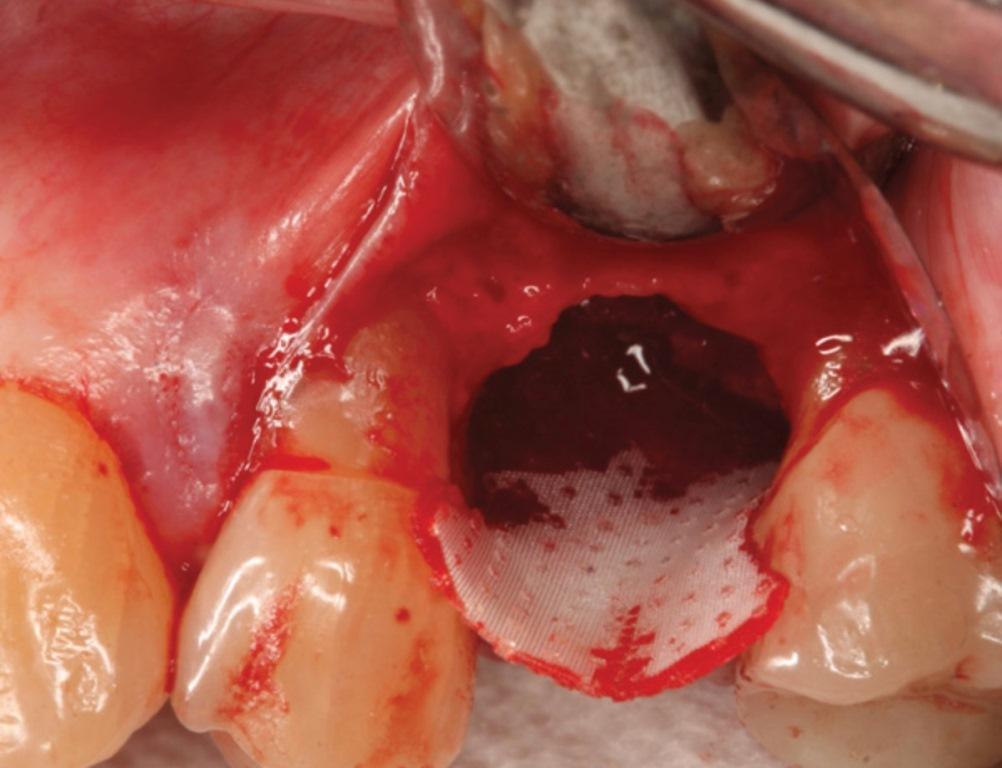
Фото 10. Вид окончательно-полученной формы гребня.
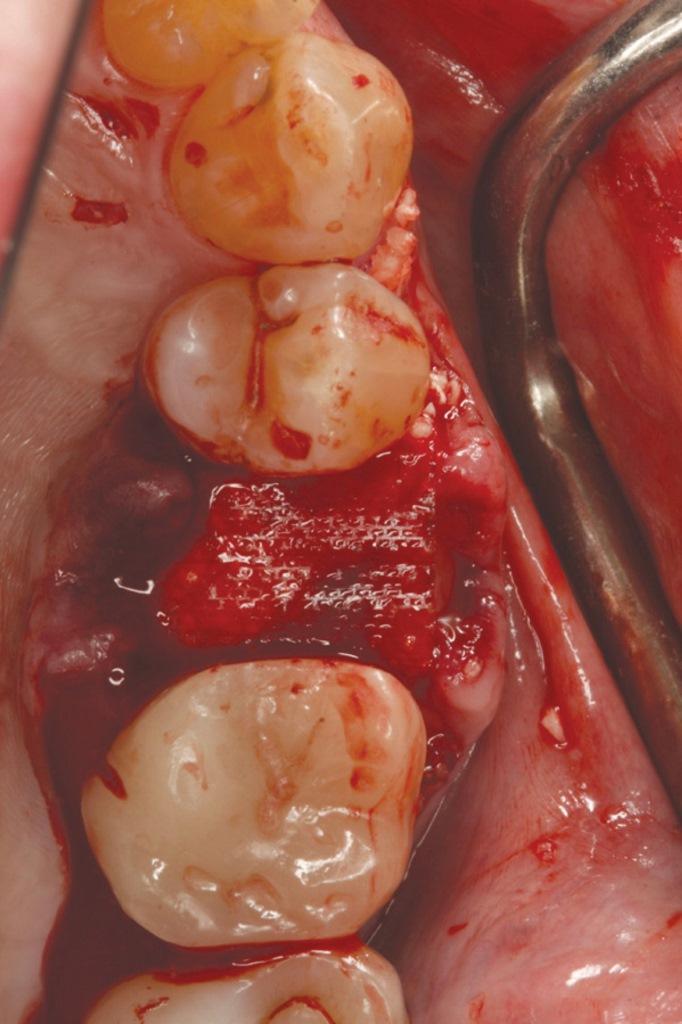
Фото 11. Вид через 6 недель после заживления.
Наполнители
Учитывая недостатки порошковых форм аугментатов, некоторые их аналоги были разработаны в виде паст для многофункционального использования: реконструкции области лунок, синус-лифтинга и аугментации костного гребня. Ранее упомянутые BPCS и PLGA / TCP представляют собой как раз такие материалы. Они по сути являются комбинацией деминерализованного / минерализованного аллотрансплантата и коллагенового желатина (Optecure, Exactech), представлял таким образом полужесткий материал для реконструкции костной ткани. По данным производителей данные материала также характеризуются остеоиндуктивностью с возможностью формирования значительных объемов витальной ткани. Пациент на фото 12 обратился за помощью имея во фронтальном участке нижней челюсти ширину кости приблизительно в 1 мм. Аллографт смешивали со стерильном физиологическом растворе, и перекрывали сульфатом кальция (3D Bond, Augma Biomaterials) и мембраной Ossix Plus (Datum Dental Ltd). Имплантаты узкого диаметра (ANEW, Dentatus) были установлены 4 месяца спустя. Клинический результат лечения изображен на фото 13, представляя собой вид через 3 года после нагрузки установленных имплантатов.
Фото 12. Вид участка дефицита костной ткани во фронтальном участке нижней челюсти.
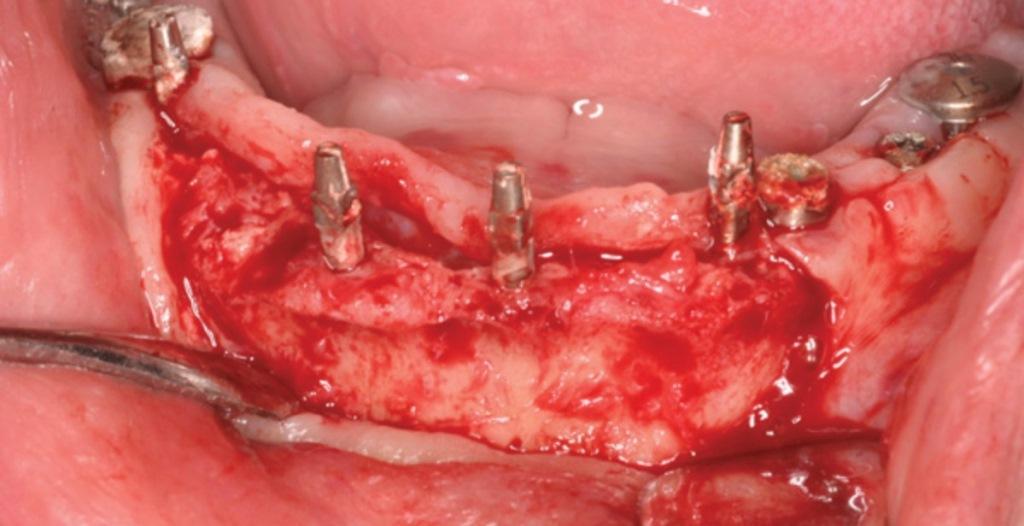
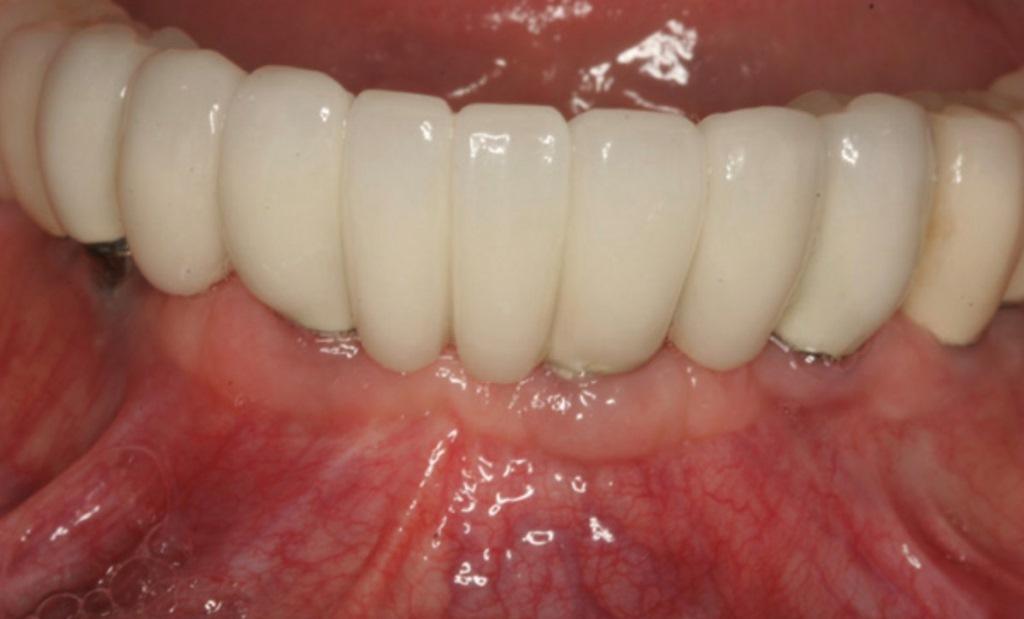
Фото 13. Вид через 3 года поле протезирования.
Неорганический трансплантат бычьего происхождения
В ранних исследованиях процедуры синус-лифтинга использования неорганический костный трансплантат бычьего происхождения. Во многих публикациях описывали применения данного ксенографта как изолировано, так и вместе с аутогенной костной тканью, или даже с определенными факторами роста. Когда ксенографт использовали изолировано, но перекрывали его мембраной, процент формирования витальной кости составлял от 12% до 17% в течение 6-10 месяцев после операции. В другом исследовании ксенографт применяли вместе с факторами роста для поднятия уровня Шнейдеровой мембраны. Результаты данного мультицентричного исследования с участием 25 пациентов продемонстрировали, что формирование костной ткани через 6 месяцев составляло около 50%, что более эффективно не только с позиции прироста тканей, но и с позиции времени, потраченного на реабилитацию.
Выводы
В обсуждении результатов гистологического исследования области реконструкции лунки зуба посредством полугидрата сульфата кальция Guarneri и коллеги утверждали следящее: «Цель любой процедуры аугментации - добиться формирования 100% живой костной ткани, окружающей имплантаты». В зависимости от размера и местоположения дефекта, специфики взаимосвязи с окружающими тканями данная цель может быть достигнутой, или же наоборот – невозможной для достижения. Согласно долгосрочным исследованиям успеха имплантатов, установленных в область аугментации, наличие в области вмешательства невитальных частиц трансплантата никаким образом не компрометирует успешность лечения. Исследования же, описывающие опыт применения резорбируемых мембран, указывают на возможность немедленной установки имплантатов при аргументированном выборе метода аугментации. Материалы для восстановления объема костного гребня, а также для изоляции области реконструкции обеспечивают врача различными возможностями для адаптации хирургического подхода в ходе комплексной реабилитации пациента. Определив конечную цель процедуры, и спрогнозировав возможны ее результат через 3, 6, 9 или более месяцев, врач может более доказательно подойти к выбору алгоритма вмешательства, основывая на предварительных данных, описанных в респектабельных научных источниках.
Авторы:
Robert A. Horowitz, DDS
Minas D. Leventis, DDS, MS, PhD
Michael D. Rohrer, DDS, MS
Hari S. Prasad, BS, MDT
История костной аугментации материалами разного происхождения достигает почти столетней глубины. Существенные проблемы, связанные с трансплантационными материалами и усилителями роста, касаются их происхождения, обоснования использования, способа их забора с учетом объема так именуемых биологических «затрат». Еще одна ключевая проблема костных трансплантатов касается аспекта потенциальной «репарации» или регенерации области вмешательства. Репарация представляет собой процесс замены дефектного участка чем-то физически подобным по структуре, но отличающимся биологически и физиологически. Регенерация, напротив, предусматривает использование разных материалов и методов, которые позволяют восстановить биологическую структуру дефектной области полностью идентичной тканью. Хирургам, планирующим проведение аугментации, нужно четко понимать, какой результат они могут прогнозировать по окончании реабилитации, и насколько успешными окажутся применяемые ими техники. Четко понимая все аспекты, врач может достигнуть консенсуса в восстановлении витальной кости, выполненного объема аугментации, скорости заживления и оптимизации процедуры ятрогенного вмешательства.

Рекомендации относительно реконструкции костной ткани
Выбор, стоящий перед хирургом во время процедуры экстракции, выполнения аугментации или синус-лифтинга касается, главным образом, следующих аспектов:
- доступа к области дефекта. Доступ может быть сформирован без сепарации лоскута – миниинвазивно, или же классически – путем сепарации объема окружающих тканей.
- источник костного материала. Аутогенная кость, аллогенные аналоги, аллопласт, ксенотрансплантаты или другие материалы – все они подходят для реконструкции параметров резидуального гребня.
- тип используемого трансплантата. Трансплантат может быть представлен в форме частиц, пасты или блока, разного размера и зернистости, а также могут быть собраны из участков разного происхождения (кортикальной или губчатой части кости).
- специфические характеристики каждого трансплантата. Костные заменители характеризуются различными уровнями минерализации и различной тенденцией к резорбции. следует учитывать, является ли материал остеокондуктивным или остеоиндуктивным и как быстро или медленно, или если вообще подлежит ли он биодеградации.
- тип используемого биологического барьера. Используемые мембраны могут быть синтетическими или коллагеновыми: также они могут быть резорбируемыми или нерезорбируемыми, биологические активными или инертными.
Ранние исследования указывают на то, что в экстракционной лунке, даже без соответствующего использования трансплантата или мембраны, все равно наблюдается формирование витальной костной ткани. Однако полагаться лишь на такой исход не стоит. В 2008 году Fickl и соавторы исследовали различия между разными подходами к экстракции (с и без сепарации лоскута) с дальнейшим заполнением лунки аугментатом или же без выполнения процедуры реконструкции. Они обнаружили, что сепарация тканей слизистой и периоста приводит к большей потере ширины и высоты альвеолярного гребня, по сравнению с теми результатами, которые были получены после реализации миниинвазвиного подхода. Также они отметили факт сохранения первичных размеров кости при заполнении лунки неорганичным трансплантатом бычьего происхождения, чего не отмечалось без проведения процедуры аугментации. Iasella и коллеги, однако, отметили, что более витальная кость формировалась в области постэкстракционных лунок без использованного какого-либо типа графта, хотя потеря изначального объема твердых тканей при этом составляла около 30%. Аналогичных последствий удалось избежать при заполнении лунки минерализованным аллографтом, перекрытым резорбируемой коллагеновой мембраной.
В другом исследовании сравнивали два разных метода аугментации. В лунки устанавливали ксенотрансплантат, полученный из крупного рогатого скота, и перекрывали его резорбируемой мембраной – таким образом удавалось добиться незначительного приросла тканей по высоте, но объем сформированной витальной кости не превышал 26%. Когда же в качестве аналога применяли деминерализованный аллотрансплантат с сульфатом кальция, который перекрывали барьером из сульфата кальция, отмечали аналогичный результат изменения геометрических параметров костного гребня, однако количество витальной кости практически в два раза превышало то, что было отмечено при использовании аллотрансплантата.
Материала для аугментации и изоляции
Сульфат кальция
Сульфат кальция является синтетическим аналогом, который используется во многих конфигурациях в качестве как трансплантата, так и стимулятора роста (фото 1). Исследование, проведенное в 2004 году, продемонстрировало, что данный материал в полугидратной форме без мембраны позволяет отлично сохранить объем тканей, и при этом отмечается приблизительно 60% формирование витальной кости. Новый материал для трансплантации костной ткани, описанный в отчете за 2012 год, является двухфазным и содержит как геми- так и дигидрат кальция сульфата. Этот материал является самоосаждаемым в присутствии крови или слюны, и может использоваться с или без барьерной мембраны. В докладе были представлены гистологические результаты его использования при нескольких типах дефектов, которые свидетельствуют о приросте костной ткани. Кроме того, также удавалось добиться ретенции и увеличения геометрических параметром альвеолярного гребня. Пациентка, изображена на фото 1, обратилась за помощью после значительного абсцесса эндодонтической этиологии, который спровоцировал убыль как вестибулярной, так и язычной костной пластинок. Покрытие двухфазного кальциевого сульфата плотной политетрафторэтиленовой (PTFE) мембраной в течение 3 недель способствовало заживлению участка дефекта. Клинически было очевидно, что объем резиудального гребня удалось сохранить на протяжении более 5 лет, который в свою очередь поддерживал поверх лежащую кератинизированную мягкую ткань (фото 2). Самое главное, что при гистологической оценке было обнаружено 58% витальной костной без остатков гранул костного трансплантата (фото 3).
Фото 1. Процедура аугментации с использованием BPCS и покрытием ПТФЭ-мембраной.

Фото 2. Вид пациента через 5 лет после лечения.

Фото 3. Результаты гистологического исследования демонстрируют 58% витальной кости через 4 месяца после аугментации.

Бета-трикальцийфосфат
Ранее существовали опасения, что трансплантационные материалы, которые полностью резервируются в короткий промежуток времени, могут провоцировать коллапс области проведенной аугментации. Чистый бета-трикальцийфосфат (ß-TCP) (фото 4) был одним из материалов, разработанных для решения этой проблемы. В ходе клинических и гистологических исследований удалось установить, что с его помощью можно обеспечить ретенцию 91% ширины костного гребня, заполняя область дефекта Cerasorb (Curasan, Inc.), и перекрывая участок вмешательства коллагеновыми, либо плотными мембранами из PTFE. Через 4-6 месяцев после аугментации, в область реконструкции были установлены дентальные имплантаты, которые также характеризовали высоким уровнем успешности. У пациента на фото 4, осталось только три зуба на верхней челюсти, которые поддерживали съемный протез. Учитывая специфические условия клинической ситуации было принято решение провести реконструкции резиудального гребня для формирования условий под установку дентальных имплантатов. Через 7 месяцев после заживления участка аугментации, провели сепарацию лоскута (фото 5), и установку имплантата. Было установлено, что аугментат позволил восстановить значительную часть предварительно зарегистрированного дефекта. Анализ полученного образца показал, что тот состоит на 85% из витальной кости в апикальной части, и на 90% в срединном участке, а β-TCP присутствовал только форме тонкой полоски на корональном участке (фото 6).
Фото 4. Бета-трикальцийфофат покрытый коллагеновой мембраной.

Фото 5. Вид через 7 месяцев после лечения в ходе повторного обнажения гребня.

Фото 6. Результаты гистологического исследования демонстрируют значительный объем витальной кости.

TCP (трикальцийфосфат) с покрытием PLGA
Для облегчения использования была разработана упаковка трикальцийфосфата в форме шприцов, материал которых непосредственно может быть использован для аугментации. Подобная система состоит из одного шприца, содержащего 99% β-TCP гранул, покрытых поли лактид-со-гликолидом (PLGA). Содержащие этого шприца смешивают с ампулой, содержащей BioLinker (N-метил-2-пирролидон и воду) (GUIDOR easy-graft, Sunstar) (фото 7). Исследование продемонстрировало биосовместимость и подходящую резорбции этого материала на примерах реконструкции лунок зубов после их удаления. Такой аугментат медленно резорбировался и длительно поддерживал необходимую форму, таким образом на данный момент являясь подходящей альтернативой для костной реконструкции с или без использования мембран. На фото 7 изображено процесс использования данного материала с целью аугментации лунки в области нижнего моляра. Область вмешательства перекрывали коллагеновой мембраной без первичного ушивания раны. Через 8 месяцев в данную область был установлен дентальный имплантата (фото 8). По фото 8 можно заметить, что значительное количество используемого материала резорбировалось и заместилось витальной костной тканью, в то же время удалось сохранить исходные параметры ширины костного гребня.
Фото 7. Упаковка PLGA-TCP в лунку удаленного зуба.

Фото 8. Вид через 8 месяцев после аугментации лунки.

Мембраны
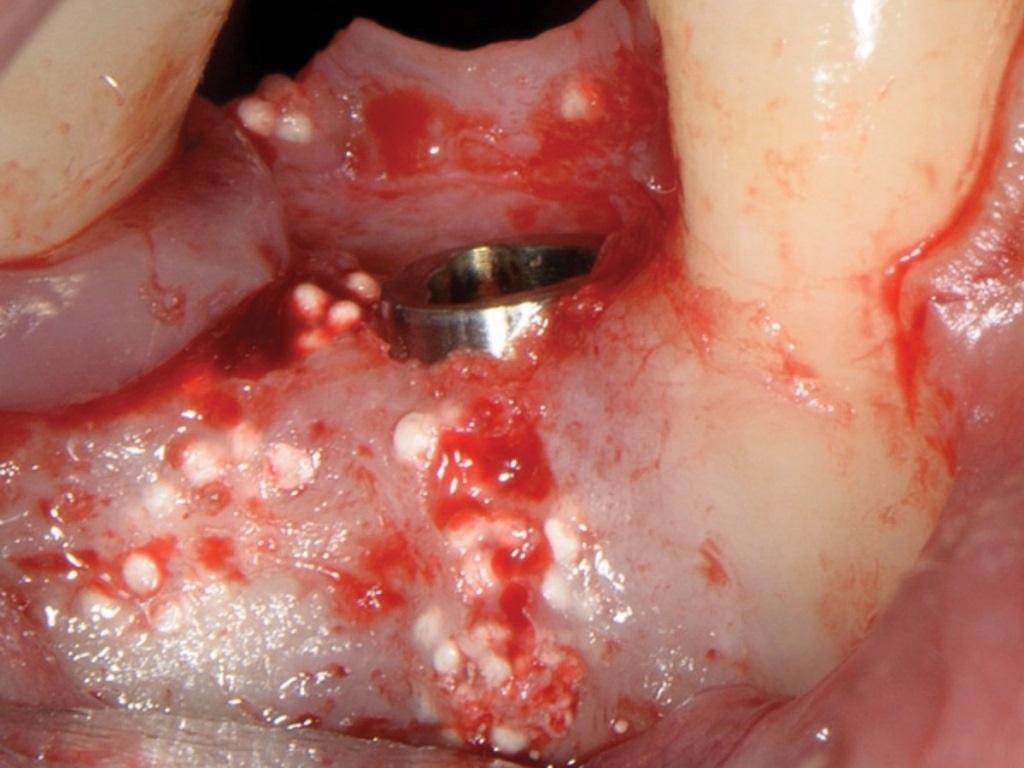
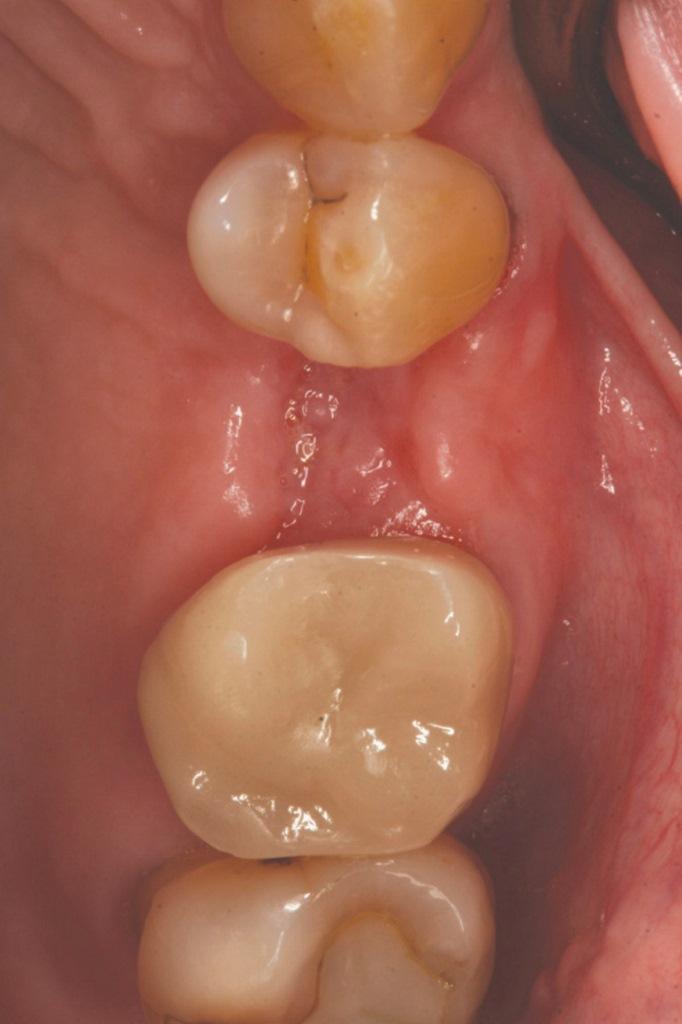
Хотя вопрос об инфицировании и обнажении ПТФЭ-мембран с широкими порами остается еще недостаточно изучен, плотные безпористые аналоги таковых уже многие годы подтверждают свою клиническую эффективность. Использование плотных видов ПТФЭ-мембран (Cytoplast TXT, Osteogenics) для защиты кровяного сгустка по данным многочисленных работ позволяет в значительной степени сохранить исходную ширину альвеолярного хребта. При этом замещение пространства лунок витальной костной тканью по данным рентгенографических и гистологических исследований отмечалось уже через 3 месяца после покрытия областей вмешательства посредством мембран. Аналогично эффективно мембраны могут быть использованы и для покрытия аугментата (фото 1-3). Резорбируемые виды мембран были разработаны для поддержки необходимого объема пространства, учитывая параметры их жесткости и расстояние между внутренним и внешним слоями (GUIDOR Matrix Barrier, Sunstar). Пористый характер поверхностей, состоящих из комбинации эфира лимонной кислоты и полимолочной кислоты, позволяет тканям несколько врасти в мембрану, таким образом обеспечивая более высокий уровень ее стабилизации. При этом частота инфицирования или воспаления тканей вокруг мембран отмечается довольно редко, что аргументирует целесообразность их использования в регенеративной стоматологии, особенно в случаях восстановления дефектов кости вокруг имплантатов или еще до момента их установки. В случае, представленном на фото 9-11 синтетическая мембрана была установлена сразу же после экстракции зуба с дефицитом костной ткани с нёбной стороны. Жесткость мембраны обеспечила формирования такого объема пространства, который являлся необходимым для восстановления определённой конфигурации костного гребня. Через шесть недель участок вмешательства демонстрировал признаки полного заживления без каких-либо следов воспаления или инфицирования. Таким образом также удалось добиться формирования более широкой зоны кератинизировнаных тканей.
Фото 9. Субпериостальная установка мембраны при значительной потере костной ткани со щечной стороны лунки.

Фото 10. Вид окончательно-полученной формы гребня.

Фото 11. Вид через 6 недель после заживления.

Наполнители
Учитывая недостатки порошковых форм аугментатов, некоторые их аналоги были разработаны в виде паст для многофункционального использования: реконструкции области лунок, синус-лифтинга и аугментации костного гребня. Ранее упомянутые BPCS и PLGA / TCP представляют собой как раз такие материалы. Они по сути являются комбинацией деминерализованного / минерализованного аллотрансплантата и коллагенового желатина (Optecure, Exactech), представлял таким образом полужесткий материал для реконструкции костной ткани. По данным производителей данные материала также характеризуются остеоиндуктивностью с возможностью формирования значительных объемов витальной ткани. Пациент на фото 12 обратился за помощью имея во фронтальном участке нижней челюсти ширину кости приблизительно в 1 мм. Аллографт смешивали со стерильном физиологическом растворе, и перекрывали сульфатом кальция (3D Bond, Augma Biomaterials) и мембраной Ossix Plus (Datum Dental Ltd). Имплантаты узкого диаметра (ANEW, Dentatus) были установлены 4 месяца спустя. Клинический результат лечения изображен на фото 13, представляя собой вид через 3 года после нагрузки установленных имплантатов.
Фото 12. Вид участка дефицита костной ткани во фронтальном участке нижней челюсти.

Фото 13. Вид через 3 года поле протезирования.

Неорганический трансплантат бычьего происхождения
В ранних исследованиях процедуры синус-лифтинга использования неорганический костный трансплантат бычьего происхождения. Во многих публикациях описывали применения данного ксенографта как изолировано, так и вместе с аутогенной костной тканью, или даже с определенными факторами роста. Когда ксенографт использовали изолировано, но перекрывали его мембраной, процент формирования витальной кости составлял от 12% до 17% в течение 6-10 месяцев после операции. В другом исследовании ксенографт применяли вместе с факторами роста для поднятия уровня Шнейдеровой мембраны. Результаты данного мультицентричного исследования с участием 25 пациентов продемонстрировали, что формирование костной ткани через 6 месяцев составляло около 50%, что более эффективно не только с позиции прироста тканей, но и с позиции времени, потраченного на реабилитацию.
Выводы
В обсуждении результатов гистологического исследования области реконструкции лунки зуба посредством полугидрата сульфата кальция Guarneri и коллеги утверждали следящее: «Цель любой процедуры аугментации - добиться формирования 100% живой костной ткани, окружающей имплантаты». В зависимости от размера и местоположения дефекта, специфики взаимосвязи с окружающими тканями данная цель может быть достигнутой, или же наоборот – невозможной для достижения. Согласно долгосрочным исследованиям успеха имплантатов, установленных в область аугментации, наличие в области вмешательства невитальных частиц трансплантата никаким образом не компрометирует успешность лечения. Исследования же, описывающие опыт применения резорбируемых мембран, указывают на возможность немедленной установки имплантатов при аргументированном выборе метода аугментации. Материалы для восстановления объема костного гребня, а также для изоляции области реконструкции обеспечивают врача различными возможностями для адаптации хирургического подхода в ходе комплексной реабилитации пациента. Определив конечную цель процедуры, и спрогнозировав возможны ее результат через 3, 6, 9 или более месяцев, врач может более доказательно подойти к выбору алгоритма вмешательства, основывая на предварительных данных, описанных в респектабельных научных источниках.
Авторы:
Robert A. Horowitz, DDS
Minas D. Leventis, DDS, MS, PhD
Michael D. Rohrer, DDS, MS
Hari S. Prasad, BS, MDT































































































































































0 комментариев