Ретроградный периимплантит (РПИ) характеризуется атипичной и часто прогрессирующей потерей костной ткани в периапикальной области дентального имплантата. Хотя, по имеющимся данным, распространенность РПИ ниже, чем маргинального периимплантита, при отсутствии лечения это состояние может привести к потере имплантатов. В данной клинической серии случаев два пациента с различными проявлениями РПИ были пролечены с использованием направленной костной регенерации (НКР) с применением костного трансплантата и коллагеновой мембраны. Долгосрочное наблюдение показало клиническое и рентгенологическое улучшение, которое выразилось в рентгенологическом костном наполнении и уменьшении глубины зондирования вокруг имплантатов. Наблюдения, представленные здесь, позволяют предположить, что НКР при дефектах, вызванных РПИ, является эффективным методом лечения.
Выделяют две формы РПИ: активную и неактивную. Активный РПИ проявляется симптоматической периапикальной рентгенопрозрачностью с увеличением размера очага, тогда как неактивный РПИ проявляется бессимптомной периапикальной рентгенопрозрачностью либо со стабильным или уменьшенным размером очага, либо с чрезмерным расширением остеотомии под имплантат. Распространенность РПИ относительно невысока (0,26% до 0,34%). Этиологические факторы, связанные с РПИ, включают эндодонтические поражения соседних зубов, бактериальную контаминацию во время установки имплантата, остаточную инфекцию в области удаления, избыточное тепловыделение во время операции по установке имплантата, компрессию кости во время операции, чрезмерное расширение подготовки остеотомии и общие заболевания.
В одном исследовании было показано, что чем меньше расстояние между имплантатом и эндодонтически леченным (т.е. после лечения корневых каналов) зубом, тем с большей вероятность возникает ретроградный периимплантит. РПИ достоверно связан со временем между установкой имплантата и лечением корневых каналов зубов, имеющих периапикальное поражение. Эта взаимосвязь также отмечалась для расстояния между соседними зубами и имплантатами. Для снижения риска РПИ рекомендуется минимальное расстояние в 2 мм между имплантатом и соседними зубами после лечения корневых каналов. Кроме того, предлагается отложить установку имплантата как минимум на 4 недели после лечения корневых каналов. Микробный фактор играет критическую роль в патогенезе РПИ, причем Porphyromonas gingivalis, Prevotella intermedia, Corynebacterium, Streptococcus и Klebsiella pneumoniae являются наиболее распространенными микроорганизмами.
Лечение РПИ зависит от точного диагноза этиологии. Ведение включает хирургические подходы, в том числе механический кюретаж костного дефекта и химическую очистку для детоксикации поверхности имплантата. При выборе метода лечения необходимо учитывать факторы конкретного случая, включая тяжесть инфекции, объем потери костной ткани и общее состояние здоровья пациента. В зависимости от ситуации может быть использована комбинация методов лечения для достижения оптимального результата.
В исследованиях сообщалось о предсказуемых результатах использования направленной костной регенерации (НКР) для замещения утраченной кости и стабилизации имплантата в случаях РПИ. В большинстве исследований сообщалось о хорошей выживаемости имплантатов (от 73,2% до 97,4%) через 1–10 лет после лечения. В другом исследовании сообщалось о кумулятивной выживаемости имплантатов 78,3% за 20 лет. Напротив, в других исследованиях сообщалось, что 35,7% имплантатов с РПИ были удалены, причем значительно более высокие показатели удаления наблюдались, когда соседние зубы имели эндодонтическую патологию.
Данная клиническая серия случаев освещает два явно различных проявления РПИ, при которых в качестве выбранного метода лечения использовалась НКР с наблюдением от 1 до 7 лет.
Материалы и методы
Клинические проявления
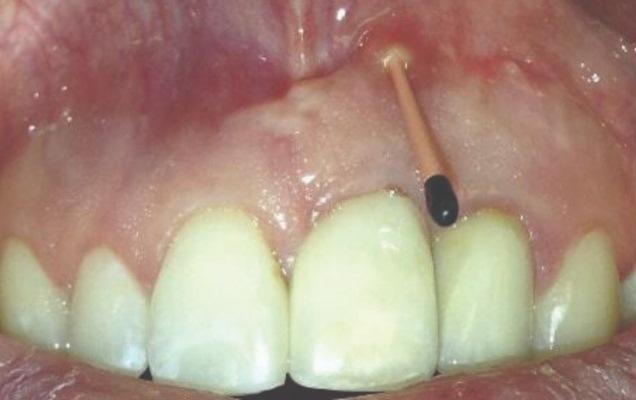
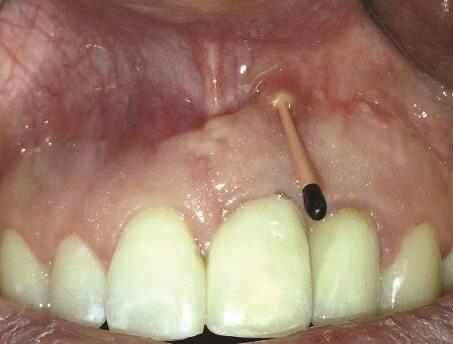
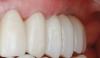
Пациент 1: Пациентка 30 лет с неосложненным медицинским анамнезом обратилась с имплантатом № 2.1, у которого диагностирован ретроградный периимплантит. Зуб № 2.1 был заменен имплантатом 8 лет назад из-за травмы в анамнезе и неудачного лечения корневых каналов. Имплантат демонстрировал периапикальную рентгенопрозрачность со свищевым ходом, ведущим к верхушке имплантата № 2.1 (Фото 1 и Фото 2). У пациентки была высокая линия улыбки с более длинными клиническими коронками зубов №№ 2.1 и 2.2 по сравнению с №№ 1.2 и 1.1 (Фото 1 и Фото 2).
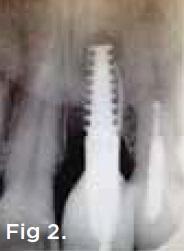
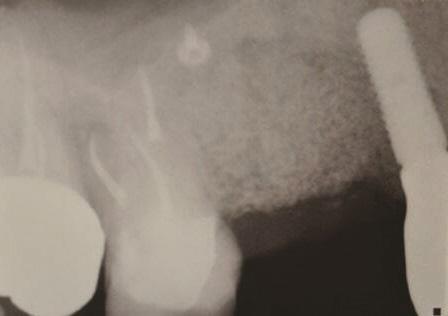
Фото 1 и Фото 2. Случай 1: Первоначальная клиническая картина с гуттаперчевым штифтом, установленным в апикальный свищ зуба № 2.1 (Фото. 1); рентгеновский снимок, показывающий гуттаперчевый штифт, ведущий к периапикальному поражению (Фото. 2).
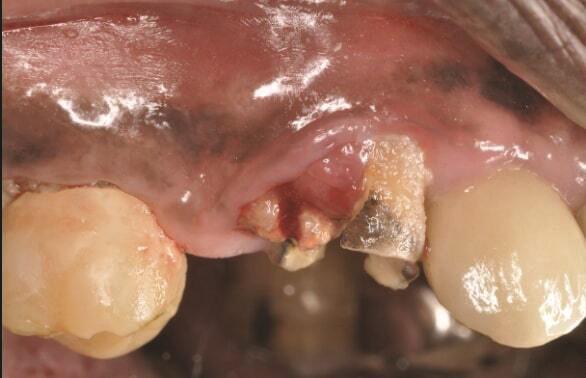
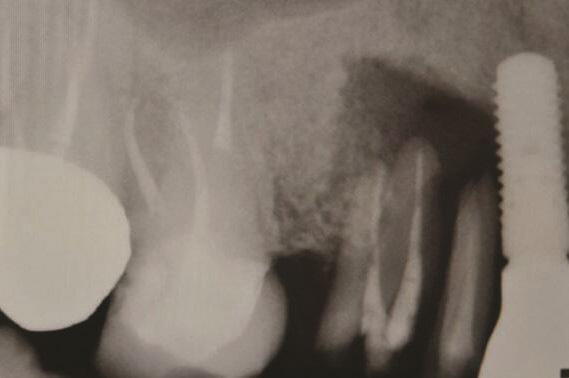
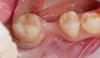
Пациент 2: Здоровый пациент мужского пола 63 лет обратился с имплантатом № 1.3, у которого диагностирован РПИ, на который повлиял ранее эндодонтически леченный и сломанный зуб № 1.4 (Фото 3 и Фото 4). Глубина зондирования вокруг имплантата составляла от 4 до 10 мм (Таблица 1), причем наиболее серьезная потеря кости наблюдалась с дистальной стороны имплантата № 1.3 (Фото 3 и Фото 4).
Фото 3 и Фото 4. Случай 2: Первоначальная клиническая картина, показывающая имплантат № 1.3 с РПИ, на который повлиял сломанный зуб № 1.4 (Фото 3); рентгеновский снимок, показывающий сломанный зуб № 1.4 с периапикальным поражением, распространяющимся на дистальную сторону имплантата № 1.3 (Фото 4).
Хирургическая процедура
Варианты лечения были обсуждены с пациентами, и оба дали согласие на лечение, включающее периимплантатный кюретаж и НКР. Каждый пациент получил 600 мг нестероидных противовоспалительных препаратов за 1 час до процедуры и прополоскал рот 15 мл 0,12% глюконата хлоргексидина; местная анестезия была проведена с использованием 2% лидокаина HCl с эпинефрином 1:100 000. В зависимости от проявления поражений форма разрезов и доступ различались для двух случаев.
В случае 1, из-за высокой линии улыбки и асимметричной длины клинических коронок, пациентке был выполнен вестибулярный разрез в области мукогингивального соединения с отслаиванием полнослойного лоскута для доступа к верхушке имплантата. Кюретаж имплантата был выполнен титановыми кюретками и щетками (Фото 5). Поверхность имплантата обрабатывали в течение 2 минут суспензией доксициклина с физиологическим раствором. Периимплантатный дефект был заполнен гранулированным лиофилизированным костным аллотрансплантатом (ЛКА) (Фото 6) и покрыт коллагеновой мембраной (Фото 7). Первичное закрытие лоскута было достигнуто с использованием рассасывающихся швов (Фото 8).
Фото 5. Случай 1: Вестибулярный вид, показывающий периапикальную потерю кости вокруг № 2.1 после кюретажа имплантата и обработки суспензией доксициклина с физиологическим раствором.
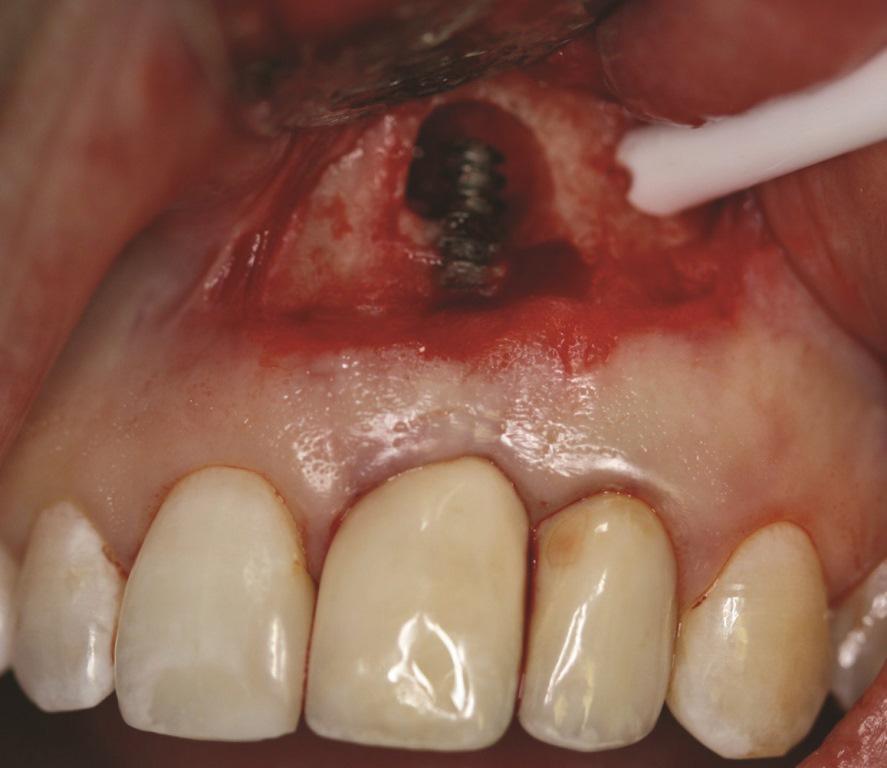
Фото 6. Случай 1: Костный аллотрансплантат ЛКА помещен для заполнения дефекта вокруг имплантата.
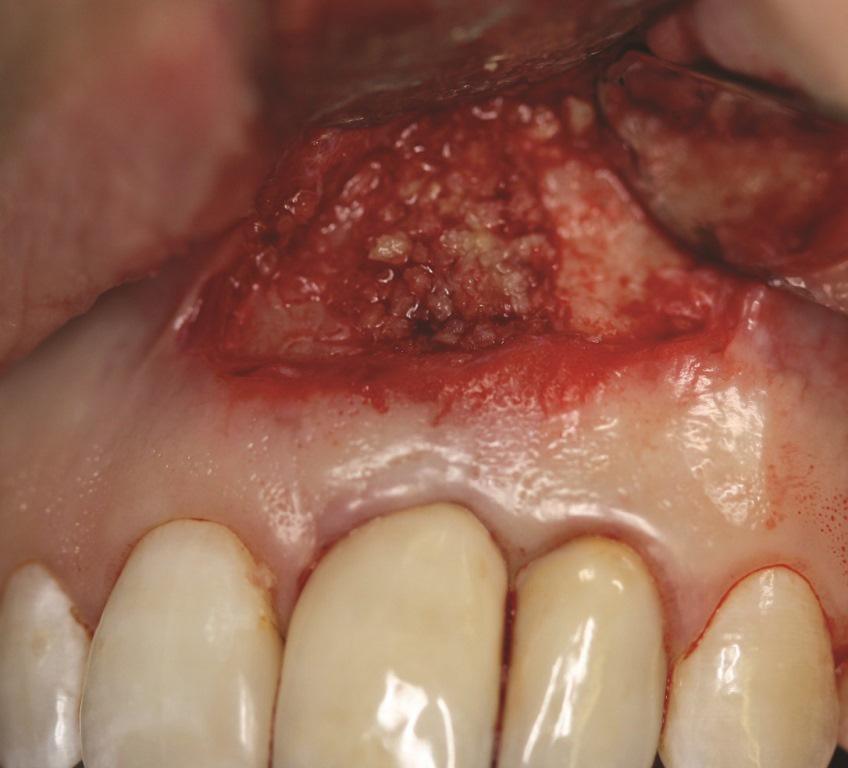
Фото 7. Случай 1: Рассасывающаяся коллагеновая мембрана помещена для покрытия дефекта.
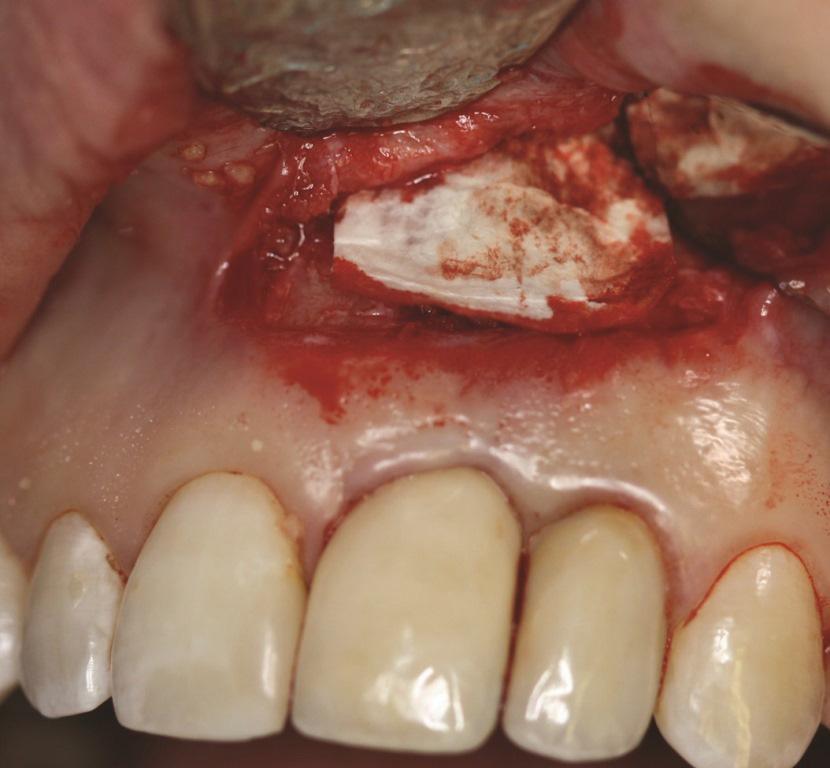
Фото 8. Случай 1: Первичное закрытие достигнуто с использованием узловых рассасывающихся швов.
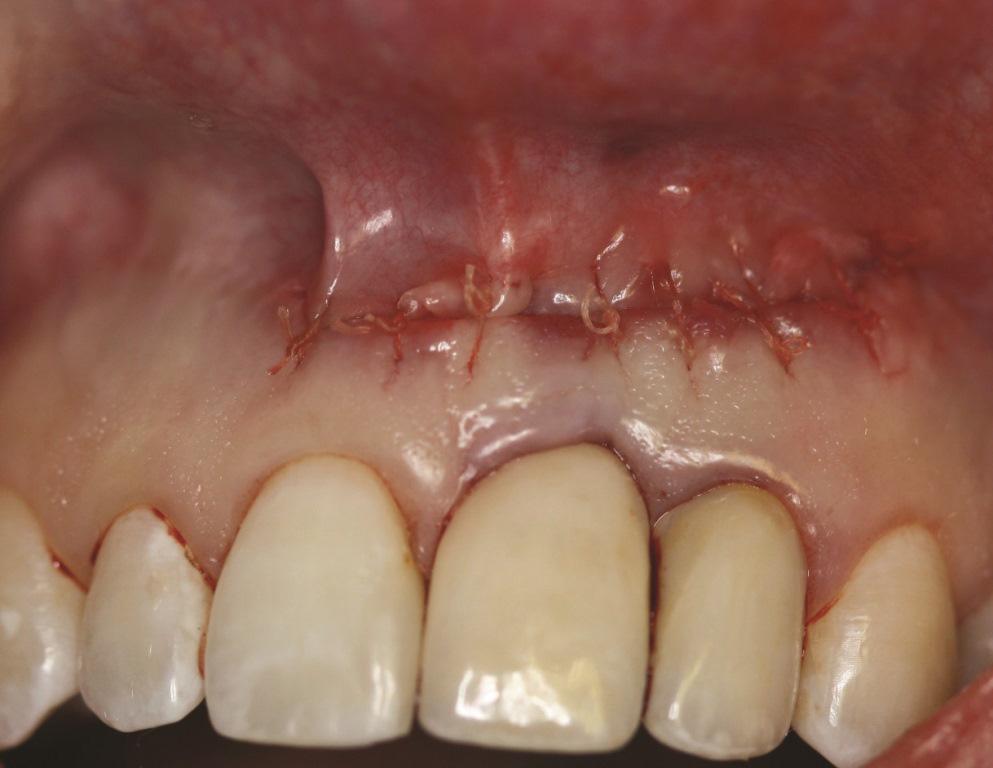
Пациенту в случае 2 был выполнен гребневой разрез с отслаиванием полнослойного лоскута, затем зуб № 1.4 был удален (Фото 9). Кюретаж имплантата проводили по тому же протоколу, что и в случае 1. ЛКА был смешан с небольшим количеством доксициклина и помещен вокруг имплантата (Фото 10). Рассасывающаяся коллагеновая мембрана (не показана) была зафиксирована с помощью пина. Первичное закрытие было достигнуто с использованием швов из расширенного политетрафторэтилена (РПТФЭ) (Фото 11). Немедленный послеоперационный рентгеновский снимок показал костное наполнение и пин (Фото 12).
Фото 9. Случай 2: Отслоение полнотолщинного лоскута, удаление зуба № 1.4, кюретаж и очистка имплантата № 1.3 титановыми скейлерами и титановой щеткой с суспензией доксициклина с физиологическим раствором. Обратите внимание на обширное обнажение резьбы имплантата, приближающееся к верхушке. Подвижности имплантата не отмечалось.
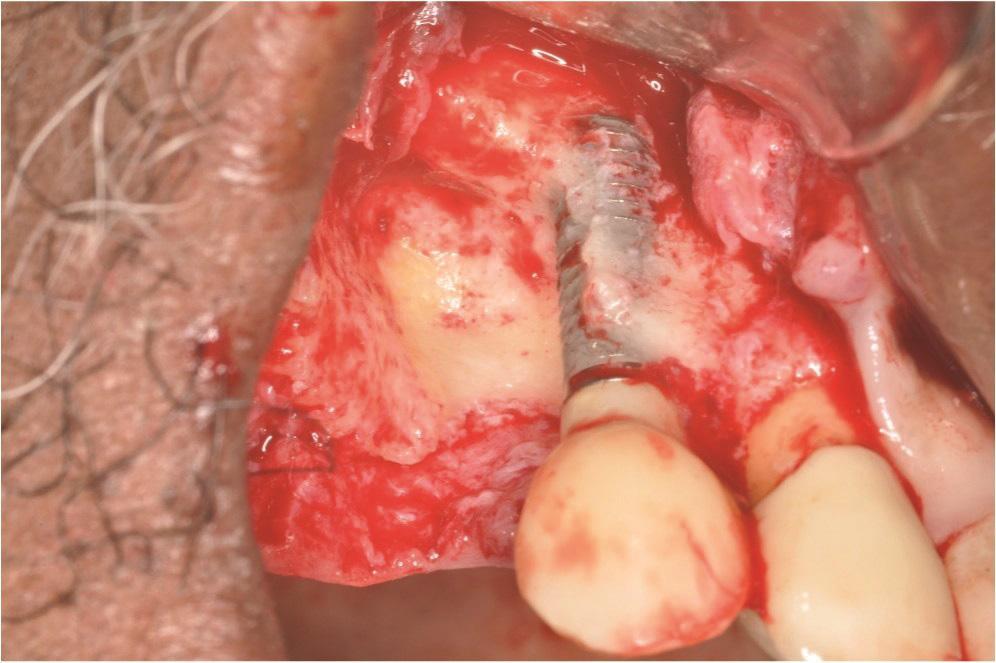
Фото 10. Случай 2: Костный аллотрансплантат ЛКА, смешанный с небольшим количеством доксициклина, помещен на дефект. Трансплантат будет покрыт рассасывающейся коллагеновой мембраной.
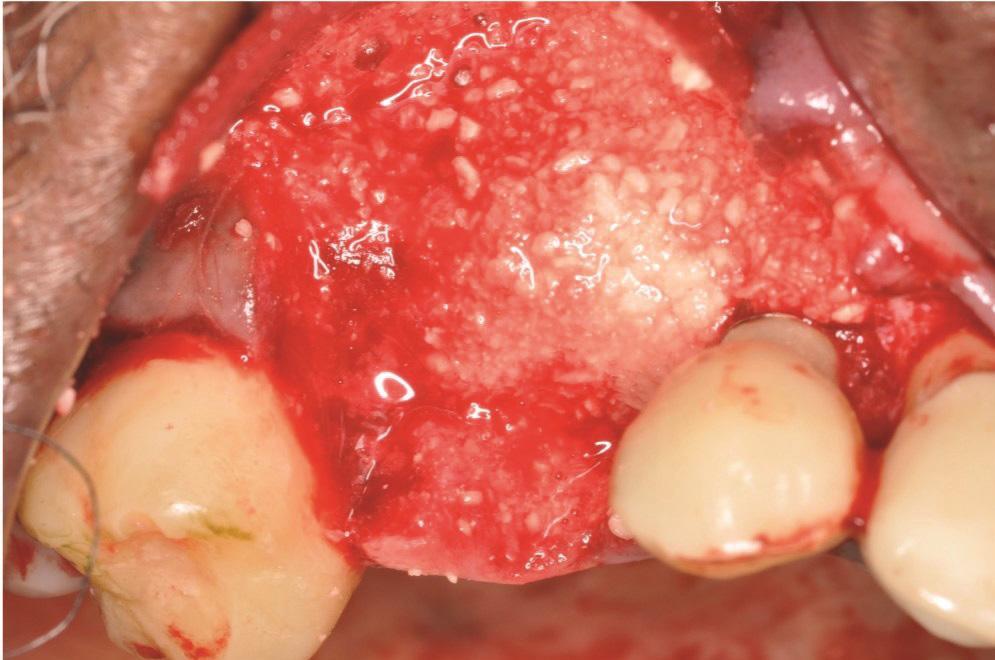
Фото 11. Случай 2: Первичное закрытие достигнуто с использованием швов РПТФЭ.
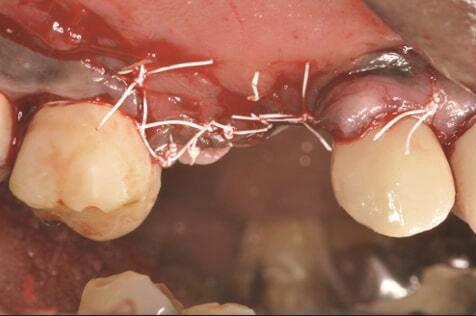
Фото 12. Случай 2: Немедленный послеоперационный рентгеновский снимок. Обратите внимание на пин, фиксирующий коллагеновую мембрану (верхняя левая часть изображения).
После операции обоим пациентам были назначены амоксициллин 500 мг и ибупрофен 800 мг три раза в день в течение 7 дней наряду с хлоргексидином. Были даны послеоперационные инструкции, и пациенты должны были возобновить мягкую чистку зубов через 4 недели. Они получали пародонтологическое поддерживающее лечение каждые 3 месяца и наблюдались после операции в течение 12 месяцев (случай 1) и от 1 до 7 лет (случай 2).
Результаты
Заживление в обоих случаях протекало без осложнений, без неблагоприятных исходов. В случае 1 наблюдалось хорошее заживление с разрешением свищевого хода через 3 месяца после операции. Рентгеновские снимки на контрольных осмотрах через 6 и 9 месяцев продемонстрировали увеличение рентгеноконтрастности кости с полным рентгенологическим костным наполнением к 12 месяцам (Фото 13 и Фото 14).
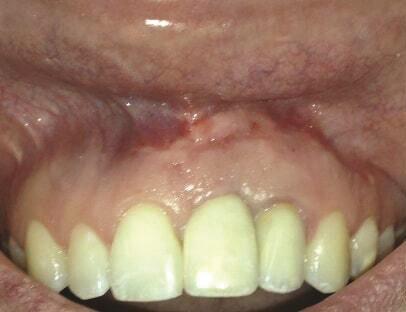
Фото 13 и Фото 14. Случай 1: Вестибулярный вид (Фото 13) и рентгеновский снимок (Фото 14) на контрольном осмотре через 12 месяцев, подтверждающие разрешение РПИ.
Контрольные осмотры через 12 месяцев и 7 лет для случая 2 показали аналогичные улучшения с нормальным заживлением мягких тканей, костным наполнением и нормальной глубиной карманов через 12 месяцев (Фото 15 и Фото 16) и через 7 лет после лечения (Фото 17 и Фото 18).
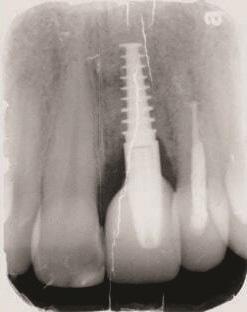
Фото 15 и Фото 16. Клинический вид (Фото 15) и рентгеновский снимок (Фото 16) на контрольном осмотре через 12 месяцев, подтверждающие разрешение периимплантатного дефекта.
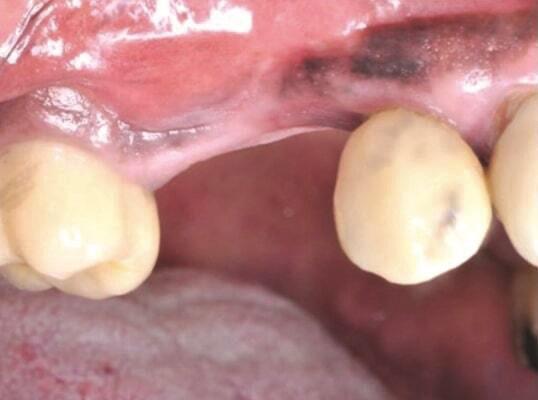
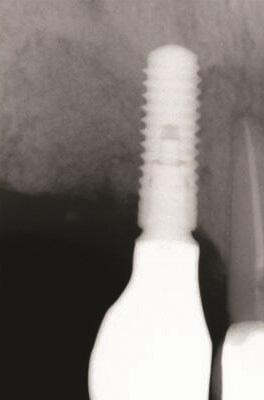
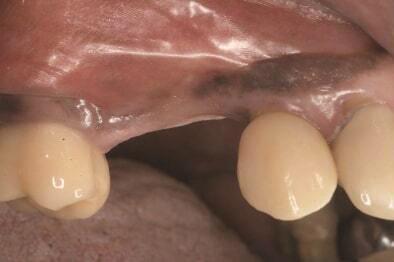
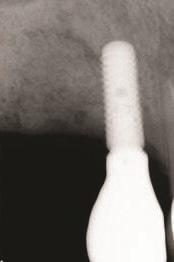
Фото 17 и Фото 18. Случай 2: Клинический вид (Фото 17) и рентгеновский снимок (Фото 18) на контрольном осмотре через 7 лет, подтверждающие стабильность периимплантатной кости.
Обсуждение
Ретроградный периимплантит представляет собой сложную клиническую проблему. Были предложены различные методы лечения, включая хирургический дебридмент, апикоэктомию и НКР. К сожалению, эффективность этих вмешательств остается неясной из-за ограниченных клинических данных, подтверждающих стандартизированные протоколы лечения. Несмотря на отсутствие убедительных данных об эффективности, хирургическое лечение с использованием НКР, как правило, является предпочтительным. В одном систематическом обзоре сообщалось о значительном улучшении стабильности имплантата и костном наполнении при НКР, а также сообщалось о долгосрочных показателях выживаемости имплантатов.
В данной серии случаев оба пациента показали успешное разрешение РПИ, адекватное костное наполнение и стабильность периимплантатных тканей в течение 1–7 лет наблюдения. Рентгенологические оценки продемонстрировали хорошее костное наполнение и стабильную глубину зондирования с течением времени, что подтверждает эффективность регенеративных хирургических подходов в лечении РПИ. Эти результаты согласуются с предыдущими сообщениями, демонстрирующими благоприятные исходы при НКР в лечении периимплантатных дефектов.
Микробиологические данные позволяют предположить, что персистирующие бактериальные инфекции, часто от соседних пораженных зубов, играют ключевую роль в развитии РПИ. Раннее вмешательство, включающее тщательную деконтаминацию участка и антимикробную терапию, может повысить успех лечения. Продолжающиеся исследования сосредоточены на оптимизации регенеративных техник и антимикробных стратегий для улучшения клинических результатов.Использование новых биоматериалов, таких как амнион-хориальные мембраны и биоактивные костные заместители, показало перспективность в улучшении заживления периимплантатных дефектов. Эти материалы обладают противовоспалительными и антибактериальными свойствами, потенциально снижая частоту рецидивов и усиливая регенерацию.
Будущие исследования должны быть направлены на совершенствование протоколов лечения и установление основанных на доказательствах рекомендаций по ведению РПИ. Хотя текущие данные подтверждают хирургическое вмешательство как наиболее эффективное лечение, необходимы дополнительные исследования для обеспечения предсказуемого долгосрочного успеха.
Заключение
Характеризуясь необычной и часто прогрессирующей потерей костной ткани в периапексе дентального имплантата, РПИ представляет собой трудную клиническую проблему. Были предложены различные методы лечения, включая хирургический дебридмент, апикоэктомию и НКР. Хотя текущие данные подтверждают хирургическое вмешательство как наиболее эффективный подход к лечению, результаты следует интерпретировать с осторожностью из-за ограниченного количества долгосрочных исследований, вариабельности протоколов лечения и отсутствия стандартизированных диагностических критериев. Необходимы дальнейшие исследования для установления более предсказуемого и основанного на доказательствах подхода к лечению РПИ.
Авторы:
Anthony L. Neely, DDS, M.Dent.Sc., PhD
Minkie Kim, DDS
Joseph Samona, DDS
Jung I. Yoon, DMD
Bassam M. Kinaia, DDS, MS
Ретроградный периимплантит (РПИ) характеризуется атипичной и часто прогрессирующей потерей костной ткани в периапикальной области дентального имплантата. Хотя, по имеющимся данным, распространенность РПИ ниже, чем маргинального периимплантита, при отсутствии лечения это состояние может привести к потере имплантатов. В данной клинической серии случаев два пациента с различными проявлениями РПИ были пролечены с использованием направленной костной регенерации (НКР) с применением костного трансплантата и коллагеновой мембраны. Долгосрочное наблюдение показало клиническое и рентгенологическое улучшение, которое выразилось в рентгенологическом костном наполнении и уменьшении глубины зондирования вокруг имплантатов. Наблюдения, представленные здесь, позволяют предположить, что НКР при дефектах, вызванных РПИ, является эффективным методом лечения.

Выделяют две формы РПИ: активную и неактивную. Активный РПИ проявляется симптоматической периапикальной рентгенопрозрачностью с увеличением размера очага, тогда как неактивный РПИ проявляется бессимптомной периапикальной рентгенопрозрачностью либо со стабильным или уменьшенным размером очага, либо с чрезмерным расширением остеотомии под имплантат. Распространенность РПИ относительно невысока (0,26% до 0,34%). Этиологические факторы, связанные с РПИ, включают эндодонтические поражения соседних зубов, бактериальную контаминацию во время установки имплантата, остаточную инфекцию в области удаления, избыточное тепловыделение во время операции по установке имплантата, компрессию кости во время операции, чрезмерное расширение подготовки остеотомии и общие заболевания.
В одном исследовании было показано, что чем меньше расстояние между имплантатом и эндодонтически леченным (т.е. после лечения корневых каналов) зубом, тем с большей вероятность возникает ретроградный периимплантит. РПИ достоверно связан со временем между установкой имплантата и лечением корневых каналов зубов, имеющих периапикальное поражение. Эта взаимосвязь также отмечалась для расстояния между соседними зубами и имплантатами. Для снижения риска РПИ рекомендуется минимальное расстояние в 2 мм между имплантатом и соседними зубами после лечения корневых каналов. Кроме того, предлагается отложить установку имплантата как минимум на 4 недели после лечения корневых каналов. Микробный фактор играет критическую роль в патогенезе РПИ, причем Porphyromonas gingivalis, Prevotella intermedia, Corynebacterium, Streptococcus и Klebsiella pneumoniae являются наиболее распространенными микроорганизмами.
Лечение РПИ зависит от точного диагноза этиологии. Ведение включает хирургические подходы, в том числе механический кюретаж костного дефекта и химическую очистку для детоксикации поверхности имплантата. При выборе метода лечения необходимо учитывать факторы конкретного случая, включая тяжесть инфекции, объем потери костной ткани и общее состояние здоровья пациента. В зависимости от ситуации может быть использована комбинация методов лечения для достижения оптимального результата.
В исследованиях сообщалось о предсказуемых результатах использования направленной костной регенерации (НКР) для замещения утраченной кости и стабилизации имплантата в случаях РПИ. В большинстве исследований сообщалось о хорошей выживаемости имплантатов (от 73,2% до 97,4%) через 1–10 лет после лечения. В другом исследовании сообщалось о кумулятивной выживаемости имплантатов 78,3% за 20 лет. Напротив, в других исследованиях сообщалось, что 35,7% имплантатов с РПИ были удалены, причем значительно более высокие показатели удаления наблюдались, когда соседние зубы имели эндодонтическую патологию.
Данная клиническая серия случаев освещает два явно различных проявления РПИ, при которых в качестве выбранного метода лечения использовалась НКР с наблюдением от 1 до 7 лет.
Материалы и методы
Клинические проявления
Пациент 1: Пациентка 30 лет с неосложненным медицинским анамнезом обратилась с имплантатом № 2.1, у которого диагностирован ретроградный периимплантит. Зуб № 2.1 был заменен имплантатом 8 лет назад из-за травмы в анамнезе и неудачного лечения корневых каналов. Имплантат демонстрировал периапикальную рентгенопрозрачность со свищевым ходом, ведущим к верхушке имплантата № 2.1 (Фото 1 и Фото 2). У пациентки была высокая линия улыбки с более длинными клиническими коронками зубов №№ 2.1 и 2.2 по сравнению с №№ 1.2 и 1.1 (Фото 1 и Фото 2).
Фото 1 и Фото 2. Случай 1: Первоначальная клиническая картина с гуттаперчевым штифтом, установленным в апикальный свищ зуба № 2.1 (Фото. 1); рентгеновский снимок, показывающий гуттаперчевый штифт, ведущий к периапикальному поражению (Фото. 2).


Пациент 2: Здоровый пациент мужского пола 63 лет обратился с имплантатом № 1.3, у которого диагностирован РПИ, на который повлиял ранее эндодонтически леченный и сломанный зуб № 1.4 (Фото 3 и Фото 4). Глубина зондирования вокруг имплантата составляла от 4 до 10 мм (Таблица 1), причем наиболее серьезная потеря кости наблюдалась с дистальной стороны имплантата № 1.3 (Фото 3 и Фото 4).
Фото 3 и Фото 4. Случай 2: Первоначальная клиническая картина, показывающая имплантат № 1.3 с РПИ, на который повлиял сломанный зуб № 1.4 (Фото 3); рентгеновский снимок, показывающий сломанный зуб № 1.4 с периапикальным поражением, распространяющимся на дистальную сторону имплантата № 1.3 (Фото 4).


Хирургическая процедура
Варианты лечения были обсуждены с пациентами, и оба дали согласие на лечение, включающее периимплантатный кюретаж и НКР. Каждый пациент получил 600 мг нестероидных противовоспалительных препаратов за 1 час до процедуры и прополоскал рот 15 мл 0,12% глюконата хлоргексидина; местная анестезия была проведена с использованием 2% лидокаина HCl с эпинефрином 1:100 000. В зависимости от проявления поражений форма разрезов и доступ различались для двух случаев.
В случае 1, из-за высокой линии улыбки и асимметричной длины клинических коронок, пациентке был выполнен вестибулярный разрез в области мукогингивального соединения с отслаиванием полнослойного лоскута для доступа к верхушке имплантата. Кюретаж имплантата был выполнен титановыми кюретками и щетками (Фото 5). Поверхность имплантата обрабатывали в течение 2 минут суспензией доксициклина с физиологическим раствором. Периимплантатный дефект был заполнен гранулированным лиофилизированным костным аллотрансплантатом (ЛКА) (Фото 6) и покрыт коллагеновой мембраной (Фото 7). Первичное закрытие лоскута было достигнуто с использованием рассасывающихся швов (Фото 8).
Фото 5. Случай 1: Вестибулярный вид, показывающий периапикальную потерю кости вокруг № 2.1 после кюретажа имплантата и обработки суспензией доксициклина с физиологическим раствором.

Фото 6. Случай 1: Костный аллотрансплантат ЛКА помещен для заполнения дефекта вокруг имплантата.

Фото 7. Случай 1: Рассасывающаяся коллагеновая мембрана помещена для покрытия дефекта.

Фото 8. Случай 1: Первичное закрытие достигнуто с использованием узловых рассасывающихся швов.

Пациенту в случае 2 был выполнен гребневой разрез с отслаиванием полнослойного лоскута, затем зуб № 1.4 был удален (Фото 9). Кюретаж имплантата проводили по тому же протоколу, что и в случае 1. ЛКА был смешан с небольшим количеством доксициклина и помещен вокруг имплантата (Фото 10). Рассасывающаяся коллагеновая мембрана (не показана) была зафиксирована с помощью пина. Первичное закрытие было достигнуто с использованием швов из расширенного политетрафторэтилена (РПТФЭ) (Фото 11). Немедленный послеоперационный рентгеновский снимок показал костное наполнение и пин (Фото 12).
Фото 9. Случай 2: Отслоение полнотолщинного лоскута, удаление зуба № 1.4, кюретаж и очистка имплантата № 1.3 титановыми скейлерами и титановой щеткой с суспензией доксициклина с физиологическим раствором. Обратите внимание на обширное обнажение резьбы имплантата, приближающееся к верхушке. Подвижности имплантата не отмечалось.

Фото 10. Случай 2: Костный аллотрансплантат ЛКА, смешанный с небольшим количеством доксициклина, помещен на дефект. Трансплантат будет покрыт рассасывающейся коллагеновой мембраной.

Фото 11. Случай 2: Первичное закрытие достигнуто с использованием швов РПТФЭ.

Фото 12. Случай 2: Немедленный послеоперационный рентгеновский снимок. Обратите внимание на пин, фиксирующий коллагеновую мембрану (верхняя левая часть изображения).

После операции обоим пациентам были назначены амоксициллин 500 мг и ибупрофен 800 мг три раза в день в течение 7 дней наряду с хлоргексидином. Были даны послеоперационные инструкции, и пациенты должны были возобновить мягкую чистку зубов через 4 недели. Они получали пародонтологическое поддерживающее лечение каждые 3 месяца и наблюдались после операции в течение 12 месяцев (случай 1) и от 1 до 7 лет (случай 2).
Результаты
Заживление в обоих случаях протекало без осложнений, без неблагоприятных исходов. В случае 1 наблюдалось хорошее заживление с разрешением свищевого хода через 3 месяца после операции. Рентгеновские снимки на контрольных осмотрах через 6 и 9 месяцев продемонстрировали увеличение рентгеноконтрастности кости с полным рентгенологическим костным наполнением к 12 месяцам (Фото 13 и Фото 14).
Фото 13 и Фото 14. Случай 1: Вестибулярный вид (Фото 13) и рентгеновский снимок (Фото 14) на контрольном осмотре через 12 месяцев, подтверждающие разрешение РПИ.


Контрольные осмотры через 12 месяцев и 7 лет для случая 2 показали аналогичные улучшения с нормальным заживлением мягких тканей, костным наполнением и нормальной глубиной карманов через 12 месяцев (Фото 15 и Фото 16) и через 7 лет после лечения (Фото 17 и Фото 18).
Фото 15 и Фото 16. Клинический вид (Фото 15) и рентгеновский снимок (Фото 16) на контрольном осмотре через 12 месяцев, подтверждающие разрешение периимплантатного дефекта.


Фото 17 и Фото 18. Случай 2: Клинический вид (Фото 17) и рентгеновский снимок (Фото 18) на контрольном осмотре через 7 лет, подтверждающие стабильность периимплантатной кости.


Обсуждение
Ретроградный периимплантит представляет собой сложную клиническую проблему. Были предложены различные методы лечения, включая хирургический дебридмент, апикоэктомию и НКР. К сожалению, эффективность этих вмешательств остается неясной из-за ограниченных клинических данных, подтверждающих стандартизированные протоколы лечения. Несмотря на отсутствие убедительных данных об эффективности, хирургическое лечение с использованием НКР, как правило, является предпочтительным. В одном систематическом обзоре сообщалось о значительном улучшении стабильности имплантата и костном наполнении при НКР, а также сообщалось о долгосрочных показателях выживаемости имплантатов.
В данной серии случаев оба пациента показали успешное разрешение РПИ, адекватное костное наполнение и стабильность периимплантатных тканей в течение 1–7 лет наблюдения. Рентгенологические оценки продемонстрировали хорошее костное наполнение и стабильную глубину зондирования с течением времени, что подтверждает эффективность регенеративных хирургических подходов в лечении РПИ. Эти результаты согласуются с предыдущими сообщениями, демонстрирующими благоприятные исходы при НКР в лечении периимплантатных дефектов.
Микробиологические данные позволяют предположить, что персистирующие бактериальные инфекции, часто от соседних пораженных зубов, играют ключевую роль в развитии РПИ. Раннее вмешательство, включающее тщательную деконтаминацию участка и антимикробную терапию, может повысить успех лечения. Продолжающиеся исследования сосредоточены на оптимизации регенеративных техник и антимикробных стратегий для улучшения клинических результатов.Использование новых биоматериалов, таких как амнион-хориальные мембраны и биоактивные костные заместители, показало перспективность в улучшении заживления периимплантатных дефектов. Эти материалы обладают противовоспалительными и антибактериальными свойствами, потенциально снижая частоту рецидивов и усиливая регенерацию.
Будущие исследования должны быть направлены на совершенствование протоколов лечения и установление основанных на доказательствах рекомендаций по ведению РПИ. Хотя текущие данные подтверждают хирургическое вмешательство как наиболее эффективное лечение, необходимы дополнительные исследования для обеспечения предсказуемого долгосрочного успеха.
Заключение
Характеризуясь необычной и часто прогрессирующей потерей костной ткани в периапексе дентального имплантата, РПИ представляет собой трудную клиническую проблему. Были предложены различные методы лечения, включая хирургический дебридмент, апикоэктомию и НКР. Хотя текущие данные подтверждают хирургическое вмешательство как наиболее эффективный подход к лечению, результаты следует интерпретировать с осторожностью из-за ограниченного количества долгосрочных исследований, вариабельности протоколов лечения и отсутствия стандартизированных диагностических критериев. Необходимы дальнейшие исследования для установления более предсказуемого и основанного на доказательствах подхода к лечению РПИ.
Авторы:
Anthony L. Neely, DDS, M.Dent.Sc., PhD
Minkie Kim, DDS
Joseph Samona, DDS
Jung I. Yoon, DMD
Bassam M. Kinaia, DDS, MS































































































































































0 комментариев