Поскольку лечение с использованием дентальных имплантатов уже стало неким мейнстримом в стоматологической практике, сегодняшняя цель врачей-стоматологов – это обеспечить индивидуализированный подход к каждому пациенту уже после лечения, на этапах мониторинга, в форме специфических протоколов поддерживающей терапии. В данной статье описан клинический случай 13-летней поддержки пациента с патологиями агрессивного генерализированного пародонтита и бруксизма после его стоматологической реабилитации с использованием дентальных имплантатов Branemark TiUnite, которые характеризуются наличием нетекстурированной шейки.
Курение, низкая плотность костной ткани, действие радиации, влияние инфекционных факторов, относительная перегрузка, наличие пародонтита в анамнезе и парафункциональные нарушения по типу бруксизма – все это факторы риска, которые в определённых случаях могут спровоцировать потерю дентального имплантата. Данные систематического обзора свидетельствуют, что пациенты с парафункциональными нарушениями и наличием пародонтита в анамнезе характеризуются в разы высшим уровнем риска потери эндоосальной конструкции по сравнению с теми, у которых бруксизм был диагностирован без сопутствующего пародонтита. В течение первого года после установки вокруг имплантата отмечается небольшая потеря уровня маргинальной кости, что, очевидно, связано с ее адаптацией и ремоделированием после хирургического вмешательства. В ходе функционирования имплантата данная потеря сводится к минимуму, и не является клинически значимой. Исходя из сформированных критериев успешности, уровень костной редукции в пери-имплантатной области должен составлять не более 1,0 мм в первый год после нагрузки опоры, не более 0,2 мм в каждый последующий в ходе долгосрочного периода наблюдения. Продолжительная потеря уровня костной ткани с клиническими признаками инфицирования периимплантатной области, а именно с симптомами кровотечения и нагноения, именуется периимплантитом, независимо от этиологии развития такового. Исходя из разных определений данной патологии, распространённость таковой колеблется в диапазоне 7,7-39,7%. Пациенты со здоровым состоянием пародонта, а также таковые, у кого пародонтит развивается в качестве хронического процесса, практически не отличаются, с точки зрения перспективных прогнозированных результатов успешности использования у них дентальных имплантатов. Но если же патология пародонтита носит генерализированный агрессивный характер, риск развития периимплантита увеличивается в несколько раз, что, в свою очередь, приводит к прогрессирующей потере костной ткани и более низкой выживаемости имплантатов. Интересно, что при адекватной поддерживающей терапии наличие периодонтита в анамнезе почти никак негативно не сказывается на показателях выживаемости имплантатов в сравнительно короткие периоды наблюдения. В долгосрочной же перспективе, у пациентов, страдающих раннее от пародонтита риск компрометации состояния имплантатов увеличивается почти в два раза по сравнению с больными, у которых патологии пародонта предварительно отсутствовали. Аналогичная ситуация отмечается и у пациентов с бруксизмом: среди таких пациентов более часто отмечается технические осложнения, связанные с дентальными имплантатами. В данной статье описан случай 13-летней поддержки и мониторинга пациента с патологиями генерализированного агрессивного пародонтита и бруксизма, который был реабилитирован посредством Branemark TiUnite (Nobel Biocare, Yorba Linda, CA, США). На верхней челюсти у него был зафиксирован протез с кросс-дуговой фиксацией, а на нижней – частичный протез в условиях сохранения нескольких собственных зубов.
Клинический случай
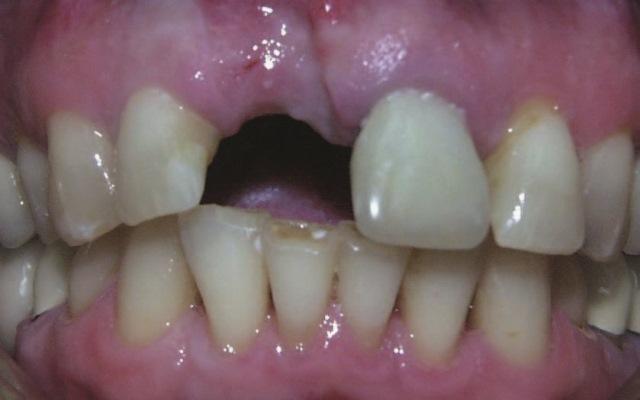
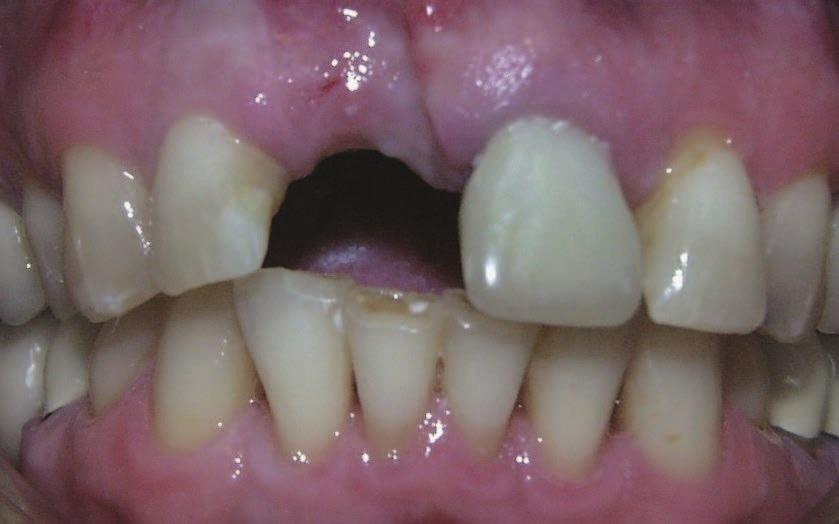
57-летняя женщина с наличием в анамнезе генерализированного агрессивного пародонтита обратилась в нашу клинику с целью консультации. Несмотря на то, что пациентке проводилась надлежащая обработка зубов, несколько оперативных вмешательств, а сама она принимала необходимые антибиотики, у нее продолжалась отмечаться прогрессирующая потеря костной ткани. Через два года после первичной консультации и длительного лечения в ходе комплексного обследования у больной были верифицированы рецидивирующие пародонтальные абсцессы с продолжающейся редукцией уровня костной ткани из-за прогрессирования хронической патологии пародонта (фото 1). Кроме того, все данные симптомы осложнялись из-за чрезмерной подвижности зубов, поражения области фуркации корней верхних моляров и окклюзионной нестабильности, спровоцированной наличием бруксизма.
Фото 1. Фронтальный вид до лечения.
Предварительно с пациенткой обсудили все возможные варианты лечения, начиная от полных съемных протезов до частичных и съемных протезов с опорой на имплантатах. В конце концов, больная согласилась на реабилитацию посредством ортопедических конструкций с опорой на внутрикостные дентальные имплантаты. Было решено удалить все оставшиеся зубы верхней челюсти. Пациентка также понимала, что из-за пародонтита и бруксизма риск возможной неуспешности лечения все равно остается достаточно высоким, а также то, что собственные зубы могут играть негативную роль резервуара пародонто-патогенных микроорганизмов. В среднем успешность лечения пациентов с использованием имплантатов составляет 98,05% в 10-летней перспективе, но, учитывая все вышеупомянутые сложности в данном клиническом случае, показатель успешности в 10-летней перспективе не превышал 90%. Также результат лечения зависит от того, насколько пациент строго придерживается рекомендаций врача, поддерживает соответствующий уровень гигиены и является на контрольные визиты к стоматологу.
После комплексного клинического и рентгенологического обследования в области эндодонтически скомпрометированного и удаленного в 1999 году левого центрального резца верхней челюсти был установлен имплантат Branemark System MkIII, Nobel Biocare. Через три месяца после удаления оставшихся зубов на верхнюю челюсть установили 7 имплантатов (Nobel Biocare). В это же посещение провели экстракцию подвижных зубов в правом сегменте нижней челюсти. Через четыре месяца после их удаления на нижней челюсти провели установку трех дентальных имплантатов. Потребности в аугментанции челюстей в области всех участков попросту не наблюдалось. Все установленные внутрикостные опоры полностью интегрировались и демонстрировали отличные параметры стабильности, величина их клинического торка через три месяца достигала 35 Нсм. После этого провели фиксацию формирователей десен (фото 2 и 3). Через три года функции пациентке был переделан протез на верхней челюсти из-за скола керамики в эстетической области. После этого больной также была сделана ночная каппа, и каких-либо осложнений с ортопедической конструкцией не наблюдалось на протяжении последующих 11 лет.
Фото 2. Вид имплантатов, установленных на верхней челюсти.
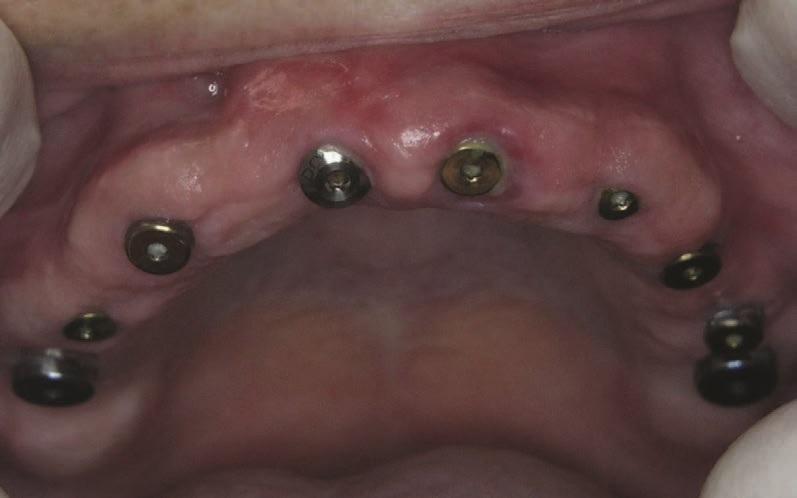
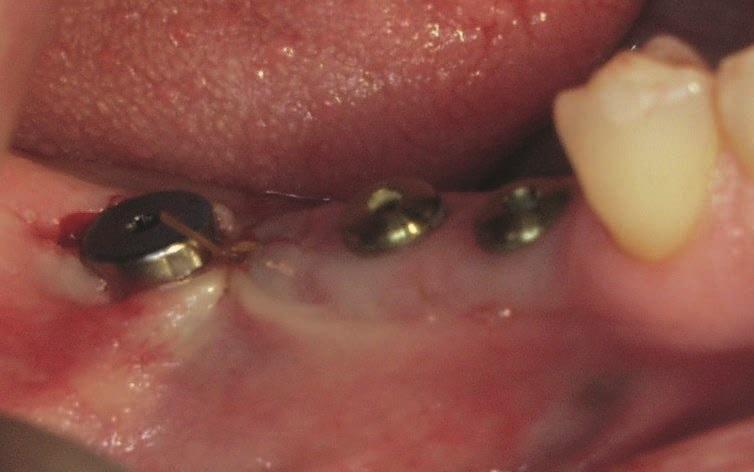
Фото 3. Вид имплантатов, установленных на нижней челюсти.
Тем не менее, в области первого моляра нижней челюсти наблюдалась прогрессирующая потеря костной ткани с поражением фуркации зуба по 3 классу (фото 4). В 2003 на данном участке была проведена резекция корня, и после этого некоторое время зуб оставался стабильным (фото 5).
Фото 4. Вид зубов, пораженных пародонтитом в левом сегменте нижней челюсти.
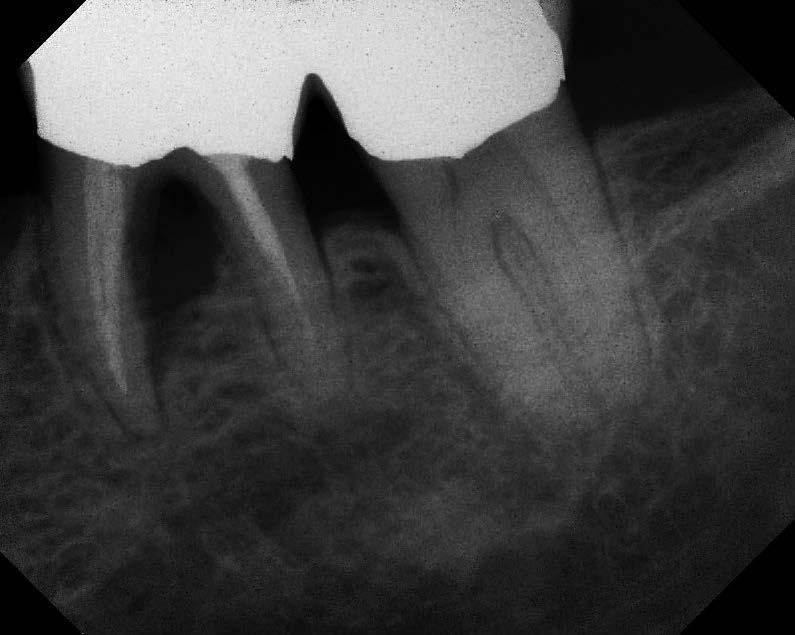
Фото 5. Резекция корня первого моляра нижней челюсти слева.
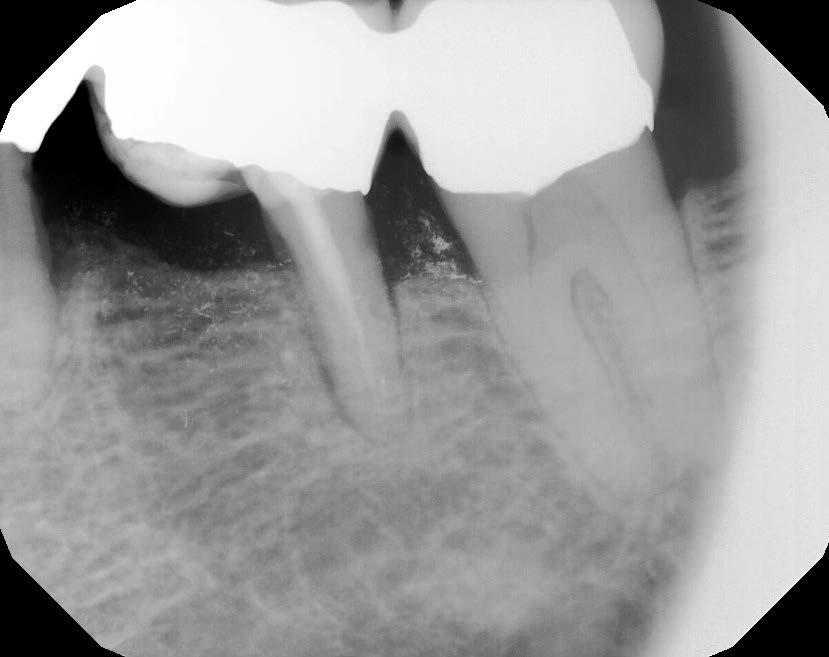
При этом было отмечено некое снижение активности пародонтита, очевидно связанное с удалением значительного количества зубов, которые служили резервуарами для пародонто-патологических бактерий, а также связанное с ежедневным приемом 100 мг миноциклина начиная с 2004 года. В 2008 больная перешла на дозу 100 мг доксициклина, которую принимала в четыре приема на протяжении дня ежедневно. Очевидно, что в связи с этим потеря костной ткани в области не пораженных периимплантитом конструкций составляла не более 0,5 мм. Однако с левой стороны верхней челюсти все же были отмечены явления периимплантитного поражения, что привело к тому, что через 3 года после установки данные имплантаты были потеряны. Причинами такого исхода также могли быть слишком близкое положение имплантатов друг к другу, а также дефицит места в данной области для адекватного проведения гигиены (фото 6 и 7).
Фото 6. Два имплантата, пораженные периимплантитом, на верхней челюсти.
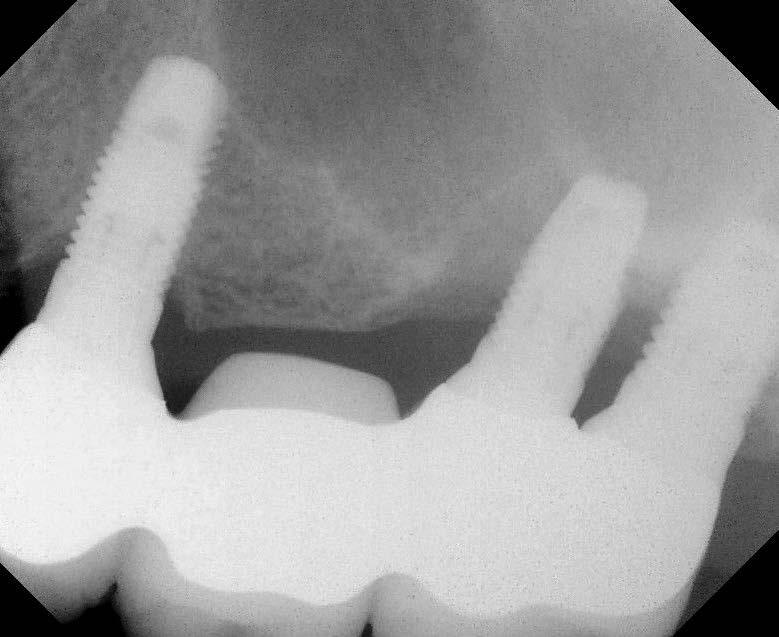
Фото 7. Эксплантация.
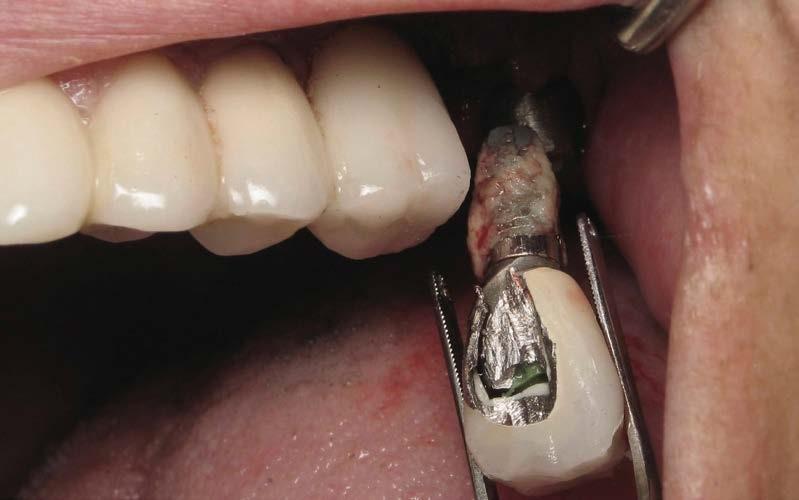
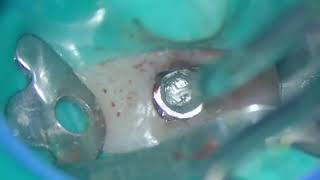
Повторная установка инфраконструкций не проводилась, а протез просто был модифицирован нависающей частью в области моляров. Через 6 лет функционирования, явления периимплантита также наблюдались в области титановой опоры, установленной на месте второго моляра нижней челюсти (фото 8).
Фото 8. Потеря костной ткани в результате периимплантита в области второго моляра на нижней челюсти слева.
Такое осложнение могло быть связано с фактом цементной фиксации протетического элемента в данной области. После сепарации лоскута провели обработку поверхности имплантата лимонной кислотой, а стенки дефекта модифицировали, перекрыв их частью лоскута. Через 7 лет на контрольном осмотре провели обработку данной области посредством поддесневой ирригации микрочастицами миноциклина гидрохлорида (Arestin, OraPharma, Valeant Pharmaceuticals International, Laval, Quebec, Canada). Через год данный участок практически полностью восстановился (фото 9).
Фото 9. Восстановление области второго моляра на нижней челюсти слева.
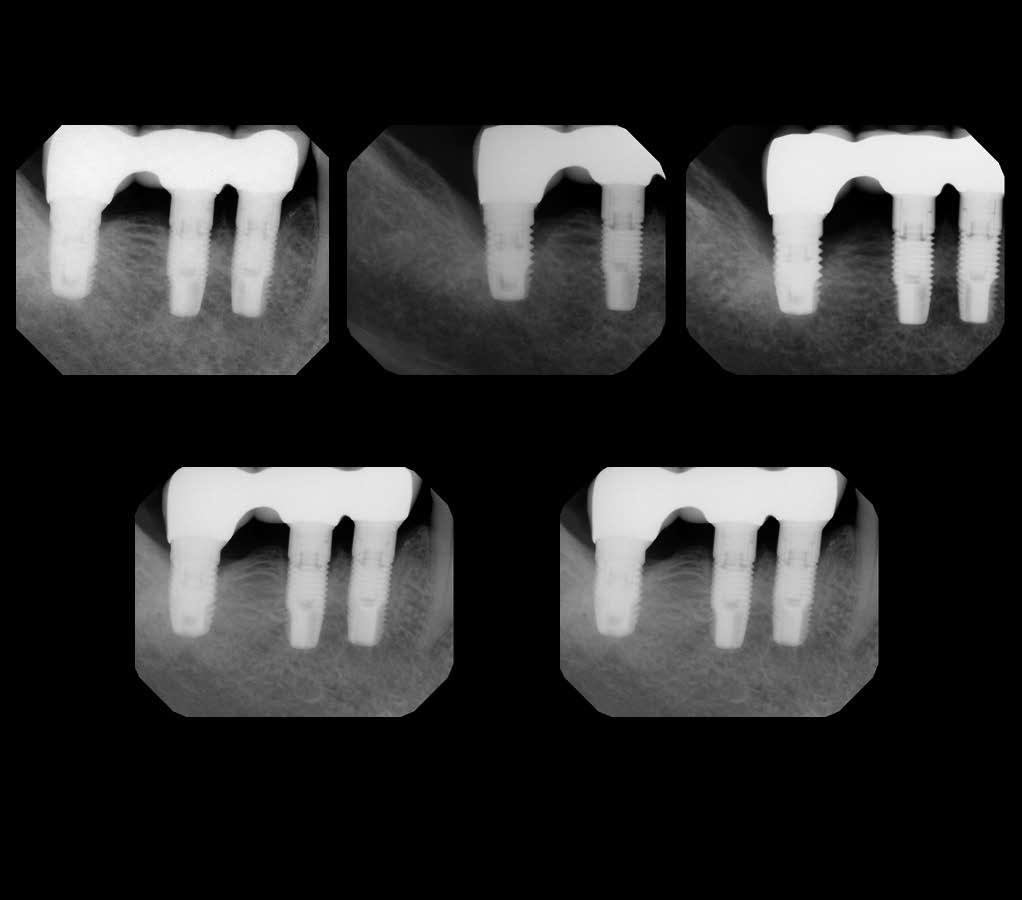
Благодаря активной поддерживающей пародонтальной терапии в ходе клинического осмотра и рентгенологического контроля удалось подтвердить успешность результатов функционирования оставшихся дентальных имплантатов в 8-летней ретроспективе (фото 10-12).
Фото 10. Новый протез: рентгенограммы.
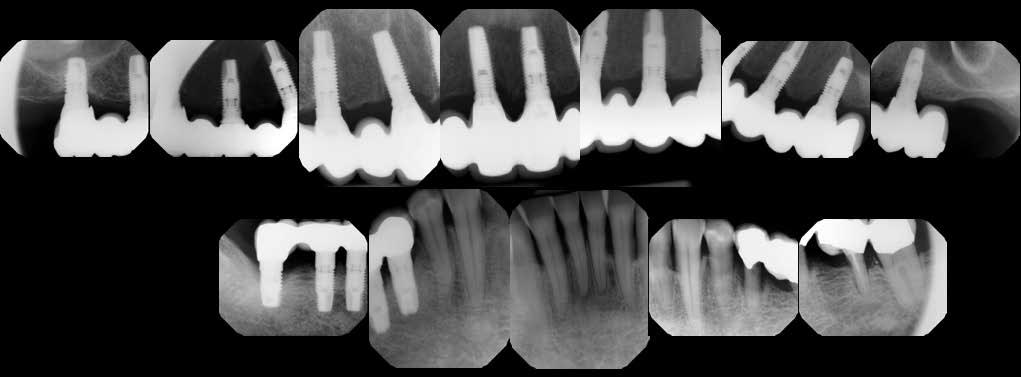
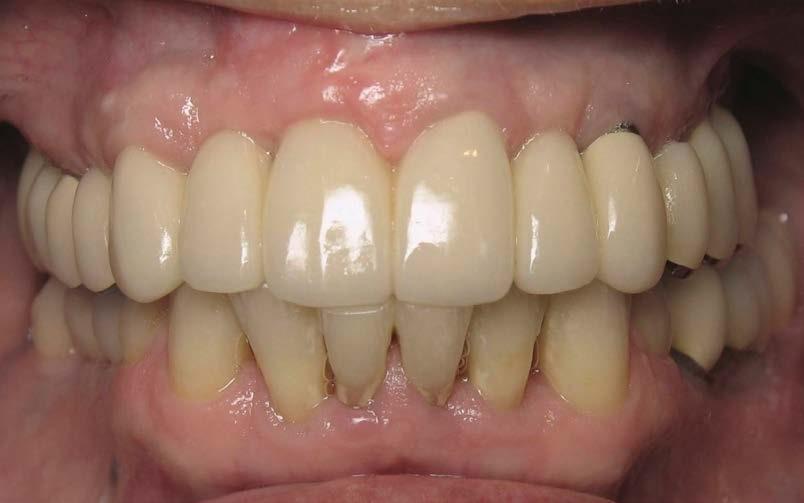
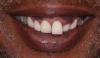
Фото 11. Новый протез: вид спереди через 8 лет.
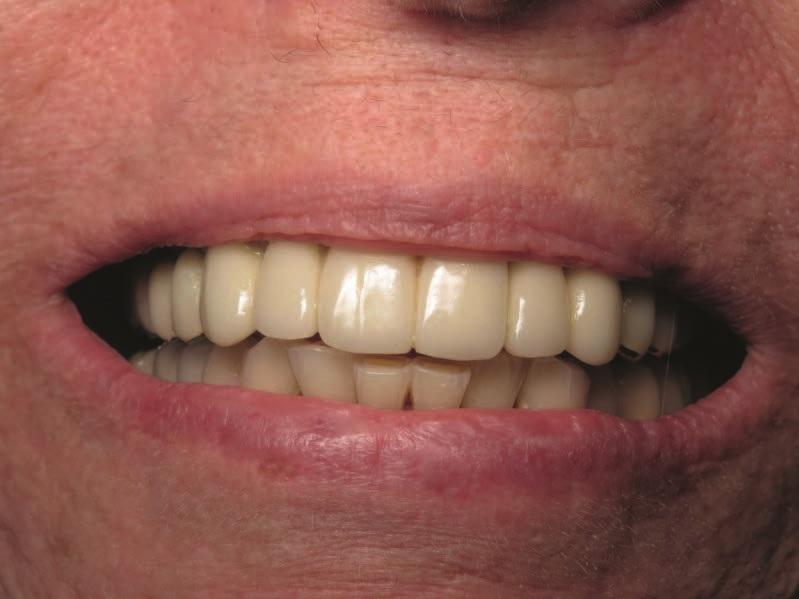
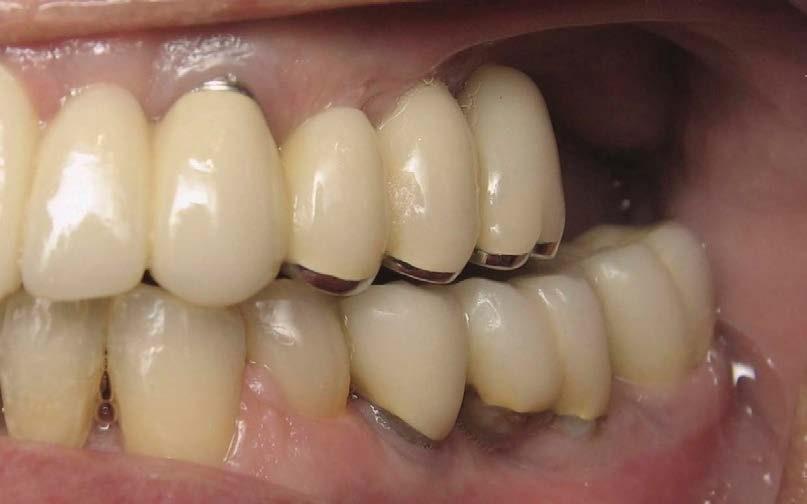
Фото 12. Новый протез: вид сбоку через 8 лет.
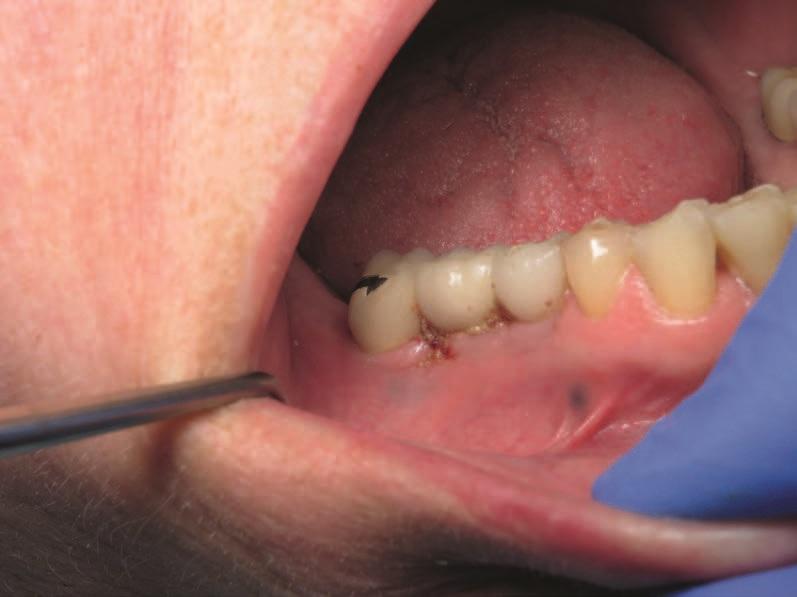
В ходе контрольного визита через 13 лет после имплантации опора в области второго моляра продолжала оставаться стабильной. Результаты клинического осмотра и рентгенологического контроля подтвердили достаточный функциональный уровень инфраконструкции, а также надлежащий уровень гигиены у пациента (фото 13-15).
Фото 13. Вид через 13 лет.
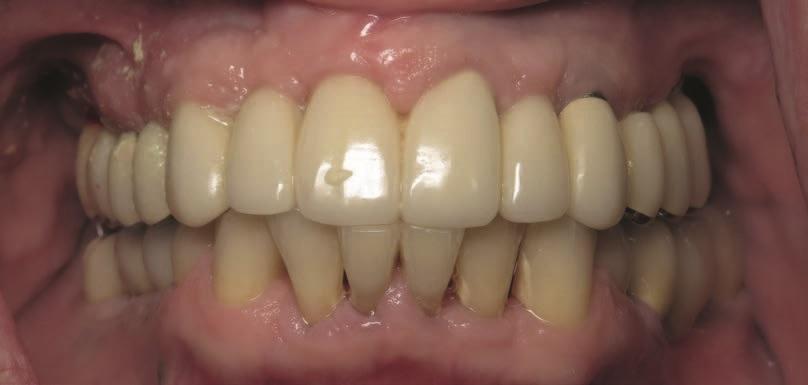
Фото 14. Вид через 13 лет.
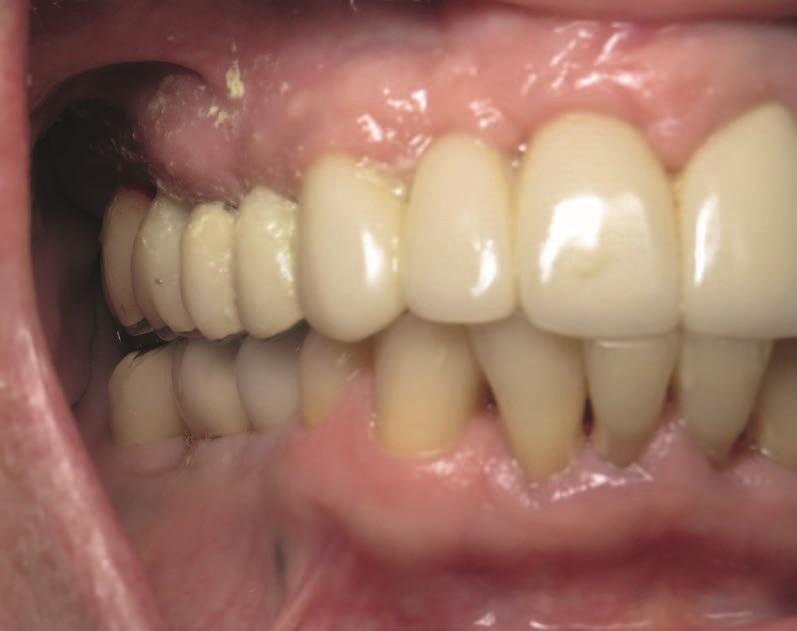
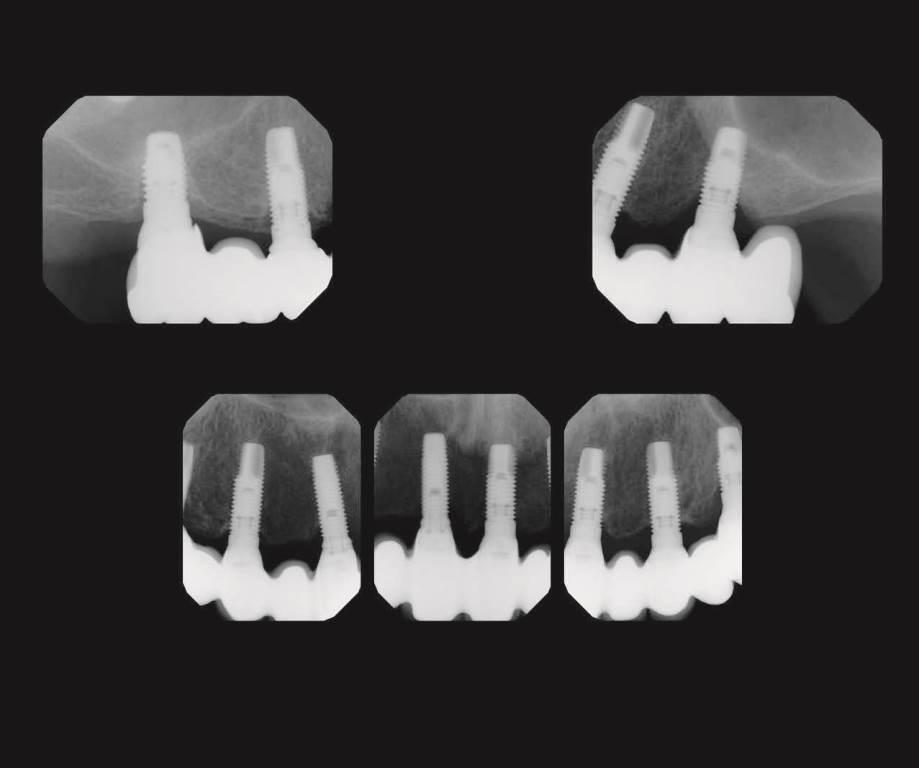
Фото 15.
а. Рентгенограммы области моляров верхней челюсти через 13 лет.
b. Рентгенограммы области моляра нижней челюсти от начала периимплантита до периода 13 года функционирования имплантата.
Обсуждение
На самом деле, мало что известно о долгосрочном прогнозе функционирования имплантатов с оксидированной поверхностью, особенно если таковые использовались при реабилитации пациентов с пародонтитом. В данном случае ситуация была еще сложнее, ведь кроме агрессивного пародонтита у пациента отмечался бруксизм. Поддерживающая пародонтальная терапия, адекватная оценка всех потенциальных рисков лечения и продолжительный мониторинг за пациентом помогли добиться достаточно хороших результатов комплексной реабилитации. Потеря двух имплантатов на протяжении 3-х летнего периода аналогична уже ранее описанным случаям в литературе. В данном случае свою роль также сыграли факторы близости позиционирования имплантатов и цементный тип фиксации супраконструкций. Независимо от различных предпринятых мер, уровень редукции костной ткани в периимплантатной области может значительно варьировать. Поэтому врачу нужно обеспечить условия не только для ретенции исходного уровня резидуального гребня, но и для формирования достаточного мягкотканного барьера вокруг установленных абатментов.
Однако, даже в случае реализации данных аспектов потеря костной ткани все равно может продолжаться с прогрессирующей скоростью, и объяснить это явление в полной мере пока что никому не удалось. По мнению некоторых авторов, факторами, ассоциированными с потерей маргинальной кости, являются хирургическая травма, восстановление параметра биологической ширины, отсутствие пассивной подгонки супраконструкции, наличие микрозазора между имплантатом и абатментом, а также окклюзионная перегрузка. Непрерывная потеря костного объема с клиническими признаками инфицирования, кровотечения и нагноения идентифицируется как периимплантит, независимо от причин возникновения данных последствий. Исходя из различных определений данной патологии, ее распространённость колеблется в диапазоне 7,7-39,7%, хотя некоторые авторы считают данные цифры слишком уж завышенными. В данное время большинство имплантатов характеризуются специфической обработкой поверхности по типу ее абразивного улучшения, протравливания, анодного окисления и комбинации данных методов, чтобы спровоцировать более позитивную реакцию кости на установленный титановый элемент. Умеренно шероховатая, высококристаллическая и фосфатно-обогащенная поверхность имплантатов TiUnite характеризуется наличием увеличенного слоя диоксида титана, который вместе с определенной шероховатостью помогает увеличить площадь остеоинтеграции опорного элемента, а также уровень адгезии клеток-остеобластов MG-63. Были высказаны опасения, что потеря костной ткани и последующее обнажение шероховатой поверхности имплантата может спровоцировать развитие периимплантатной патологии, что было подтверждено в ходе исследований на животных, но осталось недоказанным при использовании подобных имплантатов в ходе реабилитации стоматологических пациентов.
В описанном выше клиническом случае пациентка желала заменить безнадёжные зубы на имплантаты, но при этом оставить часть собственных единиц зубного ряда в полости рта. Учитывая факт пародонтита, больная была предупреждена о риске такого подхода. Результаты лечения по большей мере зависели от того, насколько пациентка будет придерживаться сформированной для нее программы поддерживающего пародонтологического лечения. В области 47 зуба со временем пришлось провести сепарацию лоскута для удаления остатков цемента, а также обеспечить при этом лучшие условия для антибактериальной терапии в области имплантата. В конце концов, удалось добиться достаточно стабильных результатов вмешательства, что также может свидетельствовать о том, что шероховатая поверхность – это не всегда главный фактор, провоцирующий развитие периимплантита. Для снижения риска развития потенциальных биологических и технических осложнений пациентке также была изготовлена каппа на ночь. Данные систематического осмотра свидетельствуют о том, что бруксизм чаще провоцирует развитие технических осложнений, нежели биологических. Но все же стоит помнить, что риск перегрузки имплантата у больных с парафункциями все же значительно выше, чем у пациентов без таковых, что, в свою очередь, может повлиять на качество остеоинтеграции. Помня об этом, следует контролировать адекватность распределения жевательной нагрузки, и, кроме того, всегда проверять уровень гигиены полости рта, дабы избежать потенциального риска развития перимиплантита.
Выводы
Лечение с использованием имплантатов у пациентов с активным заболеванием пародонта и бруксизмом не является противопоказанным при условии обеспечения адекватного контроля инфекции и имплементации индивидуальной программы поддерживающей терапии. Результаты вышеизложенного случая иллюстрируют хорошие клинические и рентгенологические результаты имплантации в долгосрочной перспективе, а также свидетельствуют о том, что шероховатая поверхность имплантата не является фактором, определяющим динамику и объем потери костной ткани в периимплантатной области.
Авторы: David French, Erta Xhanari
Поскольку лечение с использованием дентальных имплантатов уже стало неким мейнстримом в стоматологической практике, сегодняшняя цель врачей-стоматологов – это обеспечить индивидуализированный подход к каждому пациенту уже после лечения, на этапах мониторинга, в форме специфических протоколов поддерживающей терапии. В данной статье описан клинический случай 13-летней поддержки пациента с патологиями агрессивного генерализированного пародонтита и бруксизма после его стоматологической реабилитации с использованием дентальных имплантатов Branemark TiUnite, которые характеризуются наличием нетекстурированной шейки.

Курение, низкая плотность костной ткани, действие радиации, влияние инфекционных факторов, относительная перегрузка, наличие пародонтита в анамнезе и парафункциональные нарушения по типу бруксизма – все это факторы риска, которые в определённых случаях могут спровоцировать потерю дентального имплантата. Данные систематического обзора свидетельствуют, что пациенты с парафункциональными нарушениями и наличием пародонтита в анамнезе характеризуются в разы высшим уровнем риска потери эндоосальной конструкции по сравнению с теми, у которых бруксизм был диагностирован без сопутствующего пародонтита. В течение первого года после установки вокруг имплантата отмечается небольшая потеря уровня маргинальной кости, что, очевидно, связано с ее адаптацией и ремоделированием после хирургического вмешательства. В ходе функционирования имплантата данная потеря сводится к минимуму, и не является клинически значимой. Исходя из сформированных критериев успешности, уровень костной редукции в пери-имплантатной области должен составлять не более 1,0 мм в первый год после нагрузки опоры, не более 0,2 мм в каждый последующий в ходе долгосрочного периода наблюдения. Продолжительная потеря уровня костной ткани с клиническими признаками инфицирования периимплантатной области, а именно с симптомами кровотечения и нагноения, именуется периимплантитом, независимо от этиологии развития такового. Исходя из разных определений данной патологии, распространённость таковой колеблется в диапазоне 7,7-39,7%. Пациенты со здоровым состоянием пародонта, а также таковые, у кого пародонтит развивается в качестве хронического процесса, практически не отличаются, с точки зрения перспективных прогнозированных результатов успешности использования у них дентальных имплантатов. Но если же патология пародонтита носит генерализированный агрессивный характер, риск развития периимплантита увеличивается в несколько раз, что, в свою очередь, приводит к прогрессирующей потере костной ткани и более низкой выживаемости имплантатов. Интересно, что при адекватной поддерживающей терапии наличие периодонтита в анамнезе почти никак негативно не сказывается на показателях выживаемости имплантатов в сравнительно короткие периоды наблюдения. В долгосрочной же перспективе, у пациентов, страдающих раннее от пародонтита риск компрометации состояния имплантатов увеличивается почти в два раза по сравнению с больными, у которых патологии пародонта предварительно отсутствовали. Аналогичная ситуация отмечается и у пациентов с бруксизмом: среди таких пациентов более часто отмечается технические осложнения, связанные с дентальными имплантатами. В данной статье описан случай 13-летней поддержки и мониторинга пациента с патологиями генерализированного агрессивного пародонтита и бруксизма, который был реабилитирован посредством Branemark TiUnite (Nobel Biocare, Yorba Linda, CA, США). На верхней челюсти у него был зафиксирован протез с кросс-дуговой фиксацией, а на нижней – частичный протез в условиях сохранения нескольких собственных зубов.
Клинический случай
57-летняя женщина с наличием в анамнезе генерализированного агрессивного пародонтита обратилась в нашу клинику с целью консультации. Несмотря на то, что пациентке проводилась надлежащая обработка зубов, несколько оперативных вмешательств, а сама она принимала необходимые антибиотики, у нее продолжалась отмечаться прогрессирующая потеря костной ткани. Через два года после первичной консультации и длительного лечения в ходе комплексного обследования у больной были верифицированы рецидивирующие пародонтальные абсцессы с продолжающейся редукцией уровня костной ткани из-за прогрессирования хронической патологии пародонта (фото 1). Кроме того, все данные симптомы осложнялись из-за чрезмерной подвижности зубов, поражения области фуркации корней верхних моляров и окклюзионной нестабильности, спровоцированной наличием бруксизма.
Фото 1. Фронтальный вид до лечения.

Предварительно с пациенткой обсудили все возможные варианты лечения, начиная от полных съемных протезов до частичных и съемных протезов с опорой на имплантатах. В конце концов, больная согласилась на реабилитацию посредством ортопедических конструкций с опорой на внутрикостные дентальные имплантаты. Было решено удалить все оставшиеся зубы верхней челюсти. Пациентка также понимала, что из-за пародонтита и бруксизма риск возможной неуспешности лечения все равно остается достаточно высоким, а также то, что собственные зубы могут играть негативную роль резервуара пародонто-патогенных микроорганизмов. В среднем успешность лечения пациентов с использованием имплантатов составляет 98,05% в 10-летней перспективе, но, учитывая все вышеупомянутые сложности в данном клиническом случае, показатель успешности в 10-летней перспективе не превышал 90%. Также результат лечения зависит от того, насколько пациент строго придерживается рекомендаций врача, поддерживает соответствующий уровень гигиены и является на контрольные визиты к стоматологу.
После комплексного клинического и рентгенологического обследования в области эндодонтически скомпрометированного и удаленного в 1999 году левого центрального резца верхней челюсти был установлен имплантат Branemark System MkIII, Nobel Biocare. Через три месяца после удаления оставшихся зубов на верхнюю челюсть установили 7 имплантатов (Nobel Biocare). В это же посещение провели экстракцию подвижных зубов в правом сегменте нижней челюсти. Через четыре месяца после их удаления на нижней челюсти провели установку трех дентальных имплантатов. Потребности в аугментанции челюстей в области всех участков попросту не наблюдалось. Все установленные внутрикостные опоры полностью интегрировались и демонстрировали отличные параметры стабильности, величина их клинического торка через три месяца достигала 35 Нсм. После этого провели фиксацию формирователей десен (фото 2 и 3). Через три года функции пациентке был переделан протез на верхней челюсти из-за скола керамики в эстетической области. После этого больной также была сделана ночная каппа, и каких-либо осложнений с ортопедической конструкцией не наблюдалось на протяжении последующих 11 лет.
Фото 2. Вид имплантатов, установленных на верхней челюсти.

Фото 3. Вид имплантатов, установленных на нижней челюсти.

Тем не менее, в области первого моляра нижней челюсти наблюдалась прогрессирующая потеря костной ткани с поражением фуркации зуба по 3 классу (фото 4). В 2003 на данном участке была проведена резекция корня, и после этого некоторое время зуб оставался стабильным (фото 5).
Фото 4. Вид зубов, пораженных пародонтитом в левом сегменте нижней челюсти.

Фото 5. Резекция корня первого моляра нижней челюсти слева.

При этом было отмечено некое снижение активности пародонтита, очевидно связанное с удалением значительного количества зубов, которые служили резервуарами для пародонто-патологических бактерий, а также связанное с ежедневным приемом 100 мг миноциклина начиная с 2004 года. В 2008 больная перешла на дозу 100 мг доксициклина, которую принимала в четыре приема на протяжении дня ежедневно. Очевидно, что в связи с этим потеря костной ткани в области не пораженных периимплантитом конструкций составляла не более 0,5 мм. Однако с левой стороны верхней челюсти все же были отмечены явления периимплантитного поражения, что привело к тому, что через 3 года после установки данные имплантаты были потеряны. Причинами такого исхода также могли быть слишком близкое положение имплантатов друг к другу, а также дефицит места в данной области для адекватного проведения гигиены (фото 6 и 7).
Фото 6. Два имплантата, пораженные периимплантитом, на верхней челюсти.

Фото 7. Эксплантация.

Повторная установка инфраконструкций не проводилась, а протез просто был модифицирован нависающей частью в области моляров. Через 6 лет функционирования, явления периимплантита также наблюдались в области титановой опоры, установленной на месте второго моляра нижней челюсти (фото 8).
Фото 8. Потеря костной ткани в результате периимплантита в области второго моляра на нижней челюсти слева.

Такое осложнение могло быть связано с фактом цементной фиксации протетического элемента в данной области. После сепарации лоскута провели обработку поверхности имплантата лимонной кислотой, а стенки дефекта модифицировали, перекрыв их частью лоскута. Через 7 лет на контрольном осмотре провели обработку данной области посредством поддесневой ирригации микрочастицами миноциклина гидрохлорида (Arestin, OraPharma, Valeant Pharmaceuticals International, Laval, Quebec, Canada). Через год данный участок практически полностью восстановился (фото 9).
Фото 9. Восстановление области второго моляра на нижней челюсти слева.

Благодаря активной поддерживающей пародонтальной терапии в ходе клинического осмотра и рентгенологического контроля удалось подтвердить успешность результатов функционирования оставшихся дентальных имплантатов в 8-летней ретроспективе (фото 10-12).
Фото 10. Новый протез: рентгенограммы.

Фото 11. Новый протез: вид спереди через 8 лет.

Фото 12. Новый протез: вид сбоку через 8 лет.

В ходе контрольного визита через 13 лет после имплантации опора в области второго моляра продолжала оставаться стабильной. Результаты клинического осмотра и рентгенологического контроля подтвердили достаточный функциональный уровень инфраконструкции, а также надлежащий уровень гигиены у пациента (фото 13-15).
Фото 13. Вид через 13 лет.

Фото 14. Вид через 13 лет.

Фото 15.
а. Рентгенограммы области моляров верхней челюсти через 13 лет.
b. Рентгенограммы области моляра нижней челюсти от начала периимплантита до периода 13 года функционирования имплантата.


Обсуждение
На самом деле, мало что известно о долгосрочном прогнозе функционирования имплантатов с оксидированной поверхностью, особенно если таковые использовались при реабилитации пациентов с пародонтитом. В данном случае ситуация была еще сложнее, ведь кроме агрессивного пародонтита у пациента отмечался бруксизм. Поддерживающая пародонтальная терапия, адекватная оценка всех потенциальных рисков лечения и продолжительный мониторинг за пациентом помогли добиться достаточно хороших результатов комплексной реабилитации. Потеря двух имплантатов на протяжении 3-х летнего периода аналогична уже ранее описанным случаям в литературе. В данном случае свою роль также сыграли факторы близости позиционирования имплантатов и цементный тип фиксации супраконструкций. Независимо от различных предпринятых мер, уровень редукции костной ткани в периимплантатной области может значительно варьировать. Поэтому врачу нужно обеспечить условия не только для ретенции исходного уровня резидуального гребня, но и для формирования достаточного мягкотканного барьера вокруг установленных абатментов.
Однако, даже в случае реализации данных аспектов потеря костной ткани все равно может продолжаться с прогрессирующей скоростью, и объяснить это явление в полной мере пока что никому не удалось. По мнению некоторых авторов, факторами, ассоциированными с потерей маргинальной кости, являются хирургическая травма, восстановление параметра биологической ширины, отсутствие пассивной подгонки супраконструкции, наличие микрозазора между имплантатом и абатментом, а также окклюзионная перегрузка. Непрерывная потеря костного объема с клиническими признаками инфицирования, кровотечения и нагноения идентифицируется как периимплантит, независимо от причин возникновения данных последствий. Исходя из различных определений данной патологии, ее распространённость колеблется в диапазоне 7,7-39,7%, хотя некоторые авторы считают данные цифры слишком уж завышенными. В данное время большинство имплантатов характеризуются специфической обработкой поверхности по типу ее абразивного улучшения, протравливания, анодного окисления и комбинации данных методов, чтобы спровоцировать более позитивную реакцию кости на установленный титановый элемент. Умеренно шероховатая, высококристаллическая и фосфатно-обогащенная поверхность имплантатов TiUnite характеризуется наличием увеличенного слоя диоксида титана, который вместе с определенной шероховатостью помогает увеличить площадь остеоинтеграции опорного элемента, а также уровень адгезии клеток-остеобластов MG-63. Были высказаны опасения, что потеря костной ткани и последующее обнажение шероховатой поверхности имплантата может спровоцировать развитие периимплантатной патологии, что было подтверждено в ходе исследований на животных, но осталось недоказанным при использовании подобных имплантатов в ходе реабилитации стоматологических пациентов.
В описанном выше клиническом случае пациентка желала заменить безнадёжные зубы на имплантаты, но при этом оставить часть собственных единиц зубного ряда в полости рта. Учитывая факт пародонтита, больная была предупреждена о риске такого подхода. Результаты лечения по большей мере зависели от того, насколько пациентка будет придерживаться сформированной для нее программы поддерживающего пародонтологического лечения. В области 47 зуба со временем пришлось провести сепарацию лоскута для удаления остатков цемента, а также обеспечить при этом лучшие условия для антибактериальной терапии в области имплантата. В конце концов, удалось добиться достаточно стабильных результатов вмешательства, что также может свидетельствовать о том, что шероховатая поверхность – это не всегда главный фактор, провоцирующий развитие периимплантита. Для снижения риска развития потенциальных биологических и технических осложнений пациентке также была изготовлена каппа на ночь. Данные систематического осмотра свидетельствуют о том, что бруксизм чаще провоцирует развитие технических осложнений, нежели биологических. Но все же стоит помнить, что риск перегрузки имплантата у больных с парафункциями все же значительно выше, чем у пациентов без таковых, что, в свою очередь, может повлиять на качество остеоинтеграции. Помня об этом, следует контролировать адекватность распределения жевательной нагрузки, и, кроме того, всегда проверять уровень гигиены полости рта, дабы избежать потенциального риска развития перимиплантита.
Выводы
Лечение с использованием имплантатов у пациентов с активным заболеванием пародонта и бруксизмом не является противопоказанным при условии обеспечения адекватного контроля инфекции и имплементации индивидуальной программы поддерживающей терапии. Результаты вышеизложенного случая иллюстрируют хорошие клинические и рентгенологические результаты имплантации в долгосрочной перспективе, а также свидетельствуют о том, что шероховатая поверхность имплантата не является фактором, определяющим динамику и объем потери костной ткани в периимплантатной области.
Авторы: David French, Erta Xhanari




























































































































































0 комментариев