Как известно, пародонтит является фактором риска развития заболеваний сердечно-сосудистой системы. Наконец ученые смогли объяснить механизм действия данной взаимосвязи: жизнедеятельность патогенных микроорганизмов, вызывающих пародонтит, также влияет на экспрессию генов, увеличивающих риск воспаления и развития атеросклероза в гладкомышечных клетках аорты.
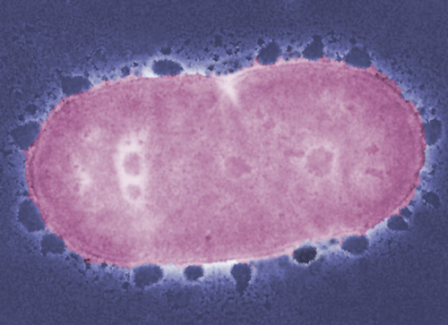
К исследованию ученых подтолкнул ряд косвенных доказательств. Во-первых, возбудитель пародонтита Porphyromonas gingivalis был найден в бляшках коронарных бактерий у пациентов с инфарктом миокарда. Проведенные испытания на животных показали, что патогенный микроорганизм P. gingivalis вызывает и ускоряет образование атеросклеротических бляшек в коронарных артериях и аорте. Клеточный механизм развития заболеваний удалось описать д-ру Тербьерну Бенгтссону с факультета Клинической медицины Школы наук о здравоохранении при университете Оребро.
Д-р Бенгтссон и его коллеги культивировали гладкомышечные клетки аорты и заразили их бактерией P. gingivalis. Было обнаружено, что протеаза P. gingivalis, являющаяся ее фактором вирулентности, значительно повышает экспрессию воспалительного ангиопоэтина 2 в гладкомышечных клетках, одновременно подавляя экспрессию противовоспалительного гена ангиопоэтина 1 в гладкомышечных клетках. При этом, суммарный эффект, оказываемый бактерией P. gingivalis, выражается в усилении воспалительного процесса, во многом способствующего развитию атеросклероза.
«Стоит отметить, что даже при отсутствии стимуляции гладкомышечные клетки аорты производят ангиопоэтин 2, но в достаточно малых дозах. При этом деятельность бактерий P. gingivalis значительно повышает экспрессию ангиопоэтина 2», - говорят авторы исследования.
«Ангиопоэтин 2 увеличивает миграцию гладкомышечных клеток аорты. Как известно, миграция гладкомышечных клеток связана с патогенными процессами образования атеросклеротических бляшек», - утверждает один из авторов работы Бокси Чанг.
«Фактор вирулернтности P. Gingivalis можно сравнить с фактором некроза опухоли – противосполительным цитокином и фактором риска сердечно-сосудистых заболеваний, который также вызывает и способствует развитию атеросклероза путем экспрессии двух типов ангиопоэтина. Однако исследования показывают, что два данных фактора вирулентности действуют вне зависимости друг от друга», - говорит д-р Бенгтссон.
«Наше исследование позволило объяснить механизм взаимосвязи пародонтита и сердечно-сосудистых заболеваний. Наша следующая цель – выявить биомаркеры, которые позволят диагностировать и лечить каждое из этих заболеваний».
Как известно, пародонтит является фактором риска развития заболеваний сердечно-сосудистой системы. Наконец ученые смогли объяснить механизм действия данной взаимосвязи: жизнедеятельность патогенных микроорганизмов, вызывающих пародонтит, также влияет на экспрессию генов, увеличивающих риск воспаления и развития атеросклероза в гладкомышечных клетках аорты.

К исследованию ученых подтолкнул ряд косвенных доказательств. Во-первых, возбудитель пародонтита Porphyromonas gingivalis был найден в бляшках коронарных бактерий у пациентов с инфарктом миокарда. Проведенные испытания на животных показали, что патогенный микроорганизм P. gingivalis вызывает и ускоряет образование атеросклеротических бляшек в коронарных артериях и аорте. Клеточный механизм развития заболеваний удалось описать д-ру Тербьерну Бенгтссону с факультета Клинической медицины Школы наук о здравоохранении при университете Оребро.
Д-р Бенгтссон и его коллеги культивировали гладкомышечные клетки аорты и заразили их бактерией P. gingivalis. Было обнаружено, что протеаза P. gingivalis, являющаяся ее фактором вирулентности, значительно повышает экспрессию воспалительного ангиопоэтина 2 в гладкомышечных клетках, одновременно подавляя экспрессию противовоспалительного гена ангиопоэтина 1 в гладкомышечных клетках. При этом, суммарный эффект, оказываемый бактерией P. gingivalis, выражается в усилении воспалительного процесса, во многом способствующего развитию атеросклероза.
«Стоит отметить, что даже при отсутствии стимуляции гладкомышечные клетки аорты производят ангиопоэтин 2, но в достаточно малых дозах. При этом деятельность бактерий P. gingivalis значительно повышает экспрессию ангиопоэтина 2», - говорят авторы исследования.
«Ангиопоэтин 2 увеличивает миграцию гладкомышечных клеток аорты. Как известно, миграция гладкомышечных клеток связана с патогенными процессами образования атеросклеротических бляшек», - утверждает один из авторов работы Бокси Чанг.
«Фактор вирулернтности P. Gingivalis можно сравнить с фактором некроза опухоли – противосполительным цитокином и фактором риска сердечно-сосудистых заболеваний, который также вызывает и способствует развитию атеросклероза путем экспрессии двух типов ангиопоэтина. Однако исследования показывают, что два данных фактора вирулентности действуют вне зависимости друг от друга», - говорит д-р Бенгтссон.
«Наше исследование позволило объяснить механизм взаимосвязи пародонтита и сердечно-сосудистых заболеваний. Наша следующая цель – выявить биомаркеры, которые позволят диагностировать и лечить каждое из этих заболеваний».
































































































































































0 комментариев