Стабилизация комплекса "трансплантат-мембрана" в процессе управляемой костной регенерации является критически важным аспектом имплантационной стоматологии. В нескольких статьях литературы по стоматологии описано использование периостальных прокалывающих стабилизирующих швов вместо фиксирующих винтов и штифтов для стабилизации биорассасывающейся коллагеновой мембраны. В данной статье рассматривается концепция стабилизации с помощью швов при регенерации пародонта и описывается альтернативный метод стабилизации биорассасывающейся мембраны — методика Ribroast Technique, при которой для достижения достаточной стабилизации по всей длине дефекта накладываются одиночные периостальные прокалывающие горизонтальные матрацные швы. Представлены два случая, которые подчеркивают практичность этой методики. Также обсуждаются рекомендации и ограничения по использованию периостальных прокалывающих швов, а также соображения и протоколы, которые могут быть полезны для улучшения результатов лечения.
При использовании нерезорбируемой мембраны необходимо обеспечить достаточную долгосрочную стабилизацию жесткого изделия, поэтому рекомендуется использовать винты и штифты для мембраны. Винты и штифты для фиксации мембраны могут быть сложными для установки по таким практическим причинам, как наличие плотной кортикальной кости и затрудненный доступ в различных отделах полости рта. Хотя использование пилотных отверстий в плотной кортикальной кости, прочных штифтов и винтов, которые не гнутся, и усовершенствованные протоколы привели к улучшению результатов лечения с помощью комбинации фиксирующих штифтов и рассасывающихся коллагеновых мембран, повышенные технические требования к процедуре очевидны. Кроме того, состав и эксплуатационные свойства коллагеновых мембран различны, и многие биорассасывающиеся коллагеновые мембраны не могут быть стабилизированы винтами и штифтами без разрыва. По этим причинам многие авторы описали методы стабилизации коллагеновой мембраны с помощью периостальных прокалывающих швов, а не штифтов и винтов. В 2016 году Urban et al описали использование вертикальных матрасных периостальных швов, а Neiva et al продемонстрировали успешные результаты при использовании методики лассо, при которой для стабилизации комплекса "трансплантат-мембрана" используется непрерывный периостальный прокалывающий шов.
В данной статье описывается методика Ribroast Technique (торговая марка автора MF), которая является модификацией описанных ранее методов стабилизации мембран. Это альтернативный вариант стабилизации комплекса "трансплантат-мембрана". В качестве иллюстрации практичности методики представлены два случая.
Описание методики
После проведения местной анестезии лезвием 15c делается гребневой разрез над беззубым гребнем, по возможности с рассечением полосы кератинизированной ткани. Для улучшения хирургического доступа к глубине дефекта, а также для доступа к фиксации апикальной надкостницы в пределах внутренней стороны щечного лоскута при стабилизации мембраны с помощью швов можно сделать вертикальный разгружающий разрез на один или два зуба мезиальнее или дистальнее дефекта, выходящий за пределы мукогингивального соединения (МГС).
После выполнения разрезов поднимают полнослойный мукопериостальный лоскут, начиная с одного угла разреза и выходя за край дефекта на 3-5 мм. Место операции дополнительно подготавливается с помощью внутрикостных проколов, чтобы обнажить медуллярное кровоснабжение; авторы также рекомендуют в это время получить аутогенную кость путем кортикального выскабливания.
Перед адаптацией костного трансплантата и мембраны к дефекту и последующей стабилизацией необходимо провести периостальное рассечение, чтобы снять натяжение лоскута, и создать вторичный внутренний лоскут, который можно использовать для фиксации швов на щечной стороне. Авторы рекомендуют технику, наиболее полно описанную Ronda и Stacci. Он включает в себя глубокий периостальный разрез глубиной 1 мм в одной плоскости по всей длине лоскута апикально к МГС. После выполнения начального неглубокого разреза микроэлеватор или другой подобный инструмент используется для растяжения в пределах этой линии разреза, захватывая при этом край лоскута с достаточным натяжением. Это снимает напряжение в лоскуте для последующего двухслойного первичного закрытия, чтобы минимизировать риск потери биоматериалов и послеоперационных осложнений, таких как расхождение краев линии разреза. Этот маневр также позволяет создать отдельный внутренний лоскут, который больше не связан с щечным лоскутом, расположенным коронально к разгружающему разрезу, а, скорее, с костью на самом апикальном участке лоскута, где надкостница не откинута от альвеолярной кости. Причина выполнения этого этапа до адаптации биоматериалов к дефекту двоякая: Периостальный разрез, разгружающий дефект, как правило, вызывает повышенное кровотечение сразу после этого этапа, что усложнит работу с трансплантатом и мембраной, если она будет выполнена после адаптации биоматериалов. Кроме того, поскольку стабилизация с помощью швов зависит от использования апикальной надкостницы в качестве опоры, выполнение периостальной разгрузки после стабилизации невозможно без потери натяжения стабилизационных швов и может привести к чрезмерному истончению щечного лоскута и даже перфорации лоскута.
После того как будет достигнута достаточная степень разгрузки лоскута, можно приступать к стабилизации. Сложный трансплантат, состоящий из аллотрансплантата и аутогенных костных соскобов, накладывается на дефект, и рассасывающаяся коллагеновая мембрана может быть адаптирована для фиксации костного трансплантата в дефекте. Мембрана должна выходить за пределы дефекта не менее чем на 3-5 мм. В это время рекомендуется оказывать умеренное давление на трансплантат и вышележащую мембрану с помощью стерильной марли, пропитанной физиологическим раствором, для достижения начальной стабильности комплекса путем прилегания мембраны к трансплантату, что облегчает стабилизацию комплекса с помощью швов.
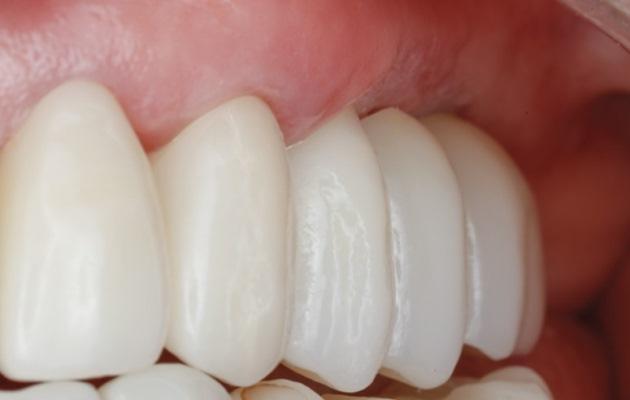
Если используется только один вертикальный разгружающий разрез, авторы рекомендуют начинать стабилизацию в месте, наиболее удаленном от этого разреза (фото 1). Это позволит облегчить доступ к надкостнице для дальнейшего наложения швов. Если первый надкостничный прокалывающий шов находится близко к вертикальному разрезу, доступ к апикальной надкостнице на другом конце мембраны будет затруднен.
Фото 1: Пример периостальных стабилизирующих швов для НКР с рассасывающейся коллагеновой мембраной.
Для начала стабилизации делается один прокол шовной иглой в надкостницу апикально от периостального разгружающего разреза на 3 мм - 5 мм латеральнее краев дефекта. Затем шов накладывается на мембрану и входит в небный или язычный лоскут с внутренней стороны на внешнюю, на 5-7 мм апикальнее края лоскута. Оператор должен медленно и точно натягивать шов, чтобы удержать его над адаптированной мембраной. Шов снова входит в небный или язычный лоскут на 3-5 мм латеральнее предыдущего прокола на том же апикокоронарном уровне, проходя обратно через небный лоскут. В это время шов натягивается, и стабилизирующий шов можно завязать с умеренным давлением. В идеале стабилизирующие швы располагаются над коллагеновой мембраной, над нативной костью за краями дефекта, а не над частицами трансплантата, что может привести к сдавливанию частиц трансплантата и ограничить потенциал сохранения пространства при использовании данной методики.
При необходимости можно наложить дополнительные стабилизирующие швы, чтобы зафиксировать трансплантат и мембрану в дефекте. При незначительных горизонтальных дефектах гребня в пределах контура гребня один периостальный шов может обеспечить достаточную стабильность. При дефектах большой протяженности и дефектах за пределами альвеолярного отростка рекомендуется накладывать дополнительные стабилизирующие швы. В этом сценарии после наложения первого стабилизирующего шва на дефект может быть наложен дополнительный трансплантационный материал, который может быть дополнительно адаптирован для улучшения сохранения пространства внутри дефекта перед наложением дополнительных стабилизирующих швов таким же образом, как описано выше.
После достижения адекватной стабилизации щечный и небный или язычный лоскут должен быть способен пассивно лежать над участком без потери натяжения стабилизирующих швов. Таким образом, важно отметить, что при прокалывании тканей с небной или язычной сторон должен быть перемещен и удерживаться коронально, чтобы стабилизирующий шов оставался натянутым во время первичного закрытия. Также важно, чтобы прокол лоскута с небной или язычной стороны находился на расстоянии более 5-7 мм от края лоскута, чтобы обеспечить возможность двухслойного ушивания, при этом идеальная граница между соединительной тканью и лоскутом должна составлять 5-7 мм.
В некоторых случаях может оказаться полезным наложение стабилизирующих швов через небный или язычный лоскут. Затем шов накладывается на мембрану и прокалывает апикальную надкостницу с щечной стороны, а затем, что важно, возвращается через небный или язычный лоскут на расстояние от 3 до 5 мм от первоначального прокола. В такой ситуации шов можно завязать, и узел будет находиться на небной или язычной поверхности, а не под лоскутами, что позволит оказывать умеренное давление на дефект. Кроме того, это позволяет очень точно направлять и накладывать швы на мембрану.
Следующие два случая демонстрируют использование методики Ribroast Technique для горизонтальной направленной регенерации кости.
Клинический случай 1
Пациентка, 55 лет, без сопутствующего анамнеза обратилась для замены левого первого премоляра и первого моляра верхней челюсти несъемной реставрацией с опорой на имплантаты. Первый моляр был удален за 10 лет до этого, и на этом месте наблюдалась нехватка ширины гребня умеренной степени. После проведения местной анестезии лезвием 15c был сделан срединный крестальный разрез на беззубом участке. После откидывания полнослойного лоскута были удалены левые первые и вторые премоляры верхней челюсти, проведена подготовка имплантационного ложа для имплантатов и установлены имплантаты (Tapered Plus bone level, BioHorizons) в положении для протезирования в области первого премоляра и первого моляра. В месте установки имплантата первого моляра наблюдался остаток щечной пластинки менее 1 мм (фото 2). Затем было выполнено надрезание и отслоение надкостницы для снятия натяжения и создания доступа к апикальной части надкостницы для наложения стабилизирующих швов, как описано выше (фото 3).
Фото 2: После установки имплантата наблюдалась вогнутость с щечной стороны и минимальное количество кости с щечной стороны по отношению к имплантату в области первого моляра.
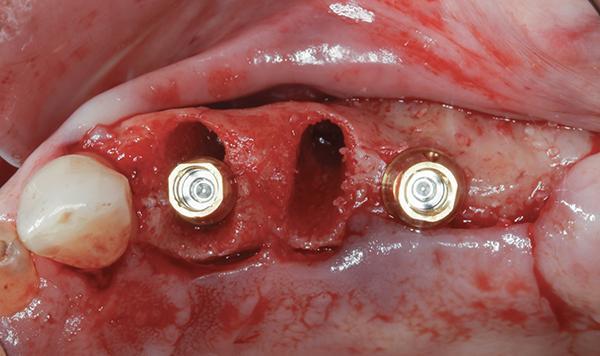
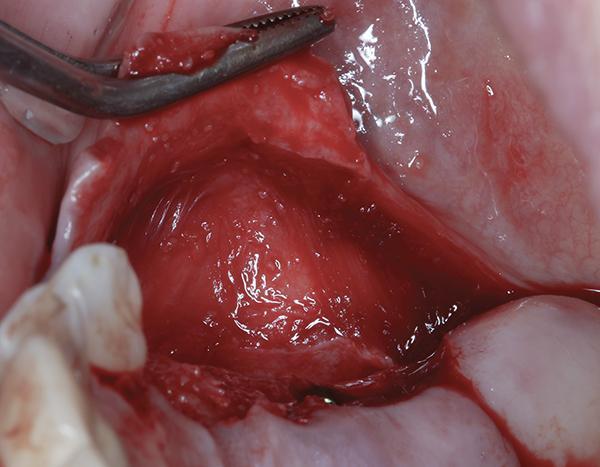
Фото 3: Расслоение надкостницы проведено для снятия натяжения и получения доступа к надкостнице в апикальной части.
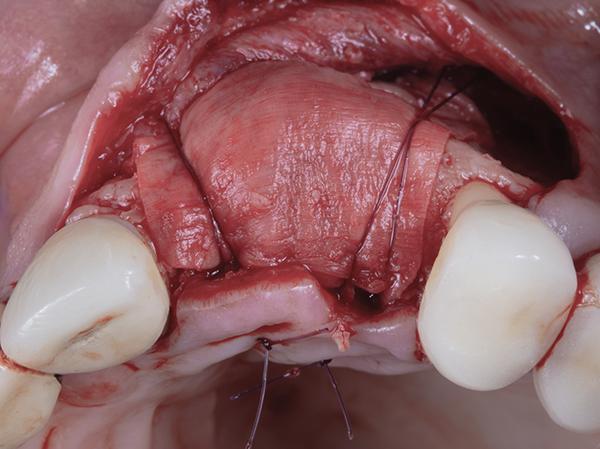
Аутогенная кость, собранная с соседнего участка с помощью одноразового костного скребка (Safescraper TWIST, Geistlich Pharma), была смешана с сублимированным костным аллотрансплантатом (MinerOss Cortical and Cancellous, BioHorizons) в соотношении 1:1 и адаптирована к дефекту щечной пластинки на месте первого моляра и к альвеолам зубов после удаления первого и второго премоляров. Сетчатая коллагеновая мембрана (OSSIX Plus, Datum Dental Ltd.) была адаптирована поверх гребня, и был наложен один периостальный прокалывающий стабилизирующий шов для, как описано выше (фото 4). Первичное закрытие было достигнуто путем наложения двух горизонтальных матрацных швов на расстоянии от 7 до 10 мм друг от друга с последующим наложением нескольких одиночных прерывистых швов через каждые 3-5 мм по всей длине лоскута.
Фото 4: Коллагеновая мембрана стабилизирована периостальным прокалывающим горизонтальным матрацным швом.
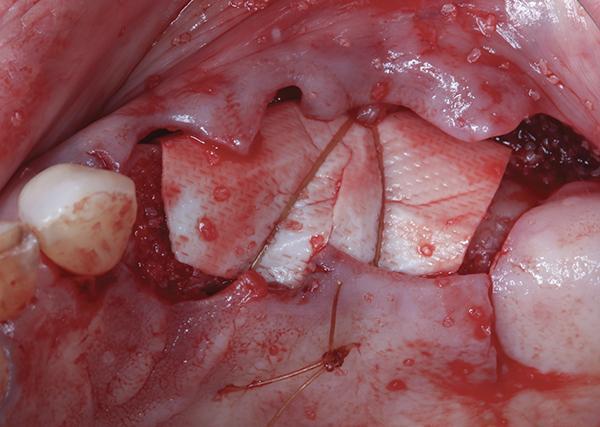
Пациентка наблюдалась через 2 недели, 2 месяца и 4 месяца после операции и не имела признаков боли, отека или инфекции. Через 5 месяцев после операции пациентка явилась для открытия имплантата (фото 5). В связи со смещением МГС в корональном направлении был проведен небный смещенный гребневой разрез и откинут полнослойный лоскут для обнажения зажившего гребня (фото 6). Было отмечено полное заполнение дефекта и значительное увеличение ширины гребня щечно по отношению к имплантату первого моляра. После установки формирователей десны высотой 3 мм с внутренней стороны небного лоскута был взят соединительнотканный трансплантат и зафиксирован на щечной стороне имплантатов для повышения качества и количества мягких тканей (фото 7). Впоследствии была проведена реставрация с помощью керамического моста с винтовой фиксацией на имплантатах (фото 8).
Фото 5: Заживление на контрольном приеме после операции.
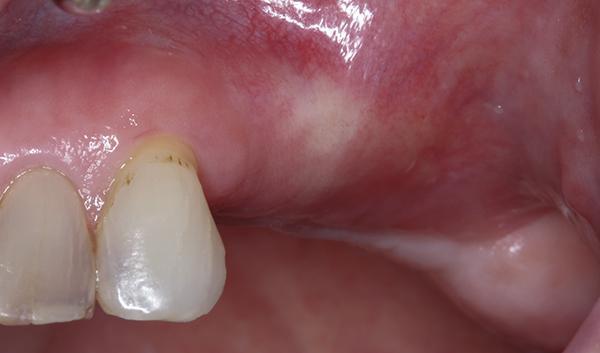
Фото 6: При раскрытии участка для установки формирователей десны было выявлено полное заполнение дефекта и регенерация.
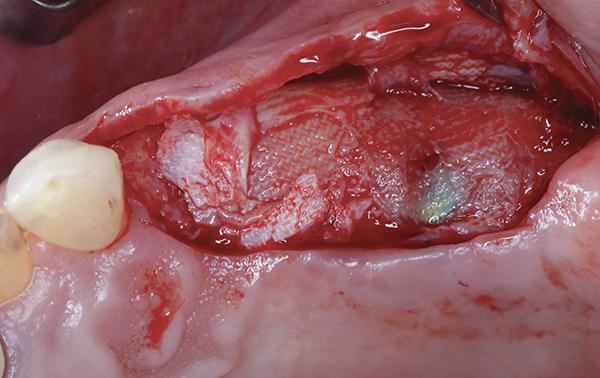
Фото 7: Соединительнотканный трансплантат был использован во время раскрытия имплантата для улучшения профиля мягких тканей.
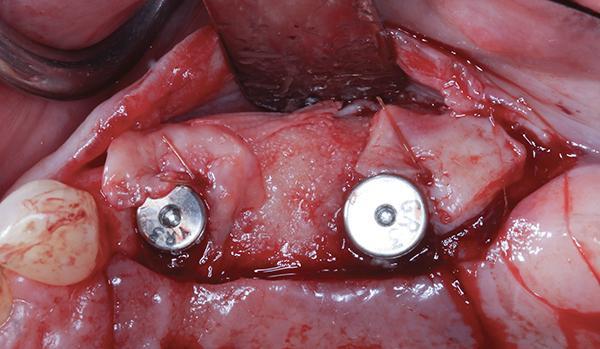
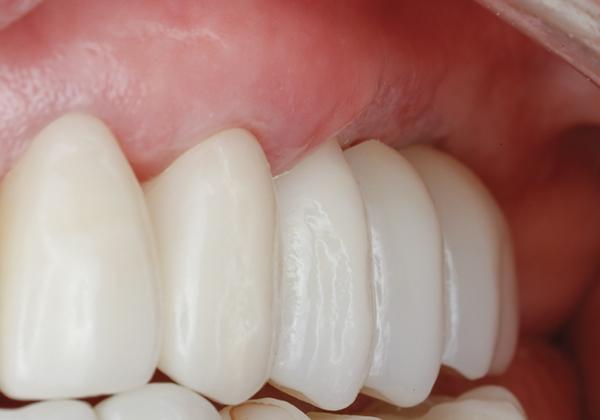
Фото 8: Вид со щечной стороны после установки несъемного частичного протеза с опорой на имплантаты.
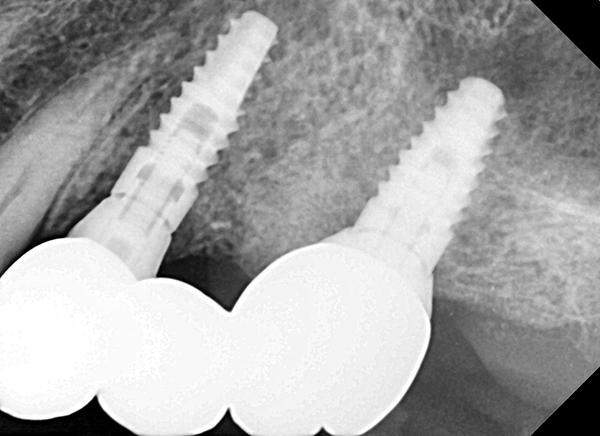
На фото 9 показана периапикальная рентгенограмма через 2 года после установки коронки, демонстрирующая стабильный уровень костной ткани после реабилитации с помощью мостовидного протеза с опорой на имплантаты.
Фото 9: Периапикальная рентгенограмма через 2 года после операции.
Клинический случай 2
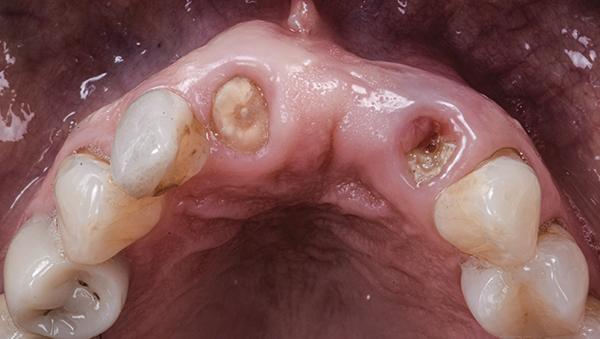
Пациентка, 75 лет, была направлена на реабилитацию с помощью дентальных имплантатов после перелома и разрушения несъемного протеза на три единицы на месте правого центрального и левого бокового резцов верхней челюсти (фото 10). Оба зуба полностью утратили коронковую структуру и были признаны не подлежащими восстановлению. Левый латеральный резец имел глубину пародонтального кармана с вестибулярной стороны 7 мм с полной потерей лабиальной пластинки, как было отмечено на КЛКТ. Был согласован план лечения, включающий замену разрушенных зубов дентальными имплантатами для поддержки несъемного протеза на три единицы с опорой на имплантаты.
Фото 10: Вид с окклюзионной стороны в момент приема.
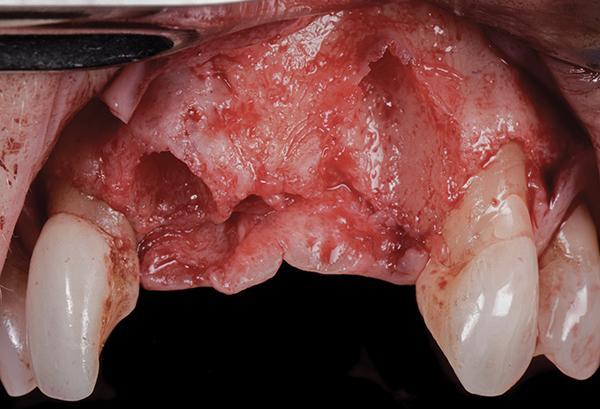
После проведения достаточной местной анестезии был сделан внутрикостный разрез со срединным крестальным разрезом в области правого центрального резца и вертикальными освобождающими разрезами дистальнее правого латерального резца и левого клыка. Полнослойный лоскут был поднят, правый центральный и левый боковой резцы были удалены, а место удаления левого бокового резца было тщательно дегранулировано, пока не стала видна вся протяженность широкого лабиального дефекта, простирающегося до верхушки зубной альвеолы (фото 11). Вестибулярная пластинка правого центрального резца имела толщину около 1 мм и вертикальную линию перелома вдоль мезиальной стороны. Аутогенную кортикальную стружку получали из вестибулярной стороны альвеолярного гребня, прилегающего к реципиентному участку, с помощью костного скребка (Safescraper TWIST) и смешивали с кортикально-губчатым минерализованным аллотрансплантатом (OraGraft Cortical/Cancellous Mineralized Particulate 50/50 Mix, Lifenet Health) в соотношении примерно 1:3, а также сывороткой, богатой лейкоцитами и тромбоцитами (L-PRF), для улучшения свойств трансплантата.
Фото 11: После удаления зуба и поднятия полнослойного лоскута были отмечены серьезные дефекты со щечной стороны.
Новое лезвие скальпеля 15c использовалось для выполнения периостального разреза 1 мм в направлении апикальной области лабиального лоскута, а микрохирургический периостальный элеватор (Mini Me, Hu-Friedy) использовался для растягивания лоскута от линии разреза в направлении резцов, чтобы в достаточной степени освободить лоскут. Затем композитный гранулярный трансплантат был помещен в альвеолы и на вестибулрную сторону альвеолярного гребня со значительным пересаживанием или наращиванием щечного контура (фото 12). После увлажнения нормальным физиологическим раствором была обрезана и адаптирована сетчатая коллагеновая мембрана, чтобы покрыть весь трансплантат, как с вестибулярной, так и с окклюзионной сторон.
Фото 12: Нанесение на дефект частиц костного трансплантата с L-PRF.
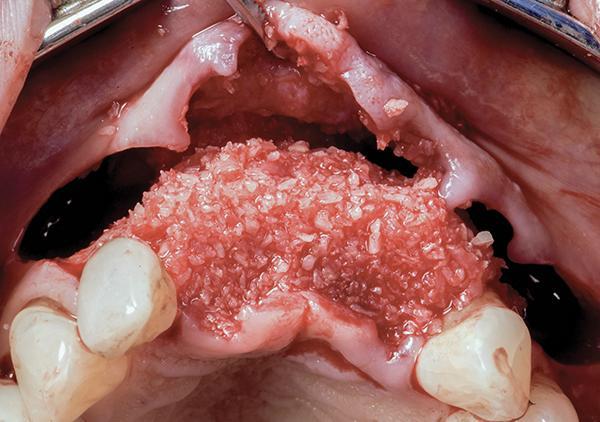
Периостальные швы накладывались следующим образом: Шов 6-0 использовался для прокалывания основания апикальной надкостницы (части, которая была отделена от лабиального лоскута) в области правого центрального резца. Затем шов накладывался на мембрану, входя в небный лоскут со стороны надкостницы. Затем шов проходил через эпителиальную часть небного лоскута на 5-7 мм медиальнее и завязывался узлом на вестибулярной стороне мембраны. Эта процедура была повторена на участке левого центрального резца, после чего был установлен дополнительный трансплантат на вестибулярной стороне левого латерального резца. Затем повторяли наложение периостального прокалывающего шва, прочно удерживая мембрану на мезиальной стороне левого клыка, в то время как повторный прокол на небной стороне располагался дистальнее левого клыка. Это позволило сохранить контакт мембраны с родным гребнем и предотвратить дистальную миграцию частиц трансплантата. Тот же протокол был повторен вокруг правого латерального резца (фото 13 и фото 14).
Фото 13: Адаптация коллагеновой мембраны над дефектом и фиксация множественными периостальными прокалывающими горизонтальными матрацными швами.
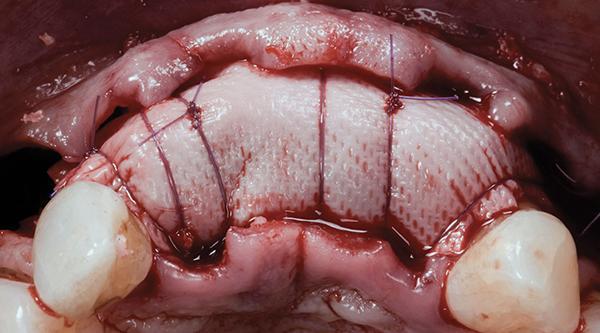
Фото 14: Стабилизация: вид со щечной стороны.
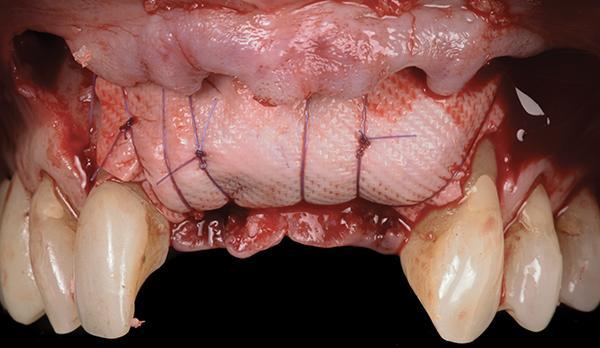
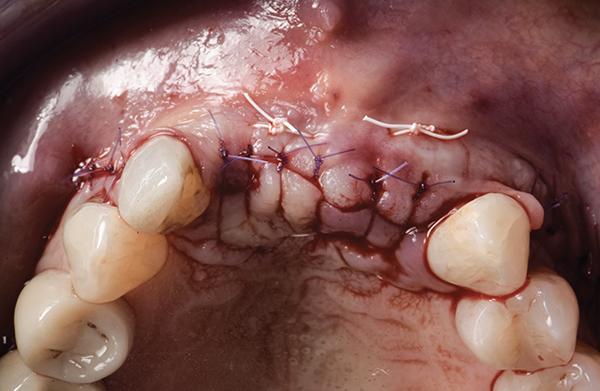
После того как стабильность комплекса "трансплантат-мембрана" была проверена, поверх рассасывающейся коллагеновой мембраны и конкретно под линией разреза были установлены мембраны с L-PRF (IntraSpin, Intra-Lock, BioHorizons) (фото 15). Два горизонтальных матрасных шва из плотного политетрафторэтилена (пПТФЭ) 3-0 были наложены для снятия натяжения лоскута по линии разреза. Затем накладывались простые прерывистые швы 6-0 для закрытия гребневых и вертикальных разрезов, что позволило закрыть первичный разрез без натяжения (фото 16).
Фото 15: Установка мембран PRF над комплексом перед первичным закрытием.
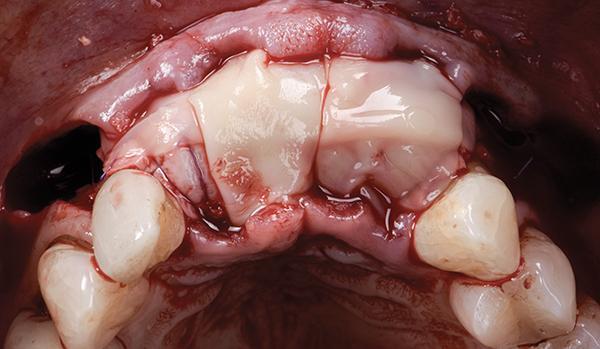
Фото 16: Вид с окклюзионной стороны после первичного закрытия.
Спустя 7 месяцев после заживления участок был повторно обработан, и была отмечена отличная регенерация кости (фото 17). Имплантаты (Straumann BLT, Straumann) были установлены в запланированные положения реставрации с помощью напечатанного на 3D-принтере хирургического шаблона (фото 18 и фото 19). Коллагеновый матрикс со стабильным объемом (Fibro-Gide, Geistlich Pharma) был обрезан и помещен под лабиальный лоскут для утолщения десны (фото 20 и фото 21). После заживления в течение 3 месяцев был изготовлен и поставлен несъемный протез на три единицы с опорой на имплантаты (фото 22).
Фото 17: Гребень после заживления: вид с окклюзионной стороны.
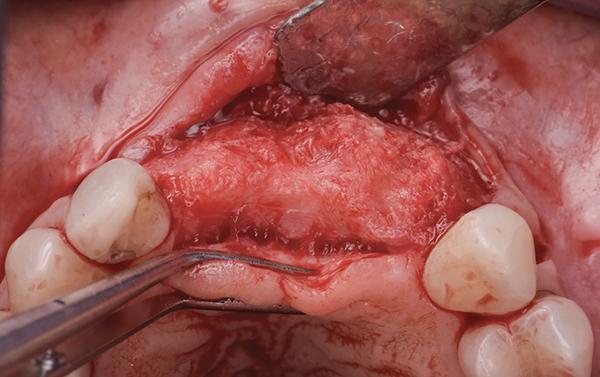
Фото 18: Хирургический шаблон, используемый для установки имплантатов.
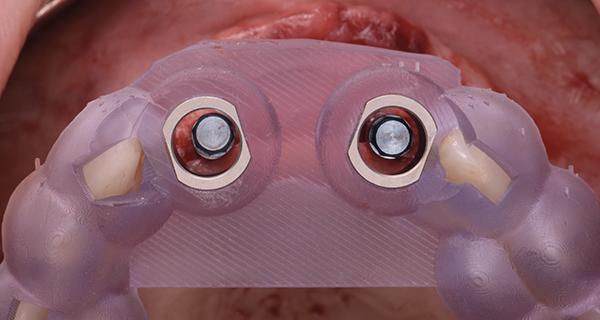
Фото 19: Вид с окклюзионной стороны после установки имплантата.
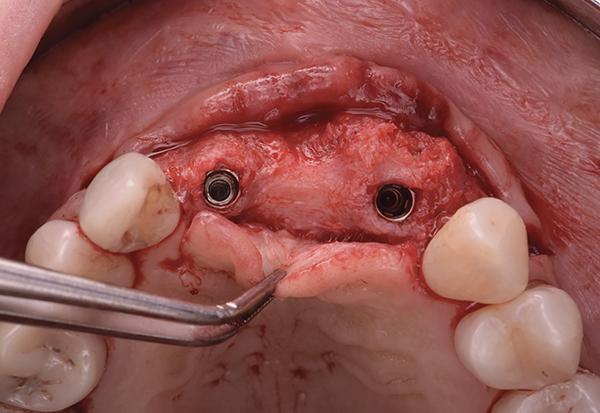
Фото 20: Использование коллагенового каркаса во время установки имплантата для улучшения контуров мягких тканей.
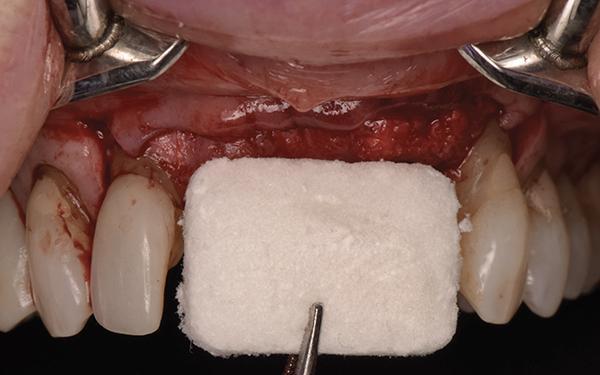
Фото 21: Размещение коллагенового каркаса: вид с окклюзионной стороны.
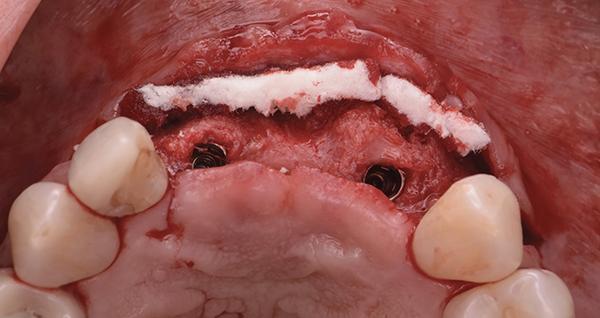
Фото 22: Окончательная реставрация с опорой на имплантаты: вид с окклюзионной стороны.
Обсуждение
Стабилизация комплекса "трансплантат-мембрана" необходима для оптимальной регенерации. Когда использование винтов или штифтов противопоказано из-за хрупкости рассасывающейся мембраны, затрудненного доступа для установки штифтов или винтов, или когда использование фиксирующих винтов и штифтов по другим причинам не является оптимальным вариантом, может быть полезно наложение периостальных прокалывающих швов.
Преимущество наложения нескольких отдельных горизонтальных матрасных швов по сравнению с одним непрерывным швом заключается в двух аспектах. Наложение и фиксация стабилизирующего шва на одном конце дефекта позволяет лечащему врачу затем добавить дополнительные материалы для костного трансплантата и адаптировать трансплантат для точного заполнения дефекта перед наложением дополнительных стабилизирующих швов. Кроме того, отдельные периостальные швы легче накладывать и они более щадящие, чем непрерывный шов, который может ослабнуть, что приведет к полной потере стабилизации. Натяжение отдельных швов на мембране можно легко корректировать, в то время как после наложения непрерывного шва корректировка одного участка изменяет натяжение всего комплекса. Количество необходимых стабилизирующих швов зависит от анатомии и характеристик дефекта, который подвергается трансплантации, а также от регенеративных потребностей конкретного случая. Преимуществом является использование материалов для костных трансплантатов с улучшенной управляемостью. Например, "липкая" кость обеспечивает трансплантат, который прилипает к дефекту и с которым легче работать.
Хотя с помощью этой методики можно добиться легкой вертикальной регенерации, авторы рекомендуют использовать нерезорбируемые мембраны, такие как армированный титаном ПТФЭ (ti-ПТФЭ), титановую сетку, или костные пластины Khoury, когда успех зависит от регенерации значительной высоты альвеолярной кости. Кроме того, не рекомендуется использовать стабилизирующие швы для стабилизации мембран титановой сетки и ti-ПТФЭ, поскольку для полной фиксации этих материалов требуется время, превышающее время рассасывания швов.
Заключение
При использовании методики Ribroast Technique отдельные периостальные прокалывающие горизонтальные матрасные стабилизирующие швы используются для фиксации комплекса "трансплантат-мембрана" с целью аугментации гребня. Использование периостальных прокалывающих стабилизирующих швов может быть целесообразным вариантом для регенерации дефектов ширины гребня в противовес штифтам и винтам. Участки с вогнутыми дефектами и дефектами в пределах предопределенной генетической скелетной оболочки являются хорошими кандидатами для этой методики. Кроме того, эта методика может быть использована в сочетании с винтами для улучшения сохранения пространства при дефектах, требующих регенерации кости за пределами альвеолярного контура, однако необходимо провести дополнительные исследования, чтобы определить степень тяжести дефектов, которые можно предсказуемо лечить с помощью этой методики.
Авторы:
Matthew Fien, DDS
Israel Puterman, DMD, MSD
Juan Mesquida, DDS
Guillermo Bauza, PhD
Ignacio Ginebreda, DDS
Стабилизация комплекса "трансплантат-мембрана" в процессе управляемой костной регенерации является критически важным аспектом имплантационной стоматологии. В нескольких статьях литературы по стоматологии описано использование периостальных прокалывающих стабилизирующих швов вместо фиксирующих винтов и штифтов для стабилизации биорассасывающейся коллагеновой мембраны. В данной статье рассматривается концепция стабилизации с помощью швов при регенерации пародонта и описывается альтернативный метод стабилизации биорассасывающейся мембраны — методика Ribroast Technique, при которой для достижения достаточной стабилизации по всей длине дефекта накладываются одиночные периостальные прокалывающие горизонтальные матрацные швы. Представлены два случая, которые подчеркивают практичность этой методики. Также обсуждаются рекомендации и ограничения по использованию периостальных прокалывающих швов, а также соображения и протоколы, которые могут быть полезны для улучшения результатов лечения.

При использовании нерезорбируемой мембраны необходимо обеспечить достаточную долгосрочную стабилизацию жесткого изделия, поэтому рекомендуется использовать винты и штифты для мембраны. Винты и штифты для фиксации мембраны могут быть сложными для установки по таким практическим причинам, как наличие плотной кортикальной кости и затрудненный доступ в различных отделах полости рта. Хотя использование пилотных отверстий в плотной кортикальной кости, прочных штифтов и винтов, которые не гнутся, и усовершенствованные протоколы привели к улучшению результатов лечения с помощью комбинации фиксирующих штифтов и рассасывающихся коллагеновых мембран, повышенные технические требования к процедуре очевидны. Кроме того, состав и эксплуатационные свойства коллагеновых мембран различны, и многие биорассасывающиеся коллагеновые мембраны не могут быть стабилизированы винтами и штифтами без разрыва. По этим причинам многие авторы описали методы стабилизации коллагеновой мембраны с помощью периостальных прокалывающих швов, а не штифтов и винтов. В 2016 году Urban et al описали использование вертикальных матрасных периостальных швов, а Neiva et al продемонстрировали успешные результаты при использовании методики лассо, при которой для стабилизации комплекса "трансплантат-мембрана" используется непрерывный периостальный прокалывающий шов.
В данной статье описывается методика Ribroast Technique (торговая марка автора MF), которая является модификацией описанных ранее методов стабилизации мембран. Это альтернативный вариант стабилизации комплекса "трансплантат-мембрана". В качестве иллюстрации практичности методики представлены два случая.
Описание методики
После проведения местной анестезии лезвием 15c делается гребневой разрез над беззубым гребнем, по возможности с рассечением полосы кератинизированной ткани. Для улучшения хирургического доступа к глубине дефекта, а также для доступа к фиксации апикальной надкостницы в пределах внутренней стороны щечного лоскута при стабилизации мембраны с помощью швов можно сделать вертикальный разгружающий разрез на один или два зуба мезиальнее или дистальнее дефекта, выходящий за пределы мукогингивального соединения (МГС).
После выполнения разрезов поднимают полнослойный мукопериостальный лоскут, начиная с одного угла разреза и выходя за край дефекта на 3-5 мм. Место операции дополнительно подготавливается с помощью внутрикостных проколов, чтобы обнажить медуллярное кровоснабжение; авторы также рекомендуют в это время получить аутогенную кость путем кортикального выскабливания.
Перед адаптацией костного трансплантата и мембраны к дефекту и последующей стабилизацией необходимо провести периостальное рассечение, чтобы снять натяжение лоскута, и создать вторичный внутренний лоскут, который можно использовать для фиксации швов на щечной стороне. Авторы рекомендуют технику, наиболее полно описанную Ronda и Stacci. Он включает в себя глубокий периостальный разрез глубиной 1 мм в одной плоскости по всей длине лоскута апикально к МГС. После выполнения начального неглубокого разреза микроэлеватор или другой подобный инструмент используется для растяжения в пределах этой линии разреза, захватывая при этом край лоскута с достаточным натяжением. Это снимает напряжение в лоскуте для последующего двухслойного первичного закрытия, чтобы минимизировать риск потери биоматериалов и послеоперационных осложнений, таких как расхождение краев линии разреза. Этот маневр также позволяет создать отдельный внутренний лоскут, который больше не связан с щечным лоскутом, расположенным коронально к разгружающему разрезу, а, скорее, с костью на самом апикальном участке лоскута, где надкостница не откинута от альвеолярной кости. Причина выполнения этого этапа до адаптации биоматериалов к дефекту двоякая: Периостальный разрез, разгружающий дефект, как правило, вызывает повышенное кровотечение сразу после этого этапа, что усложнит работу с трансплантатом и мембраной, если она будет выполнена после адаптации биоматериалов. Кроме того, поскольку стабилизация с помощью швов зависит от использования апикальной надкостницы в качестве опоры, выполнение периостальной разгрузки после стабилизации невозможно без потери натяжения стабилизационных швов и может привести к чрезмерному истончению щечного лоскута и даже перфорации лоскута.
После того как будет достигнута достаточная степень разгрузки лоскута, можно приступать к стабилизации. Сложный трансплантат, состоящий из аллотрансплантата и аутогенных костных соскобов, накладывается на дефект, и рассасывающаяся коллагеновая мембрана может быть адаптирована для фиксации костного трансплантата в дефекте. Мембрана должна выходить за пределы дефекта не менее чем на 3-5 мм. В это время рекомендуется оказывать умеренное давление на трансплантат и вышележащую мембрану с помощью стерильной марли, пропитанной физиологическим раствором, для достижения начальной стабильности комплекса путем прилегания мембраны к трансплантату, что облегчает стабилизацию комплекса с помощью швов.
Если используется только один вертикальный разгружающий разрез, авторы рекомендуют начинать стабилизацию в месте, наиболее удаленном от этого разреза (фото 1). Это позволит облегчить доступ к надкостнице для дальнейшего наложения швов. Если первый надкостничный прокалывающий шов находится близко к вертикальному разрезу, доступ к апикальной надкостнице на другом конце мембраны будет затруднен.
Фото 1: Пример периостальных стабилизирующих швов для НКР с рассасывающейся коллагеновой мембраной.

Для начала стабилизации делается один прокол шовной иглой в надкостницу апикально от периостального разгружающего разреза на 3 мм - 5 мм латеральнее краев дефекта. Затем шов накладывается на мембрану и входит в небный или язычный лоскут с внутренней стороны на внешнюю, на 5-7 мм апикальнее края лоскута. Оператор должен медленно и точно натягивать шов, чтобы удержать его над адаптированной мембраной. Шов снова входит в небный или язычный лоскут на 3-5 мм латеральнее предыдущего прокола на том же апикокоронарном уровне, проходя обратно через небный лоскут. В это время шов натягивается, и стабилизирующий шов можно завязать с умеренным давлением. В идеале стабилизирующие швы располагаются над коллагеновой мембраной, над нативной костью за краями дефекта, а не над частицами трансплантата, что может привести к сдавливанию частиц трансплантата и ограничить потенциал сохранения пространства при использовании данной методики.
При необходимости можно наложить дополнительные стабилизирующие швы, чтобы зафиксировать трансплантат и мембрану в дефекте. При незначительных горизонтальных дефектах гребня в пределах контура гребня один периостальный шов может обеспечить достаточную стабильность. При дефектах большой протяженности и дефектах за пределами альвеолярного отростка рекомендуется накладывать дополнительные стабилизирующие швы. В этом сценарии после наложения первого стабилизирующего шва на дефект может быть наложен дополнительный трансплантационный материал, который может быть дополнительно адаптирован для улучшения сохранения пространства внутри дефекта перед наложением дополнительных стабилизирующих швов таким же образом, как описано выше.
После достижения адекватной стабилизации щечный и небный или язычный лоскут должен быть способен пассивно лежать над участком без потери натяжения стабилизирующих швов. Таким образом, важно отметить, что при прокалывании тканей с небной или язычной сторон должен быть перемещен и удерживаться коронально, чтобы стабилизирующий шов оставался натянутым во время первичного закрытия. Также важно, чтобы прокол лоскута с небной или язычной стороны находился на расстоянии более 5-7 мм от края лоскута, чтобы обеспечить возможность двухслойного ушивания, при этом идеальная граница между соединительной тканью и лоскутом должна составлять 5-7 мм.
В некоторых случаях может оказаться полезным наложение стабилизирующих швов через небный или язычный лоскут. Затем шов накладывается на мембрану и прокалывает апикальную надкостницу с щечной стороны, а затем, что важно, возвращается через небный или язычный лоскут на расстояние от 3 до 5 мм от первоначального прокола. В такой ситуации шов можно завязать, и узел будет находиться на небной или язычной поверхности, а не под лоскутами, что позволит оказывать умеренное давление на дефект. Кроме того, это позволяет очень точно направлять и накладывать швы на мембрану.
Следующие два случая демонстрируют использование методики Ribroast Technique для горизонтальной направленной регенерации кости.
Клинический случай 1
Пациентка, 55 лет, без сопутствующего анамнеза обратилась для замены левого первого премоляра и первого моляра верхней челюсти несъемной реставрацией с опорой на имплантаты. Первый моляр был удален за 10 лет до этого, и на этом месте наблюдалась нехватка ширины гребня умеренной степени. После проведения местной анестезии лезвием 15c был сделан срединный крестальный разрез на беззубом участке. После откидывания полнослойного лоскута были удалены левые первые и вторые премоляры верхней челюсти, проведена подготовка имплантационного ложа для имплантатов и установлены имплантаты (Tapered Plus bone level, BioHorizons) в положении для протезирования в области первого премоляра и первого моляра. В месте установки имплантата первого моляра наблюдался остаток щечной пластинки менее 1 мм (фото 2). Затем было выполнено надрезание и отслоение надкостницы для снятия натяжения и создания доступа к апикальной части надкостницы для наложения стабилизирующих швов, как описано выше (фото 3).
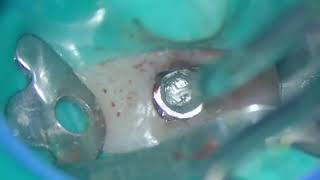
Фото 2: После установки имплантата наблюдалась вогнутость с щечной стороны и минимальное количество кости с щечной стороны по отношению к имплантату в области первого моляра.

Фото 3: Расслоение надкостницы проведено для снятия натяжения и получения доступа к надкостнице в апикальной части.

Аутогенная кость, собранная с соседнего участка с помощью одноразового костного скребка (Safescraper TWIST, Geistlich Pharma), была смешана с сублимированным костным аллотрансплантатом (MinerOss Cortical and Cancellous, BioHorizons) в соотношении 1:1 и адаптирована к дефекту щечной пластинки на месте первого моляра и к альвеолам зубов после удаления первого и второго премоляров. Сетчатая коллагеновая мембрана (OSSIX Plus, Datum Dental Ltd.) была адаптирована поверх гребня, и был наложен один периостальный прокалывающий стабилизирующий шов для, как описано выше (фото 4). Первичное закрытие было достигнуто путем наложения двух горизонтальных матрацных швов на расстоянии от 7 до 10 мм друг от друга с последующим наложением нескольких одиночных прерывистых швов через каждые 3-5 мм по всей длине лоскута.
Фото 4: Коллагеновая мембрана стабилизирована периостальным прокалывающим горизонтальным матрацным швом.

Пациентка наблюдалась через 2 недели, 2 месяца и 4 месяца после операции и не имела признаков боли, отека или инфекции. Через 5 месяцев после операции пациентка явилась для открытия имплантата (фото 5). В связи со смещением МГС в корональном направлении был проведен небный смещенный гребневой разрез и откинут полнослойный лоскут для обнажения зажившего гребня (фото 6). Было отмечено полное заполнение дефекта и значительное увеличение ширины гребня щечно по отношению к имплантату первого моляра. После установки формирователей десны высотой 3 мм с внутренней стороны небного лоскута был взят соединительнотканный трансплантат и зафиксирован на щечной стороне имплантатов для повышения качества и количества мягких тканей (фото 7). Впоследствии была проведена реставрация с помощью керамического моста с винтовой фиксацией на имплантатах (фото 8).
Фото 5: Заживление на контрольном приеме после операции.

Фото 6: При раскрытии участка для установки формирователей десны было выявлено полное заполнение дефекта и регенерация.

Фото 7: Соединительнотканный трансплантат был использован во время раскрытия имплантата для улучшения профиля мягких тканей.

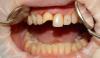
Фото 8: Вид со щечной стороны после установки несъемного частичного протеза с опорой на имплантаты.

На фото 9 показана периапикальная рентгенограмма через 2 года после установки коронки, демонстрирующая стабильный уровень костной ткани после реабилитации с помощью мостовидного протеза с опорой на имплантаты.
Фото 9: Периапикальная рентгенограмма через 2 года после операции.

Клинический случай 2
Пациентка, 75 лет, была направлена на реабилитацию с помощью дентальных имплантатов после перелома и разрушения несъемного протеза на три единицы на месте правого центрального и левого бокового резцов верхней челюсти (фото 10). Оба зуба полностью утратили коронковую структуру и были признаны не подлежащими восстановлению. Левый латеральный резец имел глубину пародонтального кармана с вестибулярной стороны 7 мм с полной потерей лабиальной пластинки, как было отмечено на КЛКТ. Был согласован план лечения, включающий замену разрушенных зубов дентальными имплантатами для поддержки несъемного протеза на три единицы с опорой на имплантаты.
Фото 10: Вид с окклюзионной стороны в момент приема.

После проведения достаточной местной анестезии был сделан внутрикостный разрез со срединным крестальным разрезом в области правого центрального резца и вертикальными освобождающими разрезами дистальнее правого латерального резца и левого клыка. Полнослойный лоскут был поднят, правый центральный и левый боковой резцы были удалены, а место удаления левого бокового резца было тщательно дегранулировано, пока не стала видна вся протяженность широкого лабиального дефекта, простирающегося до верхушки зубной альвеолы (фото 11). Вестибулярная пластинка правого центрального резца имела толщину около 1 мм и вертикальную линию перелома вдоль мезиальной стороны. Аутогенную кортикальную стружку получали из вестибулярной стороны альвеолярного гребня, прилегающего к реципиентному участку, с помощью костного скребка (Safescraper TWIST) и смешивали с кортикально-губчатым минерализованным аллотрансплантатом (OraGraft Cortical/Cancellous Mineralized Particulate 50/50 Mix, Lifenet Health) в соотношении примерно 1:3, а также сывороткой, богатой лейкоцитами и тромбоцитами (L-PRF), для улучшения свойств трансплантата.
Фото 11: После удаления зуба и поднятия полнослойного лоскута были отмечены серьезные дефекты со щечной стороны.

Новое лезвие скальпеля 15c использовалось для выполнения периостального разреза 1 мм в направлении апикальной области лабиального лоскута, а микрохирургический периостальный элеватор (Mini Me, Hu-Friedy) использовался для растягивания лоскута от линии разреза в направлении резцов, чтобы в достаточной степени освободить лоскут. Затем композитный гранулярный трансплантат был помещен в альвеолы и на вестибулрную сторону альвеолярного гребня со значительным пересаживанием или наращиванием щечного контура (фото 12). После увлажнения нормальным физиологическим раствором была обрезана и адаптирована сетчатая коллагеновая мембрана, чтобы покрыть весь трансплантат, как с вестибулярной, так и с окклюзионной сторон.
Фото 12: Нанесение на дефект частиц костного трансплантата с L-PRF.

Периостальные швы накладывались следующим образом: Шов 6-0 использовался для прокалывания основания апикальной надкостницы (части, которая была отделена от лабиального лоскута) в области правого центрального резца. Затем шов накладывался на мембрану, входя в небный лоскут со стороны надкостницы. Затем шов проходил через эпителиальную часть небного лоскута на 5-7 мм медиальнее и завязывался узлом на вестибулярной стороне мембраны. Эта процедура была повторена на участке левого центрального резца, после чего был установлен дополнительный трансплантат на вестибулярной стороне левого латерального резца. Затем повторяли наложение периостального прокалывающего шва, прочно удерживая мембрану на мезиальной стороне левого клыка, в то время как повторный прокол на небной стороне располагался дистальнее левого клыка. Это позволило сохранить контакт мембраны с родным гребнем и предотвратить дистальную миграцию частиц трансплантата. Тот же протокол был повторен вокруг правого латерального резца (фото 13 и фото 14).
Фото 13: Адаптация коллагеновой мембраны над дефектом и фиксация множественными периостальными прокалывающими горизонтальными матрацными швами.

Фото 14: Стабилизация: вид со щечной стороны.

После того как стабильность комплекса "трансплантат-мембрана" была проверена, поверх рассасывающейся коллагеновой мембраны и конкретно под линией разреза были установлены мембраны с L-PRF (IntraSpin, Intra-Lock, BioHorizons) (фото 15). Два горизонтальных матрасных шва из плотного политетрафторэтилена (пПТФЭ) 3-0 были наложены для снятия натяжения лоскута по линии разреза. Затем накладывались простые прерывистые швы 6-0 для закрытия гребневых и вертикальных разрезов, что позволило закрыть первичный разрез без натяжения (фото 16).
Фото 15: Установка мембран PRF над комплексом перед первичным закрытием.

Фото 16: Вид с окклюзионной стороны после первичного закрытия.

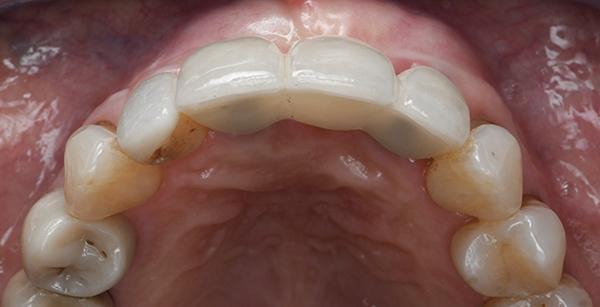
Спустя 7 месяцев после заживления участок был повторно обработан, и была отмечена отличная регенерация кости (фото 17). Имплантаты (Straumann BLT, Straumann) были установлены в запланированные положения реставрации с помощью напечатанного на 3D-принтере хирургического шаблона (фото 18 и фото 19). Коллагеновый матрикс со стабильным объемом (Fibro-Gide, Geistlich Pharma) был обрезан и помещен под лабиальный лоскут для утолщения десны (фото 20 и фото 21). После заживления в течение 3 месяцев был изготовлен и поставлен несъемный протез на три единицы с опорой на имплантаты (фото 22).
Фото 17: Гребень после заживления: вид с окклюзионной стороны.

Фото 18: Хирургический шаблон, используемый для установки имплантатов.

Фото 19: Вид с окклюзионной стороны после установки имплантата.

Фото 20: Использование коллагенового каркаса во время установки имплантата для улучшения контуров мягких тканей.

Фото 21: Размещение коллагенового каркаса: вид с окклюзионной стороны.

Фото 22: Окончательная реставрация с опорой на имплантаты: вид с окклюзионной стороны.

Обсуждение
Стабилизация комплекса "трансплантат-мембрана" необходима для оптимальной регенерации. Когда использование винтов или штифтов противопоказано из-за хрупкости рассасывающейся мембраны, затрудненного доступа для установки штифтов или винтов, или когда использование фиксирующих винтов и штифтов по другим причинам не является оптимальным вариантом, может быть полезно наложение периостальных прокалывающих швов.
Преимущество наложения нескольких отдельных горизонтальных матрасных швов по сравнению с одним непрерывным швом заключается в двух аспектах. Наложение и фиксация стабилизирующего шва на одном конце дефекта позволяет лечащему врачу затем добавить дополнительные материалы для костного трансплантата и адаптировать трансплантат для точного заполнения дефекта перед наложением дополнительных стабилизирующих швов. Кроме того, отдельные периостальные швы легче накладывать и они более щадящие, чем непрерывный шов, который может ослабнуть, что приведет к полной потере стабилизации. Натяжение отдельных швов на мембране можно легко корректировать, в то время как после наложения непрерывного шва корректировка одного участка изменяет натяжение всего комплекса. Количество необходимых стабилизирующих швов зависит от анатомии и характеристик дефекта, который подвергается трансплантации, а также от регенеративных потребностей конкретного случая. Преимуществом является использование материалов для костных трансплантатов с улучшенной управляемостью. Например, "липкая" кость обеспечивает трансплантат, который прилипает к дефекту и с которым легче работать.
Хотя с помощью этой методики можно добиться легкой вертикальной регенерации, авторы рекомендуют использовать нерезорбируемые мембраны, такие как армированный титаном ПТФЭ (ti-ПТФЭ), титановую сетку, или костные пластины Khoury, когда успех зависит от регенерации значительной высоты альвеолярной кости. Кроме того, не рекомендуется использовать стабилизирующие швы для стабилизации мембран титановой сетки и ti-ПТФЭ, поскольку для полной фиксации этих материалов требуется время, превышающее время рассасывания швов.
Заключение
При использовании методики Ribroast Technique отдельные периостальные прокалывающие горизонтальные матрасные стабилизирующие швы используются для фиксации комплекса "трансплантат-мембрана" с целью аугментации гребня. Использование периостальных прокалывающих стабилизирующих швов может быть целесообразным вариантом для регенерации дефектов ширины гребня в противовес штифтам и винтам. Участки с вогнутыми дефектами и дефектами в пределах предопределенной генетической скелетной оболочки являются хорошими кандидатами для этой методики. Кроме того, эта методика может быть использована в сочетании с винтами для улучшения сохранения пространства при дефектах, требующих регенерации кости за пределами альвеолярного контура, однако необходимо провести дополнительные исследования, чтобы определить степень тяжести дефектов, которые можно предсказуемо лечить с помощью этой методики.
Авторы:
Matthew Fien, DDS
Israel Puterman, DMD, MSD
Juan Mesquida, DDS
Guillermo Bauza, PhD
Ignacio Ginebreda, DDS





























































































































































0 комментариев