Дефицит кости резидуального гребня в области дна гайморовой пазухи решается за счет поднятия Шнейдеровой мембраны с последующим восстановлением пространства костным заменителем через латеральное окно или остеотомический канал. После проведенной процедуры можно провести установку дентального имплантата, поскольку используемые материалы помогают сохранить необходимый объем костной ткани, а также сопутствуют остеоинтеграции.
Цель данной статьи состояла в описании алгоритма использования A-PRF сгустка (обогащенного тромбоцитами фибрина) в качестве единственного материала для аугментации с дальнейшим проведением имплантации в аугментированном участке.
В ходе исследования было проведено две операции под местной анестезией. Предварительно выполняли забор венозной крови для формирования сгустка и остеотомию по технике Summers. Перфорации мембраны в обоих случаях обнаружено не было, А-PRF мембраны были помещены под дно слизистой гайморовой пазухи, после чего установленные имплантаты продемонстрировали отличную стабильность. Оттиски получали через 12 недель. По результатам КЛКТ подтвердили замещение области аугментации собственной костью и успешную интеграцию дентальных имплантататов, на которые впоследствии зафиксировали супраконструкции.
Прежние исследования
В 2003 году Lundgren и коллеги опубликовали краткий обзор, демонстрирующий самопроизвольное образование костной ткани в области гайморовой пазухи после удаления кисты. Без каких-либо операций пространство кисты просто заполнилось собственной костью пациента. Исходя из этого, Lundgren и коллеги предположили, что при ретенции пространства кость может восстанавливаться сама по себе без использования каких-либо дополнительных биоматериалов.
В 2004 году исследователи провели эксперимент, при котором установили 19 дентальных имплантатов по технике Summers без дополнительного использования трансплантата. Имплантаты, которые установили в ходе исследования, играли роль поддерживающих опор, которые приподнимали мембрану Шнайдера несколько выше костного дна верхнечелюстного синуса. Кровь, которая заполнила сформировавшееся пространство, в дальнейшем преобразовалась в костную ткань, что доказало первичное предположение исследователей. Похожие результаты были опубликованы и другими авторами. Однако существует проблема, состоящая в том, как обеспечить полное заполнение сформированного пространства кровью, и насколько объемным является размер самого кровяного сгустка.
A-PRF, в свою очередь, можно рассматривать как уже сформированный кровяной сгусток, который технически получить довольно просто. Кроме того, при использовании A-PRF можно контролировать объем выполнения сформированного пространства. Результаты, полученные Мazor и коллегами в 2009 году, которые использовали метод Lundgren с A-PRF на 20 пациентах в области 41 установленного имплантата, засвидетельствовали прирост костной ткани в диапазоне от 7 до 13 мм (среднее ±отклонение: 10,1 ± 0,9 мм). Взятые ими гистологические образцы через шесть месяцев после операции подтвердили наличие остеобластов и остеокластов в структуре лакун сформировавшейся костной ткани.
В 2013 году Тajima и его коллеги сообщили о среднем приросте костной ткани в 7,5 мм, используя тот же метод аугментации, что и их предшественники. На фото 1-10 можно увидеть, что кость не доходит до самой верхушки имплантатов. Результаты, полученные Palma и коллегами при исследованиях на животных, подтвердили, что верхушка имплантатов остается покрытой Шнейдеровой мембраной. Аспекты использования A-PRF в своих последних работах широко осветили Dohan и коллеги.
Клинические случаи
Оба пациента проходили лечения в Godt SMIL Odense на протяжении 16 месяцев. Они не были согласны на использование костного заменителя животного происхождения для проведения аугментации, следовательно, для них были использованы A-PRF сгустки. Анамнез у обоих пациентов не был отягощен, вредных привычек не наблюдалось. После получения 10 мл венозной крови (Vacuette Greiner bio-one) для каждого имплантата и дополнительных 10 мл для каждого предполагаемого миллиметра реконструкции кости, она была помещена в колбы и отцентрифугирована согласно протоколу Choukroun.
Операция
Премедикация состояла из приема 2000 мг Imadrax (амоксициллин), 1000 мг Pinex (парацетамол) и 400 мг Ibumetin (ибупрофен) за 60 минут до ятрогенного вмешательства.
Полость рта промывали 0,2% раствором хлоргексидина в течение одной минуты.
Местную анестезию выполняли со щечной и небной сторон (Xyloplyin со стоматологическим адреналином 20 мг/мл + 12,5 мкг/мл лидокаина гидрохлорид + адреналин).
Трапециевидный слизисто-надкостничный лоскут и остеотомию проводили по методике Summers. Под Шнейдерову мембрану помещали А-PRF мембраны. Симптом Вальсальвы был негативным для обоих пациентов.
В ходе имплантации использовали инфраконструкции K3Pro Sure, и последний сгусток А-PRF позиционировали непосредственно под линией разреза. Оба имплантата демонстрировали хорошую первичную стабильность. Ушивание проводили при помощи нитей Glycolon 6-0 (Resorba). Никаких дальнейших аугментаций костной ткани не проводилось.
В послеоперационный период пациентам назначали Imadrax (амоксициллин), 500 мг 4 раза в день в течение трех дней, Ibumetin (ибупрофен, 400 мг) в сочетании с 1000 мг Pinex (парацетамол) по мере необходимости. Обоим пациентам была рекомендована мягкая диета в течение последующих двух дней и никакой физической активности в течение семи дней после вмешательства.
Через двенадцать недель на имплантаты зафиксировали цельно-керамические коронки Prettau.
Обсуждение
При такой маленькой выборке получить достоверные результаты исследований попросту невозможно, но факт остается фактом – вокруг имплантатов был сформирован достаточный объем костной ткани, и оба из них были достаточно стабильными на протяжении последующих 6 месяцев. Признаков кровотечения при зондировании в ходе контрольного визита через 3 месяца не наблюдалось. Предыдущие публикации, посвященные этому же вопросу, подтверждают, что использование A-PRF является безопасным и надежным методом для увеличения объема костной ткани в области дна гайморовой пазухи по методике Summers. Для формулировки однозначных заключений требуется проведение дополнительных более обширных исследований.
Фото 1. Установка трех колб с венозной кровью в центрифугу.

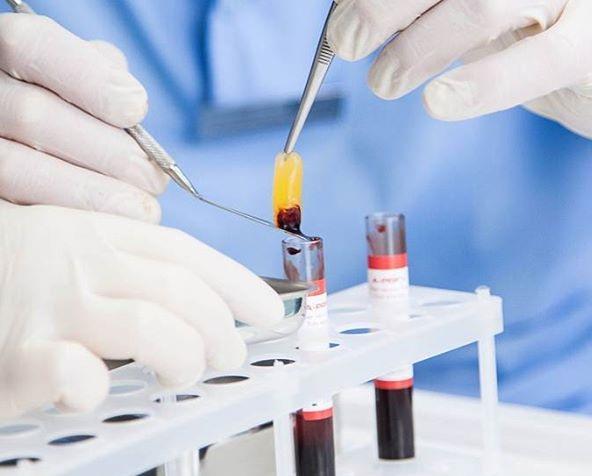
Фото 2. A-PRF сгусток.
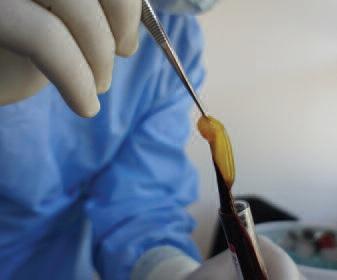
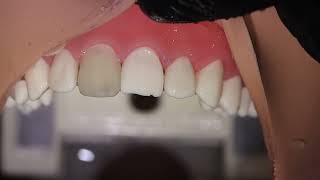
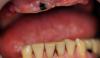
Фото 3. Клинический случай №1, до лечения.
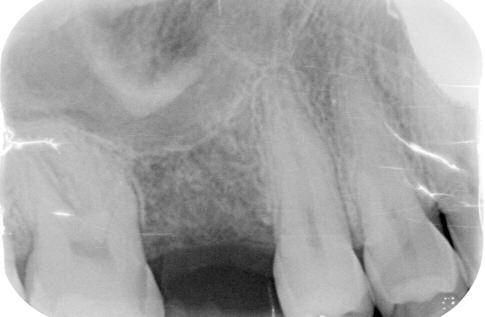
Фото 4. Клинический случай №1, вид сразу после операции.
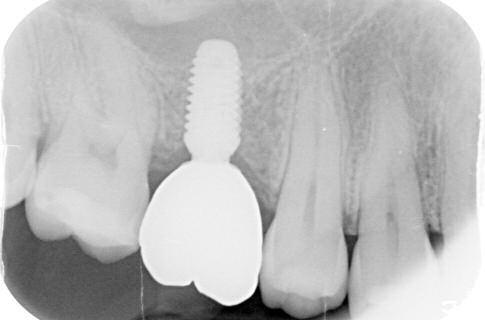
Фото 5. Клинический случай №1, вид через 14 недель после операции.
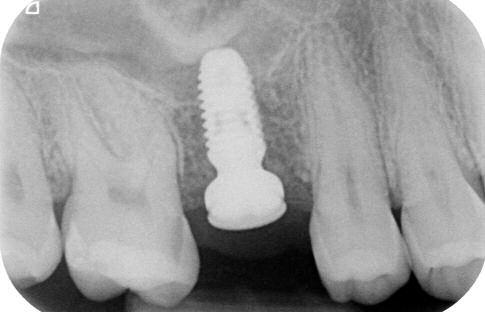
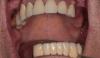
Фото 6 и 7. Клинический случай №1, вид через 6 месяцев после операции.
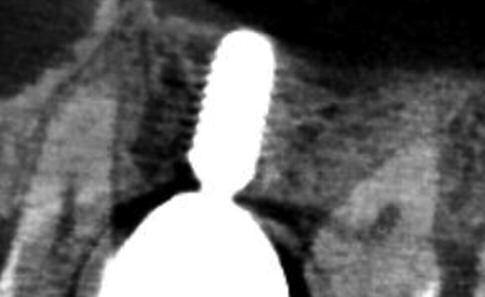
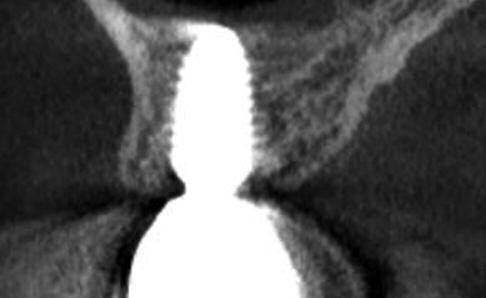
Фото 8. Клинический случай №2, до лечения.
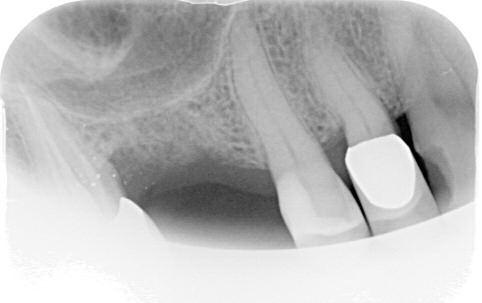
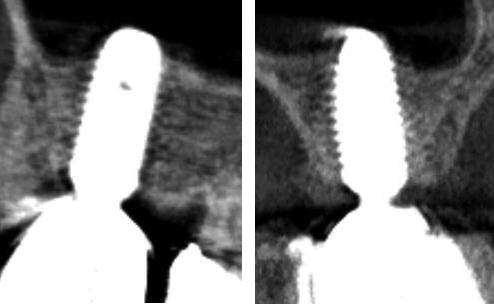
Фото 9 и 10. Клинический случай №2, вид через 6 месяцев после операции.
Автор: Dadi Hrafnkelsson
Дефицит кости резидуального гребня в области дна гайморовой пазухи решается за счет поднятия Шнейдеровой мембраны с последующим восстановлением пространства костным заменителем через латеральное окно или остеотомический канал. После проведенной процедуры можно провести установку дентального имплантата, поскольку используемые материалы помогают сохранить необходимый объем костной ткани, а также сопутствуют остеоинтеграции.
Цель данной статьи состояла в описании алгоритма использования A-PRF сгустка (обогащенного тромбоцитами фибрина) в качестве единственного материала для аугментации с дальнейшим проведением имплантации в аугментированном участке.

В ходе исследования было проведено две операции под местной анестезией. Предварительно выполняли забор венозной крови для формирования сгустка и остеотомию по технике Summers. Перфорации мембраны в обоих случаях обнаружено не было, А-PRF мембраны были помещены под дно слизистой гайморовой пазухи, после чего установленные имплантаты продемонстрировали отличную стабильность. Оттиски получали через 12 недель. По результатам КЛКТ подтвердили замещение области аугментации собственной костью и успешную интеграцию дентальных имплантататов, на которые впоследствии зафиксировали супраконструкции.
Прежние исследования
В 2003 году Lundgren и коллеги опубликовали краткий обзор, демонстрирующий самопроизвольное образование костной ткани в области гайморовой пазухи после удаления кисты. Без каких-либо операций пространство кисты просто заполнилось собственной костью пациента. Исходя из этого, Lundgren и коллеги предположили, что при ретенции пространства кость может восстанавливаться сама по себе без использования каких-либо дополнительных биоматериалов.
В 2004 году исследователи провели эксперимент, при котором установили 19 дентальных имплантатов по технике Summers без дополнительного использования трансплантата. Имплантаты, которые установили в ходе исследования, играли роль поддерживающих опор, которые приподнимали мембрану Шнайдера несколько выше костного дна верхнечелюстного синуса. Кровь, которая заполнила сформировавшееся пространство, в дальнейшем преобразовалась в костную ткань, что доказало первичное предположение исследователей. Похожие результаты были опубликованы и другими авторами. Однако существует проблема, состоящая в том, как обеспечить полное заполнение сформированного пространства кровью, и насколько объемным является размер самого кровяного сгустка.
A-PRF, в свою очередь, можно рассматривать как уже сформированный кровяной сгусток, который технически получить довольно просто. Кроме того, при использовании A-PRF можно контролировать объем выполнения сформированного пространства. Результаты, полученные Мazor и коллегами в 2009 году, которые использовали метод Lundgren с A-PRF на 20 пациентах в области 41 установленного имплантата, засвидетельствовали прирост костной ткани в диапазоне от 7 до 13 мм (среднее ±отклонение: 10,1 ± 0,9 мм). Взятые ими гистологические образцы через шесть месяцев после операции подтвердили наличие остеобластов и остеокластов в структуре лакун сформировавшейся костной ткани.
В 2013 году Тajima и его коллеги сообщили о среднем приросте костной ткани в 7,5 мм, используя тот же метод аугментации, что и их предшественники. На фото 1-10 можно увидеть, что кость не доходит до самой верхушки имплантатов. Результаты, полученные Palma и коллегами при исследованиях на животных, подтвердили, что верхушка имплантатов остается покрытой Шнейдеровой мембраной. Аспекты использования A-PRF в своих последних работах широко осветили Dohan и коллеги.
Клинические случаи
Оба пациента проходили лечения в Godt SMIL Odense на протяжении 16 месяцев. Они не были согласны на использование костного заменителя животного происхождения для проведения аугментации, следовательно, для них были использованы A-PRF сгустки. Анамнез у обоих пациентов не был отягощен, вредных привычек не наблюдалось. После получения 10 мл венозной крови (Vacuette Greiner bio-one) для каждого имплантата и дополнительных 10 мл для каждого предполагаемого миллиметра реконструкции кости, она была помещена в колбы и отцентрифугирована согласно протоколу Choukroun.
Операция
Премедикация состояла из приема 2000 мг Imadrax (амоксициллин), 1000 мг Pinex (парацетамол) и 400 мг Ibumetin (ибупрофен) за 60 минут до ятрогенного вмешательства.
Полость рта промывали 0,2% раствором хлоргексидина в течение одной минуты.
Местную анестезию выполняли со щечной и небной сторон (Xyloplyin со стоматологическим адреналином 20 мг/мл + 12,5 мкг/мл лидокаина гидрохлорид + адреналин).
Трапециевидный слизисто-надкостничный лоскут и остеотомию проводили по методике Summers. Под Шнейдерову мембрану помещали А-PRF мембраны. Симптом Вальсальвы был негативным для обоих пациентов.
В ходе имплантации использовали инфраконструкции K3Pro Sure, и последний сгусток А-PRF позиционировали непосредственно под линией разреза. Оба имплантата демонстрировали хорошую первичную стабильность. Ушивание проводили при помощи нитей Glycolon 6-0 (Resorba). Никаких дальнейших аугментаций костной ткани не проводилось.
В послеоперационный период пациентам назначали Imadrax (амоксициллин), 500 мг 4 раза в день в течение трех дней, Ibumetin (ибупрофен, 400 мг) в сочетании с 1000 мг Pinex (парацетамол) по мере необходимости. Обоим пациентам была рекомендована мягкая диета в течение последующих двух дней и никакой физической активности в течение семи дней после вмешательства.
Через двенадцать недель на имплантаты зафиксировали цельно-керамические коронки Prettau.
Обсуждение
При такой маленькой выборке получить достоверные результаты исследований попросту невозможно, но факт остается фактом – вокруг имплантатов был сформирован достаточный объем костной ткани, и оба из них были достаточно стабильными на протяжении последующих 6 месяцев. Признаков кровотечения при зондировании в ходе контрольного визита через 3 месяца не наблюдалось. Предыдущие публикации, посвященные этому же вопросу, подтверждают, что использование A-PRF является безопасным и надежным методом для увеличения объема костной ткани в области дна гайморовой пазухи по методике Summers. Для формулировки однозначных заключений требуется проведение дополнительных более обширных исследований.
Фото 1. Установка трех колб с венозной кровью в центрифугу.

Фото 2. A-PRF сгусток.

Фото 3. Клинический случай №1, до лечения.

Фото 4. Клинический случай №1, вид сразу после операции.

Фото 5. Клинический случай №1, вид через 14 недель после операции.

Фото 6 и 7. Клинический случай №1, вид через 6 месяцев после операции.


Фото 8. Клинический случай №2, до лечения.

Фото 9 и 10. Клинический случай №2, вид через 6 месяцев после операции.

Автор: Dadi Hrafnkelsson






























































































































































0 комментариев