Использование 3D-визуализации стало стандартом диагностики и планирования лечения при проведении многих медицинских и стоматологических процедур. Впервые такая визуализация была доступна с помощью широкоформатных медицинских компьютерных томографов, которые предоставляли клиницистам, исследователям и инженерам статичные видеоизображения на пленке. На ранних этапах компьютерной томографии была получена серия изображений поперечного сечения, которые были записаны на пленку. Это была та же самая среда, которая использовалась для обычных рентгенограмм и требовала химической разработки. Рентгенографические пленки требовали больших световых коробов для визуализации анатомии пациента. Наступление цифровой эры и совершенствование технологий привели к разработке пленок для сухой обработки. В настоящее время компьютерная томография в основном отображается на мониторах компьютеров в виде цифровых изображений, а печать на пленке стала менее распространенным вариантом. Визуализация была и остается дорогостоящей для пациента.

Исторически сложилось так, что использование физического моделирования на основе компьютерной томографии появилось в конце 1980-х и начале 1990-х годов, вскоре после коммерческого внедрения стереолитографии. Челюстно-лицевая хирургия стала передовой областью применения этой технологии, поскольку хирурги использовали напечатанные на 3D-принтере модели черепа для планирования реконструкций и разработки имплантатов для конкретных пациентов. Да, раннее производство было дорогостоящим и требовало больших технических затрат, но оно продемонстрировало, как можно сочетать медицинскую визуализацию и аддитивное производство для повышения точности и улучшения результатов лечения. По мере развития программного обеспечения в 1990-х и 2000-х годах рабочие процессы CT-to-STL становились все более эффективными. Автоматизированная сегментация, инструменты для восстановления сетки (для исправления ошибок в сетках STL) и все более доступные принтеры позволили использовать 3D-модели в ортопедии, сердечно-сосудистой хирургии и онкологии. Возможность использования различных материалов в стереолитографии еще больше расширила ее клиническую ценность, позволив изготавливать модели, имитирующие как твердые, так и мягкие ткани.
КЛКТ, представленная в начале 2000-х годов, стала доступна в виде стационарного устройства благодаря своей более низкой стоимости и компактности, обеспечивая немедленный доступ к важным 3D-данным при снижении радиационного облучения и затратах. Особенно значительным достижением в стоматологии стало изготовление на заказ поднадкостничных (субпериостальных) имплантатов - устройств, которые крепятся к поверхности кости под надкостницей для поддержки протезированных зубов. Традиционно поднадкостничные имплантаты требовали предварительной хирургической процедуры для обнажения челюстной кости и создания физического слепка, который затем использовался для ручной установки металлического каркаса — процесса, связанного со значительной болезненностью и неточностью. Появление компьютерного моделирования на основе компьютерной томографии коренным образом изменило этот рабочий процесс. Компьютерная томография с высоким разрешением позволила получить точную форму альвеолярного отростка пациента без инвазивного снятия слепка. Разделив челюстную кость на сегменты по данным компьютерной томографии и создав модель для 3D-печати, лаборатории смогли разработать индивидуальные поднадкостничные каркасы, которые с гораздо большей точностью соответствовали бы анатомии пациента. Такие пионеры, как Х.П. Труитт и Леонард Линкоу, помогли обучить индустрию тому, как эту технологию можно использовать для изготовления поднадкостничных имплантатов; однако при использовании компьютерной томографии существовало существенное ограничение: разрешение поперечного сечения и доступное программное обеспечение не всегда позволяли создавать точные 3D-модели.
Благодаря постоянному прогрессу в области объемного челюстно-лицевого сканирования с высоким разрешением, а также распространению лабораторных и офисных 3D-принтеров создание цифровых моделей кости нижней и верхней челюстей стало значительно более распространенным явлением. Традиционный конвейер — сбор данных, сегментация, реконструкция поверхности, восстановление сетки, CAD, стереолитография или производство металлических припоев — позволяет создавать как анатомические модели, так и имплантаты и хирургические направляющие для конкретного пациента. Для пациентов с тяжелой формой альвеолярной атрофии, которым не могут быть установлены обычные корневидные имплантаты, в качестве предсказуемой альтернативы вновь появились специальные поднадкостничные каркасы, изготовленные с помощью цифровых технологий. В клинических отчетах описаны титановые поднадкостничные имплантаты, напечатанные на 3D-принтере для атрофированной нижней и верхнечелюстной кости, которые по сравнению с аналогичными рабочими процессами улучшают посадку, сокращают время пребывания в кресле и упрощают реабилитацию при протезировании. Современные костные имплантаты для конкретных пациентов, которые изготавливаются с использованием передовых технологических процессов, включающих сегментацию и стереолитографию или производство металлических припоев, начинают проникать на рынок; однако из-за уникального технологического процесса они остаются дорогостоящими и ограничены в использовании и доступности по сравнению с обычными зубными имплантатами. Тем не менее, этот процесс доказал эффективность усовершенствованной сегментации кости при применении зубных имплантатов и, особенно, хирургических направляющих.
STL-файлы, созданные с помощью расширенной сегментации, теперь можно экспортировать на настольные 3D-принтеры. Таким образом, клиницисты и зуботехнические лаборатории теперь могут печатать модели нижней и верхней челюстей с высоким разрешением. Кроме того, с появлением собственной технологии 3D-печати клиницисты и лаборатории разработали и напечатали хирургические направляющие для имплантации зубов, мягких тканей и костей. Независимо от конечного желаемого результата, разрешение и детализация поверхности анатомических моделей зависят от процесса сегментации. Внедрение искусственного интеллекта (ИИ) для облегчения утомительной задачи сегментации позволило добиться значительных улучшений, включая полную автоматизацию процесса сегментации костей и зубов. Поскольку усовершенствованная сегментация, созданная с помощью ИИ, становится доступной с помощью бесплатного программного обеспечения, такого как Blue Sky Plan (Blue Sky Bio), которое обеспечивает более быстрые, точные, воспроизводимые и чистые результаты, можно с большей эффективностью разрабатывать хирургические направляющие для костной хирургии. Кроме того, усовершенствованный процесс проектирования может способствовать внедрению инноваций, о чем свидетельствует недавно представленный направляющий штифт для носо-небного канала с поворотным контуром, который разработан для верхней челюсти. Исследование новой конструкции выявило 22 последовательных случая, в которых носоглотка использовалась для стабилизации костных хирургических направляющих. В серии случаев было удалено 152 зуба и установлено 123 имплантата для поддержки 18 несъемных протезов и четырех съёмных накладных протезов, что стало возможным благодаря усовершенствованной анатомической сегментации, сгенерированной ИИ. Данный клинический случай представляет собой продолжение оригинальной серии случаев, которая была расширена до 45 пациентов.
Клинический случай
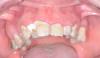
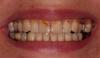
49-летний мужчина обратился с жалобами на разрушение зубов верхней и нижней челюсти. Результаты клинических и рентгенологических исследований показали тяжелое заболевание пародонта, общую потерю костной ткани, увеличение расстояния между передними зубами и подвижность зубов, а также общее неудовлетворительное соблюдение гигиены (фото 1a-b, 2a). Пациент был проинформирован о результатах исследования и было обсуждено несколько вариантов лечения, включая полные и/или частичные протезы, съемные протезы на имплантатах и несъемные протезы на имплантатах. После обсуждения вариантов пациент выбрал несъемные протезы на имплантатах для всей челюсти.
Фото 1a: Дооперационная ситуация. Интраоральный ретракционный снимок верхней челюсти, показывающий прогрессирующее заболевание пародонта и расстояние между зубами.

Фото 1b: Дооперационная ситуация. Интраоральный ретракционный вид верхней и нижней челюсти в окклюзии.

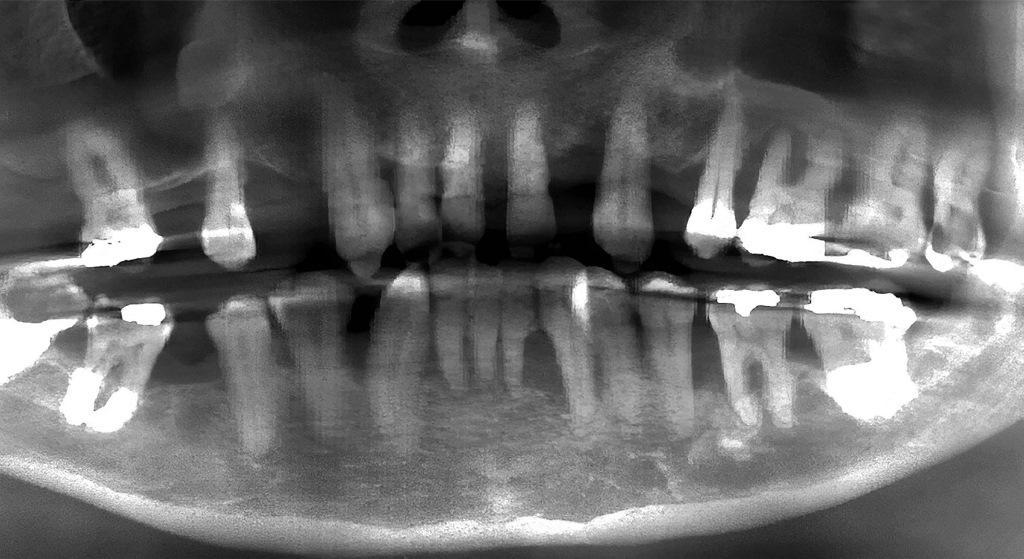
Фото 2a: Предоперационная панорамная рентгенограмма, показывающая обширную потерю костной ткани.
Первоначальный план восстановления верхней челюсти состоял в удалении всех оставшихся зубов, установке шести имплантатов и использовании костного материала там, где это необходимо, для заполнения лунки и других углублений или отверстий. Имитированные имплантаты были визуализированы на панорамной реконструкции, включая фиксирующий штифт, расположенный по средней линии, соединяющей носоглотку (фото 2b). Используя расширенные возможности для различения объектов на основе их радиопрозрачности, интерактивное программное обеспечение для планирования лечения (Blue Sky Plan) и настраиваемую пользователем избирательную прозрачность, можно в полной мере оценить имитацию имплантатов при 3D-визуализации верхнечелюстной кости (фото 3a–c).
Фото 2b: Имитация верхнечелюстного имплантата на панорамной рентгенограмме, показывающей шесть имплантатов и штифт для носоглотки.

Фото 3a: Выборочные прозрачные изображения имитируемых имплантатов в верхнечелюстной дуге, включая имплантаты с наклоном назад, чтобы избежать попадания в верхнечелюстную пазуху, фронтальный вид.

Фото 3b: Вид слева.

Фото 3c: Вид справа.

Усовершенствованная сегментация костей и зубов с помощью ИИ была применена к верхнечелюстной дуге, чтобы помочь в постановке окончательного диагноза и составлении плана лечения для каждого потенциального места установки имплантата (фото 4a). Можно визуализировать расстояние между существующими естественными зубами и полную топографию верхнечелюстной кости, предоставляя важную информацию, необходимую для правильной установки имплантата (фото 4b). Сегментированные естественные зубы были практически удалены, чтобы можно было легко оценить контуры кости и дефекты лунки (фото 4c).
Фото 4a: Объемная 3D-реконструкция верхней челюсти. Степень потери костной ткани и расстояние между передними зубами.

Фото 4b: Окклюзионный вид имитируемых имплантатов с желтыми абатментами для отображения траектории отверстий для доступа к винтам.

Фото 4c: Окклюзионный вид имитируемых удалений и имплантатов в верхней челюсти.

Программное обеспечение позволяет выбирать реалистичные имплантаты из библиотеки производителя для достижения максимальной точности. Все имплантаты были имплантатами IS-III Active с поверхностью SLA корейской компании NeoBiotech. Первоначальное планирование было завершено сначала с помощью срезов изображения в поперечном сечении, которые позволяют получить 360-градусный обзор потенциального места установки имплантата. Каждый срез в поперечном сечении был снабжен комментариями, отражающими длину и диаметр имплантатов, а также степень любых повреждений или отверстий для удаления (фото 5a–h). Аналогичный план был разработан для нижнечелюстной дуги с шестью параллельными имплантатами для поддержки фиксированной реставрации (фото 6).
Фото 5a–h: Имитация поперечного сечения имплантатов с указанием длины и диаметра имплантатов на основе данных КЛКТ-сканирования.

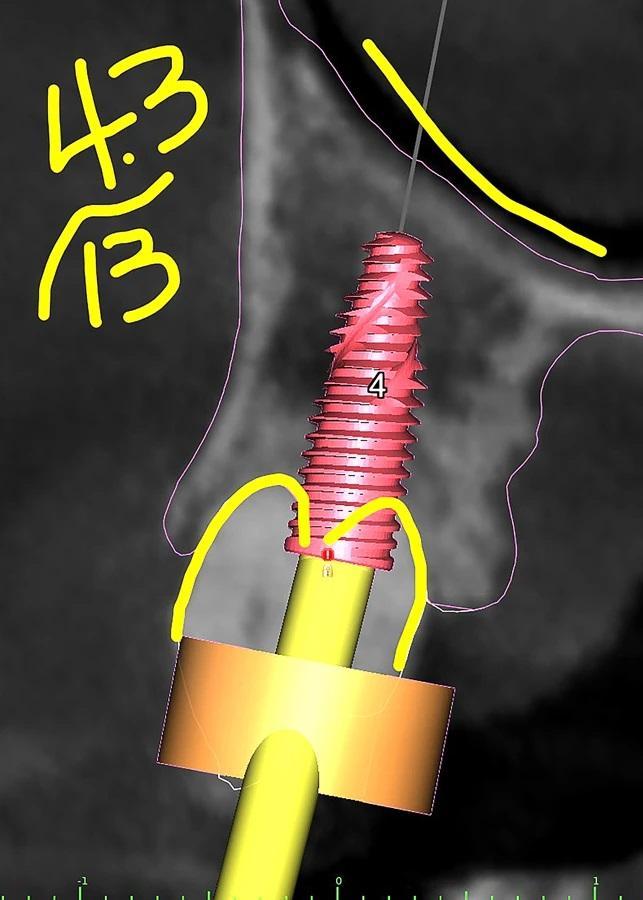


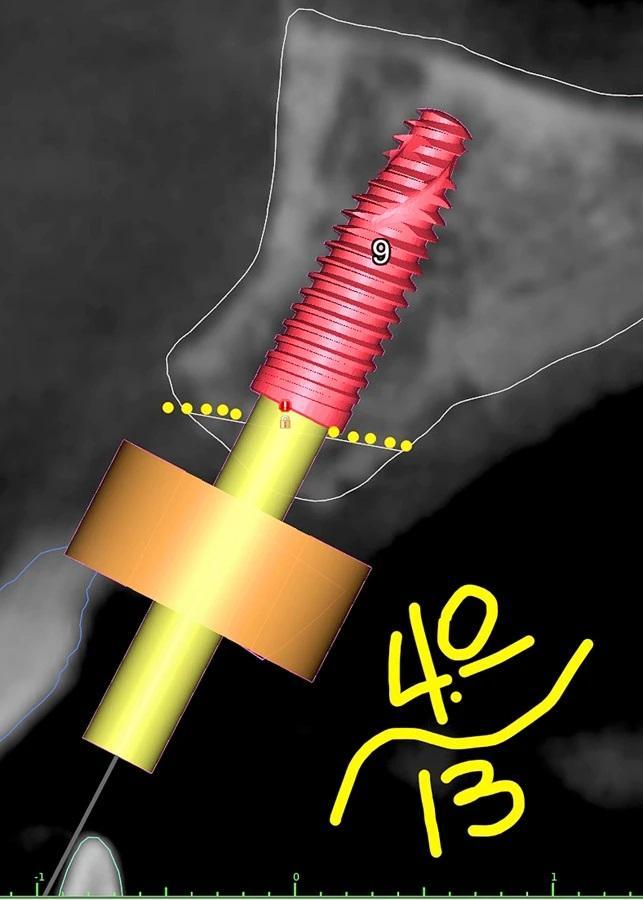



Фото 6: Шесть имитированных имплантатов с тремя анкерными штифтами на нижней челюсти.

С использованием Blue Sky Plan и бесплатной программы для редактирования STL-файлов и других сеточных форматов MeshMixer (Autodesk) была разработана инновационная хирургическая направляющая для верхнечелюстной дуги. Направляющая была разработана на основе реконструированной 3D-модели, которая, в свою очередь, была разработана на основе сегментированных данных в Blue Sky Plan (фото 7a). Уникальность направляющей заключается в передних посадочных местах, которые поворачиваются на место со стороны буккальной части верхнечелюстной кости (фото 7b). Конструкция траектории вращения позволяет направляющей плотно соприкасаться с буккальной костью, а затем поворачиваться до тех пор, пока она не будет установлена сзади в положительном положении на двух опорах (фото 8a-b). Направляющая была бы достаточно устойчивой, если бы ее установили на альвеолярном отростке, но потребовалась бы дополнительная устойчивость, обеспечиваемая одним фиксирующим штифтом, помещенным непосредственно в носоглотку (фото 9).
Фото 7a: Имитация новой траектории вращения направляющей штифта носоглотки (синего цвета), установленной на верхнечелюстной кости. Фронтальный вид с выборочной прозрачностью для визуализации расположения имплантатов.

Фото 7b: Имитация новой траектории вращения направляющего штифта носоглотки (синего цвета), установленного на верхнечелюстной кости. Окклюзионный вид, иллюстрирующий три буккальные опоры с посадочными местами (желтые стрелки).
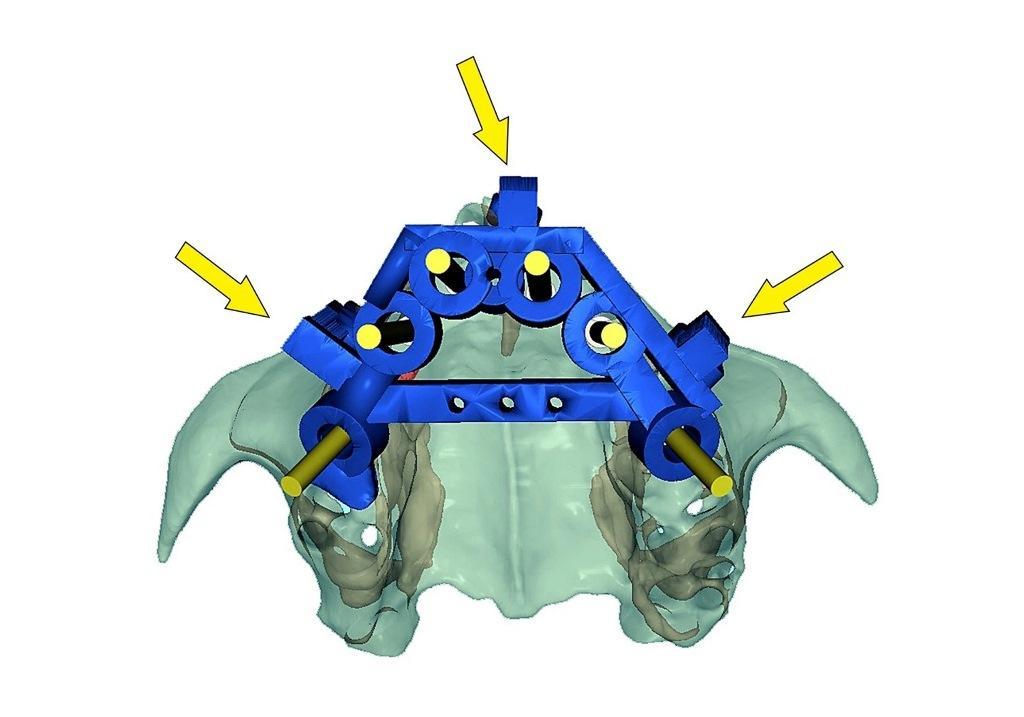
Фото 8a: Имитация хирургической направляющей для верхней челюсти. Боковой вид слева, показывающий передние и задние опоры, а также задний наклонный имплантат, визуализируемый желтым выступом абатмента.

Фото 8b: Имитация хирургической направляющей для верхней челюсти. Боковой вид справа, на котором видны передние и задние опоры, задний наклонный имплантат с желтым выступом абатмента и костные фенестрации.

Фото 9: Увеличенный вид штифта для носоглотки, направляющей штифта для носоглотки (синяя) и верхнечелюстной кости, показывающей передние костные впадины.

Верхняя зубная дуга
В соответствии с планом, основанным на КЛКТ, сначала были удалены зубы верхней челюсти. Зубы нижней челюсти были удалены после завершения формирования верхнечелюстной дуги (фото 10). Новая концепция дизайна обеспечила отличную видимость и доступ для внешней ирригации во время обработки корневых каналов. Хирургическая направляющая была напечатана на 3D-принтере AccuFab-CEL (SHINING 3D) с использованием автоклавируемой биосовместимой фотополимерной смолы, промыто в спирте (91%) и полимеризована в соответствии с протоколом производителя. Направляющая для остеотомии из полимера была разработана таким образом, чтобы она было без втулок на основе используемого набора хирургических направляющих Neo NaviGuide Kit (NeoBiotech).
Фото 10: Удаленные зубы верхней и нижней челюсти.

Единственный анкерный штифт диаметром 2 мм для носонебного канала устанавливался с помощью давления пальца до появления сопротивления (рис. 11а). Легкие удары хирургическим молотком позволили полностью установить штифт, вдавливая направляющую в наружную буккальную кость. Еще одной уникальной особенностью направляющей была горизонтальная стабилизирующая планка, соединяющая правую и левую стороны. Горизонтальная планка содержала специально расположенные отверстия, которые обеспечивали прорези для наложения швов на ткани переднего неба, удерживая их подальше от мест остеотомии (фото 11b). Сначала были установлены передние имплантаты, и к этим имплантатам были прикреплены стабилизаторы направляющей, чтобы полностью обездвижить направляющую, облегчая подготовку к остеотомии с наклоном назад. Благодаря полностью управляемой установке имплантаты были установлены точно по плану, что обеспечило необходимую поддержку для несъемной реставрации с полной дугой (фото 12).
Фото 11a: Вид штифтовой направляющей для носонебного канала, установленной на верхнечелюстной кости с помощью единственного анкерного штифта для стабилизации направляющей.
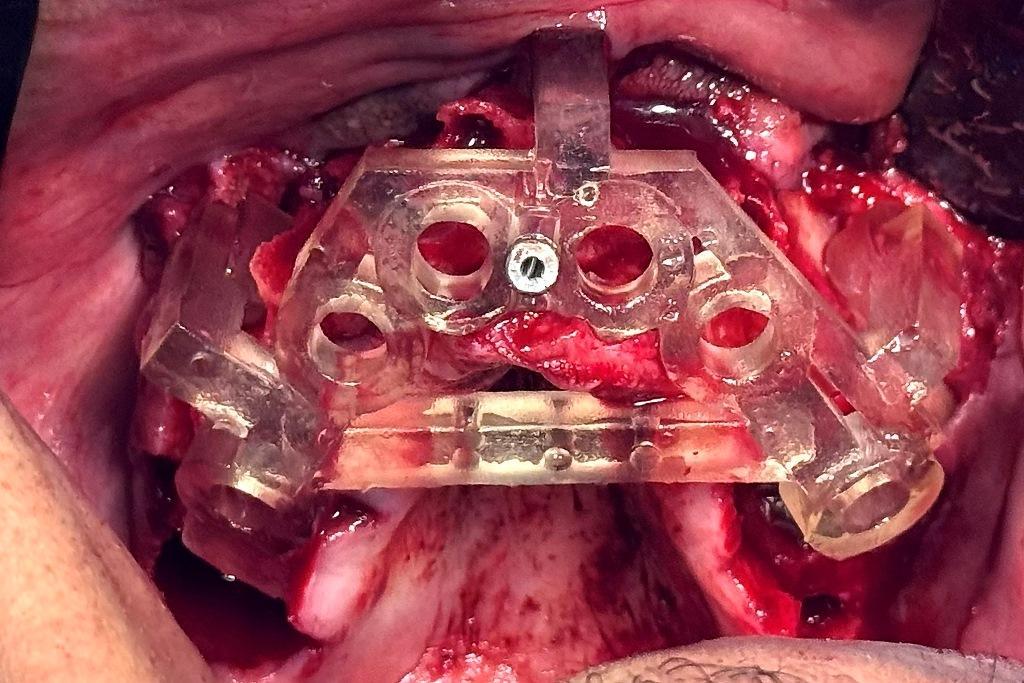
Фото 11b: Горизонтальная стабилизирующая планка (желтый овал) на направляющей с отверстиями для наложения швов для отвода небных тканей. Направляющие стабилизаторы (желтые стрелки), фиксирующие хирургическую направляющую.

Фото 12: Интраоральный вид верхних имплантатов NeoBiotech, установленных в соответствии с планом, показывает лунки после удаления остатков зубов и буккальные костные полости.
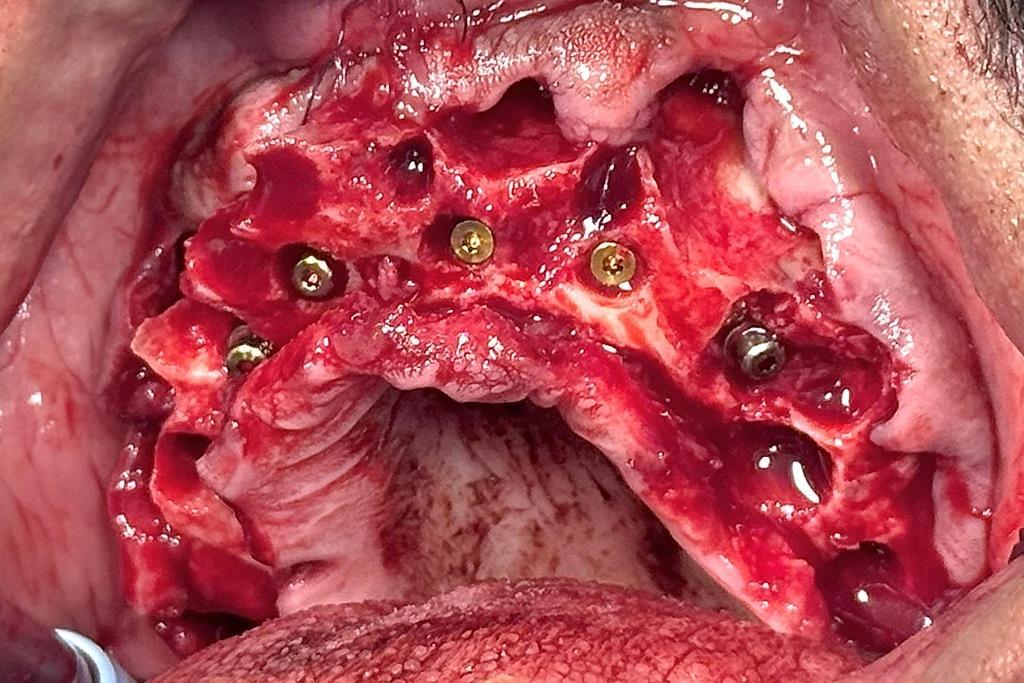
Если бы визуализация была более четкой, можно было бы разглядеть необходимость обширной пластики. Несмотря на стабильность имплантатов, значения коэффициента стабильности имплантатов (Osstell) были недостаточны для немедленной нагрузки, и, учитывая одновременную костную пластику, был определен период заживления от трех до четырех месяцев. В лунки после удаления, отверстия и углубления было помещено примерно 3 см³ минерализованной кортикальной и губчатой кости (Maxxeus). Затем места, на которых проведена операция костной пластики покрывали коллагеновыми мембранами и закрепляли глубокими горизонтальными матрацными швами. Первичное закрытие было достигнуто викриловыми швами №4-0 (Ethicon).
Нижняя зубная дуга
После удаления зубов и репозиции кости операция на нижней челюсти проводилась по аналогичному хирургическому протоколу с использованием костной хирургической направляющей. Развитая сегментация костей и зубов свидетельствовала о серьезной потере костной ткани почти до верхушки многих корней нижней челюсти (фото 13a). Используя выборочную прозрачность, можно было тщательно оценить корни и кость (фото 13b). Объемная 3D-реконструкция, имитирующая кость после удаления, позволила получить уникальное представление об анатомии кости нижней челюсти (фото 14a) и помогла окончательно определить местоположение каждого имплантата (фото 14b).
Фото 13a: Полностью сегментированный нижняя челюсть и зубы.

Фото 13b: Выборочная прозрачность: видны корни, двусторонние ментальные нервы и нижний альвеолярный нерв (желтые стрелки указывают на верхушки корней, показывая степень потери костной ткани).
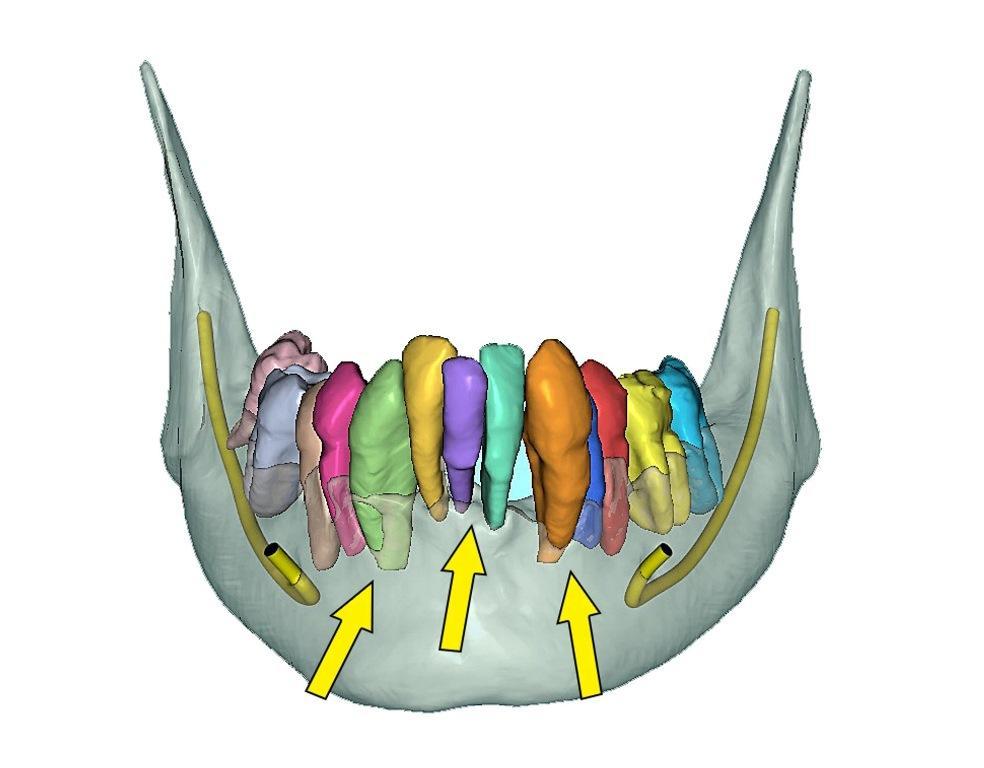
Фото 14a: Окклюзионный вид имитированных лунок после удаления в нижнечелюстной кости.

Фото 14b: Имитация параллельных имплантатов на нижней челюсти с желтыми абатментами.

Имитация уменьшения костной ткани была рассчитана только после подтверждения положения имплантата. Выборочная прозрачность также была важной характеристикой при оценке близости к двусторонним ментальным отверстиям и определяла вертикальное расположение имплантатов (фото 15a). Как только положение имплантата было подтверждено, была разработана костная направляющая двойного назначения (фото 15b). Первая цель состояла в том, чтобы перенести запланированное уменьшение кости на буккальную часть нижней челюсти, а вторая - провести остеотомию с помощью расширенной сегментации кости.
Фото 15a: Выборочная прозрачность показывает степень необходимого уменьшения костной ткани и имитацию имплантатов с желтыми абатментами.

Фото 15b: Имитация хирургической направляющей (синяя), обозначающая место вправления кости, надежно закрепленной на нижней челюсти для точной подготовки к остеотомии.

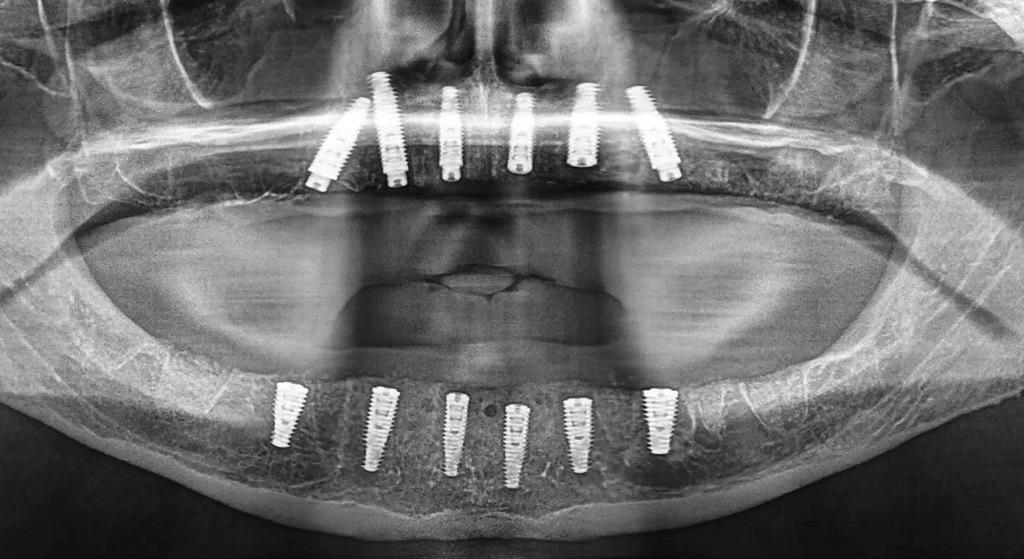
Восстановление кости нижней челюсти было выполнено с использованием пьезоэлектрической хирургии (PIEZOSURGERY, mectron) и набора вращающихся инструментов для хирургического контурирования и модификации альвеолярного отростка (Alveoplasty Surgical Kit (артикул ALV18) Meisinger), чтобы обеспечить достаточную ширину и пространство для реставрации с опорой на имплантат. После завершения редукции кости на альвеолярный отросток нижней челюсти был установлена костная остеотомическая направляющая. Усовершенствованная сегментация, созданная с помощью ИИ, обеспечила плотную посадку направляющей, которая затем была закреплена тремя горизонтальными анкерными штифтами и стабилизаторами направляющей для фиксации направляющей в процессе препарирования (фото 16a). Как только шесть имплантатов были успешно установлены, направляющая была удалена, обнажив уменьшенную кость и лунки после удаления (фото 16b). В углубления после удаления и оставшиеся отверстия было помещено примерно 1 см³ минерализованной кортикальной и губчатой кости. Значения коэффициента стабильности имплантата были недостаточны для немедленной нагрузки, и поэтому для имплантации дуги нижней челюсти был выбран двухэтапный протокол. Послеоперационная панорамная визуализация показала успешную установку в общей сложности 12 имплантатов в нижнечелюстную и в верхнечелюстную дуги (фото 17).
Фото 16a: Интраоперационный вид хирургической направляющей, установленной на нижнечелюстной кости с тремя анкерными штифтами и тремя направляющими-стабилизаторами, закрепленными на передних имплантатах.

Фото 16b: Лицевой вид нижнечелюстных имплантатов, установленных в уменьшенный гребень с остаточными лунками после удаления.

Фото 17: Послеоперационная панорамная рентгенограмма, на которой показано успешное размещение 12 имплантатов в соответствии с двухэтапным протоколом, требующим периода заживления в течение трех-четырех месяцев до раскрытия.
Обсуждение
С момента внедрения КЛКТ в стоматологическую визуализацию процесс анатомической сегментации для диагностики, планирования лечения и 3D-печати продолжает развиваться. КЛКТ обеспечивает 3D-сканирование челюстно-лицевой области с высоким разрешением и низким уровнем излучения, что идеально подходит для планирования имплантации. Стереолитография позволяет точно изготавливать как анатомические модели, так и индивидуальные каркасы имплантатов и хирургические направляющие из экспортированных данных в формате DICOM для улучшения подгонки, сокращения времени операции, повышения точности и улучшения долгосрочных результатов для пациентов. Исторически сложилось так, что важнейший этап отделения кости нижней челюсти от окружающих мягких тканей и зубов для получения точных поверхностей, пригодных для печати, занимал много времени. Исследования показали, что сегментация КЛКТ с помощью искусственного интеллекта обеспечивает объемную точность и детализацию поверхности, достаточные для 3D-печати и планирования хирургических вмешательств при дефектах верхней и нижнечелюстной кости, а также для рабочих процессов имплантации.
В представленном клиническом случае показано, как сегментация костей и зубов, созданная с помощью ИИ, может помочь в диагностике, планировании лечения и разработке направляющих для верхней и нижнечелюстной костей. Направляющие точно прилегают к костной поверхности обеих дуг, обеспечивая стабильность для точной подготовки к остеотомии в двух дугах с разной анатомической топографией. Направляющие, напечатанные на 3D-принтере, были сконструированы без втулок для максимальной точности на основе используемых сверл с широким хвостовиком. Конструкция с широким хвостовиком обеспечивает контакт с направляющим цилиндром из полимера только на внешнем конце сверла, защищая режущую поверхность сверла. Недавние исследования подтверждают превосходную точность по сравнению с металлическими втулками.
Внедрение усовершенствованной сегментации, созданной с помощью ИИ, предоставило инструменты, необходимые для разработки новой хирургической направляющей верхней челюсти, представленной в этой статье. Новая хирургическая направляющая с ротационной траекторией была разработана таким образом, чтобы располагаться на верхнечелюстной кости, захватывая буккальные вырезы, и закреплялась с помощью единственного фиксирующего штифта, введенного в носоглотку. Возможность достоверного представления топографии костной поверхности способствовала проведению первоначального исследования, а также разработке и успешному выполнению данной хирургической направляющей для установки имплантатов в челюстную дугу. Вторая направляющая также была разработана таким образом, чтобы точно прилегать к нижнечелюстной кости, что облегчало точную установку шести имплантатов для поддержки будущей несъемной реставрации.
Хирургическая направляющая для штифта носоглотки также была дополнена насадками для обеспечения точности синус-лифтинга и полностью управляемой установки скуловых и крыловидных имплантатов. Для подтверждения этих дополнительных протоколов потребуются дальнейшие исследования.
Заключение
Сегодня 3D-печатные модели, полученные с помощью компьютерной томографии и КЛКТ, прочно вошли в стоматологическую практику. Хирурги, лаборанты и инженеры полагаются на них при разработке хирургических направляющих и имплантатов для конкретных пациентов, ортопеды используют их для планирования реставраций с точным учетом анатомических особенностей, а исследователи продолжают совершенствовать цифровые рабочие процессы, которые объединяют визуализацию, CAD и аддитивное производство в единый процесс. По мере улучшения разрешения изображений и усложнения аддитивного производства синергия между 3D-печатью и стоматологической и медицинской визуализацией будет способствовать дальнейшему развитию персонализированного лечения как в медицине, так и в стоматологии, стимулируя непрерывные инновации. Внедрение ИИ для решения трудоемких задач, таких как сегментация костей и зубов, будет иметь огромное значение для будущего дентальной имплантологии и многого другого.
Автор: Dr Scott D. Ganz
Использование 3D-визуализации стало стандартом диагностики и планирования лечения при проведении многих медицинских и стоматологических процедур. Впервые такая визуализация была доступна с помощью широкоформатных медицинских компьютерных томографов, которые предоставляли клиницистам, исследователям и инженерам статичные видеоизображения на пленке. На ранних этапах компьютерной томографии была получена серия изображений поперечного сечения, которые были записаны на пленку. Это была та же самая среда, которая использовалась для обычных рентгенограмм и требовала химической разработки. Рентгенографические пленки требовали больших световых коробов для визуализации анатомии пациента. Наступление цифровой эры и совершенствование технологий привели к разработке пленок для сухой обработки. В настоящее время компьютерная томография в основном отображается на мониторах компьютеров в виде цифровых изображений, а печать на пленке стала менее распространенным вариантом. Визуализация была и остается дорогостоящей для пациента.

Исторически сложилось так, что использование физического моделирования на основе компьютерной томографии появилось в конце 1980-х и начале 1990-х годов, вскоре после коммерческого внедрения стереолитографии. Челюстно-лицевая хирургия стала передовой областью применения этой технологии, поскольку хирурги использовали напечатанные на 3D-принтере модели черепа для планирования реконструкций и разработки имплантатов для конкретных пациентов. Да, раннее производство было дорогостоящим и требовало больших технических затрат, но оно продемонстрировало, как можно сочетать медицинскую визуализацию и аддитивное производство для повышения точности и улучшения результатов лечения. По мере развития программного обеспечения в 1990-х и 2000-х годах рабочие процессы CT-to-STL становились все более эффективными. Автоматизированная сегментация, инструменты для восстановления сетки (для исправления ошибок в сетках STL) и все более доступные принтеры позволили использовать 3D-модели в ортопедии, сердечно-сосудистой хирургии и онкологии. Возможность использования различных материалов в стереолитографии еще больше расширила ее клиническую ценность, позволив изготавливать модели, имитирующие как твердые, так и мягкие ткани.
КЛКТ, представленная в начале 2000-х годов, стала доступна в виде стационарного устройства благодаря своей более низкой стоимости и компактности, обеспечивая немедленный доступ к важным 3D-данным при снижении радиационного облучения и затратах. Особенно значительным достижением в стоматологии стало изготовление на заказ поднадкостничных (субпериостальных) имплантатов - устройств, которые крепятся к поверхности кости под надкостницей для поддержки протезированных зубов. Традиционно поднадкостничные имплантаты требовали предварительной хирургической процедуры для обнажения челюстной кости и создания физического слепка, который затем использовался для ручной установки металлического каркаса — процесса, связанного со значительной болезненностью и неточностью. Появление компьютерного моделирования на основе компьютерной томографии коренным образом изменило этот рабочий процесс. Компьютерная томография с высоким разрешением позволила получить точную форму альвеолярного отростка пациента без инвазивного снятия слепка. Разделив челюстную кость на сегменты по данным компьютерной томографии и создав модель для 3D-печати, лаборатории смогли разработать индивидуальные поднадкостничные каркасы, которые с гораздо большей точностью соответствовали бы анатомии пациента. Такие пионеры, как Х.П. Труитт и Леонард Линкоу, помогли обучить индустрию тому, как эту технологию можно использовать для изготовления поднадкостничных имплантатов; однако при использовании компьютерной томографии существовало существенное ограничение: разрешение поперечного сечения и доступное программное обеспечение не всегда позволяли создавать точные 3D-модели.
Благодаря постоянному прогрессу в области объемного челюстно-лицевого сканирования с высоким разрешением, а также распространению лабораторных и офисных 3D-принтеров создание цифровых моделей кости нижней и верхней челюстей стало значительно более распространенным явлением. Традиционный конвейер — сбор данных, сегментация, реконструкция поверхности, восстановление сетки, CAD, стереолитография или производство металлических припоев — позволяет создавать как анатомические модели, так и имплантаты и хирургические направляющие для конкретного пациента. Для пациентов с тяжелой формой альвеолярной атрофии, которым не могут быть установлены обычные корневидные имплантаты, в качестве предсказуемой альтернативы вновь появились специальные поднадкостничные каркасы, изготовленные с помощью цифровых технологий. В клинических отчетах описаны титановые поднадкостничные имплантаты, напечатанные на 3D-принтере для атрофированной нижней и верхнечелюстной кости, которые по сравнению с аналогичными рабочими процессами улучшают посадку, сокращают время пребывания в кресле и упрощают реабилитацию при протезировании. Современные костные имплантаты для конкретных пациентов, которые изготавливаются с использованием передовых технологических процессов, включающих сегментацию и стереолитографию или производство металлических припоев, начинают проникать на рынок; однако из-за уникального технологического процесса они остаются дорогостоящими и ограничены в использовании и доступности по сравнению с обычными зубными имплантатами. Тем не менее, этот процесс доказал эффективность усовершенствованной сегментации кости при применении зубных имплантатов и, особенно, хирургических направляющих.
STL-файлы, созданные с помощью расширенной сегментации, теперь можно экспортировать на настольные 3D-принтеры. Таким образом, клиницисты и зуботехнические лаборатории теперь могут печатать модели нижней и верхней челюстей с высоким разрешением. Кроме того, с появлением собственной технологии 3D-печати клиницисты и лаборатории разработали и напечатали хирургические направляющие для имплантации зубов, мягких тканей и костей. Независимо от конечного желаемого результата, разрешение и детализация поверхности анатомических моделей зависят от процесса сегментации. Внедрение искусственного интеллекта (ИИ) для облегчения утомительной задачи сегментации позволило добиться значительных улучшений, включая полную автоматизацию процесса сегментации костей и зубов. Поскольку усовершенствованная сегментация, созданная с помощью ИИ, становится доступной с помощью бесплатного программного обеспечения, такого как Blue Sky Plan (Blue Sky Bio), которое обеспечивает более быстрые, точные, воспроизводимые и чистые результаты, можно с большей эффективностью разрабатывать хирургические направляющие для костной хирургии. Кроме того, усовершенствованный процесс проектирования может способствовать внедрению инноваций, о чем свидетельствует недавно представленный направляющий штифт для носо-небного канала с поворотным контуром, который разработан для верхней челюсти. Исследование новой конструкции выявило 22 последовательных случая, в которых носоглотка использовалась для стабилизации костных хирургических направляющих. В серии случаев было удалено 152 зуба и установлено 123 имплантата для поддержки 18 несъемных протезов и четырех съёмных накладных протезов, что стало возможным благодаря усовершенствованной анатомической сегментации, сгенерированной ИИ. Данный клинический случай представляет собой продолжение оригинальной серии случаев, которая была расширена до 45 пациентов.
Клинический случай
49-летний мужчина обратился с жалобами на разрушение зубов верхней и нижней челюсти. Результаты клинических и рентгенологических исследований показали тяжелое заболевание пародонта, общую потерю костной ткани, увеличение расстояния между передними зубами и подвижность зубов, а также общее неудовлетворительное соблюдение гигиены (фото 1a-b, 2a). Пациент был проинформирован о результатах исследования и было обсуждено несколько вариантов лечения, включая полные и/или частичные протезы, съемные протезы на имплантатах и несъемные протезы на имплантатах. После обсуждения вариантов пациент выбрал несъемные протезы на имплантатах для всей челюсти.
Фото 1a: Дооперационная ситуация. Интраоральный ретракционный снимок верхней челюсти, показывающий прогрессирующее заболевание пародонта и расстояние между зубами.

Фото 1b: Дооперационная ситуация. Интраоральный ретракционный вид верхней и нижней челюсти в окклюзии.

Фото 2a: Предоперационная панорамная рентгенограмма, показывающая обширную потерю костной ткани.

Первоначальный план восстановления верхней челюсти состоял в удалении всех оставшихся зубов, установке шести имплантатов и использовании костного материала там, где это необходимо, для заполнения лунки и других углублений или отверстий. Имитированные имплантаты были визуализированы на панорамной реконструкции, включая фиксирующий штифт, расположенный по средней линии, соединяющей носоглотку (фото 2b). Используя расширенные возможности для различения объектов на основе их радиопрозрачности, интерактивное программное обеспечение для планирования лечения (Blue Sky Plan) и настраиваемую пользователем избирательную прозрачность, можно в полной мере оценить имитацию имплантатов при 3D-визуализации верхнечелюстной кости (фото 3a–c).
Фото 2b: Имитация верхнечелюстного имплантата на панорамной рентгенограмме, показывающей шесть имплантатов и штифт для носоглотки.

Фото 3a: Выборочные прозрачные изображения имитируемых имплантатов в верхнечелюстной дуге, включая имплантаты с наклоном назад, чтобы избежать попадания в верхнечелюстную пазуху, фронтальный вид.

Фото 3b: Вид слева.

Фото 3c: Вид справа.

Усовершенствованная сегментация костей и зубов с помощью ИИ была применена к верхнечелюстной дуге, чтобы помочь в постановке окончательного диагноза и составлении плана лечения для каждого потенциального места установки имплантата (фото 4a). Можно визуализировать расстояние между существующими естественными зубами и полную топографию верхнечелюстной кости, предоставляя важную информацию, необходимую для правильной установки имплантата (фото 4b). Сегментированные естественные зубы были практически удалены, чтобы можно было легко оценить контуры кости и дефекты лунки (фото 4c).
Фото 4a: Объемная 3D-реконструкция верхней челюсти. Степень потери костной ткани и расстояние между передними зубами.

Фото 4b: Окклюзионный вид имитируемых имплантатов с желтыми абатментами для отображения траектории отверстий для доступа к винтам.

Фото 4c: Окклюзионный вид имитируемых удалений и имплантатов в верхней челюсти.

Программное обеспечение позволяет выбирать реалистичные имплантаты из библиотеки производителя для достижения максимальной точности. Все имплантаты были имплантатами IS-III Active с поверхностью SLA корейской компании NeoBiotech. Первоначальное планирование было завершено сначала с помощью срезов изображения в поперечном сечении, которые позволяют получить 360-градусный обзор потенциального места установки имплантата. Каждый срез в поперечном сечении был снабжен комментариями, отражающими длину и диаметр имплантатов, а также степень любых повреждений или отверстий для удаления (фото 5a–h). Аналогичный план был разработан для нижнечелюстной дуги с шестью параллельными имплантатами для поддержки фиксированной реставрации (фото 6).
Фото 5a–h: Имитация поперечного сечения имплантатов с указанием длины и диаметра имплантатов на основе данных КЛКТ-сканирования.








Фото 6: Шесть имитированных имплантатов с тремя анкерными штифтами на нижней челюсти.

С использованием Blue Sky Plan и бесплатной программы для редактирования STL-файлов и других сеточных форматов MeshMixer (Autodesk) была разработана инновационная хирургическая направляющая для верхнечелюстной дуги. Направляющая была разработана на основе реконструированной 3D-модели, которая, в свою очередь, была разработана на основе сегментированных данных в Blue Sky Plan (фото 7a). Уникальность направляющей заключается в передних посадочных местах, которые поворачиваются на место со стороны буккальной части верхнечелюстной кости (фото 7b). Конструкция траектории вращения позволяет направляющей плотно соприкасаться с буккальной костью, а затем поворачиваться до тех пор, пока она не будет установлена сзади в положительном положении на двух опорах (фото 8a-b). Направляющая была бы достаточно устойчивой, если бы ее установили на альвеолярном отростке, но потребовалась бы дополнительная устойчивость, обеспечиваемая одним фиксирующим штифтом, помещенным непосредственно в носоглотку (фото 9).
Фото 7a: Имитация новой траектории вращения направляющей штифта носоглотки (синего цвета), установленной на верхнечелюстной кости. Фронтальный вид с выборочной прозрачностью для визуализации расположения имплантатов.

Фото 7b: Имитация новой траектории вращения направляющего штифта носоглотки (синего цвета), установленного на верхнечелюстной кости. Окклюзионный вид, иллюстрирующий три буккальные опоры с посадочными местами (желтые стрелки).

Фото 8a: Имитация хирургической направляющей для верхней челюсти. Боковой вид слева, показывающий передние и задние опоры, а также задний наклонный имплантат, визуализируемый желтым выступом абатмента.

Фото 8b: Имитация хирургической направляющей для верхней челюсти. Боковой вид справа, на котором видны передние и задние опоры, задний наклонный имплантат с желтым выступом абатмента и костные фенестрации.

Фото 9: Увеличенный вид штифта для носоглотки, направляющей штифта для носоглотки (синяя) и верхнечелюстной кости, показывающей передние костные впадины.

Верхняя зубная дуга
В соответствии с планом, основанным на КЛКТ, сначала были удалены зубы верхней челюсти. Зубы нижней челюсти были удалены после завершения формирования верхнечелюстной дуги (фото 10). Новая концепция дизайна обеспечила отличную видимость и доступ для внешней ирригации во время обработки корневых каналов. Хирургическая направляющая была напечатана на 3D-принтере AccuFab-CEL (SHINING 3D) с использованием автоклавируемой биосовместимой фотополимерной смолы, промыто в спирте (91%) и полимеризована в соответствии с протоколом производителя. Направляющая для остеотомии из полимера была разработана таким образом, чтобы она было без втулок на основе используемого набора хирургических направляющих Neo NaviGuide Kit (NeoBiotech).
Фото 10: Удаленные зубы верхней и нижней челюсти.

Единственный анкерный штифт диаметром 2 мм для носонебного канала устанавливался с помощью давления пальца до появления сопротивления (рис. 11а). Легкие удары хирургическим молотком позволили полностью установить штифт, вдавливая направляющую в наружную буккальную кость. Еще одной уникальной особенностью направляющей была горизонтальная стабилизирующая планка, соединяющая правую и левую стороны. Горизонтальная планка содержала специально расположенные отверстия, которые обеспечивали прорези для наложения швов на ткани переднего неба, удерживая их подальше от мест остеотомии (фото 11b). Сначала были установлены передние имплантаты, и к этим имплантатам были прикреплены стабилизаторы направляющей, чтобы полностью обездвижить направляющую, облегчая подготовку к остеотомии с наклоном назад. Благодаря полностью управляемой установке имплантаты были установлены точно по плану, что обеспечило необходимую поддержку для несъемной реставрации с полной дугой (фото 12).
Фото 11a: Вид штифтовой направляющей для носонебного канала, установленной на верхнечелюстной кости с помощью единственного анкерного штифта для стабилизации направляющей.

Фото 11b: Горизонтальная стабилизирующая планка (желтый овал) на направляющей с отверстиями для наложения швов для отвода небных тканей. Направляющие стабилизаторы (желтые стрелки), фиксирующие хирургическую направляющую.

Фото 12: Интраоральный вид верхних имплантатов NeoBiotech, установленных в соответствии с планом, показывает лунки после удаления остатков зубов и буккальные костные полости.

Если бы визуализация была более четкой, можно было бы разглядеть необходимость обширной пластики. Несмотря на стабильность имплантатов, значения коэффициента стабильности имплантатов (Osstell) были недостаточны для немедленной нагрузки, и, учитывая одновременную костную пластику, был определен период заживления от трех до четырех месяцев. В лунки после удаления, отверстия и углубления было помещено примерно 3 см³ минерализованной кортикальной и губчатой кости (Maxxeus). Затем места, на которых проведена операция костной пластики покрывали коллагеновыми мембранами и закрепляли глубокими горизонтальными матрацными швами. Первичное закрытие было достигнуто викриловыми швами №4-0 (Ethicon).
Нижняя зубная дуга
После удаления зубов и репозиции кости операция на нижней челюсти проводилась по аналогичному хирургическому протоколу с использованием костной хирургической направляющей. Развитая сегментация костей и зубов свидетельствовала о серьезной потере костной ткани почти до верхушки многих корней нижней челюсти (фото 13a). Используя выборочную прозрачность, можно было тщательно оценить корни и кость (фото 13b). Объемная 3D-реконструкция, имитирующая кость после удаления, позволила получить уникальное представление об анатомии кости нижней челюсти (фото 14a) и помогла окончательно определить местоположение каждого имплантата (фото 14b).
Фото 13a: Полностью сегментированный нижняя челюсть и зубы.

Фото 13b: Выборочная прозрачность: видны корни, двусторонние ментальные нервы и нижний альвеолярный нерв (желтые стрелки указывают на верхушки корней, показывая степень потери костной ткани).

Фото 14a: Окклюзионный вид имитированных лунок после удаления в нижнечелюстной кости.

Фото 14b: Имитация параллельных имплантатов на нижней челюсти с желтыми абатментами.

Имитация уменьшения костной ткани была рассчитана только после подтверждения положения имплантата. Выборочная прозрачность также была важной характеристикой при оценке близости к двусторонним ментальным отверстиям и определяла вертикальное расположение имплантатов (фото 15a). Как только положение имплантата было подтверждено, была разработана костная направляющая двойного назначения (фото 15b). Первая цель состояла в том, чтобы перенести запланированное уменьшение кости на буккальную часть нижней челюсти, а вторая - провести остеотомию с помощью расширенной сегментации кости.
Фото 15a: Выборочная прозрачность показывает степень необходимого уменьшения костной ткани и имитацию имплантатов с желтыми абатментами.

Фото 15b: Имитация хирургической направляющей (синяя), обозначающая место вправления кости, надежно закрепленной на нижней челюсти для точной подготовки к остеотомии.

Восстановление кости нижней челюсти было выполнено с использованием пьезоэлектрической хирургии (PIEZOSURGERY, mectron) и набора вращающихся инструментов для хирургического контурирования и модификации альвеолярного отростка (Alveoplasty Surgical Kit (артикул ALV18) Meisinger), чтобы обеспечить достаточную ширину и пространство для реставрации с опорой на имплантат. После завершения редукции кости на альвеолярный отросток нижней челюсти был установлена костная остеотомическая направляющая. Усовершенствованная сегментация, созданная с помощью ИИ, обеспечила плотную посадку направляющей, которая затем была закреплена тремя горизонтальными анкерными штифтами и стабилизаторами направляющей для фиксации направляющей в процессе препарирования (фото 16a). Как только шесть имплантатов были успешно установлены, направляющая была удалена, обнажив уменьшенную кость и лунки после удаления (фото 16b). В углубления после удаления и оставшиеся отверстия было помещено примерно 1 см³ минерализованной кортикальной и губчатой кости. Значения коэффициента стабильности имплантата были недостаточны для немедленной нагрузки, и поэтому для имплантации дуги нижней челюсти был выбран двухэтапный протокол. Послеоперационная панорамная визуализация показала успешную установку в общей сложности 12 имплантатов в нижнечелюстную и в верхнечелюстную дуги (фото 17).
Фото 16a: Интраоперационный вид хирургической направляющей, установленной на нижнечелюстной кости с тремя анкерными штифтами и тремя направляющими-стабилизаторами, закрепленными на передних имплантатах.

Фото 16b: Лицевой вид нижнечелюстных имплантатов, установленных в уменьшенный гребень с остаточными лунками после удаления.

Фото 17: Послеоперационная панорамная рентгенограмма, на которой показано успешное размещение 12 имплантатов в соответствии с двухэтапным протоколом, требующим периода заживления в течение трех-четырех месяцев до раскрытия.

Обсуждение
С момента внедрения КЛКТ в стоматологическую визуализацию процесс анатомической сегментации для диагностики, планирования лечения и 3D-печати продолжает развиваться. КЛКТ обеспечивает 3D-сканирование челюстно-лицевой области с высоким разрешением и низким уровнем излучения, что идеально подходит для планирования имплантации. Стереолитография позволяет точно изготавливать как анатомические модели, так и индивидуальные каркасы имплантатов и хирургические направляющие из экспортированных данных в формате DICOM для улучшения подгонки, сокращения времени операции, повышения точности и улучшения долгосрочных результатов для пациентов. Исторически сложилось так, что важнейший этап отделения кости нижней челюсти от окружающих мягких тканей и зубов для получения точных поверхностей, пригодных для печати, занимал много времени. Исследования показали, что сегментация КЛКТ с помощью искусственного интеллекта обеспечивает объемную точность и детализацию поверхности, достаточные для 3D-печати и планирования хирургических вмешательств при дефектах верхней и нижнечелюстной кости, а также для рабочих процессов имплантации.
В представленном клиническом случае показано, как сегментация костей и зубов, созданная с помощью ИИ, может помочь в диагностике, планировании лечения и разработке направляющих для верхней и нижнечелюстной костей. Направляющие точно прилегают к костной поверхности обеих дуг, обеспечивая стабильность для точной подготовки к остеотомии в двух дугах с разной анатомической топографией. Направляющие, напечатанные на 3D-принтере, были сконструированы без втулок для максимальной точности на основе используемых сверл с широким хвостовиком. Конструкция с широким хвостовиком обеспечивает контакт с направляющим цилиндром из полимера только на внешнем конце сверла, защищая режущую поверхность сверла. Недавние исследования подтверждают превосходную точность по сравнению с металлическими втулками.
Внедрение усовершенствованной сегментации, созданной с помощью ИИ, предоставило инструменты, необходимые для разработки новой хирургической направляющей верхней челюсти, представленной в этой статье. Новая хирургическая направляющая с ротационной траекторией была разработана таким образом, чтобы располагаться на верхнечелюстной кости, захватывая буккальные вырезы, и закреплялась с помощью единственного фиксирующего штифта, введенного в носоглотку. Возможность достоверного представления топографии костной поверхности способствовала проведению первоначального исследования, а также разработке и успешному выполнению данной хирургической направляющей для установки имплантатов в челюстную дугу. Вторая направляющая также была разработана таким образом, чтобы точно прилегать к нижнечелюстной кости, что облегчало точную установку шести имплантатов для поддержки будущей несъемной реставрации.
Хирургическая направляющая для штифта носоглотки также была дополнена насадками для обеспечения точности синус-лифтинга и полностью управляемой установки скуловых и крыловидных имплантатов. Для подтверждения этих дополнительных протоколов потребуются дальнейшие исследования.
Заключение
Сегодня 3D-печатные модели, полученные с помощью компьютерной томографии и КЛКТ, прочно вошли в стоматологическую практику. Хирурги, лаборанты и инженеры полагаются на них при разработке хирургических направляющих и имплантатов для конкретных пациентов, ортопеды используют их для планирования реставраций с точным учетом анатомических особенностей, а исследователи продолжают совершенствовать цифровые рабочие процессы, которые объединяют визуализацию, CAD и аддитивное производство в единый процесс. По мере улучшения разрешения изображений и усложнения аддитивного производства синергия между 3D-печатью и стоматологической и медицинской визуализацией будет способствовать дальнейшему развитию персонализированного лечения как в медицине, так и в стоматологии, стимулируя непрерывные инновации. Внедрение ИИ для решения трудоемких задач, таких как сегментация костей и зубов, будет иметь огромное значение для будущего дентальной имплантологии и многого другого.
Автор: Dr Scott D. Ganz






























































































































































0 комментариев