Восстановление костной ткани при краевой аугментации становится все более важной процедурой последние годы. Это связано с тем, что мы желаем достигать максимально эстетичные результаты у наших пациентов с утраченными зубами. Иногда костные дефекты весьма объемные и поэтому требуют большого количества материала для подсадки. Такие клинические ситуации требуют применения костных блоков или костного материала на титановой пластине, а также недавно разработанные продукты, содержащие костные протеины (BMP), которые чаще называют ростовыми факторами. Титановые пластины помогают избежать сложного второго хирургического доступа, необходимого при блоках аутоткани, при этом являясь экономически весьма разумным решением по сравнению с продуктами ростовых факторов, таких как INFUSE (Medtronix). Такая процедура регенерации костной ткани требует ушитие лоскута без натяжения и хорошего изначального закрытия, так как даже при хорошей шовной технике и адекватном раскрытии надкостницы, наиболее частое осложнение – это отслойка лоскута и обнажение трансплантата. После того как хирургическая рана открывается, а пластина оказывается обнаженной, происходит контаминация трансплантата, что приводит к частичной или полной потере материала.

Ростовые факторы последнее время находились под пристальным вниманием многих техник тканевой регенерации, конкретно в применении аутоконцентратов крови, например тромбоцитарно-обогащенной плазмы, тромбоцитарно-обогащенных ростовых факторов и тромбоцитарно-обогащенном фибрине (PRF).
PRF мембрана содержит большое количество факторов роста. Они синтезируются мегакариоцитами и хранятся в основном в альфа-гранулах тромбоцитов. После того, как тромбоциты активируются в зонах повреждения тканей, они секретируют протеины, такие как фибриноген, фибронектин, витронектин, ростовые факторы, включая BMP, ростовой фактор – бетта, тромбоцитарный ростовой фактор, инсулиноподобный ростовой фактор, сосудисто-эндотелиальный ростовой фактор, ростовой фактор фибробластов и невероятно важный коагуляционный глиикопротеин тромбоспондин-1 в течение 7 дней. Фибриновая мембрана также обеспечивает отличную основу для эпителизации, а высокая концентрация ростовых факторов и высвобождение цитокинов стимулирует процесс заживления путем микроваскуляризации и роста новых тканей.
Я видел хорошие результаты регенерации костной ткани с применением PRF мембран, в то время как процедура аугментации с титановой пластиной привела к отслойке лоскута на раннем этапе, тогда было решено применить PRF мембрану для стимуляции закрытия мягких тканей поверх обнажившейся пластины. Данная статья описывает краевую аугментацию, в которой на раннем этапе произошло обнажение пластины, а также этапы по коррекции данного осложнения.
Клинический случай
Диагностика и план лечения
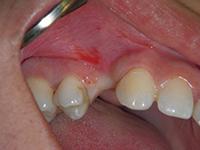
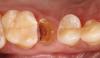
В клинику обратилась здоровая 30-летняя женщина с крупным дефектом альвеолярного гребня в зоне верхнего правого первого премоляра, образовавшегося после удаления инфицированного зуба (Фото 1). При восстановлении дефекта зубного ряда протезом или имплантатом без коррекции костного края возможны неудачи в эстетическом плане.
Фото 1: Фотография недостаточного альвеолярного гребня
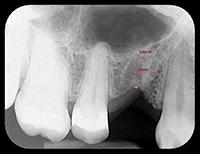
Прицельный рентгеновский снимок показывает двухмерный вид места экстракции и недостаточную высоту костного гребня (Фото 2).
Фото 2: Рентгенограмма недостаточного альвеолярного гребня
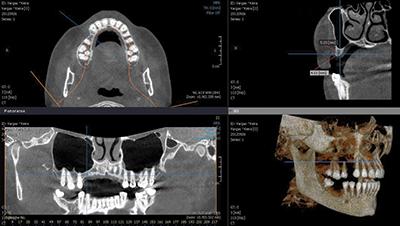
Спиральная томография также была проведена для тщательного планирования лечения. На снимке заметна костная ткань высотой 5,5 мм до дна гайморовой пазухи и шириной менее 3 мм по гребню (Фото 3).
Фото 3: КТ недостаточного альвеолярного гребня
Клинический протокол
Проведена подсадка трансплантата после отслаивания полного мукопериостального лоскута, создавая множественные кортикальные перфорации (Фото 4) для вызова феномена региональной акселерации. Использована титановая пластина с костной массой NovaBone (ACE Surgical) (Фото 5). Титановая пластина стабилизирована тремя титановыми шурупами (MiniPlate Impladent) (Фото 6) и лоскут был ушит Cytoplast Polytetrafluoroethylene (PTFE) нитью (Osteogenics Biomedical) (Фото 7). Рентгенограмма после хирургического вмешательства показала, что трансплантат костной ткани был хорошо фиксирован на титановой пластине, закрепленной тремя шурупами (Фото 8).
Фото 4: Лоскут и кортикальные перфорации
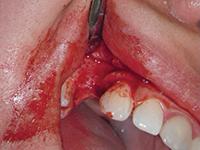
Фото 5: Костная масса на титановой пластине

Фото 6: Фиксация титановой пластины шурупами
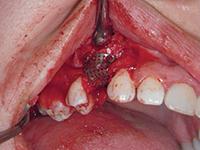
Фото 7: Ушитие лоскута
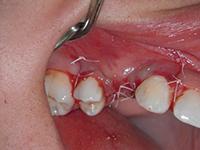
Фото 8: Рентгенограмма после операции
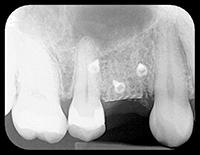
Неделю спустя после вмешательства, на контрольном посещении, рана имела признаки легкого раскрытия по швам (Фото 9) и через две недели, в месте операции появилась обнаженная титановая пластина.
Фото 9: Раннее расхождение швов
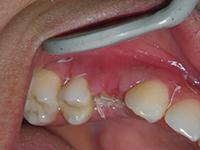
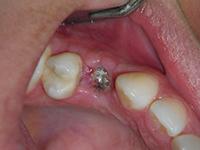
Пациенту было рекомендовано осуществлять полоскания раствором хлоргексидина (Peridex 3M ESPE) дважды в день, а также еженедельно являться для осмотра. Три недели спустя после операции пластина все больше обнажалась с образованием окна в 5 мм, признаки воспаления и инфицирования отсутствовали (Фото 10).
Фото 10: Обнажение пластины спустя три недели
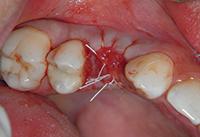
Пациент был предупрежден о риске отторжения трансплантата и согласился на восстановительную терапию PRF. Зона анестезирована, и ткани вокруг обнаженной пластины освежены скальпелем. Под образовавшиеся края введены PRF мембраны, а затем рана ушита PTFE швами (Фото 11).
Фото 11: Обнаженную пластину закрыли тромбоцит обогащенным фибрином (PRF)
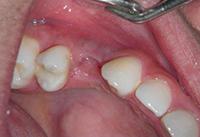
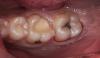
Полное закрытие титановой пластины произошло спустя 2 недели (Фото 12).
Фото 12: Полное закрытие пластины после лечения PRF
Заключительный комментарий
Полученные результаты показывают эффективность PRF мембран при стимулировании эпителизации, а ростовые факторы индуцируют быстрый рост тканей и заживление. По мнению авторов, это один из множества способов применения PRF в ежедневной стоматологической практике.
Автор: Carlos Boudet, DDS
Восстановление костной ткани при краевой аугментации становится все более важной процедурой последние годы. Это связано с тем, что мы желаем достигать максимально эстетичные результаты у наших пациентов с утраченными зубами. Иногда костные дефекты весьма объемные и поэтому требуют большого количества материала для подсадки. Такие клинические ситуации требуют применения костных блоков или костного материала на титановой пластине, а также недавно разработанные продукты, содержащие костные протеины (BMP), которые чаще называют ростовыми факторами. Титановые пластины помогают избежать сложного второго хирургического доступа, необходимого при блоках аутоткани, при этом являясь экономически весьма разумным решением по сравнению с продуктами ростовых факторов, таких как INFUSE (Medtronix). Такая процедура регенерации костной ткани требует ушитие лоскута без натяжения и хорошего изначального закрытия, так как даже при хорошей шовной технике и адекватном раскрытии надкостницы, наиболее частое осложнение – это отслойка лоскута и обнажение трансплантата. После того как хирургическая рана открывается, а пластина оказывается обнаженной, происходит контаминация трансплантата, что приводит к частичной или полной потере материала.

Ростовые факторы последнее время находились под пристальным вниманием многих техник тканевой регенерации, конкретно в применении аутоконцентратов крови, например тромбоцитарно-обогащенной плазмы, тромбоцитарно-обогащенных ростовых факторов и тромбоцитарно-обогащенном фибрине (PRF).
PRF мембрана содержит большое количество факторов роста. Они синтезируются мегакариоцитами и хранятся в основном в альфа-гранулах тромбоцитов. После того, как тромбоциты активируются в зонах повреждения тканей, они секретируют протеины, такие как фибриноген, фибронектин, витронектин, ростовые факторы, включая BMP, ростовой фактор – бетта, тромбоцитарный ростовой фактор, инсулиноподобный ростовой фактор, сосудисто-эндотелиальный ростовой фактор, ростовой фактор фибробластов и невероятно важный коагуляционный глиикопротеин тромбоспондин-1 в течение 7 дней. Фибриновая мембрана также обеспечивает отличную основу для эпителизации, а высокая концентрация ростовых факторов и высвобождение цитокинов стимулирует процесс заживления путем микроваскуляризации и роста новых тканей.
Я видел хорошие результаты регенерации костной ткани с применением PRF мембран, в то время как процедура аугментации с титановой пластиной привела к отслойке лоскута на раннем этапе, тогда было решено применить PRF мембрану для стимуляции закрытия мягких тканей поверх обнажившейся пластины. Данная статья описывает краевую аугментацию, в которой на раннем этапе произошло обнажение пластины, а также этапы по коррекции данного осложнения.
Клинический случай
Диагностика и план лечения
В клинику обратилась здоровая 30-летняя женщина с крупным дефектом альвеолярного гребня в зоне верхнего правого первого премоляра, образовавшегося после удаления инфицированного зуба (Фото 1). При восстановлении дефекта зубного ряда протезом или имплантатом без коррекции костного края возможны неудачи в эстетическом плане.
Фото 1: Фотография недостаточного альвеолярного гребня

Прицельный рентгеновский снимок показывает двухмерный вид места экстракции и недостаточную высоту костного гребня (Фото 2).
Фото 2: Рентгенограмма недостаточного альвеолярного гребня

Спиральная томография также была проведена для тщательного планирования лечения. На снимке заметна костная ткань высотой 5,5 мм до дна гайморовой пазухи и шириной менее 3 мм по гребню (Фото 3).
Фото 3: КТ недостаточного альвеолярного гребня

Клинический протокол
Проведена подсадка трансплантата после отслаивания полного мукопериостального лоскута, создавая множественные кортикальные перфорации (Фото 4) для вызова феномена региональной акселерации. Использована титановая пластина с костной массой NovaBone (ACE Surgical) (Фото 5). Титановая пластина стабилизирована тремя титановыми шурупами (MiniPlate Impladent) (Фото 6) и лоскут был ушит Cytoplast Polytetrafluoroethylene (PTFE) нитью (Osteogenics Biomedical) (Фото 7). Рентгенограмма после хирургического вмешательства показала, что трансплантат костной ткани был хорошо фиксирован на титановой пластине, закрепленной тремя шурупами (Фото 8).
Фото 4: Лоскут и кортикальные перфорации

Фото 5: Костная масса на титановой пластине

Фото 6: Фиксация титановой пластины шурупами

Фото 7: Ушитие лоскута

Фото 8: Рентгенограмма после операции

Неделю спустя после вмешательства, на контрольном посещении, рана имела признаки легкого раскрытия по швам (Фото 9) и через две недели, в месте операции появилась обнаженная титановая пластина.
Фото 9: Раннее расхождение швов

Пациенту было рекомендовано осуществлять полоскания раствором хлоргексидина (Peridex 3M ESPE) дважды в день, а также еженедельно являться для осмотра. Три недели спустя после операции пластина все больше обнажалась с образованием окна в 5 мм, признаки воспаления и инфицирования отсутствовали (Фото 10).
Фото 10: Обнажение пластины спустя три недели

Пациент был предупрежден о риске отторжения трансплантата и согласился на восстановительную терапию PRF. Зона анестезирована, и ткани вокруг обнаженной пластины освежены скальпелем. Под образовавшиеся края введены PRF мембраны, а затем рана ушита PTFE швами (Фото 11).
Фото 11: Обнаженную пластину закрыли тромбоцит обогащенным фибрином (PRF)

Полное закрытие титановой пластины произошло спустя 2 недели (Фото 12).
Фото 12: Полное закрытие пластины после лечения PRF

Заключительный комментарий
Полученные результаты показывают эффективность PRF мембран при стимулировании эпителизации, а ростовые факторы индуцируют быстрый рост тканей и заживление. По мнению авторов, это один из множества способов применения PRF в ежедневной стоматологической практике.
Автор: Carlos Boudet, DDS































































































































































0 комментариев