Непосредственная установка имплантата после экстракции зуба или корня является процедурой уже хорошо проверенной временем. Но случаи непосредственной установки имплантата после удаления остеоинтегрированного его предшественника не так хорошо известны ни в литературе, ни в клинической практике.
Поколения имплантатов приходят и уходят из рынка, но некоторые системы продолжают быть активными конкурентами. В случае перелома имплантата процедура его удаления часто является единственным выходом из сложившейся ситуации. Поэтому хирург должен сделать важное решение: можно ли установить следующий имплантат непосредственно после удаления предыдущего или лучше использовать отсроченный протокол лечения?
Достоинствами непосредственного подхода являются минимизация количества хирургических процедур и сокращение как продолжительности чувства болезненности у пациента, так и общего времени лечения. Адекватную повторную установку имплантата можно провести только с использованием 3-мерной рентгенографии (компьютерной томографии или конусно-лучевой компьютерной томографии – КЛКТ), которая поможет определить, является ли выбранная позиция установки ортопедически целесообразной.
При повторной установке следует учитывать и другие факторы, влияющие на общий прогноз лечения, среди которых присутствие очагов активной инфекции, состояние мягких тканей в области хирургического вмешательства и общесоматический статус пациента. Удаление сломанного имплантата должно быть минимально травматическим, с максимальным сохранением окружающей костной ткани, а также минимизацией риска механического или термического повреждения, поскольку влияние травмы может поставить под угрозу заживление раны и эффективность остеоинтеграции будущей интраоссальной конструкции.
Костная аугментация обеспечивает сохранение и возобновление трехмерной формы альвеолярного гребня, которая является критическим параметром в плане долгосрочного успеха. Алгоритм ее выполнения после удаления имплантата аналогичен таковому после удаления зуба, а успешность реконструкции гребня определяет и успешность имплантации в целом.
В данной статье представлен клинический случай перелома имплантата, который вместе со смежным зубом были удалены и заменены двумя имплантатами в один хирургический прием.
Клинический случай
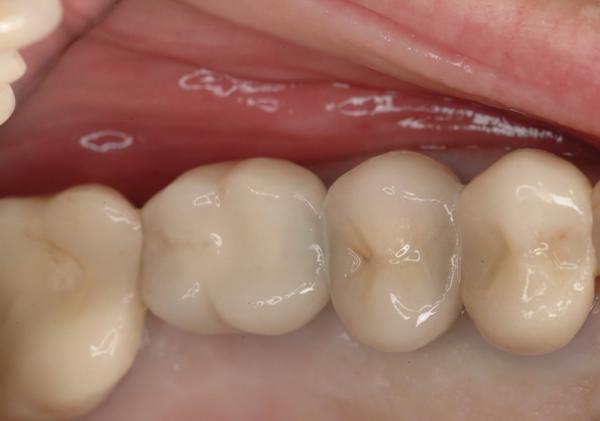
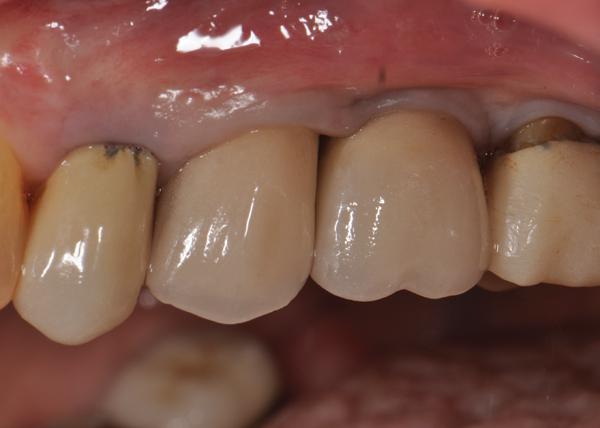
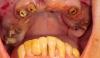
74-летняя пациентка обратилась в клинику по поводу боли в левом квадранте верхней челюсти. Зуб 1.3 был чувствителен к перкуссии и характеризовался подвижностью второй степени. Коронка, зафиксированная на имплантате в области 1.4, также отличалась подвижностью, а при зондировании, которое сопровождалось кровотечением и гноевыделением, были обнаружены карманы глубиной до восьми миллиметров (фото 1).
Фото 1. Пациент обратился за помощью с коронкой на имплантате в области 1.4 зуба. Во время зондирования обнаружены признаки кровотечения, гноетечения и глубина карманов в 8 мм.
Было установлено, что зуб 1.3 был сломлен, таким образом, он подлежал экстракции. Имплантат в области 1.4 также был изломан в месте фиксации супраконструкции, в результате чего абатмент и коронка свободно вращались. План лечения, которое предполагалось провести в один прием, включал экстракцию зуба 1.3 и извлечение не подлежащего восстановлению имплантата в области 1.4 с последующей непосредственной установкой двух имплантатов. Пациент также был проинформирован о том, что подобное вмешательство может потребовать имплементации дополнительного поэтапного подхода.
Лечение
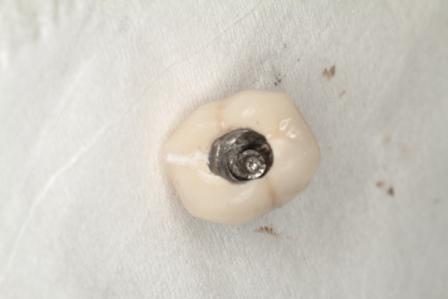
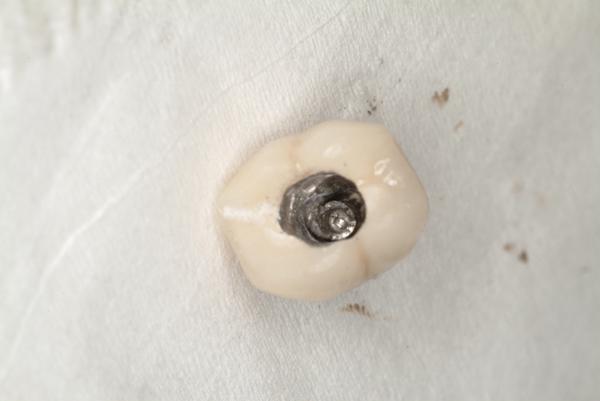
После проведения местной анестезии (Septocaine с адреналином 1: 100000, Septodont) доступ к изломанному имплантату обеспечивали через окклюзионную поверхность путем удаления зафиксированной коронки вместе с абатментом (фото 2).
Фото 2. Доступ сформирован через окклюзионную поверхность коронки, зафиксированной на имплантате.
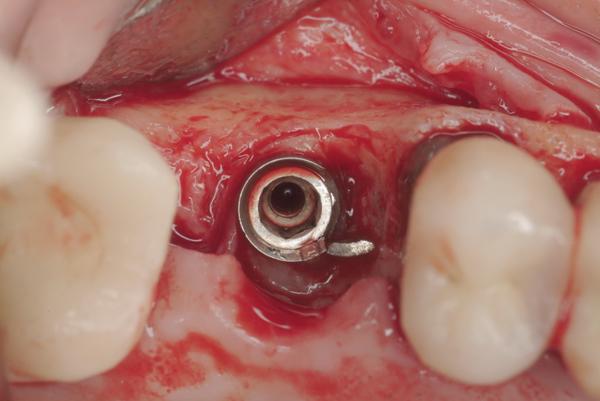
После этого проводили разрез по альвеолярному гребню от 1.2 до 1.5 с выполнением вертикального послабляющего разреза в мезио-букальном направлении. Таким образом, сформировали полный лоскут, при сепарации которого можно было свободно увидеть проблемный имплантат (фото 3).
Фото 3. Сепарация полного лоскута для визуализации имплантата.
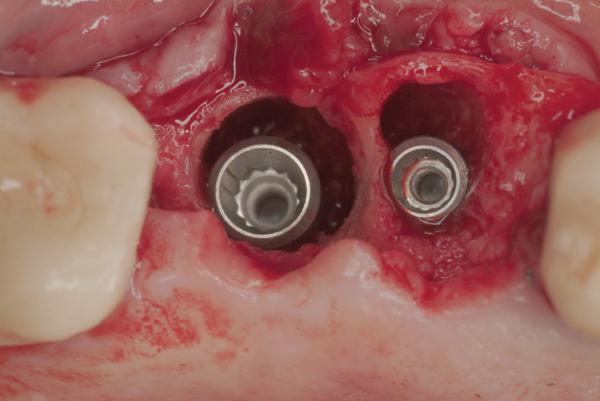
С помощью трепана диаметром 6.00 мм аккуратно удалили сломанный имплантат, а позже и проблемный зуб 1.3. Раны обработали с помощью ручных и ультразвуковых инструментов, а потом промыли раствором доксициклина в течение примерно 3 минут. После тщательной ирригации в области 1.3 установили стандартный 4,0-мм х 13,0 мм имплантат (Astra Tech Implant System, DENTSPLY Implants). После проведения алгоритма BAOSFE (bone-added osteotome sinus floor elevation – аугментация с целью поднятия уровня дна гайморовой пазухи) на месте 1.4 установили имплантат с размерами 5,0-мм х 11-мм (фото 4). Закрытый синус-лифтинг проводили с использованием лиофилизированного трансплантата кортикальной кости (FDBA, LIFENET Health), которым также заполнили промежутки между стенкой альвеолы и установленными имплантатами. Последнюю процедуру выполнили для того, чтобы компенсировать резорбцию альвеолярного гребня в постэкстракционный период. Cardaropoli и коллеги в ходе своих исследований доказали, что использование костного трансплантата и коллагеновой мембраны может минимизировать негативные изменения костной ткани вокруг имплантатов, установленных непосредственно после удаления зубов.
Фото 4. После проведения синус-лифтинга провели установку нового имплантата на месте 1.4 зуба.
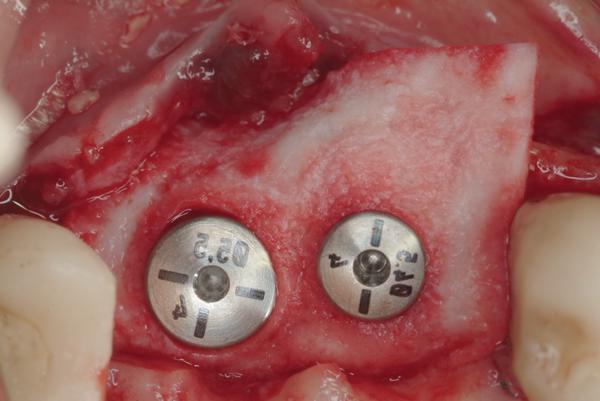
Дермальный аллотрансплантат (PerioDerm Acellular Dermis, DENTSPLY Implants) сформировали с помощью мукотома и адаптировали вокруг формирователей десен, а также поверх щечной и нёбной кортикальных пластинок верхней челюсти (фото 5). Parma-Benfenati и коллеги доказали эффективность использования дермального аллографта в качестве барьерной мембраны для поддержания объема тканей вокруг дентальных имплантатов. Linkevicius в ходе исследований пришел к выводу, что утолщение мягких тканей в периимплантантной области с помощью дермального аллотрансплантата помогает сохранить ткани альвеолярного гребня в большей мере, чем без проведения подобной манипуляции. Его исследование было основано на предположении о том, что толщина мягких тканей влияет на формирование биологической ширины кости без какого-либо ущерба для альвеолярного гребня, а также обеспечивает восстановление вертикальных параметров периимплантатной области.
Фото 5. Адаптация дермального трансплантата со щечной и палатинальной сторон кортикальной пластинки.
Лоскуты адаптировали вокруг формирователей десен и ушили монофиламентными нитями (CV5, GORE-TEX). Мезиобуккальный вертикальный разрез ушили с помощью рассасывающегося шва толщиной 5-0 (Vicryl Rapide, Ethicon). Для контроля правильности проведения манипуляции проводили послеоперационную рентгенографию (фото 6). Учитывая высокую первичную стабильность имплантатов, был реализован трансмукозный вариант заживления. Cordaro и коллеги доказали, что использование подобного подхода не провоцирует чрезмерной потери кости по сравнению с установкой имплантатов полностью погруженных под десну при проведении непосредственной имплантации. На повторном визите через шесть недель клинически и рентгенологически было зарегистрировано физиологическое заживление места вмешательства без каких-либо осложнений (фото 7).
Фото 6. Рентгенограмма, сделанная сразу после операции.
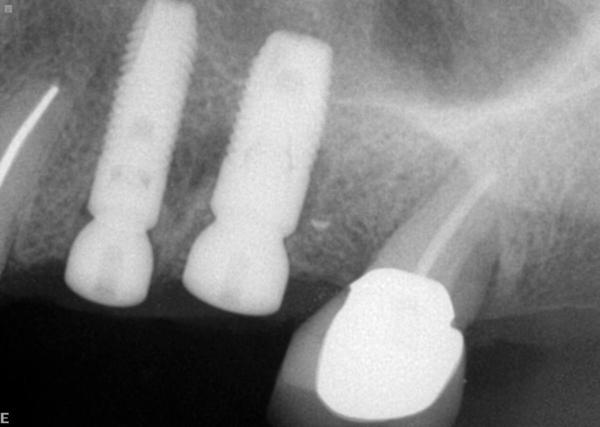
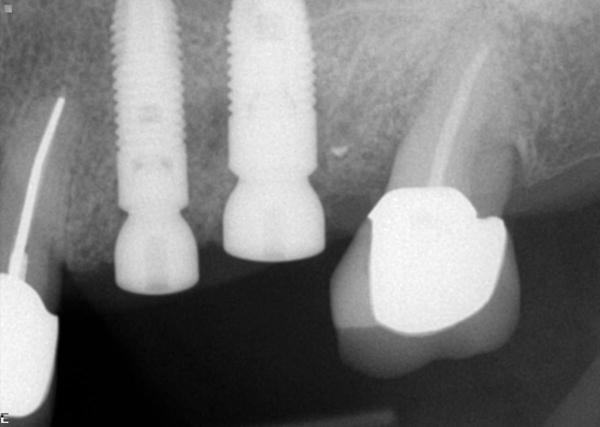
Фото 7. Рентгенограмма, сделанная через 6 недель после вмешательства.
Протетический этап лечения, состоящий из винтовой фиксации двух отдельных коронок, провели примерно через 10 недель после операции. При повторном клиническом осмотре через 18 месяцев после фиксации коронок не было обнаружено никаких признаков воспаления мягких тканях, а конструкция продолжала функционировать безупречно (фото 8).
Фото 8. Через 18 месяцев не обнаружено никаких признаков воспаления мягких тканей, подтверждена полная функциональность конструкции.
Обсуждение
Данный клинический случай описывает подход к реабилитации пациента в один визит. Классический протокол замены сломленных имплантатов, как правило, требует нескольких визитов и проведения серии процедур. Методика непосредственной установки имплантата после удаления зубов довольно хорошо известна и доказательно документирована, однако если говорить о непосредственной замене имплантата с помощью аналогической интраоссальной конструкции, то информации о подобных случаях не так-то много. Часто в случаях переломов имплантатов наблюдаются признаки воспаления и потери костной ткани. Подобные условия не позволяют провести удаление дефектного юнита и повторную имплантацию в один визит, но в нашем случае перелом произошел выше уровня альвеолярного гребня, что не спровоцировало воспалительной реакции твердых и мягких тканей.
Результаты предоперационного КЛКТ- сканирования продемонстрировали наличие необходимого объема здоровой кости с апикальной и палатинальной сторон от дефектного имплантата. Предусматривалось провести замену имплантата с предварительным аккуратным удалением сломанной инфраконструкции. С целью предупреждения постэктракциооного ремоделирования и минимизации уровня резорбции кости была проведена процедура аугментации. Botticelli с коллегами изучили значительные негативные изменения костной ткани, которые возникают после проведения непосредственной имплантации, поэтому для предупреждения подобных было проведено поднятие уровня дна гайморовой пазухи с аугментацией гребня для обеспечения достаточной первичной стабильности имплантата.
Установку имплантата на месте 1.3 зуба и замену конструкции в области 1.4 зуба проводили одновременно с использованием аналогичного клинического подхода.
Если бы имплантат не удалось установить в нужной позиции, пациенту был бы предложен сегментированный поэтапный алгоритм лечения, но поскольку ортопедические условия после имплантации оказались благоприятными – все процедуры были праведны в один визит. Для проведения менеджмента мягких тканей и аугментации кости был сформирован и отсепарирован полный слизисто-надкостничный лоскут, что обеспечило полный доступ к области вмешательства. Реконструкция места имплантации с использованием минимального «закрытого» доступа, согласно данным литературы, является довольно сомнительной, тем более что подобный подход может скомпрометировать эстетический исход проведенного лечения.
Выводы
Адекватный объем диагностической информации, полученный в ходе проведения КЛКТ-сканирования, рентгенографии, анализа окклюзии, а также аргументированный выбор алгоритма лечения помогли обеспечить реабилитацию пациента с проведением экстракции зуба и заменой дефектного имплантата в один визит.
Авторы: Barry P. Levin, DMD; Michael Weiss, DDS
Производители:
Непосредственная установка имплантата после экстракции зуба или корня является процедурой уже хорошо проверенной временем. Но случаи непосредственной установки имплантата после удаления остеоинтегрированного его предшественника не так хорошо известны ни в литературе, ни в клинической практике.

Поколения имплантатов приходят и уходят из рынка, но некоторые системы продолжают быть активными конкурентами. В случае перелома имплантата процедура его удаления часто является единственным выходом из сложившейся ситуации. Поэтому хирург должен сделать важное решение: можно ли установить следующий имплантат непосредственно после удаления предыдущего или лучше использовать отсроченный протокол лечения?
Достоинствами непосредственного подхода являются минимизация количества хирургических процедур и сокращение как продолжительности чувства болезненности у пациента, так и общего времени лечения. Адекватную повторную установку имплантата можно провести только с использованием 3-мерной рентгенографии (компьютерной томографии или конусно-лучевой компьютерной томографии – КЛКТ), которая поможет определить, является ли выбранная позиция установки ортопедически целесообразной.
При повторной установке следует учитывать и другие факторы, влияющие на общий прогноз лечения, среди которых присутствие очагов активной инфекции, состояние мягких тканей в области хирургического вмешательства и общесоматический статус пациента. Удаление сломанного имплантата должно быть минимально травматическим, с максимальным сохранением окружающей костной ткани, а также минимизацией риска механического или термического повреждения, поскольку влияние травмы может поставить под угрозу заживление раны и эффективность остеоинтеграции будущей интраоссальной конструкции.
Костная аугментация обеспечивает сохранение и возобновление трехмерной формы альвеолярного гребня, которая является критическим параметром в плане долгосрочного успеха. Алгоритм ее выполнения после удаления имплантата аналогичен таковому после удаления зуба, а успешность реконструкции гребня определяет и успешность имплантации в целом.
В данной статье представлен клинический случай перелома имплантата, который вместе со смежным зубом были удалены и заменены двумя имплантатами в один хирургический прием.
Клинический случай
74-летняя пациентка обратилась в клинику по поводу боли в левом квадранте верхней челюсти. Зуб 1.3 был чувствителен к перкуссии и характеризовался подвижностью второй степени. Коронка, зафиксированная на имплантате в области 1.4, также отличалась подвижностью, а при зондировании, которое сопровождалось кровотечением и гноевыделением, были обнаружены карманы глубиной до восьми миллиметров (фото 1).
Фото 1. Пациент обратился за помощью с коронкой на имплантате в области 1.4 зуба. Во время зондирования обнаружены признаки кровотечения, гноетечения и глубина карманов в 8 мм.

Было установлено, что зуб 1.3 был сломлен, таким образом, он подлежал экстракции. Имплантат в области 1.4 также был изломан в месте фиксации супраконструкции, в результате чего абатмент и коронка свободно вращались. План лечения, которое предполагалось провести в один прием, включал экстракцию зуба 1.3 и извлечение не подлежащего восстановлению имплантата в области 1.4 с последующей непосредственной установкой двух имплантатов. Пациент также был проинформирован о том, что подобное вмешательство может потребовать имплементации дополнительного поэтапного подхода.
Лечение
После проведения местной анестезии (Septocaine с адреналином 1: 100000, Septodont) доступ к изломанному имплантату обеспечивали через окклюзионную поверхность путем удаления зафиксированной коронки вместе с абатментом (фото 2).
Фото 2. Доступ сформирован через окклюзионную поверхность коронки, зафиксированной на имплантате.

После этого проводили разрез по альвеолярному гребню от 1.2 до 1.5 с выполнением вертикального послабляющего разреза в мезио-букальном направлении. Таким образом, сформировали полный лоскут, при сепарации которого можно было свободно увидеть проблемный имплантат (фото 3).
Фото 3. Сепарация полного лоскута для визуализации имплантата.

С помощью трепана диаметром 6.00 мм аккуратно удалили сломанный имплантат, а позже и проблемный зуб 1.3. Раны обработали с помощью ручных и ультразвуковых инструментов, а потом промыли раствором доксициклина в течение примерно 3 минут. После тщательной ирригации в области 1.3 установили стандартный 4,0-мм х 13,0 мм имплантат (Astra Tech Implant System, DENTSPLY Implants). После проведения алгоритма BAOSFE (bone-added osteotome sinus floor elevation – аугментация с целью поднятия уровня дна гайморовой пазухи) на месте 1.4 установили имплантат с размерами 5,0-мм х 11-мм (фото 4). Закрытый синус-лифтинг проводили с использованием лиофилизированного трансплантата кортикальной кости (FDBA, LIFENET Health), которым также заполнили промежутки между стенкой альвеолы и установленными имплантатами. Последнюю процедуру выполнили для того, чтобы компенсировать резорбцию альвеолярного гребня в постэкстракционный период. Cardaropoli и коллеги в ходе своих исследований доказали, что использование костного трансплантата и коллагеновой мембраны может минимизировать негативные изменения костной ткани вокруг имплантатов, установленных непосредственно после удаления зубов.
Фото 4. После проведения синус-лифтинга провели установку нового имплантата на месте 1.4 зуба.

Дермальный аллотрансплантат (PerioDerm Acellular Dermis, DENTSPLY Implants) сформировали с помощью мукотома и адаптировали вокруг формирователей десен, а также поверх щечной и нёбной кортикальных пластинок верхней челюсти (фото 5). Parma-Benfenati и коллеги доказали эффективность использования дермального аллографта в качестве барьерной мембраны для поддержания объема тканей вокруг дентальных имплантатов. Linkevicius в ходе исследований пришел к выводу, что утолщение мягких тканей в периимплантантной области с помощью дермального аллотрансплантата помогает сохранить ткани альвеолярного гребня в большей мере, чем без проведения подобной манипуляции. Его исследование было основано на предположении о том, что толщина мягких тканей влияет на формирование биологической ширины кости без какого-либо ущерба для альвеолярного гребня, а также обеспечивает восстановление вертикальных параметров периимплантатной области.
Фото 5. Адаптация дермального трансплантата со щечной и палатинальной сторон кортикальной пластинки.

Лоскуты адаптировали вокруг формирователей десен и ушили монофиламентными нитями (CV5, GORE-TEX). Мезиобуккальный вертикальный разрез ушили с помощью рассасывающегося шва толщиной 5-0 (Vicryl Rapide, Ethicon). Для контроля правильности проведения манипуляции проводили послеоперационную рентгенографию (фото 6). Учитывая высокую первичную стабильность имплантатов, был реализован трансмукозный вариант заживления. Cordaro и коллеги доказали, что использование подобного подхода не провоцирует чрезмерной потери кости по сравнению с установкой имплантатов полностью погруженных под десну при проведении непосредственной имплантации. На повторном визите через шесть недель клинически и рентгенологически было зарегистрировано физиологическое заживление места вмешательства без каких-либо осложнений (фото 7).
Фото 6. Рентгенограмма, сделанная сразу после операции.

Фото 7. Рентгенограмма, сделанная через 6 недель после вмешательства.

Протетический этап лечения, состоящий из винтовой фиксации двух отдельных коронок, провели примерно через 10 недель после операции. При повторном клиническом осмотре через 18 месяцев после фиксации коронок не было обнаружено никаких признаков воспаления мягких тканях, а конструкция продолжала функционировать безупречно (фото 8).
Фото 8. Через 18 месяцев не обнаружено никаких признаков воспаления мягких тканей, подтверждена полная функциональность конструкции.

Обсуждение
Данный клинический случай описывает подход к реабилитации пациента в один визит. Классический протокол замены сломленных имплантатов, как правило, требует нескольких визитов и проведения серии процедур. Методика непосредственной установки имплантата после удаления зубов довольно хорошо известна и доказательно документирована, однако если говорить о непосредственной замене имплантата с помощью аналогической интраоссальной конструкции, то информации о подобных случаях не так-то много. Часто в случаях переломов имплантатов наблюдаются признаки воспаления и потери костной ткани. Подобные условия не позволяют провести удаление дефектного юнита и повторную имплантацию в один визит, но в нашем случае перелом произошел выше уровня альвеолярного гребня, что не спровоцировало воспалительной реакции твердых и мягких тканей.
Результаты предоперационного КЛКТ- сканирования продемонстрировали наличие необходимого объема здоровой кости с апикальной и палатинальной сторон от дефектного имплантата. Предусматривалось провести замену имплантата с предварительным аккуратным удалением сломанной инфраконструкции. С целью предупреждения постэктракциооного ремоделирования и минимизации уровня резорбции кости была проведена процедура аугментации. Botticelli с коллегами изучили значительные негативные изменения костной ткани, которые возникают после проведения непосредственной имплантации, поэтому для предупреждения подобных было проведено поднятие уровня дна гайморовой пазухи с аугментацией гребня для обеспечения достаточной первичной стабильности имплантата.
Установку имплантата на месте 1.3 зуба и замену конструкции в области 1.4 зуба проводили одновременно с использованием аналогичного клинического подхода.
Если бы имплантат не удалось установить в нужной позиции, пациенту был бы предложен сегментированный поэтапный алгоритм лечения, но поскольку ортопедические условия после имплантации оказались благоприятными – все процедуры были праведны в один визит. Для проведения менеджмента мягких тканей и аугментации кости был сформирован и отсепарирован полный слизисто-надкостничный лоскут, что обеспечило полный доступ к области вмешательства. Реконструкция места имплантации с использованием минимального «закрытого» доступа, согласно данным литературы, является довольно сомнительной, тем более что подобный подход может скомпрометировать эстетический исход проведенного лечения.
Выводы
Адекватный объем диагностической информации, полученный в ходе проведения КЛКТ-сканирования, рентгенографии, анализа окклюзии, а также аргументированный выбор алгоритма лечения помогли обеспечить реабилитацию пациента с проведением экстракции зуба и заменой дефектного имплантата в один визит.
Авторы: Barry P. Levin, DMD; Michael Weiss, DDS






























































































































































0 комментариев