Повреждение ветвей тройничного нерва (например, нижнего альвеолярного, языкового, подбородочного или подглазничного) является потенциальным осложнением, которое может развиться в ходе выполнения процедуры дентальной имплантации.
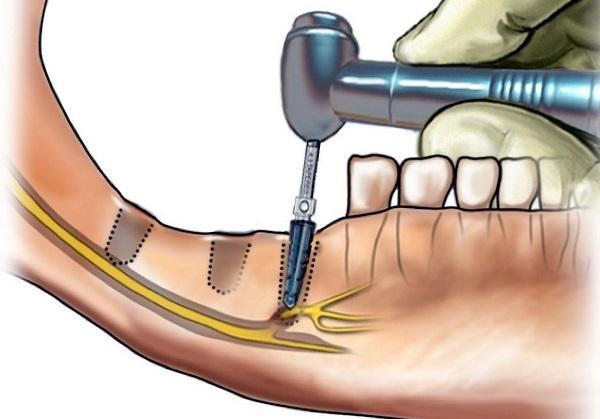
В данной статье мы обсудим подходы к лечению стоматологических пациентов с поражением нервов челюстно-лицевой области ассоциированных с процедурой дентальной имплантации, а также основные аспекты этиологии и патогенеза подобных патологий в целом.
Анатомия и гистология тройничного нерва
Тройничный нерв представляет собой пятую и наибольшую пару черепных нервов, которая состоит из следующих ветвей: очного нерва (V1), верхнечелюстного нерва (V2) и нижнечелюстного нерва (V3). Нижнечелюстной нерв является самой большой ветвью и иннервирует нижнюю губу, область подбородка, зубы, смежные мягкие ткани, нижнюю челюсть и часть наружного уха. Двигательные волокна нижнечелюстного нерва не поддаются повреждению во время процедуры имплантации, поскольку они отходят от основной ветви V3 еще до выхода из подбородочного отверстия. Основной структурной единицей нерва является нервное волокно. В структуре V3 преобладают миелинизированные нервные волокна. Каждый аксон и шванновская клетка покрыты соединительной тканью, которая называется эндоневрием. Группы нервных волокон формируют пучки, которые окружены эпиневрием. Поражение любой части нервного пучка может привести к нейросенсорным нарушениям. Тройничный нерв состоит с 7000-12000 аксонов, а количество пучков варьирует в разных участках челюстно-лицевой области. Нижний альвеолярный нерв (НАН) является полипучковым (состоит больше чем из 10 пучков), в то время как язычный нерв включает лишь несколько аналогичных нервных структур. Поскольку НАН характеризуется большим количеством нервных пучков его регенераторные способности также значительно выше по сравнению с язычным нервом.
Типы нервных поражений
Поражения тройничного нерва могут быть спровоцированы компрессией, растяжением, полным или же частичным нарушением целостности нервного волокна. Повреждения могут привести к нейросенсорным изменениям в отношении чувствительности прикосновения, давления, температуры и боли. Подобные патологии заметно влияют на комфорт и возможность пациента нормально разговаривать, кушать, целоваться, бриться, наносить макияж, чистить зубы и пить. Кроме того, нейросенсорные нарушения также влияют на возможность пациента нормально взаимодействовать в социуме. Признаки данных патологий могут быть идентифицированы непосредственно во время проведения хирургического вмешательства (при наличие болевого симптома), так и в процессе длительного мониторинга за состоянием пациента. Для описания травматических поражений аксонов разной степени сложности используют следующие термины:
- нейропраксия – поражение при котором сохраняется целостность нервного волокна, а механизм травмы связан с растяжением или воздействием по типу тупой травмы; чувствительность, как правило, нормализируется на протяжении нескольких дней или недель.
- аксонотмезис – поражение нерва, при котором развиваются процессы его дегенерации и регенерации, однако сам аксон при этом не теряет своей целостности, и чувствительность нормализируется на протяжении 2-4 месяцев; однако чувствительность после восстановления может быть несколько меньше, чем до вмешательства, а в отдельных клинических случаях характеризуется сопровождающей дизестезией.
- нейротмезис – поражение нерва, при котором отмечается нарушение его целостности, а прогноз восстановления нормальной чувствительности является неблагоприятным.
Международная ассоциация по изучению боли стандартизировала номенклатуру, касающуюся травматических поражений нервов. В частности, было изменено определение термина парестезия, которое раньше использовалось для обозначения потери чувствительности. Актуальная терминология предусматривает следующие определения:
- парестезия – изменение чувствительности без сопутствующих неприятных ощущений;
- дизестезия – изменение чувствительности, которое сопровождается неприятными ощущениями;
- анестезия – потеря чувствительности.
Для описания изменений нейросенсорных функций также используются такие термины, как аллодиния (возникновение боли на раздражители, которые в норме болевых ощущений не провоцируют), каузалгия (наличие персистирующей жгучей боли), гипостезия (снижение чувствительности на действие раздражителей), гиперестезия (повышение чувствительности на действие раздражителей).
Когда нервы растягиваются или сжимаются, периневрий защищает пучки от повреждения. Однако удлинение нерва более чем на 30% может спровоцировать его структурное поражение. При полном нарушении целостности нерва отмечается развитие симптомов анестезии и снижение определенных сенсорных функций. При частичном нарушении целостности нервного волокна могут наблюдаться различные симптомы поражения, включающие дизестезию. Следует отметить, что наличие персистирующей боли после оперативного вмешательства не является критерием для определения потенциальной возможности потенциального полного восстановления функции пораженного волокна.
После повреждения периферического нерва начинает развиваться валлеровская дегенерация, которая продолжается на протяжении нескольких недель и даже месяцев. Дистальнее места травматического пересечения развивается некроз аксонов. Дегенерация в подобных случаях является прогрессирующей и необратимой и длиться на протяжении до 18 месяцев. На возможность заживления пораженной области нерва влияют такие факторы как общее состояние здоровья пациента, возраст и тип поражения. Ключевым моментом в процессе восстановления нерва после поражения является формирование рубцовой ткани в области эндоневральных тубул.
Оценка травматических поражений тройничного нерва
Чаще всего в ходе установки дентальных имплантатов поражается НАН. Признаки поражения нижнего альвеолярного нерва включаются анестезию, парестезию или дизестезию в области кожи, нижней губы, щеки и десен до участка второго моляра. Пациенты же с повреждением язычного нерва характеризуются неконтролируемым слюноотделением, надкусыванием языка, ощущением изжоги, потерей вкуса, изменениями речи и функции глотания, онемением слизистой и языка. Как в ходе операции, так и после нее все потенциальные симптомы нарушения нейросенсорных функций должны быть задокументированы. Области измененной чувствительности картируют (как по локализации, так и по площади пораженного участка). Таким образом, удается проводить мониторинг за изменением всех параметров в будущем, и определить нуждается ли пациент в микрохирургическом вмешательстве или нет. Для идентификации и определения степени нарушений используют как объективные, так и субъективные диагностические тесты, которые условно делятся на механоцептивные (реакция на механические раздражители и компрессию) и ноцицептивные (ощущение боли).
Механоцептивные тесты включают статическое касание мягкой щеточкой, двухточечное распознавание и определение направления движения кисти. Ощущение укола иглой и распознавание термических раздражителей относят к ноцицептивным диагностическим процедурам. Для сравнения показателей всегда диагностируют не только область поражения, но и симметрический участок, таким образом, точно идентифицируя факт и степень нейросенсорных нарушений. При жалобах пациента на потерю вкуса для диагностики используют ватный тампон, смоченный солью или сахаром.
Распространенность травматических поражений нервов
После имплантации постоянное нарушение чувствительности в области губы вследствие травматического поражений нервных волокон отмечается в 0-36% клинических случаев. Однако эти данные можно считать несколько устаревшими, и не соответствующими подходам современной имплантологической практики. Ведь раньше в ходе операции хирурги-стоматологи использовали чаще вестибулярные разрезы, из-за которых и развивалось нарушение чувствительности. На сегодняшний день в процессе установки дентальных имплантатов выполняют срединные разрезы слизистой по вершине резидуального гребня, а всю процедуру предварительно планируют, учитывая данные, полученные после компьютерно-томографического исследования. Таким образом, можно предположить, что распространенность поражений нервных волокон в результате имплантации значительно меньше 36%.
Dannan и коллеги сообщили, что частота поражения нервов при имплантации достигает 2,95% (5 из 169 пролеченных пациентов) в случаях временных нейросенсорных изменений, и 1,7% в случаях, необратимых имплантат-ассоциированных нейропатий. В другом исследовании было указано, что частота поражений нервов после проведения хирургических вмешательств в челюстно-лицевой области достигает 2,69% (42 из 1559 пациентов), при этом процент необратимых нейросенсорных нарушений составляет еще меньше, но точное число таковых не было указано в исследовании. По мнению автора, однако, даже такие показатели имплантат-ассоциированных поражений нервных структур являются слишком высокими для клинической практики. Транзиторное нарушение чувствительности губы часто может быть связано с отеком, который наблюдается на протяжении первых двух недель после хирургического вмешательства.
Травматическое поражение язычного нерва в ходе выполнения хирургических манипуляций
Язычный нерв в области моляров нижней челюсти проходит в мягких тканях с язычной стороны челюсти. Иногда нерв находиться корональнее поверхности костной ткани и плотно прилегает к кортикальной костной пластинке с язычной стороны. Поэтому в данной области нужно очень аккуратно проводить какие-либо хирургические вмешательства. После удаления третьих моляров нижней челюсти поражения язычного нерва отмечаются в 0,5-2,1% клинических случаев. Травматические же нарушения язычного нерва в ходе дентальной имплантации – явление не распространенное и регистрируется достаточно редко. Для профилактики подобных осложнений при установке дентальных имплантатов следует придерживаться следующих правил: можно выполнять лишь внутрибороздковые разрезы без послабляющих разрезов и сепарации лоскута с язычной стороны; в ходе сепарации лоскута нужно избегать его перерастягивания и придерживаться безопасного расстояния при выполнении остеотомии. 90% всех регистрируемых случаев нейросенсорных изменений, связанных поражениями язычного нерва, разрешаются на протяжении 8-10 недель после оперативного вмешательства.
Предоперационное планирование: профилактика травматических поражений нервов
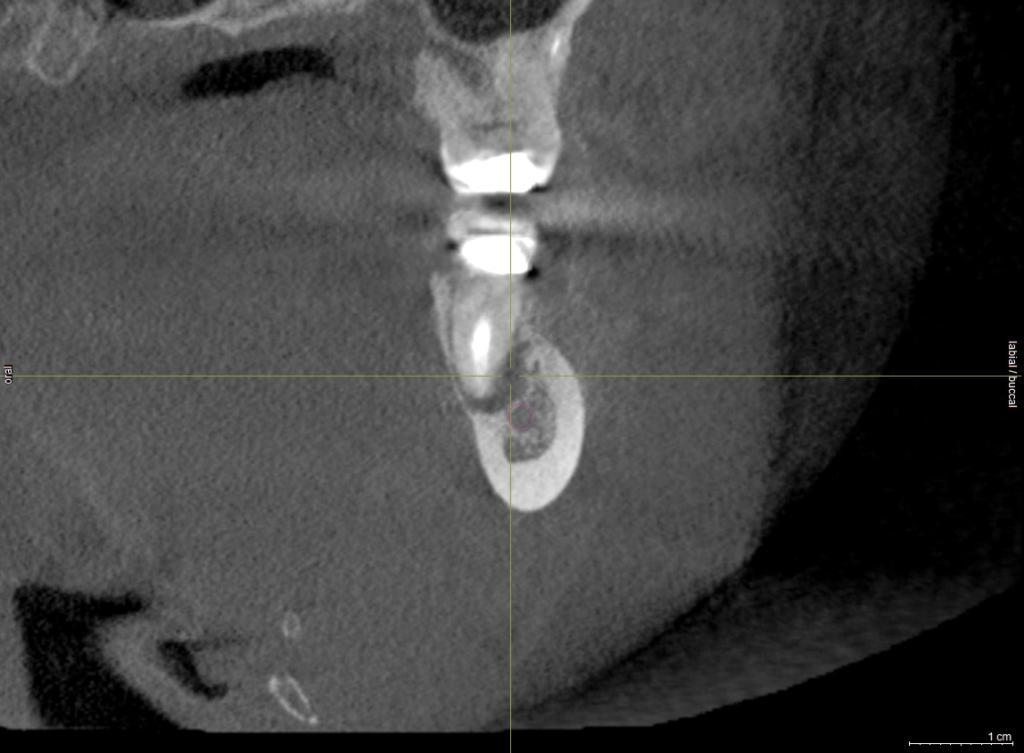
Для профилактики большинства осложнений, связанных с установкой дентальных имплантатов, необходимо обеспечить тщательное планирование оперативного вмешательства. Использование возможностей компьютерной томографии и хирургических шаблонов позволяет избежать непредвиденных исходов ятрогенного вмешательства. При установке дентального имплантата между апикальной его частью и корональной частью канала нижнечелюстного нерва должно быть оставлено минимум 2 мм толщины костной ткани. Кроме того, важно придерживаться установленной длины остеотомии и четко следовать протоколу препарирования костной ткани. Наличие 2 мм толщины костной ткани также позволяет избежать чрезмерной костной компрессии в области нерва после установки титановой внутрикостной опоры (фото 1 - 2).
Фото 1. Имплантат был установлен в области 30 зуба. После того, как действие анестезии закончилось, пациент начал жаловаться на наличие парастезии в области правой губы и подбородка. На рентгенограмме, сделанной сразу после имплантации, признаков пенетрации имплантата в канал нижнечелюстного нерва не видно.
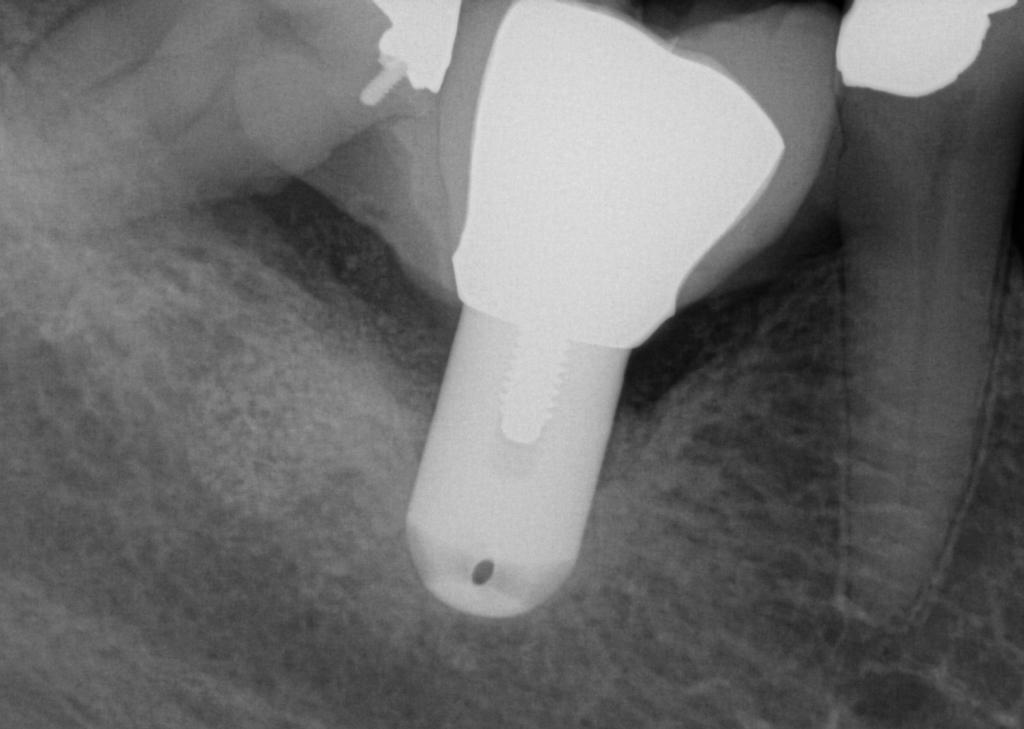
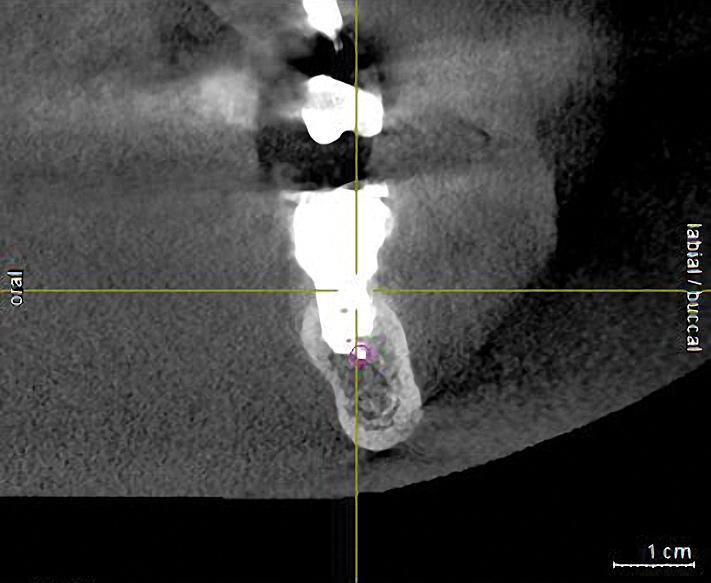
Фото 2. Установка имплантата была проведена 10 лет назад, и за этом время пациент смог адаптироваться к изменениям чувствительности. На КЛКТ-снимке видно, что имплантат в области 30 зуба намного ближе к каналу нерва, чем казалось раньше.
При необходимости с целью обеспечения безопасности вмешательства могут быть использованы короткие дентальные имплантаты. Врачу также важно быть ознакомленным с абсолютной длиной всех сверл, которые используются в ходе манипуляции, поскольку неучет данных параметров может спровоцировать чрезмерное углубление более чем на 0,4-1,5 мм относительно выбранной безопасной границы. Для контроля углубления в костную ткань рекомендуется также использовать специальные стопперы. Тем не менее, врач должен понимать, что ни толщина, ни плотность костной ткани над областью нерва не обеспечивают безопасность его состояния в ходе выполнения процедуры остеотомии, поэтому приложение слишком больших усилий и давлений в процессе препарирования костной ткани строго воспрещается. Наконец, следует отметить, что до 50% судебных исков, связанных с повреждением нерва после имплантации, спровоцированы отсутствием информированного согласия со стороны пациента, которое врач должен получить до операции. Неплохо также провести оценку нейросенсорных параметров пациента до вмешательства, чтобы сравнить их с теми данными, которые будут получены после имплантации.
Местная анестезия: потенциальная причина повреждения нерва
Травматические поражения нижнечелюстного и язычного нервов могут возникнуть в процессе выполнения анестезии по причине травмы иглой, гематомы и воздействия составляющих анестезирующего раствора. Механизмы подобных поражений до сих пор достаточно неизученные. В одном ретроспективном исследовании было указано, что частота поражения нервов в ходе выполнения анестезии составляет от 1 / 26 762 до 1/160 571 6 случаев, тогда как Haas и Lennon прогнозировали частоту развития подобных осложнений на уровне 1/785 000. Другие данные свидетельствуют о том, что распространенность кратковременных транзиторных поражений нижнечелюстного и язычного нервов в результате проведения анестезии составляет от 0,15% до 0,54%. Тогда как случаи развития постоянных изменений чувствительности той же этиологии встречаются довольно редко, с распространённостью в 0,0001-0,01%. После выполнения нижнечелюстной анестезии у 3-7% пациентов отмечаются ощущения по типу электрического воздействия, которые со временем саморазрешаются. Однако, когда клиницист отметил, что пациент слишком резко среагировал на введение иглы, последнюю нужно немного вывести и репозиционировать. Методов для лечения или профилактики нервных осложнений, связанных с выполнением процедуры анестезии до сих пор не разработано. От 70% до 89% случаев нейросенсорных поражений, связанных с анестезией, развиваются в области язычного нерва. Такая тенденция может быть объяснена тем, что язычный нерв состоит лишь из нескольких пучков, в то время как нижний альвеолярный из огромного их количества, что, в свою очередь, повышает его потенциал к регенерации. С геометрической точки зрения все объясняется гораздо проще: размер иглы составляет в среднем 0,45 мм, в то время как диаметр язычного нерва – 1,86 мм, а диаметр нижнего альвеолярного нерва – 3 мм.
Ассоциированная с анестезией нефропатия чаще всего развивается после обезболивания 4% растворами артикаина или пилокарпина. По отношению к лидокаину, пилокарпин и артикаин вызывают в 7,3 и 3,6 раза больше нейросенсорных нарушений. Garisto и коллеги сообщили, что в 4 из 9 исследований, частота осложнений при введении 4% растворов прилокаина или артикаина была выше, чем при инъекции анестетиков с более низкой концентрацией. По мнению авторов, выполнение местной анестезии данным препаратами следует избегать, дабы снизить частоту ассоциированных нейропатий после ятрогенных вмешательств. Однако, по мнению Malamed, случаи, при которых арктикаин продемонстрировал большую связь с нейропатиями, чем лидокаин, являются эпизодическими, и не имеют под собой достаточной доказательной аргументации. Аналогичным образом, в 2013 году после обширного обзора литературы Toma и коллеги пришли к выводу, что исследования, предполагающие высшую нейротоксичность артикаина, являются по своему дизайну ретроспективными, данные представленные в них характеризуются высоким риском наличия ошибок, и полученные результаты не следует расценивать как достаточные доказательства. Авторы пришли к выводу, что непосредственная травма нервного волокна является преобладающей причиной развития нейросенсорных нарушений, и последние мало связаны с химической токсичностью используемых анестетиков. В целом в литературе имеются разногласия по этому вопросу; поэтому клиницисты должны принимать решения в отношении использования более высоких концентраций анестетиков на основе условий каждого отдельного клинического случая, интерпретируя при этом уже предварительно полученную информацию и учитывая рекомендации производителей лекарственных средств.
Процедура остеотомии при имплантации
Процедуру остеотомии следует проводить посредством хорошо заточенных сверл и при обильной ирригации. Гипотетически, перегрев области вмешательства при остеотомии может спровоцировать травматическое поражение нерва. Размер некротизирования кости, вызванного перегревом, прямо пропорционален температуре препарирования в условиях которой проводилось ятрогенное вмешательство.
Eriksson и Albrektsson резюмировали, что выполнение остеотомии при температуре в 47ºС в течение 1 минуты может спровоцировать последующую резорбцию костной ткани. В случаях прогрессивной резорбции, учитывая смещение позиции подбородочного отверстия, проводить транскретальный разрез противопоказано, вместо этого он должен быть смещен в лингвальную сторону. При установке имплантатов кпереди от подбородочного отверстия следует тщательно провести анализ КТ-снимков, которые могут помочь обнаружить наличие петли подбородочного нерва.
Процедуры сепарации лоскута
Как правило, сепарация лоскута не провоцирует каких-либо нейросенсорных нарушений, однако врачу все равно следует уделять огромное внимание при выполнении данного ятрогенного вмешательства в подбородочной области. Врач четко должен понимать, где подбородочный нерв выходит из подбородочного отверстия, дабы при сепарации лоскута не спровоцировать повреждения нервного волокна.
Экстракция зубов
Перед экстракцией моляров и премоляров на нижней челюсти для последующей установки дентальных имплантатов, следует тщательно изучить соотношении положения их корней относительно хода нижнего альвеолярного и подбородочного нервов. Также следует очень аккуратно проводить кюретаж лунок после резекции, поскольку периапикальные поражения часто могут находиться вблизи нервных структур (фото 3 - 4).
Фото 3. Пациент обратился за помощью по поводу боли в области 31 зуба. На рентгенограмме визуализированы признаки острого апикального пародонтита.
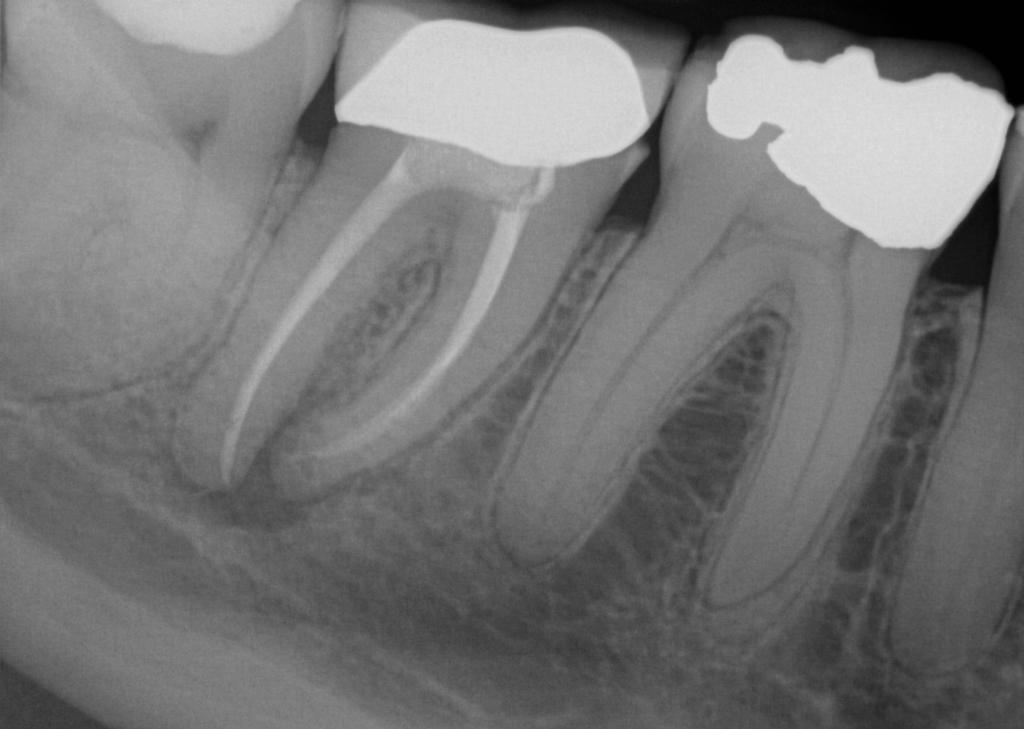
Фото 4. Результаты КЛКТ-диагностики указывают на то, что патологический очаг находиться вблизи канала нерва. Зуб был аккуратно удален с последующим осторожным кюретажем области дефекта.
Фармакологическая терапия невропатий, ассоциированных с установкой дентальных имплантатов
Однозначного мнения относительно того, какие препараты лучше использовать при диагностике травматических поражений нервов челюстно-лицевой области нет. Некоторые авторы отдают предпочтение кортикостероидам и нестероидным противоспалительным препаратам (НПЗП). При этом стоит помнить, что использование различных фармакологических средств актуально лишь при сохранении целостности нервного волокна в целом. В случаях нарушения чувствительности после инъекции пациенту можно вести дексаметазон 4 г/мл прямо в область повреждения, и через 3 дня повысить дозу стероидов. При сдавливании нерва или травмы волокна в ходе хирургического вмешательства вводят 1-2 мл дексаметазона внутривенно, после чего на протяжении 6 дней назначают дексаметазон перорально (4 мг, 2 таблетки после еды – три дня, потом 1 таблетку после еды – еще три дня). При нарушении целостности нерва стероиды могут назначить на период от 5 до 7 дней. Нарушение чувствительности могут помочь купировать 800 мг ибупрофена, которые следует принимать трижды на день на протяжении 3 недель. Если нейропатия развилась после удаления имплантата пациентам можно назначать также 800 мг ибупрофена трижды на день и с такой же частотой 500 мг амоксицилина на протяжении 5-7 дней. Параллельно с этим назначают 50 г преднизолона, снижая дозу на 10 мг каждый день (на протяжении 5 дней). Посттравматическую нейропатию можно попробовать купировать низкими дозами антидепрессантов и противоэпилептических препаратов.
В сочетании с фармацевтическим подходом, Renton и Yilma рекомендуют проводить для пациентов с хронической нейропатией также физиотерапевтические вмешательства. Цель подобного алгоритма лечения состоит в том, чтобы снизить чувство дискомфорта у пациента, и помочь ему избавиться от боли. Bagheri and Meyer вообще ставят под сомнение эффективность кортикостероидов при лечении травматических поражений нижнего альвеолярного нерва, поскольку плотность костной ткани формирующей канал нерва настолько высока, что медикаментам попросту невозможно достичь их пространства. На данное время, пока что не получено результатов клинических исследований, которые подтверждают целесообразность и успешность использовать кортикостероиды или НПЗП при травматических нейропатиях, ассоциированных с процедурой установки дентальных имплантатов.
Когда направлять пациента к микрохирургу
Универсальных рекомендаций относительно того, когда нужно направлять пациентов с травматическими нейропатиями тройничного нерва к микрохирургу пока что не разработано. Одни авторы утверждают, что пациента следует направить к специалисту сразу же после того, как он отметил нарушения чувствительности после проведения процедуры имплантации. Другие же исследователи рекомендуют проводить направление к микрохирургу через 2, 3, 4 или даже 6 месяцев мониторинга, если на протяжении таковых наблюдались признаки травматической нейропатии. Ziccardi and Zuniga рекомендуют проводить микрохирургическое вмешательство на протяжении до 1 года после проведения процедуры имплантации, поскольку через год после вмешательства эффективность микрохирургической коррекции заметно снижается. При констатации факта травматической нейропатии после имплантации врач должен установить, нуждается ли пациент в направлении к микрохирургу, или можно ли улучшить ситуацию с использованием различных фармакологических препаратов.
Иногда эксплантация, или незначительное «вывинчивание» имплантата из кости может способствовать разрешению симптомов травматического нарушения сенсорной функции. Результаты отдельных исследований указывают на то, что целесообразность направления к микрохирургу аргументирована лишь констатацией факта полного нарушения целостности нерва. Когда же врач уверен, что он не нарушал целостности костного канала нерва, то нарушение чувствительности может быть вызвано компрессией нервного волокна или же воспалительным эффектом. В таких случаях может помочь и фармакологический подход к лечению. Между тем, врач должен понимать, что даже если он не перфорировал основной нервный канал, часто у нерва имеются дополнительные ветви, предсказать ход которых довольно сложно. Последнее является возможным только при тщательном анализе данных, полученных после КЛКТ-сканирования, ведь двухмерные рентгенограммы провоцируют суперимпозицию отдельных анатомических структур, следовательно, прогноз возможного травматического поражения нервов с их помощью является неэффективным (фото 1-2).
В случаях ощущения дискомфорта после установки имплантата, если можно подтвердить, что интраоссальная опора не находиться вблизи канала нерва, алгоритмы лечения являются вариативными. Bagheri и Meyer предлагают проводить мониторинг на протяжении 3-4 месяцев, чтобы увидеть наблюдаются ли улучшения показателей чувствительности, перед тем как направить пациента к микрохирургу. Также авторы утверждают, что при слишком близкой позиции имплантата к нерву, уровень компрессии последнего можно уменьшить незначительным реверсивным движением имплантата. Другие исследователи предлагают эксплантировать интраоссальную конструкцию на протяжении 36 часов и сразу же назначать стероидные препараты, если после оперативного вмешательства у пациента отмечаются признаки нейросенсорных нарушений.
Khawaja and Renton описали четыре клинических случая развития симптомов нарушения чувствительности после установки дентальных имплантатов, при которых интраоссальная конструкция не находилась вблизи нерва. Однако, при эксплантации симптомы нейросенсорных нарушений разрешились у двух из четырех пациентов достаточно быстро. Интересно, что позитивная динамика наблюдалась у пациентов, которым удаление имплантатов проводили на протяжении 18 и 36 часов, а резидуальные симптомы отмечались у пациентов, эксплантация которым проводилась через 3 и 4 дня после оперативного вмешательства.
Renton, Dawood и коллеги предполагают, что период мониторинга за пациентами с подобными симптомами не должен превышать 3 месяцев, поскольку по истечении данного срока риск развития нейронных изменений превышает уровень потенциальной успешности микрохирургического вмешательства. Ziccardi и Steinberg в своей обзорной статье рекомендуют проводить начальный мониторинг на протяжении 1 месяца, и, если симптоматика улучшается – продолжать наблюдаться за пациентом. Если же симптоматика не улучшается или же усугубляется, необходимо направить больного к микрохирургу. Результаты исследований указывают на то, что пациенты, прооперированные по причине нейросенсорных нарушений через 6-8 месяцев после имплантации, характеризуются таким же уровнем успешности, как и пациенты, прооперированы в более короткий период после ятрогенного вмешательства. По мнению авторов, более ранее вмешательство возможно и является более эффективным, однако доказательных данных для подтверждения этого предположения пока что нет. Кроме того, выполнение микрохирургической операции в случаях лишь незначительных нейросенсорных изменений не показано, поскольку риск от самого вмешательства в таких случаях превышает прогнозированный уровень успешности. Существует также принцип 12-недельного ожидания – в среднем именно столько времени надо врачу, чтобы определиться в необходимости направления пациента на микрохирургическую операцию.
Логично, что в случаях наличия у пациентов острой боли ждать 12 недель необязательно. Перед аргументацией тех или иных подходов к лечению врач должен объективно сопоставить данные рентгенологического контроля и клинические симптомы, после чего учесть все возможны медико-правовые аспекты нарушений.
Хирургическое восстановления поврежденного тройничного нерва
Существуют конкретные причины, которые аргументируют необходимость микрохирургического восстановления повреждённого тройничного нерва, и контрактные факторы, которые определяют прогноз данной манипуляции. Ziccardi и Zuniga сформулировали следующий список причин, которые обосновывают направление пациента к микрохирургу: нарушение чувствительности, которое персистирует на протяжении более чем 3 месяцев и нарушает нормальную жизненную активность пациента, подтверждение факта пересечения нерва, отсутствие улучшений признаков гипостезии, развитие болевых ощущений после имплантации. После выполнения микрохирургической коррекции на успешность таковой влияет ряд факторов: время ожидания после имплантации, тип и объем поражения, степень васкуляризации области поражения, опыт хирурга, метод забора и подготовки трансплантата, наличие натяжения в области восстановления, возраст и общее состояние здоровья пациента.
По сути, микрохирургическое восстановление ветвей язычного и нижнего альвеолярного нервов возможно. Однако уровень успешности подобных манипуляций является весьма вариативным – в среднем исследователи указывают лишь на 50-59,4% эффективность такого лечения, и лишь в двух исследованиях результаты вмешательства достигали уровней 81,7% и 63,1%. Во всех проведённых исследованиях число субъектов является довольно незначительным, поэтому сравнивать конечные результаты таковых методологически невозможно. Тем не менее, 50-60% пациентов после микрохирургической коррекции демонстрируют признаки улучшения неврологических нарушений. Ziccardi and Zuniga предупреждают, что пациенты с тяжелыми нейросенсорными поражениями должны быть проинформированы о том, что полноценная их реабилитация фактически является невозможной. Также многие исследователи указывают на то, что эффективность микрохирургических процедур в случаях терапии анестезии, дизестезии и спонтанных болевых ощущений является преувеличенной. Если резюмировать, то микрохирургическая коррекция может помочь отдельными пациентам, но уровень прогнозированности результатов подобного лечения является неоднозначным. Таким образом, лучшая терапия нейросенсорных нарушений, связанных с имплантацией – это их профилактика.
Заключение
В клинической практике часто встречается дилемма: если имплантат успешно остеоинтегрирован, но вызывает умеренную парестезию без боли, что с ним делать? Ведь эксплантация не всегда может способствовать разрешению симптомов, а ретенция имплантата в кости при фактическом поражение нерва может спровоцировать развитие невромы. Последняя формируется в результате чрезмерного заживления области поврежденного нерва и гиперплазии смежных тканей, и очень часто требует последующего хирургического удаления. Решение о выборе возможного метода лечения должно приниматься вместе с пациентом после тщательной дискуссии всех возможных вариантов, и перед началом реабилитации пациент официально должен подтвердить свое согласие посредством заполнения специальной письменной формы.
Авторы:
Gary Greenstein, DDS, MS
Joseph R. Carpentieri, DDS
John Cavallaro, DDS
Повреждение ветвей тройничного нерва (например, нижнего альвеолярного, языкового, подбородочного или подглазничного) является потенциальным осложнением, которое может развиться в ходе выполнения процедуры дентальной имплантации.

В данной статье мы обсудим подходы к лечению стоматологических пациентов с поражением нервов челюстно-лицевой области ассоциированных с процедурой дентальной имплантации, а также основные аспекты этиологии и патогенеза подобных патологий в целом.
Анатомия и гистология тройничного нерва
Тройничный нерв представляет собой пятую и наибольшую пару черепных нервов, которая состоит из следующих ветвей: очного нерва (V1), верхнечелюстного нерва (V2) и нижнечелюстного нерва (V3). Нижнечелюстной нерв является самой большой ветвью и иннервирует нижнюю губу, область подбородка, зубы, смежные мягкие ткани, нижнюю челюсть и часть наружного уха. Двигательные волокна нижнечелюстного нерва не поддаются повреждению во время процедуры имплантации, поскольку они отходят от основной ветви V3 еще до выхода из подбородочного отверстия. Основной структурной единицей нерва является нервное волокно. В структуре V3 преобладают миелинизированные нервные волокна. Каждый аксон и шванновская клетка покрыты соединительной тканью, которая называется эндоневрием. Группы нервных волокон формируют пучки, которые окружены эпиневрием. Поражение любой части нервного пучка может привести к нейросенсорным нарушениям. Тройничный нерв состоит с 7000-12000 аксонов, а количество пучков варьирует в разных участках челюстно-лицевой области. Нижний альвеолярный нерв (НАН) является полипучковым (состоит больше чем из 10 пучков), в то время как язычный нерв включает лишь несколько аналогичных нервных структур. Поскольку НАН характеризуется большим количеством нервных пучков его регенераторные способности также значительно выше по сравнению с язычным нервом.
Типы нервных поражений
Поражения тройничного нерва могут быть спровоцированы компрессией, растяжением, полным или же частичным нарушением целостности нервного волокна. Повреждения могут привести к нейросенсорным изменениям в отношении чувствительности прикосновения, давления, температуры и боли. Подобные патологии заметно влияют на комфорт и возможность пациента нормально разговаривать, кушать, целоваться, бриться, наносить макияж, чистить зубы и пить. Кроме того, нейросенсорные нарушения также влияют на возможность пациента нормально взаимодействовать в социуме. Признаки данных патологий могут быть идентифицированы непосредственно во время проведения хирургического вмешательства (при наличие болевого симптома), так и в процессе длительного мониторинга за состоянием пациента. Для описания травматических поражений аксонов разной степени сложности используют следующие термины:
- нейропраксия – поражение при котором сохраняется целостность нервного волокна, а механизм травмы связан с растяжением или воздействием по типу тупой травмы; чувствительность, как правило, нормализируется на протяжении нескольких дней или недель.
- аксонотмезис – поражение нерва, при котором развиваются процессы его дегенерации и регенерации, однако сам аксон при этом не теряет своей целостности, и чувствительность нормализируется на протяжении 2-4 месяцев; однако чувствительность после восстановления может быть несколько меньше, чем до вмешательства, а в отдельных клинических случаях характеризуется сопровождающей дизестезией.
- нейротмезис – поражение нерва, при котором отмечается нарушение его целостности, а прогноз восстановления нормальной чувствительности является неблагоприятным.
Международная ассоциация по изучению боли стандартизировала номенклатуру, касающуюся травматических поражений нервов. В частности, было изменено определение термина парестезия, которое раньше использовалось для обозначения потери чувствительности. Актуальная терминология предусматривает следующие определения:
- парестезия – изменение чувствительности без сопутствующих неприятных ощущений;
- дизестезия – изменение чувствительности, которое сопровождается неприятными ощущениями;
- анестезия – потеря чувствительности.
Для описания изменений нейросенсорных функций также используются такие термины, как аллодиния (возникновение боли на раздражители, которые в норме болевых ощущений не провоцируют), каузалгия (наличие персистирующей жгучей боли), гипостезия (снижение чувствительности на действие раздражителей), гиперестезия (повышение чувствительности на действие раздражителей).
Когда нервы растягиваются или сжимаются, периневрий защищает пучки от повреждения. Однако удлинение нерва более чем на 30% может спровоцировать его структурное поражение. При полном нарушении целостности нерва отмечается развитие симптомов анестезии и снижение определенных сенсорных функций. При частичном нарушении целостности нервного волокна могут наблюдаться различные симптомы поражения, включающие дизестезию. Следует отметить, что наличие персистирующей боли после оперативного вмешательства не является критерием для определения потенциальной возможности потенциального полного восстановления функции пораженного волокна.
После повреждения периферического нерва начинает развиваться валлеровская дегенерация, которая продолжается на протяжении нескольких недель и даже месяцев. Дистальнее места травматического пересечения развивается некроз аксонов. Дегенерация в подобных случаях является прогрессирующей и необратимой и длиться на протяжении до 18 месяцев. На возможность заживления пораженной области нерва влияют такие факторы как общее состояние здоровья пациента, возраст и тип поражения. Ключевым моментом в процессе восстановления нерва после поражения является формирование рубцовой ткани в области эндоневральных тубул.
Оценка травматических поражений тройничного нерва
Чаще всего в ходе установки дентальных имплантатов поражается НАН. Признаки поражения нижнего альвеолярного нерва включаются анестезию, парестезию или дизестезию в области кожи, нижней губы, щеки и десен до участка второго моляра. Пациенты же с повреждением язычного нерва характеризуются неконтролируемым слюноотделением, надкусыванием языка, ощущением изжоги, потерей вкуса, изменениями речи и функции глотания, онемением слизистой и языка. Как в ходе операции, так и после нее все потенциальные симптомы нарушения нейросенсорных функций должны быть задокументированы. Области измененной чувствительности картируют (как по локализации, так и по площади пораженного участка). Таким образом, удается проводить мониторинг за изменением всех параметров в будущем, и определить нуждается ли пациент в микрохирургическом вмешательстве или нет. Для идентификации и определения степени нарушений используют как объективные, так и субъективные диагностические тесты, которые условно делятся на механоцептивные (реакция на механические раздражители и компрессию) и ноцицептивные (ощущение боли).
Механоцептивные тесты включают статическое касание мягкой щеточкой, двухточечное распознавание и определение направления движения кисти. Ощущение укола иглой и распознавание термических раздражителей относят к ноцицептивным диагностическим процедурам. Для сравнения показателей всегда диагностируют не только область поражения, но и симметрический участок, таким образом, точно идентифицируя факт и степень нейросенсорных нарушений. При жалобах пациента на потерю вкуса для диагностики используют ватный тампон, смоченный солью или сахаром.
Распространенность травматических поражений нервов
После имплантации постоянное нарушение чувствительности в области губы вследствие травматического поражений нервных волокон отмечается в 0-36% клинических случаев. Однако эти данные можно считать несколько устаревшими, и не соответствующими подходам современной имплантологической практики. Ведь раньше в ходе операции хирурги-стоматологи использовали чаще вестибулярные разрезы, из-за которых и развивалось нарушение чувствительности. На сегодняшний день в процессе установки дентальных имплантатов выполняют срединные разрезы слизистой по вершине резидуального гребня, а всю процедуру предварительно планируют, учитывая данные, полученные после компьютерно-томографического исследования. Таким образом, можно предположить, что распространенность поражений нервных волокон в результате имплантации значительно меньше 36%.
Dannan и коллеги сообщили, что частота поражения нервов при имплантации достигает 2,95% (5 из 169 пролеченных пациентов) в случаях временных нейросенсорных изменений, и 1,7% в случаях, необратимых имплантат-ассоциированных нейропатий. В другом исследовании было указано, что частота поражений нервов после проведения хирургических вмешательств в челюстно-лицевой области достигает 2,69% (42 из 1559 пациентов), при этом процент необратимых нейросенсорных нарушений составляет еще меньше, но точное число таковых не было указано в исследовании. По мнению автора, однако, даже такие показатели имплантат-ассоциированных поражений нервных структур являются слишком высокими для клинической практики. Транзиторное нарушение чувствительности губы часто может быть связано с отеком, который наблюдается на протяжении первых двух недель после хирургического вмешательства.
Травматическое поражение язычного нерва в ходе выполнения хирургических манипуляций
Язычный нерв в области моляров нижней челюсти проходит в мягких тканях с язычной стороны челюсти. Иногда нерв находиться корональнее поверхности костной ткани и плотно прилегает к кортикальной костной пластинке с язычной стороны. Поэтому в данной области нужно очень аккуратно проводить какие-либо хирургические вмешательства. После удаления третьих моляров нижней челюсти поражения язычного нерва отмечаются в 0,5-2,1% клинических случаев. Травматические же нарушения язычного нерва в ходе дентальной имплантации – явление не распространенное и регистрируется достаточно редко. Для профилактики подобных осложнений при установке дентальных имплантатов следует придерживаться следующих правил: можно выполнять лишь внутрибороздковые разрезы без послабляющих разрезов и сепарации лоскута с язычной стороны; в ходе сепарации лоскута нужно избегать его перерастягивания и придерживаться безопасного расстояния при выполнении остеотомии. 90% всех регистрируемых случаев нейросенсорных изменений, связанных поражениями язычного нерва, разрешаются на протяжении 8-10 недель после оперативного вмешательства.
Предоперационное планирование: профилактика травматических поражений нервов
Для профилактики большинства осложнений, связанных с установкой дентальных имплантатов, необходимо обеспечить тщательное планирование оперативного вмешательства. Использование возможностей компьютерной томографии и хирургических шаблонов позволяет избежать непредвиденных исходов ятрогенного вмешательства. При установке дентального имплантата между апикальной его частью и корональной частью канала нижнечелюстного нерва должно быть оставлено минимум 2 мм толщины костной ткани. Кроме того, важно придерживаться установленной длины остеотомии и четко следовать протоколу препарирования костной ткани. Наличие 2 мм толщины костной ткани также позволяет избежать чрезмерной костной компрессии в области нерва после установки титановой внутрикостной опоры (фото 1 - 2).
Фото 1. Имплантат был установлен в области 30 зуба. После того, как действие анестезии закончилось, пациент начал жаловаться на наличие парастезии в области правой губы и подбородка. На рентгенограмме, сделанной сразу после имплантации, признаков пенетрации имплантата в канал нижнечелюстного нерва не видно.

Фото 2. Установка имплантата была проведена 10 лет назад, и за этом время пациент смог адаптироваться к изменениям чувствительности. На КЛКТ-снимке видно, что имплантат в области 30 зуба намного ближе к каналу нерва, чем казалось раньше.

При необходимости с целью обеспечения безопасности вмешательства могут быть использованы короткие дентальные имплантаты. Врачу также важно быть ознакомленным с абсолютной длиной всех сверл, которые используются в ходе манипуляции, поскольку неучет данных параметров может спровоцировать чрезмерное углубление более чем на 0,4-1,5 мм относительно выбранной безопасной границы. Для контроля углубления в костную ткань рекомендуется также использовать специальные стопперы. Тем не менее, врач должен понимать, что ни толщина, ни плотность костной ткани над областью нерва не обеспечивают безопасность его состояния в ходе выполнения процедуры остеотомии, поэтому приложение слишком больших усилий и давлений в процессе препарирования костной ткани строго воспрещается. Наконец, следует отметить, что до 50% судебных исков, связанных с повреждением нерва после имплантации, спровоцированы отсутствием информированного согласия со стороны пациента, которое врач должен получить до операции. Неплохо также провести оценку нейросенсорных параметров пациента до вмешательства, чтобы сравнить их с теми данными, которые будут получены после имплантации.
Местная анестезия: потенциальная причина повреждения нерва
Травматические поражения нижнечелюстного и язычного нервов могут возникнуть в процессе выполнения анестезии по причине травмы иглой, гематомы и воздействия составляющих анестезирующего раствора. Механизмы подобных поражений до сих пор достаточно неизученные. В одном ретроспективном исследовании было указано, что частота поражения нервов в ходе выполнения анестезии составляет от 1 / 26 762 до 1/160 571 6 случаев, тогда как Haas и Lennon прогнозировали частоту развития подобных осложнений на уровне 1/785 000. Другие данные свидетельствуют о том, что распространенность кратковременных транзиторных поражений нижнечелюстного и язычного нервов в результате проведения анестезии составляет от 0,15% до 0,54%. Тогда как случаи развития постоянных изменений чувствительности той же этиологии встречаются довольно редко, с распространённостью в 0,0001-0,01%. После выполнения нижнечелюстной анестезии у 3-7% пациентов отмечаются ощущения по типу электрического воздействия, которые со временем саморазрешаются. Однако, когда клиницист отметил, что пациент слишком резко среагировал на введение иглы, последнюю нужно немного вывести и репозиционировать. Методов для лечения или профилактики нервных осложнений, связанных с выполнением процедуры анестезии до сих пор не разработано. От 70% до 89% случаев нейросенсорных поражений, связанных с анестезией, развиваются в области язычного нерва. Такая тенденция может быть объяснена тем, что язычный нерв состоит лишь из нескольких пучков, в то время как нижний альвеолярный из огромного их количества, что, в свою очередь, повышает его потенциал к регенерации. С геометрической точки зрения все объясняется гораздо проще: размер иглы составляет в среднем 0,45 мм, в то время как диаметр язычного нерва – 1,86 мм, а диаметр нижнего альвеолярного нерва – 3 мм.
Ассоциированная с анестезией нефропатия чаще всего развивается после обезболивания 4% растворами артикаина или пилокарпина. По отношению к лидокаину, пилокарпин и артикаин вызывают в 7,3 и 3,6 раза больше нейросенсорных нарушений. Garisto и коллеги сообщили, что в 4 из 9 исследований, частота осложнений при введении 4% растворов прилокаина или артикаина была выше, чем при инъекции анестетиков с более низкой концентрацией. По мнению авторов, выполнение местной анестезии данным препаратами следует избегать, дабы снизить частоту ассоциированных нейропатий после ятрогенных вмешательств. Однако, по мнению Malamed, случаи, при которых арктикаин продемонстрировал большую связь с нейропатиями, чем лидокаин, являются эпизодическими, и не имеют под собой достаточной доказательной аргументации. Аналогичным образом, в 2013 году после обширного обзора литературы Toma и коллеги пришли к выводу, что исследования, предполагающие высшую нейротоксичность артикаина, являются по своему дизайну ретроспективными, данные представленные в них характеризуются высоким риском наличия ошибок, и полученные результаты не следует расценивать как достаточные доказательства. Авторы пришли к выводу, что непосредственная травма нервного волокна является преобладающей причиной развития нейросенсорных нарушений, и последние мало связаны с химической токсичностью используемых анестетиков. В целом в литературе имеются разногласия по этому вопросу; поэтому клиницисты должны принимать решения в отношении использования более высоких концентраций анестетиков на основе условий каждого отдельного клинического случая, интерпретируя при этом уже предварительно полученную информацию и учитывая рекомендации производителей лекарственных средств.
Процедура остеотомии при имплантации
Процедуру остеотомии следует проводить посредством хорошо заточенных сверл и при обильной ирригации. Гипотетически, перегрев области вмешательства при остеотомии может спровоцировать травматическое поражение нерва. Размер некротизирования кости, вызванного перегревом, прямо пропорционален температуре препарирования в условиях которой проводилось ятрогенное вмешательство.
Eriksson и Albrektsson резюмировали, что выполнение остеотомии при температуре в 47ºС в течение 1 минуты может спровоцировать последующую резорбцию костной ткани. В случаях прогрессивной резорбции, учитывая смещение позиции подбородочного отверстия, проводить транскретальный разрез противопоказано, вместо этого он должен быть смещен в лингвальную сторону. При установке имплантатов кпереди от подбородочного отверстия следует тщательно провести анализ КТ-снимков, которые могут помочь обнаружить наличие петли подбородочного нерва.
Процедуры сепарации лоскута
Как правило, сепарация лоскута не провоцирует каких-либо нейросенсорных нарушений, однако врачу все равно следует уделять огромное внимание при выполнении данного ятрогенного вмешательства в подбородочной области. Врач четко должен понимать, где подбородочный нерв выходит из подбородочного отверстия, дабы при сепарации лоскута не спровоцировать повреждения нервного волокна.
Экстракция зубов
Перед экстракцией моляров и премоляров на нижней челюсти для последующей установки дентальных имплантатов, следует тщательно изучить соотношении положения их корней относительно хода нижнего альвеолярного и подбородочного нервов. Также следует очень аккуратно проводить кюретаж лунок после резекции, поскольку периапикальные поражения часто могут находиться вблизи нервных структур (фото 3 - 4).
Фото 3. Пациент обратился за помощью по поводу боли в области 31 зуба. На рентгенограмме визуализированы признаки острого апикального пародонтита.

Фото 4. Результаты КЛКТ-диагностики указывают на то, что патологический очаг находиться вблизи канала нерва. Зуб был аккуратно удален с последующим осторожным кюретажем области дефекта.

Фармакологическая терапия невропатий, ассоциированных с установкой дентальных имплантатов
Однозначного мнения относительно того, какие препараты лучше использовать при диагностике травматических поражений нервов челюстно-лицевой области нет. Некоторые авторы отдают предпочтение кортикостероидам и нестероидным противоспалительным препаратам (НПЗП). При этом стоит помнить, что использование различных фармакологических средств актуально лишь при сохранении целостности нервного волокна в целом. В случаях нарушения чувствительности после инъекции пациенту можно вести дексаметазон 4 г/мл прямо в область повреждения, и через 3 дня повысить дозу стероидов. При сдавливании нерва или травмы волокна в ходе хирургического вмешательства вводят 1-2 мл дексаметазона внутривенно, после чего на протяжении 6 дней назначают дексаметазон перорально (4 мг, 2 таблетки после еды – три дня, потом 1 таблетку после еды – еще три дня). При нарушении целостности нерва стероиды могут назначить на период от 5 до 7 дней. Нарушение чувствительности могут помочь купировать 800 мг ибупрофена, которые следует принимать трижды на день на протяжении 3 недель. Если нейропатия развилась после удаления имплантата пациентам можно назначать также 800 мг ибупрофена трижды на день и с такой же частотой 500 мг амоксицилина на протяжении 5-7 дней. Параллельно с этим назначают 50 г преднизолона, снижая дозу на 10 мг каждый день (на протяжении 5 дней). Посттравматическую нейропатию можно попробовать купировать низкими дозами антидепрессантов и противоэпилептических препаратов.
В сочетании с фармацевтическим подходом, Renton и Yilma рекомендуют проводить для пациентов с хронической нейропатией также физиотерапевтические вмешательства. Цель подобного алгоритма лечения состоит в том, чтобы снизить чувство дискомфорта у пациента, и помочь ему избавиться от боли. Bagheri and Meyer вообще ставят под сомнение эффективность кортикостероидов при лечении травматических поражений нижнего альвеолярного нерва, поскольку плотность костной ткани формирующей канал нерва настолько высока, что медикаментам попросту невозможно достичь их пространства. На данное время, пока что не получено результатов клинических исследований, которые подтверждают целесообразность и успешность использовать кортикостероиды или НПЗП при травматических нейропатиях, ассоциированных с процедурой установки дентальных имплантатов.
Когда направлять пациента к микрохирургу
Универсальных рекомендаций относительно того, когда нужно направлять пациентов с травматическими нейропатиями тройничного нерва к микрохирургу пока что не разработано. Одни авторы утверждают, что пациента следует направить к специалисту сразу же после того, как он отметил нарушения чувствительности после проведения процедуры имплантации. Другие же исследователи рекомендуют проводить направление к микрохирургу через 2, 3, 4 или даже 6 месяцев мониторинга, если на протяжении таковых наблюдались признаки травматической нейропатии. Ziccardi and Zuniga рекомендуют проводить микрохирургическое вмешательство на протяжении до 1 года после проведения процедуры имплантации, поскольку через год после вмешательства эффективность микрохирургической коррекции заметно снижается. При констатации факта травматической нейропатии после имплантации врач должен установить, нуждается ли пациент в направлении к микрохирургу, или можно ли улучшить ситуацию с использованием различных фармакологических препаратов.
Иногда эксплантация, или незначительное «вывинчивание» имплантата из кости может способствовать разрешению симптомов травматического нарушения сенсорной функции. Результаты отдельных исследований указывают на то, что целесообразность направления к микрохирургу аргументирована лишь констатацией факта полного нарушения целостности нерва. Когда же врач уверен, что он не нарушал целостности костного канала нерва, то нарушение чувствительности может быть вызвано компрессией нервного волокна или же воспалительным эффектом. В таких случаях может помочь и фармакологический подход к лечению. Между тем, врач должен понимать, что даже если он не перфорировал основной нервный канал, часто у нерва имеются дополнительные ветви, предсказать ход которых довольно сложно. Последнее является возможным только при тщательном анализе данных, полученных после КЛКТ-сканирования, ведь двухмерные рентгенограммы провоцируют суперимпозицию отдельных анатомических структур, следовательно, прогноз возможного травматического поражения нервов с их помощью является неэффективным (фото 1-2).
В случаях ощущения дискомфорта после установки имплантата, если можно подтвердить, что интраоссальная опора не находиться вблизи канала нерва, алгоритмы лечения являются вариативными. Bagheri и Meyer предлагают проводить мониторинг на протяжении 3-4 месяцев, чтобы увидеть наблюдаются ли улучшения показателей чувствительности, перед тем как направить пациента к микрохирургу. Также авторы утверждают, что при слишком близкой позиции имплантата к нерву, уровень компрессии последнего можно уменьшить незначительным реверсивным движением имплантата. Другие исследователи предлагают эксплантировать интраоссальную конструкцию на протяжении 36 часов и сразу же назначать стероидные препараты, если после оперативного вмешательства у пациента отмечаются признаки нейросенсорных нарушений.
Khawaja and Renton описали четыре клинических случая развития симптомов нарушения чувствительности после установки дентальных имплантатов, при которых интраоссальная конструкция не находилась вблизи нерва. Однако, при эксплантации симптомы нейросенсорных нарушений разрешились у двух из четырех пациентов достаточно быстро. Интересно, что позитивная динамика наблюдалась у пациентов, которым удаление имплантатов проводили на протяжении 18 и 36 часов, а резидуальные симптомы отмечались у пациентов, эксплантация которым проводилась через 3 и 4 дня после оперативного вмешательства.
Renton, Dawood и коллеги предполагают, что период мониторинга за пациентами с подобными симптомами не должен превышать 3 месяцев, поскольку по истечении данного срока риск развития нейронных изменений превышает уровень потенциальной успешности микрохирургического вмешательства. Ziccardi и Steinberg в своей обзорной статье рекомендуют проводить начальный мониторинг на протяжении 1 месяца, и, если симптоматика улучшается – продолжать наблюдаться за пациентом. Если же симптоматика не улучшается или же усугубляется, необходимо направить больного к микрохирургу. Результаты исследований указывают на то, что пациенты, прооперированные по причине нейросенсорных нарушений через 6-8 месяцев после имплантации, характеризуются таким же уровнем успешности, как и пациенты, прооперированы в более короткий период после ятрогенного вмешательства. По мнению авторов, более ранее вмешательство возможно и является более эффективным, однако доказательных данных для подтверждения этого предположения пока что нет. Кроме того, выполнение микрохирургической операции в случаях лишь незначительных нейросенсорных изменений не показано, поскольку риск от самого вмешательства в таких случаях превышает прогнозированный уровень успешности. Существует также принцип 12-недельного ожидания – в среднем именно столько времени надо врачу, чтобы определиться в необходимости направления пациента на микрохирургическую операцию.
Логично, что в случаях наличия у пациентов острой боли ждать 12 недель необязательно. Перед аргументацией тех или иных подходов к лечению врач должен объективно сопоставить данные рентгенологического контроля и клинические симптомы, после чего учесть все возможны медико-правовые аспекты нарушений.
Хирургическое восстановления поврежденного тройничного нерва
Существуют конкретные причины, которые аргументируют необходимость микрохирургического восстановления повреждённого тройничного нерва, и контрактные факторы, которые определяют прогноз данной манипуляции. Ziccardi и Zuniga сформулировали следующий список причин, которые обосновывают направление пациента к микрохирургу: нарушение чувствительности, которое персистирует на протяжении более чем 3 месяцев и нарушает нормальную жизненную активность пациента, подтверждение факта пересечения нерва, отсутствие улучшений признаков гипостезии, развитие болевых ощущений после имплантации. После выполнения микрохирургической коррекции на успешность таковой влияет ряд факторов: время ожидания после имплантации, тип и объем поражения, степень васкуляризации области поражения, опыт хирурга, метод забора и подготовки трансплантата, наличие натяжения в области восстановления, возраст и общее состояние здоровья пациента.
По сути, микрохирургическое восстановление ветвей язычного и нижнего альвеолярного нервов возможно. Однако уровень успешности подобных манипуляций является весьма вариативным – в среднем исследователи указывают лишь на 50-59,4% эффективность такого лечения, и лишь в двух исследованиях результаты вмешательства достигали уровней 81,7% и 63,1%. Во всех проведённых исследованиях число субъектов является довольно незначительным, поэтому сравнивать конечные результаты таковых методологически невозможно. Тем не менее, 50-60% пациентов после микрохирургической коррекции демонстрируют признаки улучшения неврологических нарушений. Ziccardi and Zuniga предупреждают, что пациенты с тяжелыми нейросенсорными поражениями должны быть проинформированы о том, что полноценная их реабилитация фактически является невозможной. Также многие исследователи указывают на то, что эффективность микрохирургических процедур в случаях терапии анестезии, дизестезии и спонтанных болевых ощущений является преувеличенной. Если резюмировать, то микрохирургическая коррекция может помочь отдельными пациентам, но уровень прогнозированности результатов подобного лечения является неоднозначным. Таким образом, лучшая терапия нейросенсорных нарушений, связанных с имплантацией – это их профилактика.
Заключение
В клинической практике часто встречается дилемма: если имплантат успешно остеоинтегрирован, но вызывает умеренную парестезию без боли, что с ним делать? Ведь эксплантация не всегда может способствовать разрешению симптомов, а ретенция имплантата в кости при фактическом поражение нерва может спровоцировать развитие невромы. Последняя формируется в результате чрезмерного заживления области поврежденного нерва и гиперплазии смежных тканей, и очень часто требует последующего хирургического удаления. Решение о выборе возможного метода лечения должно приниматься вместе с пациентом после тщательной дискуссии всех возможных вариантов, и перед началом реабилитации пациент официально должен подтвердить свое согласие посредством заполнения специальной письменной формы.
Авторы:
Gary Greenstein, DDS, MS
Joseph R. Carpentieri, DDS
John Cavallaro, DDS































































































































































0 комментариев