Слизистая оболочка полости рта и лимфоидный аппарат челюстно-лицевой области играют уникальную роль во взаимодействии организма человека с окружающим его миром микробов. В процессе эволюции между человеком и микроорганизмами полости рта сформировались сложные многокомпонентные и противоречивые отношения. Поэтому роль микробов в жизнедеятельности человека далеко неоднозначна.
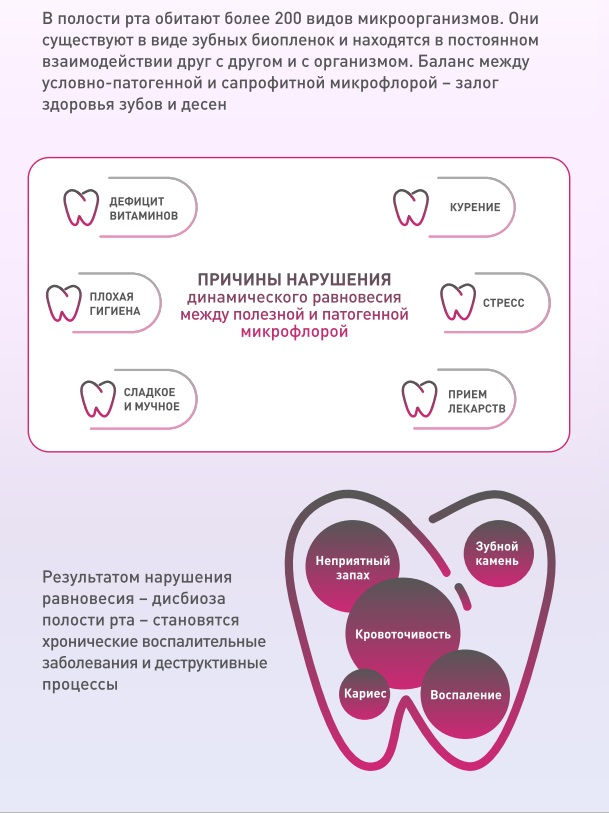
Постоянная флора полости рта участвует в переваривании пищи, в синтезе витаминов, оказывает большое позитивное воздействие на иммунную систему человека, является мощным антагонистом патогенной флоры, однако при определенных состояниях организма она оказывает токсичное действие на ткани десны, приобретая способность к инвазии, с последующим развитием воспалительных заболеваний полости рта. Исследование роли бактериальной колонизации в развитии и течении заболеваний соединительного аппарата зуба продолжается уже более 100 лет. В настоящее время среди множества теории, объясняющих возникновение пародонтопатий, бактериальная флора зубных бляшек рассматривается как первичный фактор, вызывающий поражение тканей, окружающих зуб, при гингивите и пародонтите. Как общепринятый термин «зубной налет» означает скопление колоний микроорганизмов, обитающих в ротовой полости. Впервые о ведущей роли микроорганизмов зубного налета в этиологии гингивита сообщил Зоненверт (1959), а в 1963 году Розбери подтвердил эту точку зрения. Длительное время воспалительные заболевания пародонта рассматривались как следствие неспецифического инфицирования микроорганизмами зубной бляшки (гипотеза о неспецифическом инфицировании налетом). Многие ученые в эти годы исходили из того, что пародонтит развивается из-за увеличения количества бактерий зубной бляшки. В 1975-1983 годах на первое место вышла гипотеза специфичной микрофлоры зубной бляшки. Благодаря исследованиям F. Slots (1979), W. Loesche (1992) и др. в полости рта обнаружены новые микроорганизмы и признано существование пародонтопатогенных бактерий, которые отличаются от других высокими адгезивными, инвазивными и токсическими свойствами по отношению к тканям пародонта. К этой группе отнесены Bacteroides forsithus, Prevotella intermedia, Porphiromonas gingivalis, Actinobacillus actinomycetemcommitans, Treponema denticola, Veillonella recta, Рерtоstreрtососсus micros, Streptococcus intermedius, Асtiпотусеs паеs1ипdii, Асtiпотусеs israelii. Согласно теории Socransky (1979) воспалительные заболевания пародонта не вызываются общим количеством бактерий или зубной бляшкой. По его мнению, среди постоянных представителей микрофлоры полости рта есть три группы потенциальных возбудителей гингивитов и пародонтитов с различной степенью активности. В первую группу им были включены патогены с выраженной ассоциацией с заболеваниями пародонта, это Actinobacillus actinomycetecomitans, Porphyromonas gingivalis и Bacteroides forsythus. Во вторую группу были объединены патогены с умеренной ассоциацией с заболеваниями пародонта: Treponema denticola, Prevotella intermedia, Campylobacter rectus, Peptostreptococcus micros, Eikenella corredens, Fusobacterium spp., Eubacterium spp., бета-гемолизирующие стрептококки. Третью группу составили патогены имеющие место лишь в отдельных случаях возникновения заболевания, это Staphylococcus spp., Pseudomonas spp., Candida spp., энтерококки и кишечные палочки. С точки зрения Y. Hirano (2003), наиболее выраженное токсическое действие на ткани десны наряду с актинобациллами оказывают представители пигментообразующих видов бактероидов — Роrрhуrотопаs gingivalis и Рrevоtеllа intermediа; по мнению Slots (1985), подобное состояние вызывают грамположительные представители пародонтопатогенной микрофлоры — Асtiпотусеs паеs1ипdii, А. israelii и анаэробные стрептококки Рерtоstreрtососсus micros, Streptococcus теlaninogenicus. Среди представителей патогенов с выраженной ассоциацией с заболеваниями пародонта в 2002 году И.В. Безрукова и А.И. Грудянов выявили группу патогенов, обладающих особой агрессивностью, таких как Actinobacillus actinomycetecomitans, Porphyromonas gingivalis, Рrevоtеllа intermediа. Однако, по мнению Е.В. Боровского и В.К. Леонтьева, при заболеваниях пародонта воспалительного характера инфекция в полости рта всегда эндогенная, и процесс в отсутствие специфического возбудителя может быть обусловлен действием различных микроорганизмов, зачастую несколькими видами одновременно: один и тот же микроорганизм может при определенном состоянии внутренних системных факторов вызывать различные патологические процессы. На основании вышеизложенного, можно сделать предварительный вывод, что на сегодняшний день нет единого мнения о роли отдельных групп микробов в патогенезе заболеваний пародонта.
Тем не менее, изучение микробиоты полости рта продолжается и результатом этого становится появление новых продуктов категории ORAL CARE, обладающих свойствами нормализовывать оральный микробиоценоз. На отечественном рынке появилась новая линейка средств по уходу за полостью рта ДентаБаланс®. Она основана на синбиотическом действии активных компонентов, иными словами, содержит сочетание пробиотика и пребиотиков. В качестве пробиотика выступает лизат культуры термофильного стрептококка (Streptococcus thermophyllus). Именно он отвечает за нормализацию микробиоты ротовой полости, подавление активности условно-патогенной флоры и стабилизацию местного иммунитета. Кроме того, Streptococcus thermophyllus оказывает так называемый Anti-Quorum Sensing-эффект, заключающийся в подавлении сигнальной коммуникации между микробами и снижении их агрессивности. Параллельно происходит стабилизация pH полости рта до физиологических значений (7,2-7,5), что понижает патогенный потенциал ряда микроорганизмов. В сочетании с пребиотиками развивается также антибиопленочный эффект, в результате чего создается неблагоприятная среда для формирования микробного налета.


Инновационная линейка ДентаБаланс® представлена продуктами, призванными решать конкретные проблемы полости рта: кариес, кровоточивость десен, галитоз, гиперчувствительность зубов и т.д. Выбор той или иной лекарственной формы обусловлен удобством и комфортом ее применения. Продукты данной линейки можно использовать как курсами, так и более продолжительное время. Это зависит от стоматологической проблемы, ее тяжести и характера протекания, особенностей гигиены полости рта пациента и т.д. Не менее важно то, что линейка ДентаБаланс® не содержит в составе SLS, парабенов, хлоргексидина и других «жестких» компонентов, ограничивающих временные рамки ее использования. Одним из преимуществ продукции ДентаБаланс® - возможность ее использования у лиц, страдающих сахарным диабетом, так как она не влияет на гликемию.



Таким образом, современный рынок средств гигиены полости рта предлагает широкий ассортимент продуктов, призванных решать различные стоматологические проблемы. Одно из важных и достойных мест в этом ряду занимает инновационная линейка ДентаБаланс®.
Производители:
Слизистая оболочка полости рта и лимфоидный аппарат челюстно-лицевой области играют уникальную роль во взаимодействии организма человека с окружающим его миром микробов. В процессе эволюции между человеком и микроорганизмами полости рта сформировались сложные многокомпонентные и противоречивые отношения. Поэтому роль микробов в жизнедеятельности человека далеко неоднозначна.


Постоянная флора полости рта участвует в переваривании пищи, в синтезе витаминов, оказывает большое позитивное воздействие на иммунную систему человека, является мощным антагонистом патогенной флоры, однако при определенных состояниях организма она оказывает токсичное действие на ткани десны, приобретая способность к инвазии, с последующим развитием воспалительных заболеваний полости рта. Исследование роли бактериальной колонизации в развитии и течении заболеваний соединительного аппарата зуба продолжается уже более 100 лет. В настоящее время среди множества теории, объясняющих возникновение пародонтопатий, бактериальная флора зубных бляшек рассматривается как первичный фактор, вызывающий поражение тканей, окружающих зуб, при гингивите и пародонтите. Как общепринятый термин «зубной налет» означает скопление колоний микроорганизмов, обитающих в ротовой полости. Впервые о ведущей роли микроорганизмов зубного налета в этиологии гингивита сообщил Зоненверт (1959), а в 1963 году Розбери подтвердил эту точку зрения. Длительное время воспалительные заболевания пародонта рассматривались как следствие неспецифического инфицирования микроорганизмами зубной бляшки (гипотеза о неспецифическом инфицировании налетом). Многие ученые в эти годы исходили из того, что пародонтит развивается из-за увеличения количества бактерий зубной бляшки. В 1975-1983 годах на первое место вышла гипотеза специфичной микрофлоры зубной бляшки. Благодаря исследованиям F. Slots (1979), W. Loesche (1992) и др. в полости рта обнаружены новые микроорганизмы и признано существование пародонтопатогенных бактерий, которые отличаются от других высокими адгезивными, инвазивными и токсическими свойствами по отношению к тканям пародонта. К этой группе отнесены Bacteroides forsithus, Prevotella intermedia, Porphiromonas gingivalis, Actinobacillus actinomycetemcommitans, Treponema denticola, Veillonella recta, Рерtоstreрtососсus micros, Streptococcus intermedius, Асtiпотусеs паеs1ипdii, Асtiпотусеs israelii. Согласно теории Socransky (1979) воспалительные заболевания пародонта не вызываются общим количеством бактерий или зубной бляшкой. По его мнению, среди постоянных представителей микрофлоры полости рта есть три группы потенциальных возбудителей гингивитов и пародонтитов с различной степенью активности. В первую группу им были включены патогены с выраженной ассоциацией с заболеваниями пародонта, это Actinobacillus actinomycetecomitans, Porphyromonas gingivalis и Bacteroides forsythus. Во вторую группу были объединены патогены с умеренной ассоциацией с заболеваниями пародонта: Treponema denticola, Prevotella intermedia, Campylobacter rectus, Peptostreptococcus micros, Eikenella corredens, Fusobacterium spp., Eubacterium spp., бета-гемолизирующие стрептококки. Третью группу составили патогены имеющие место лишь в отдельных случаях возникновения заболевания, это Staphylococcus spp., Pseudomonas spp., Candida spp., энтерококки и кишечные палочки. С точки зрения Y. Hirano (2003), наиболее выраженное токсическое действие на ткани десны наряду с актинобациллами оказывают представители пигментообразующих видов бактероидов — Роrрhуrотопаs gingivalis и Рrevоtеllа intermediа; по мнению Slots (1985), подобное состояние вызывают грамположительные представители пародонтопатогенной микрофлоры — Асtiпотусеs паеs1ипdii, А. israelii и анаэробные стрептококки Рерtоstreрtососсus micros, Streptococcus теlaninogenicus. Среди представителей патогенов с выраженной ассоциацией с заболеваниями пародонта в 2002 году И.В. Безрукова и А.И. Грудянов выявили группу патогенов, обладающих особой агрессивностью, таких как Actinobacillus actinomycetecomitans, Porphyromonas gingivalis, Рrevоtеllа intermediа. Однако, по мнению Е.В. Боровского и В.К. Леонтьева, при заболеваниях пародонта воспалительного характера инфекция в полости рта всегда эндогенная, и процесс в отсутствие специфического возбудителя может быть обусловлен действием различных микроорганизмов, зачастую несколькими видами одновременно: один и тот же микроорганизм может при определенном состоянии внутренних системных факторов вызывать различные патологические процессы. На основании вышеизложенного, можно сделать предварительный вывод, что на сегодняшний день нет единого мнения о роли отдельных групп микробов в патогенезе заболеваний пародонта.
Тем не менее, изучение микробиоты полости рта продолжается и результатом этого становится появление новых продуктов категории ORAL CARE, обладающих свойствами нормализовывать оральный микробиоценоз. На отечественном рынке появилась новая линейка средств по уходу за полостью рта ДентаБаланс®. Она основана на синбиотическом действии активных компонентов, иными словами, содержит сочетание пробиотика и пребиотиков. В качестве пробиотика выступает лизат культуры термофильного стрептококка (Streptococcus thermophyllus). Именно он отвечает за нормализацию микробиоты ротовой полости, подавление активности условно-патогенной флоры и стабилизацию местного иммунитета. Кроме того, Streptococcus thermophyllus оказывает так называемый Anti-Quorum Sensing-эффект, заключающийся в подавлении сигнальной коммуникации между микробами и снижении их агрессивности. Параллельно происходит стабилизация pH полости рта до физиологических значений (7,2-7,5), что понижает патогенный потенциал ряда микроорганизмов. В сочетании с пребиотиками развивается также антибиопленочный эффект, в результате чего создается неблагоприятная среда для формирования микробного налета.


Инновационная линейка ДентаБаланс® представлена продуктами, призванными решать конкретные проблемы полости рта: кариес, кровоточивость десен, галитоз, гиперчувствительность зубов и т.д. Выбор той или иной лекарственной формы обусловлен удобством и комфортом ее применения. Продукты данной линейки можно использовать как курсами, так и более продолжительное время. Это зависит от стоматологической проблемы, ее тяжести и характера протекания, особенностей гигиены полости рта пациента и т.д. Не менее важно то, что линейка ДентаБаланс® не содержит в составе SLS, парабенов, хлоргексидина и других «жестких» компонентов, ограничивающих временные рамки ее использования. Одним из преимуществ продукции ДентаБаланс® - возможность ее использования у лиц, страдающих сахарным диабетом, так как она не влияет на гликемию.



Таким образом, современный рынок средств гигиены полости рта предлагает широкий ассортимент продуктов, призванных решать различные стоматологические проблемы. Одно из важных и достойных мест в этом ряду занимает инновационная линейка ДентаБаланс®.





































































































































































0 комментариев