Гайморит эндодонтической этиологии представляет собой на самом деле довольно трудную для лечения патологию, которая развивается при распространении апикального периодонтита с дистальных зубов верхней челюсти на область верхнечелюстной пазухи. Развитию данного нарушения способствует тесное взаимоположение апексов жевательных зубов верхней челюсти и дна гайморовой пазухи. При этом апексы зубов могут находиться в непосредственном контакте с дном синуса, позиционироваться вдоль дна, или же непосредственно выступать в область пазухи. Наиболее близко с верхнечелюстным синусом контактируют второй премоляр, первый, второй и третий моляры. Протрузия корней этих зубов в пространство пазухи отмечается более, чем у 45% пациентов, что, в свою очередь, формирует свободный путь для одонтогенной инфекции и воспалительных медиаторов для распространения в просвет синуса.
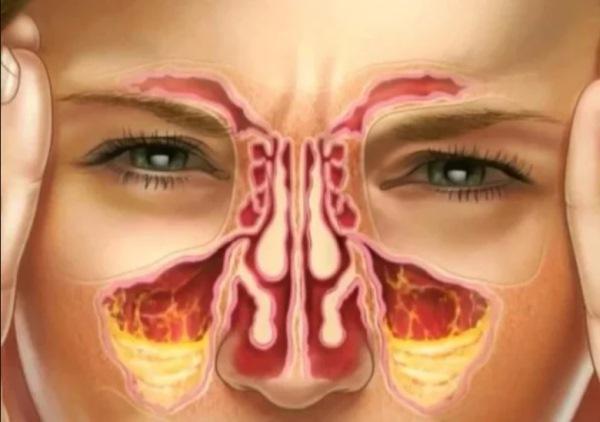
Этиология и патогенез одонтогенного поражения синуса
Хотя механизм распространение инфекции из одной области в другую довольно понятен, природа такого инфицирования может характеризоваться наличием разных форм. Воспаления гайморовой пазухи могут иметь разную клиническую манифестацию и проявляться по-разному. Так, например, риносинусит регистрируется при одновременном воспалении области носа и околоносовых пазух. В ЛОР-практике такой термин также является более приемлемым, нежели просто термины ринита и синусита, ведь подобные патологии возникают, как правило, в совокупности. Хронический риносинусит диагностируется при продолжительности воспаления на протяжении больше, чем 12 недель. Хроническая форма риносинусита развивается в условиях компрометированного состояния Шнайдеровой мембраны в результате предварительно проведенной пародонтальной операции, синус-лифта, удаления зубов, травмы, наличия чужеродного тела, опухоли, или непосредственного контакта с очагом одонтогенной инфекции. На самом деле, хронический риносинусит наиболее часто имеет одонтогенную этиологию из-за длительного контакта с пораженными воспалением участками апексов зубов. Риносинусит одонтогенной этиологии часто в литературе классифицируется как одонтогенный синусит, одонтогенный верхнечелюстной синусит или одонтогенный риносинусит. Термин «верхнечелюстной синусит одонтогенной эитологии», предложенный AAE в 2018 году, относится именно к риносинуситу вторичному по отношению к присущей эндодонтической этиологии. Поскольку одонтогенный гайморит первично развивается из-за распространения пульпарной инфекции в области периапикальных тканей и соответственно синуса, микробные ассоциации, которые чаще всего идентифицируются в синусе, аналогичны с теми, которые встречаются при некрозе пульпы и апикальном периодонтите. Некоторые виды грибков по типу Aspergillus также являются ассоциированными с гайморитом одонтогенной этиологии.
Факторы вирулентности микроорганизмов, действие лизосомальных ферментов и токсинов способствуют микробной инвазии и поражению тканей синуса через костную пластинку кости из-за начального одонтогенного очага. Местное воспаление и инфицирование альвеолярной кости и периодонта ассоциировано с утолщением слизистой гайморовой пазухи, что часто можно идентифицировать как симптом синусита на КЛКТ-сканах. Такое утолщение слизистой именуется мукозитом. Недавние исследования установили, что утолщение слизистой в области дна гайморовой пазухи в 9,5 раз с большей вероятностью встречается при одонтогенной инфекции синуса, чем при какой-либо другой этиологии ее воспаления. Мукозит с утолщением слизистой более чем на 2 мм классифицируется как патологический, что в дальнейшем ассоциировано с нарушением процесса муко-клеточной очистки пазух и ростом патогенной микрофлоры. В результате прогрессирования воспаления развивается закрытие остеомеатального комплекса, что ведёт за собой прогрессирующий отек, накопление экссудата и формирование условия для развития анаэробной микрофлоры. Все эти факторы вместе непосредственно способствуют развитию не только риносинусита, но и его осложнений. В случаях риносинуста среднее утолщение слизистой достигает 7,4 мм, и чаще всего данная патология связана с такими состояниями как поражения тканей пародонта, проведенным эндодонтическим лечением, адентией и фактором анатомической близости апексов корней зубов к дну пазухи.
Эпидемиология верхнечелюстного синусита
Хронический риносинусит поражает приблизительно 12% населения США каждый год, чаще всего людей в возрасте 30-50 лет. При отсутствии лечения данная патология может прогрессировать в пансинусит, который может распространиться на структуры орбиты и черепа и потенциально вызвать тромбоз кавернозного синуса, остеомиелит и менингит. Уровень распространения конкретно одонтогенного синусита верхней челюсти пока остается неизвестным. По данным последних исследования от 10% до 12% всех гайморитов имеют одонтогенную этиологию. Другие же данные указывают на то, что приблизительно 24-51% всех случаев хронического риносинусита связаны с первично одонтегнной инфекцией. Наиболее часто одонтогенный гайморит развивается в результат предварительно проведенных дентоальвеолярных хирургических вмешательств и эндодонтических манипуляций. Не так часто причиной поражения гайморовой пазухи являются пародонтальные патологии и имплантат-ассоциированные осложнения.
Диагностика верхнечелюстного синусита эндодонтической этиологии
Поскольку стоматологические патологии являются ответственными за 75-80% случаев развития одностороннего хронического риносинусита, пациенты с гайморитом неустановленной этиологии или же с подозрением на наличие ассоциированного поражения зубов, должны быть обязательно осмотрены врачом-стоматологом. Дифференциальная диагностика одностороннего риносинусита проводится с одонтогенным синуситом верхнечелюстного синуса, хроническим риносинуситом с образованием полипов в носовой области, аспергиломой, аллергическим грибковым синуситом, доброкачественными опухолями, карциномой, злокачественными новообразованиями, антрохоанальным полипозом и инвертированными папилломами. Если в ходе визуализации было обнаружено полное одностороннее поражение пазухи с расширением границ синуса, ставиться диагноз мукоцеле гайморовой пазухи, который аргументирует потребность в проведении ятрогенного вмешательства. Несмотря на высокую распространенность одонтогенного синусита, ЛОР-специалисты довольно редко принимают данные факты во внимание при анализе КЛКТ-снимков пазух.
Исследование, проведенное в 2011 году, установило, что дентальная патология в качестве причины гайморита, была указана лишь в 30% отчетов анализа рентгенологических снимков пациентов с диагностированным одонтогенным верхнечелюстным синуситом. Более того, даже официальные рекомендации относительно оценки состояния верхнечелюстной пазухи в условиях нормы и патологии довольно редко предусматривают необходимость проведения стоматологической диагностики.
Данные опубликованные в 2012 году опосредованно указывают на то, что значительное количество ЛОР-специалистов в неполной мере ознакомлены с фактами связи между апикальным периодонтитом и синуситом в структуре патомеханизма развития последнего. К сожалению, для специалистов, проводящих диагностику состояния верхнечелюстной пазухи, симптомы ее поражения одонтогенной и эндодонтической этиологии никак не отличаются от признаков, которые наблюдаются при неодонтогенных формах патологии. Таковые включают назальную обструкцию, экссудацию из носа, головную боль, боль в области лица, неприятный запах и привкус. При этом, однако следует помнить, что стоматологические симптомы сами по себе не могут быть использованы для постановки диагноза одонтогенного риносинусита. Ведь боль в области зубов при гайморите эндодонтической этиологии может полностью отсутствовать, когда из пазухи имеется отток и давление внутри не повышается. По данным предварительно проведенных исследований боль в области зубов отмечается лишь у 29% пациентов с установленным диагнозом одонтогенного верхнечелюстного синусита.
Процесс диагностики поражения гайморовой пазухи эндодонтической этиологии требует проведения как клинических, так и рентгенологических исследований. Клиницист должен оценить витальность зубов, состояние периапикальных тканей, реакции на перкуссию и пальпацию, состояние пародонта посредством пародонтального зондирования и оценки степени подвижности зубов. Регистрация признаков некроза пульпы, периапикального поражения, абсцесса или наличие в анамнезе факта эндодонтического лечения могут быть непосредственно ассоциированы с верхнечелюстным синуситом эндодонтической этиологии.
Учитывая высокую раздельную точность КЛКТ, данный метод остается золотым стандартом в диагностике поражений гайморовой пазухи эндодонтической этиологии. При использовании с данной целью двухмерных методов рентгенологического анализа отмечается взаимоналожение структур гайморовой пазухи и скулового отростка, что может маскировать имеющиеся признаки воспалительных изменений и апикального периодонтита. Также двумерные рентгенограммы не позволяют адекватно оценить анатомическое взаимоотношение между корнями зубов и дном гайморовой пазухи (фото 1). У пациентов с верхнечелюстным синуситом эндодонтической этиологии отмечается наличие периапикальное поражения со смежным затемнением в области гайморовой пазухи. Дополнительно можно обнаружить рентгенологические признаки периапикального мукозита и периапикального остеопериостита. Периапикальный мукозит, который проявляется утолщением слизистой, визуализируется в форме куполообразного расширения мягких тканей в области дна пазухи, примыкающей к корням зубов.
Фото 1. Рентгенограмма, демонстрирующая признаки патологии синуса за скуловой костью.
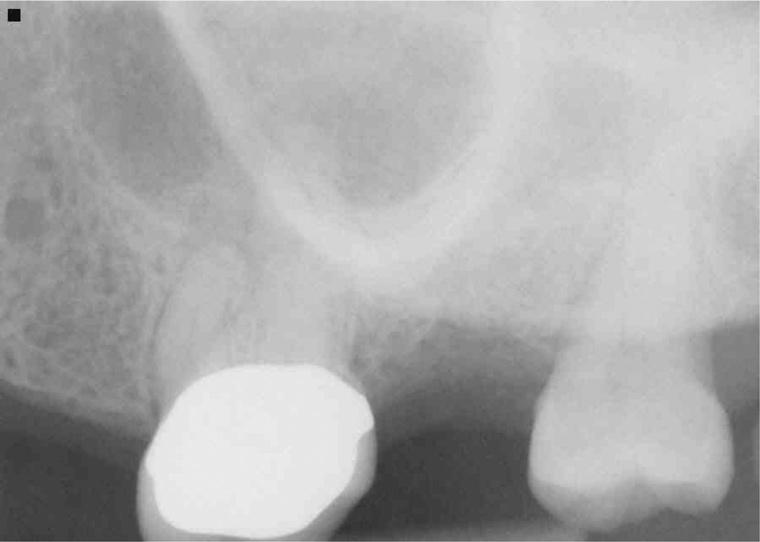
Периапикальный остеопериостит, по сути, является реактивным остеогенезом, вызванным локальной периостальной реакцией, которая провоцирует расширения надкостницы дна пазухи вовнутрь самого синуса. Данное изменение идентифицируется в форме эффекта «гало» вокруг апекса корня (фото 1-3). Периапикальный остеопериостит может быть симптоматическим и ассоциированным с отеком мягких тканей и повышением уровня экссудата в структуре пазухи. При отсутствии лечения данные изменения могут прогрессировать, приводя к формированию непосредственного контакта с между верхнечелюстным синусом и апексом корня зуба. Как правило, подобные реакции со стороны пазухи концентрируются вокруг одонтогенного очага инфекции. Полное одностороннее затемнение пазухи иногда может быть пропущено на КЛКТ-срезах, используемых в эндодонтических целях, учитывая их ограниченные параметры поля съемки (фото 4). В случаях же диагностики полного одностороннего затемнения синуса стоматолог должен обязательно направить пациента к ЛОРу или челюстно-лицевому хирургу с целью исключения диагноза инвазивной грибковой инфекции или новообразования.
Фото 2. КЛКТ-срез с визуализацией эффекта «гало», указывающим на наличие мукозита в области дна пазухи.
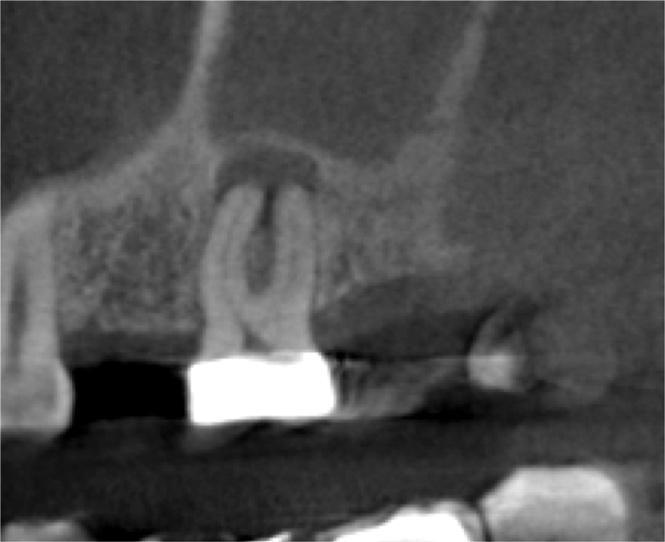
Фото 3. Корональный срез проблемного зуба.
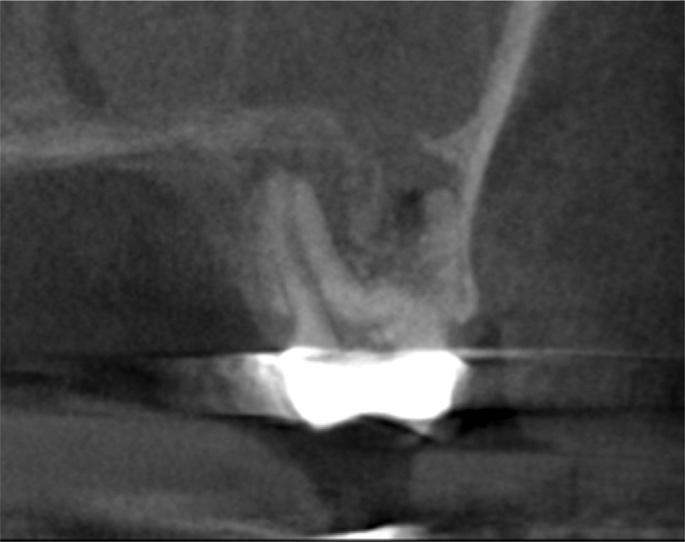
Фото 4. КЛКТ визуализация эндодонтического поражения зуба, ассоциированного с односторонней патологией пазухи.
Лечение верхнечелюстного синусита эндодонтической этиологии
Лечение верхнечелюстного синусита эндодонтической этиологии обеспечивается как за счет терапии причинного стоматологического поражения, так и за счет коррекции симптомов гайморита. Для формулировки определенного наиболее эффективного алгоритма лечения в данное время проводиться разработка доказательных рекомендаций, которые повышают прогнозированность вмешательств. Стоматологический аспект лечения верхнечелюстного одонтогенного синусита может включать проведение ортоградного эндодонтического вмешательства, повторное эндодонтическое лечение, апикальную хирургию, намеренную реплантацию или же даже экстракцию. Данные определенных исследований указывают на то, что в случаях одонтогенного гайморита процедуры удаления все же лучше избегать из-за повышения риска развития ороантрального соединения. Также совсем недавно было доказано, что при удаление третьих моляров верхней челюсти, формирование травматического устья с верхнечелюстным синусом чаще наблюдалось у пациентов с уже имеющимся воспалительным поражением пазухи. В таких условиях также осложняется процесс заживления области вмешательства. Медикаментозная терапия включает использование ирригаций полости носа и применение кортикостероидов интраназально. На данное время данных, аргументирующих целесообразность приема антибиотиков для лечения хронического риносинусита пока что не получено. По мнению AAE, антибиотики изолировано не обеспечивают надлежащего терапевтического эффекта, но могут использоваться в комбинации с другими фармацевтическими агентами. Прием антибиотиков показан при необходимости временного улучшения симптомов синусита, и в случаях чрезмерно прогрессивного распространения инфекции.
При незначительных поражениях верхнечелюстного синуса стоматологическое вмешательство может помочь полностью вылечить патологию. С другой стороны, случаи распространенного гайморита очень сложно поддаются какому-либо виду терапии. В случаях, когда медикаментозное и стоматологического лечение является неэффективным, можно провести хирургическое вмешательство с целью восстановления естественного дренажа пазухи.
Функциональная эндоскопическая хирургия пазухи (FESS) хорошо зарекомендовала себя для лечения хронического риносинусита, резистентного к стоматологическому или медикаментозному лечению. Эндоскопическое вмешательство позволяет восстановить вентиляцию и дренаж синуса через остеомеатальный комплекс, при этом данная манипуляция может проводиться под локальной анестезией. Процедура эндоскопической хирургии включает выполнение верхнечелюстной антроскопии (открытие и увеличение естественного устья), в отдельных случаях может понадобиться проведение передней этмоидэктомии (резекция и санация этмоидной буллы и воздушных клеток), задней этмоидэктомии или сфеноидотомия (в случае увеличения клиновидного устья). В случаях верхнечелюстного синусита, вызванного влиянием более крупных инородных тел, прибегают к формированию внутриротового подхода, известного как радикальная антростомия по Колдуэллу-Люку. В настоящее время FESS является более предпочтительной с точки зрения эффективности, меньшей траматичности и сниженного уровня потенциальных осложнений. Как правило, после операций обеспечивается еще соответствующая медикаментозная поддержка, ведь для разрешения симптомов может потребоваться еще несколько недель времени.
Клинический случай
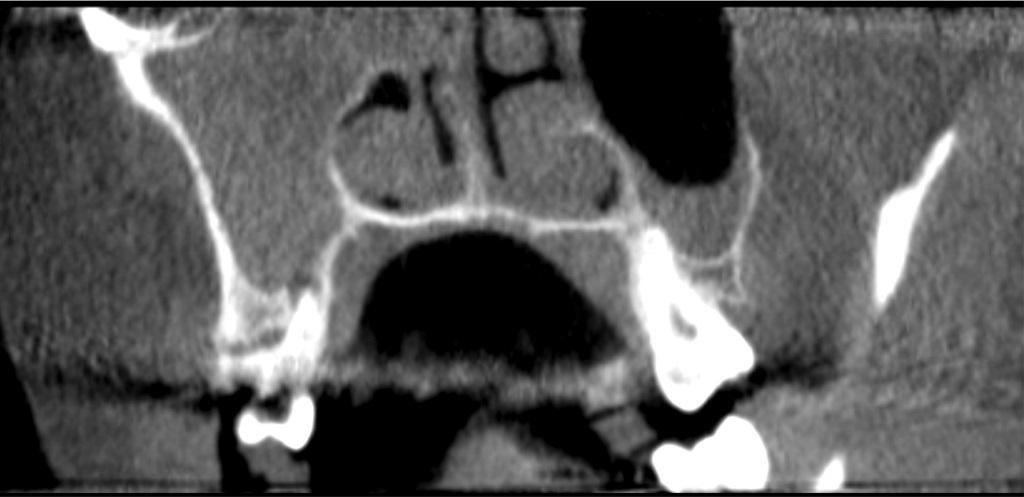
58-летняя пациентка обратилась за помощью с наличием симптомов острого синусита на протяжении последних 3 месяцев. Предварительное лечение включало 6 курсов антибиотикотерапии с применением пенициллинов, цефалоспоринов и хинолонов, но все оказалось безуспешно. После того, как ЛОР обнаружил на снимке эндодонтическую патологию в области 2 зуба, она была направлена к стоматологу. В ходе клинического осмотра было установлено, что 2 зуб был девитальным (не реагировал на холодовые и электрические раздражители), положительно реагировал на перкуссию и пальпацию. Симптомов отека, наличия свищей или пародонтальных дефектов отмечено не было. На КЛКТ-снимке был идентифицирован очаг поражения в области апексов как щечного, так и небного корней, полное рентгенологическое помутнение в области правых верхнечелюстных и придаточных пазух носа и поражение латеральной / задней стенки пазухи позади скуловерхнечелюстного контрфорса (фото 5).
Фото 5. КЛКТ-срез, демонстрирующий признаки периапикального поражения в области 2 зуба.
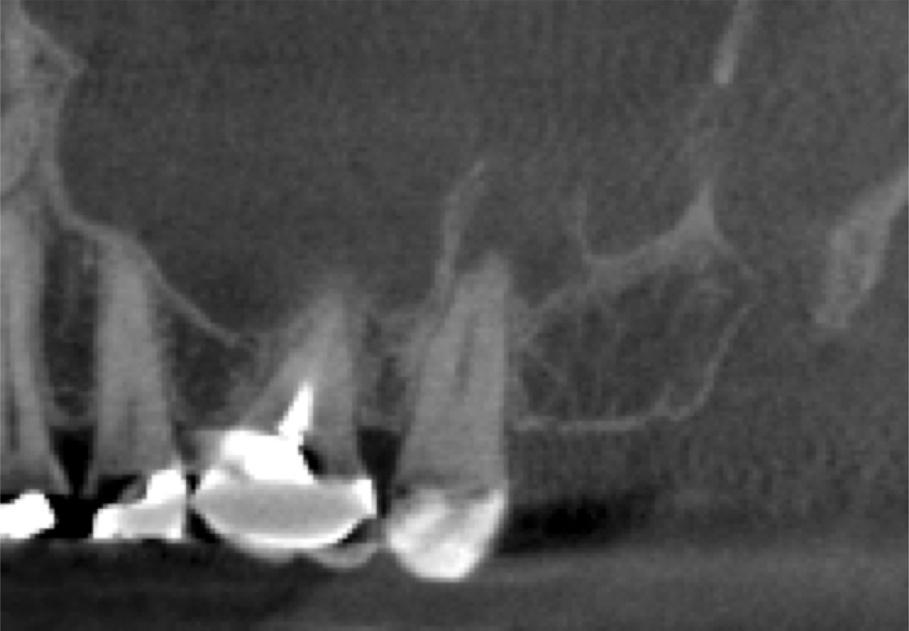
Было проведено эндодонтического лечение. В ходе формирования надлежащего доступа пульпа выглядела черной, что свидетельствовало о наличии некроза. После экстирпации пульпы в канал был помещен агент на основе гидроксида кальция. Через несколько недель симптомы поражения пазухи улучшились, но полностью не исчезли. Каналы зуба были обтурированы, и пациентка обратно была направлена к ЛОР-врачу. Последний провел процедуру эндоскопического вмешательства, в ходе реализации которой выявил выделение слизисто-гнойного экссудата через среднюю часть носового хода. После манипуляции пациентке было назначено использовать противоотёчный препарат для местного применения на протяжении 2 недель. Через 2 месяца в ходе контрольного осмотра пациент сообщил, что продолжает отмечать симптомы персистирующего синусита. Дополнительно ему была проведена процедура FESS с повторной очисткой носовых ходов с правой стороны. Через 3 недели после этого пациентка продолжала отмечать симптомы боли и давления, из-за чего врач назначил ей дополнительный курс антибиотикотерапии. Через три месяца после проведения стоматологического лечения и через месяц после проведения дополнительного эндоскопического вмешательства, пациентка явилась к эндодонтисту с целью контрольного визита. На тот момент она сообщала лишь об ощущениях незначительного давления в области пазухи, которое она сама связывала с сезонной аллергией. Признаков отека, подвижности зуба или наличия свищевого хода в ходе осмотра отмечено не было. Зуб 2 был полностью нечувствителен к перкуссии и пальпации. На КЛКТ-срезах отмечалась очистка области синуса и признаки заживления апикальной патологии (фото 6-7).
Фото 6. КЛКТ-срез, полученный через 3 месяца после эндодонтического лечения (6 недель после хирургического вмешательства на синусе).
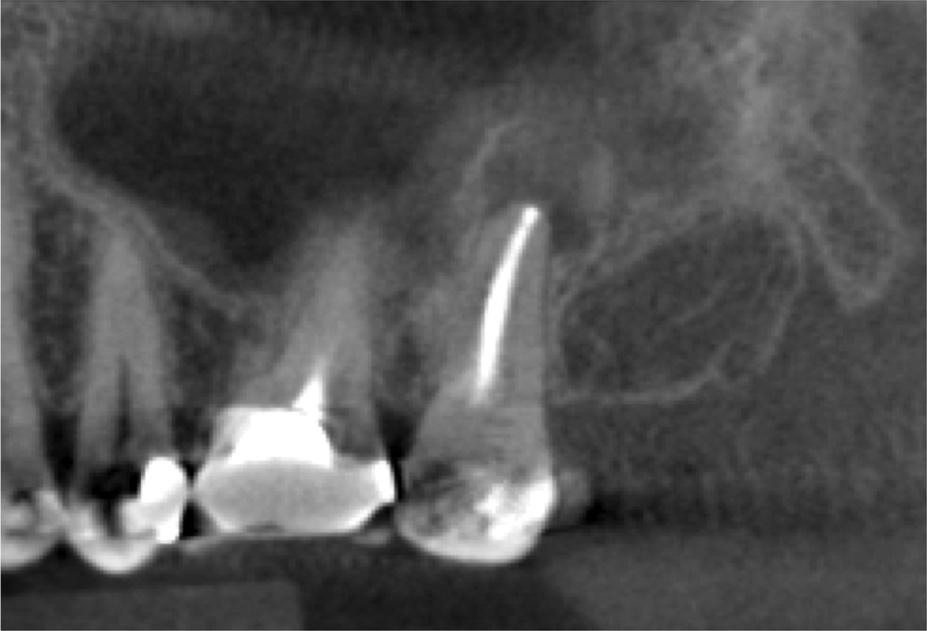
Фото 7. КЛКТ-срез, полученный через 3 месяца после эндодонтического лечения (6 недель после хирургического вмешательства на синусе).
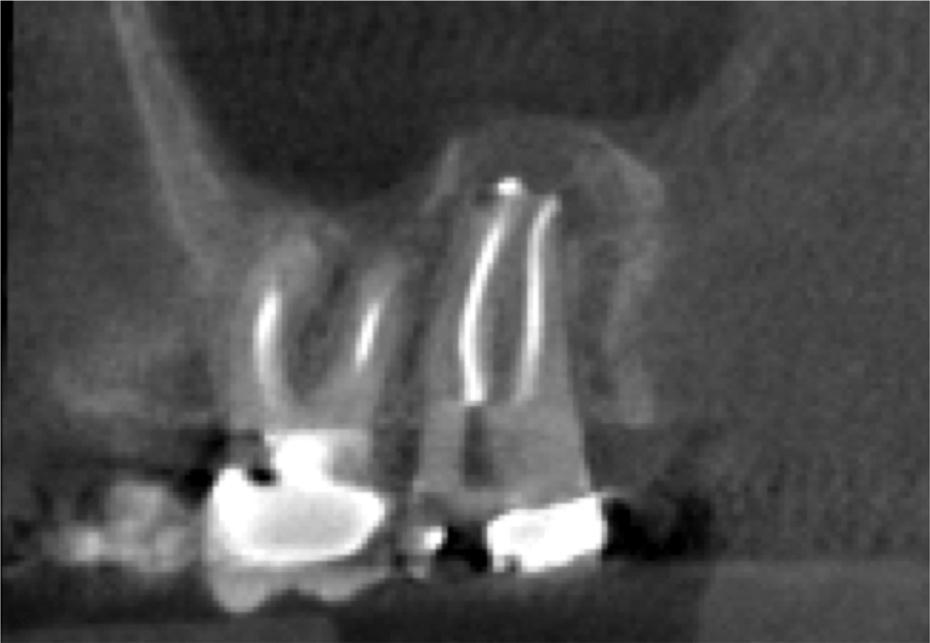
Данный случай демонстрирует классическую картину верхнечелюстного синусита эндодонтической этиологии, при котором апикальное рентгенологическое просветление перешло на кортикальную кость пазухи, что, в свою очередь, спровоцировало формирование соединения между этими двумя структурами. В результате проведенного эндодонтического лечения было отмечено заживление области апикального очага поражения с восстановлением нарушенных кортикальных границ между апексом зуба и дном пазухи. Сложность синусита аргументировала необходимость реализации комплексного медикаментозного, стоматологического и даже хирургического лечения.
Заключение
Верхнечелюстной синусит эндодонтического этиологии является сложно диагностируемой патологией с точки зрения идентификации всех причинных факторов поражения. Анатомическая близость зубов верхней челюсти с дном пазухи обосновывает патофизиологическую связь между эндодонтическими очагами инфекции и риском поражения синуса. Поскольку симптомы одонтогенного и неодонтогенного хронического риносинусита являются полностью аналогичными, проведение стоматологического осмотра с целью дифференциальной диагностики патологий является обязательным. Постановка правильного диагноза также способствуют возможности современных методов визуализации по типу КЛКТ. После постановки окончательного диагноза верхнечелюстного синусита эндодонтической этиологии лечение таких пациентов должно проводиться вместе с ЛОР-специалистом, учитывая комплексный характер патологии.
Авторы:
Jessica Langella; Brooke Blicher, DMD
Rebekah Lucier Pryles, DMD
Гайморит эндодонтической этиологии представляет собой на самом деле довольно трудную для лечения патологию, которая развивается при распространении апикального периодонтита с дистальных зубов верхней челюсти на область верхнечелюстной пазухи. Развитию данного нарушения способствует тесное взаимоположение апексов жевательных зубов верхней челюсти и дна гайморовой пазухи. При этом апексы зубов могут находиться в непосредственном контакте с дном синуса, позиционироваться вдоль дна, или же непосредственно выступать в область пазухи. Наиболее близко с верхнечелюстным синусом контактируют второй премоляр, первый, второй и третий моляры. Протрузия корней этих зубов в пространство пазухи отмечается более, чем у 45% пациентов, что, в свою очередь, формирует свободный путь для одонтогенной инфекции и воспалительных медиаторов для распространения в просвет синуса.

Этиология и патогенез одонтогенного поражения синуса
Хотя механизм распространение инфекции из одной области в другую довольно понятен, природа такого инфицирования может характеризоваться наличием разных форм. Воспаления гайморовой пазухи могут иметь разную клиническую манифестацию и проявляться по-разному. Так, например, риносинусит регистрируется при одновременном воспалении области носа и околоносовых пазух. В ЛОР-практике такой термин также является более приемлемым, нежели просто термины ринита и синусита, ведь подобные патологии возникают, как правило, в совокупности. Хронический риносинусит диагностируется при продолжительности воспаления на протяжении больше, чем 12 недель. Хроническая форма риносинусита развивается в условиях компрометированного состояния Шнайдеровой мембраны в результате предварительно проведенной пародонтальной операции, синус-лифта, удаления зубов, травмы, наличия чужеродного тела, опухоли, или непосредственного контакта с очагом одонтогенной инфекции. На самом деле, хронический риносинусит наиболее часто имеет одонтогенную этиологию из-за длительного контакта с пораженными воспалением участками апексов зубов. Риносинусит одонтогенной этиологии часто в литературе классифицируется как одонтогенный синусит, одонтогенный верхнечелюстной синусит или одонтогенный риносинусит. Термин «верхнечелюстной синусит одонтогенной эитологии», предложенный AAE в 2018 году, относится именно к риносинуситу вторичному по отношению к присущей эндодонтической этиологии. Поскольку одонтогенный гайморит первично развивается из-за распространения пульпарной инфекции в области периапикальных тканей и соответственно синуса, микробные ассоциации, которые чаще всего идентифицируются в синусе, аналогичны с теми, которые встречаются при некрозе пульпы и апикальном периодонтите. Некоторые виды грибков по типу Aspergillus также являются ассоциированными с гайморитом одонтогенной этиологии.
Факторы вирулентности микроорганизмов, действие лизосомальных ферментов и токсинов способствуют микробной инвазии и поражению тканей синуса через костную пластинку кости из-за начального одонтогенного очага. Местное воспаление и инфицирование альвеолярной кости и периодонта ассоциировано с утолщением слизистой гайморовой пазухи, что часто можно идентифицировать как симптом синусита на КЛКТ-сканах. Такое утолщение слизистой именуется мукозитом. Недавние исследования установили, что утолщение слизистой в области дна гайморовой пазухи в 9,5 раз с большей вероятностью встречается при одонтогенной инфекции синуса, чем при какой-либо другой этиологии ее воспаления. Мукозит с утолщением слизистой более чем на 2 мм классифицируется как патологический, что в дальнейшем ассоциировано с нарушением процесса муко-клеточной очистки пазух и ростом патогенной микрофлоры. В результате прогрессирования воспаления развивается закрытие остеомеатального комплекса, что ведёт за собой прогрессирующий отек, накопление экссудата и формирование условия для развития анаэробной микрофлоры. Все эти факторы вместе непосредственно способствуют развитию не только риносинусита, но и его осложнений. В случаях риносинуста среднее утолщение слизистой достигает 7,4 мм, и чаще всего данная патология связана с такими состояниями как поражения тканей пародонта, проведенным эндодонтическим лечением, адентией и фактором анатомической близости апексов корней зубов к дну пазухи.
Эпидемиология верхнечелюстного синусита
Хронический риносинусит поражает приблизительно 12% населения США каждый год, чаще всего людей в возрасте 30-50 лет. При отсутствии лечения данная патология может прогрессировать в пансинусит, который может распространиться на структуры орбиты и черепа и потенциально вызвать тромбоз кавернозного синуса, остеомиелит и менингит. Уровень распространения конкретно одонтогенного синусита верхней челюсти пока остается неизвестным. По данным последних исследования от 10% до 12% всех гайморитов имеют одонтогенную этиологию. Другие же данные указывают на то, что приблизительно 24-51% всех случаев хронического риносинусита связаны с первично одонтегнной инфекцией. Наиболее часто одонтогенный гайморит развивается в результат предварительно проведенных дентоальвеолярных хирургических вмешательств и эндодонтических манипуляций. Не так часто причиной поражения гайморовой пазухи являются пародонтальные патологии и имплантат-ассоциированные осложнения.
Диагностика верхнечелюстного синусита эндодонтической этиологии
Поскольку стоматологические патологии являются ответственными за 75-80% случаев развития одностороннего хронического риносинусита, пациенты с гайморитом неустановленной этиологии или же с подозрением на наличие ассоциированного поражения зубов, должны быть обязательно осмотрены врачом-стоматологом. Дифференциальная диагностика одностороннего риносинусита проводится с одонтогенным синуситом верхнечелюстного синуса, хроническим риносинуситом с образованием полипов в носовой области, аспергиломой, аллергическим грибковым синуситом, доброкачественными опухолями, карциномой, злокачественными новообразованиями, антрохоанальным полипозом и инвертированными папилломами. Если в ходе визуализации было обнаружено полное одностороннее поражение пазухи с расширением границ синуса, ставиться диагноз мукоцеле гайморовой пазухи, который аргументирует потребность в проведении ятрогенного вмешательства. Несмотря на высокую распространенность одонтогенного синусита, ЛОР-специалисты довольно редко принимают данные факты во внимание при анализе КЛКТ-снимков пазух.
Исследование, проведенное в 2011 году, установило, что дентальная патология в качестве причины гайморита, была указана лишь в 30% отчетов анализа рентгенологических снимков пациентов с диагностированным одонтогенным верхнечелюстным синуситом. Более того, даже официальные рекомендации относительно оценки состояния верхнечелюстной пазухи в условиях нормы и патологии довольно редко предусматривают необходимость проведения стоматологической диагностики.
Данные опубликованные в 2012 году опосредованно указывают на то, что значительное количество ЛОР-специалистов в неполной мере ознакомлены с фактами связи между апикальным периодонтитом и синуситом в структуре патомеханизма развития последнего. К сожалению, для специалистов, проводящих диагностику состояния верхнечелюстной пазухи, симптомы ее поражения одонтогенной и эндодонтической этиологии никак не отличаются от признаков, которые наблюдаются при неодонтогенных формах патологии. Таковые включают назальную обструкцию, экссудацию из носа, головную боль, боль в области лица, неприятный запах и привкус. При этом, однако следует помнить, что стоматологические симптомы сами по себе не могут быть использованы для постановки диагноза одонтогенного риносинусита. Ведь боль в области зубов при гайморите эндодонтической этиологии может полностью отсутствовать, когда из пазухи имеется отток и давление внутри не повышается. По данным предварительно проведенных исследований боль в области зубов отмечается лишь у 29% пациентов с установленным диагнозом одонтогенного верхнечелюстного синусита.
Процесс диагностики поражения гайморовой пазухи эндодонтической этиологии требует проведения как клинических, так и рентгенологических исследований. Клиницист должен оценить витальность зубов, состояние периапикальных тканей, реакции на перкуссию и пальпацию, состояние пародонта посредством пародонтального зондирования и оценки степени подвижности зубов. Регистрация признаков некроза пульпы, периапикального поражения, абсцесса или наличие в анамнезе факта эндодонтического лечения могут быть непосредственно ассоциированы с верхнечелюстным синуситом эндодонтической этиологии.
Учитывая высокую раздельную точность КЛКТ, данный метод остается золотым стандартом в диагностике поражений гайморовой пазухи эндодонтической этиологии. При использовании с данной целью двухмерных методов рентгенологического анализа отмечается взаимоналожение структур гайморовой пазухи и скулового отростка, что может маскировать имеющиеся признаки воспалительных изменений и апикального периодонтита. Также двумерные рентгенограммы не позволяют адекватно оценить анатомическое взаимоотношение между корнями зубов и дном гайморовой пазухи (фото 1). У пациентов с верхнечелюстным синуситом эндодонтической этиологии отмечается наличие периапикальное поражения со смежным затемнением в области гайморовой пазухи. Дополнительно можно обнаружить рентгенологические признаки периапикального мукозита и периапикального остеопериостита. Периапикальный мукозит, который проявляется утолщением слизистой, визуализируется в форме куполообразного расширения мягких тканей в области дна пазухи, примыкающей к корням зубов.
Фото 1. Рентгенограмма, демонстрирующая признаки патологии синуса за скуловой костью.

Периапикальный остеопериостит, по сути, является реактивным остеогенезом, вызванным локальной периостальной реакцией, которая провоцирует расширения надкостницы дна пазухи вовнутрь самого синуса. Данное изменение идентифицируется в форме эффекта «гало» вокруг апекса корня (фото 1-3). Периапикальный остеопериостит может быть симптоматическим и ассоциированным с отеком мягких тканей и повышением уровня экссудата в структуре пазухи. При отсутствии лечения данные изменения могут прогрессировать, приводя к формированию непосредственного контакта с между верхнечелюстным синусом и апексом корня зуба. Как правило, подобные реакции со стороны пазухи концентрируются вокруг одонтогенного очага инфекции. Полное одностороннее затемнение пазухи иногда может быть пропущено на КЛКТ-срезах, используемых в эндодонтических целях, учитывая их ограниченные параметры поля съемки (фото 4). В случаях же диагностики полного одностороннего затемнения синуса стоматолог должен обязательно направить пациента к ЛОРу или челюстно-лицевому хирургу с целью исключения диагноза инвазивной грибковой инфекции или новообразования.
Фото 2. КЛКТ-срез с визуализацией эффекта «гало», указывающим на наличие мукозита в области дна пазухи.

Фото 3. Корональный срез проблемного зуба.

Фото 4. КЛКТ визуализация эндодонтического поражения зуба, ассоциированного с односторонней патологией пазухи.

Лечение верхнечелюстного синусита эндодонтической этиологии
Лечение верхнечелюстного синусита эндодонтической этиологии обеспечивается как за счет терапии причинного стоматологического поражения, так и за счет коррекции симптомов гайморита. Для формулировки определенного наиболее эффективного алгоритма лечения в данное время проводиться разработка доказательных рекомендаций, которые повышают прогнозированность вмешательств. Стоматологический аспект лечения верхнечелюстного одонтогенного синусита может включать проведение ортоградного эндодонтического вмешательства, повторное эндодонтическое лечение, апикальную хирургию, намеренную реплантацию или же даже экстракцию. Данные определенных исследований указывают на то, что в случаях одонтогенного гайморита процедуры удаления все же лучше избегать из-за повышения риска развития ороантрального соединения. Также совсем недавно было доказано, что при удаление третьих моляров верхней челюсти, формирование травматического устья с верхнечелюстным синусом чаще наблюдалось у пациентов с уже имеющимся воспалительным поражением пазухи. В таких условиях также осложняется процесс заживления области вмешательства. Медикаментозная терапия включает использование ирригаций полости носа и применение кортикостероидов интраназально. На данное время данных, аргументирующих целесообразность приема антибиотиков для лечения хронического риносинусита пока что не получено. По мнению AAE, антибиотики изолировано не обеспечивают надлежащего терапевтического эффекта, но могут использоваться в комбинации с другими фармацевтическими агентами. Прием антибиотиков показан при необходимости временного улучшения симптомов синусита, и в случаях чрезмерно прогрессивного распространения инфекции.
При незначительных поражениях верхнечелюстного синуса стоматологическое вмешательство может помочь полностью вылечить патологию. С другой стороны, случаи распространенного гайморита очень сложно поддаются какому-либо виду терапии. В случаях, когда медикаментозное и стоматологического лечение является неэффективным, можно провести хирургическое вмешательство с целью восстановления естественного дренажа пазухи.
Функциональная эндоскопическая хирургия пазухи (FESS) хорошо зарекомендовала себя для лечения хронического риносинусита, резистентного к стоматологическому или медикаментозному лечению. Эндоскопическое вмешательство позволяет восстановить вентиляцию и дренаж синуса через остеомеатальный комплекс, при этом данная манипуляция может проводиться под локальной анестезией. Процедура эндоскопической хирургии включает выполнение верхнечелюстной антроскопии (открытие и увеличение естественного устья), в отдельных случаях может понадобиться проведение передней этмоидэктомии (резекция и санация этмоидной буллы и воздушных клеток), задней этмоидэктомии или сфеноидотомия (в случае увеличения клиновидного устья). В случаях верхнечелюстного синусита, вызванного влиянием более крупных инородных тел, прибегают к формированию внутриротового подхода, известного как радикальная антростомия по Колдуэллу-Люку. В настоящее время FESS является более предпочтительной с точки зрения эффективности, меньшей траматичности и сниженного уровня потенциальных осложнений. Как правило, после операций обеспечивается еще соответствующая медикаментозная поддержка, ведь для разрешения симптомов может потребоваться еще несколько недель времени.
Клинический случай
58-летняя пациентка обратилась за помощью с наличием симптомов острого синусита на протяжении последних 3 месяцев. Предварительное лечение включало 6 курсов антибиотикотерапии с применением пенициллинов, цефалоспоринов и хинолонов, но все оказалось безуспешно. После того, как ЛОР обнаружил на снимке эндодонтическую патологию в области 2 зуба, она была направлена к стоматологу. В ходе клинического осмотра было установлено, что 2 зуб был девитальным (не реагировал на холодовые и электрические раздражители), положительно реагировал на перкуссию и пальпацию. Симптомов отека, наличия свищей или пародонтальных дефектов отмечено не было. На КЛКТ-снимке был идентифицирован очаг поражения в области апексов как щечного, так и небного корней, полное рентгенологическое помутнение в области правых верхнечелюстных и придаточных пазух носа и поражение латеральной / задней стенки пазухи позади скуловерхнечелюстного контрфорса (фото 5).
Фото 5. КЛКТ-срез, демонстрирующий признаки периапикального поражения в области 2 зуба.

Было проведено эндодонтического лечение. В ходе формирования надлежащего доступа пульпа выглядела черной, что свидетельствовало о наличии некроза. После экстирпации пульпы в канал был помещен агент на основе гидроксида кальция. Через несколько недель симптомы поражения пазухи улучшились, но полностью не исчезли. Каналы зуба были обтурированы, и пациентка обратно была направлена к ЛОР-врачу. Последний провел процедуру эндоскопического вмешательства, в ходе реализации которой выявил выделение слизисто-гнойного экссудата через среднюю часть носового хода. После манипуляции пациентке было назначено использовать противоотёчный препарат для местного применения на протяжении 2 недель. Через 2 месяца в ходе контрольного осмотра пациент сообщил, что продолжает отмечать симптомы персистирующего синусита. Дополнительно ему была проведена процедура FESS с повторной очисткой носовых ходов с правой стороны. Через 3 недели после этого пациентка продолжала отмечать симптомы боли и давления, из-за чего врач назначил ей дополнительный курс антибиотикотерапии. Через три месяца после проведения стоматологического лечения и через месяц после проведения дополнительного эндоскопического вмешательства, пациентка явилась к эндодонтисту с целью контрольного визита. На тот момент она сообщала лишь об ощущениях незначительного давления в области пазухи, которое она сама связывала с сезонной аллергией. Признаков отека, подвижности зуба или наличия свищевого хода в ходе осмотра отмечено не было. Зуб 2 был полностью нечувствителен к перкуссии и пальпации. На КЛКТ-срезах отмечалась очистка области синуса и признаки заживления апикальной патологии (фото 6-7).
Фото 6. КЛКТ-срез, полученный через 3 месяца после эндодонтического лечения (6 недель после хирургического вмешательства на синусе).

Фото 7. КЛКТ-срез, полученный через 3 месяца после эндодонтического лечения (6 недель после хирургического вмешательства на синусе).

Данный случай демонстрирует классическую картину верхнечелюстного синусита эндодонтической этиологии, при котором апикальное рентгенологическое просветление перешло на кортикальную кость пазухи, что, в свою очередь, спровоцировало формирование соединения между этими двумя структурами. В результате проведенного эндодонтического лечения было отмечено заживление области апикального очага поражения с восстановлением нарушенных кортикальных границ между апексом зуба и дном пазухи. Сложность синусита аргументировала необходимость реализации комплексного медикаментозного, стоматологического и даже хирургического лечения.
Заключение
Верхнечелюстной синусит эндодонтического этиологии является сложно диагностируемой патологией с точки зрения идентификации всех причинных факторов поражения. Анатомическая близость зубов верхней челюсти с дном пазухи обосновывает патофизиологическую связь между эндодонтическими очагами инфекции и риском поражения синуса. Поскольку симптомы одонтогенного и неодонтогенного хронического риносинусита являются полностью аналогичными, проведение стоматологического осмотра с целью дифференциальной диагностики патологий является обязательным. Постановка правильного диагноза также способствуют возможности современных методов визуализации по типу КЛКТ. После постановки окончательного диагноза верхнечелюстного синусита эндодонтической этиологии лечение таких пациентов должно проводиться вместе с ЛОР-специалистом, учитывая комплексный характер патологии.
Авторы:
Jessica Langella; Brooke Blicher, DMD
Rebekah Lucier Pryles, DMD
































































































































































2 комментария
Спасибо, интересно!
Спасибо!