Процедура периапикального хирургического вмешательства включает в себя три последовательных манипуляции: резекция верхушки корня, препарирование полости в области верхушки корня и ретроградную герметизацию. Для обеспечения успешности подобной процедуры необходимо обеспечить полное удаление патологических воспалительных тканей и максимальную очистку области верхушки корня.
В данной статье приведен анализ хирургических факторов, влияющих на эффективность процедуры остеоэктомии, и их связи с дальнейшим клиническим прогнозом.
Хирургическая техника вмешательства
Остеоэктомия предполагает удаление порции костной ткани с вестибулярной части альвеолярного гребня для формирования доступа к апексу зуба. Размер остеоэктомии определяет объем самого периапикального поражения, наличие соответствующего инструментария и близость области вмешательства к смежным анатомическим структурам (подбородочному нерву, каналу нижнечелюстного нерва и верхнечелюстному синусу). Логически, что лучше всего, если размер остеоэктомии является минимальным, однако в большинстве случаев его приходиться увеличивать для обеспечения оптимальных условий для работы кюретами и выполнения адекватного объема апикоэктомии. Остеоэктомию проводят круглыми твердосплавными борами (6-10 размера) при достаточной ирригации физиологическим раствором (фото 1).
Фото 1а. Ортопантомограмма пациента, который первично обратился за стоматологической помощью по поводу необходимости установки дентального имплантата. На снимке визуализируется периапикальное поражения левого премоляра нижней челюсти.
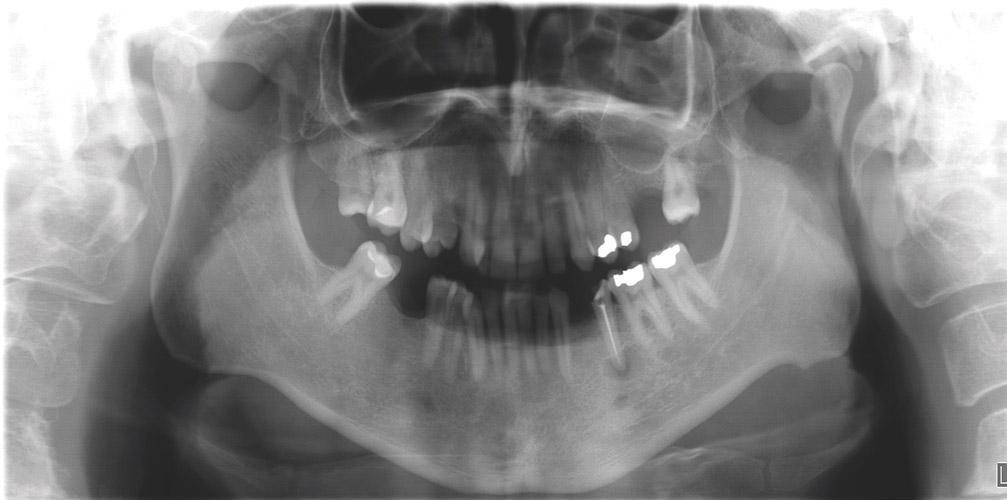
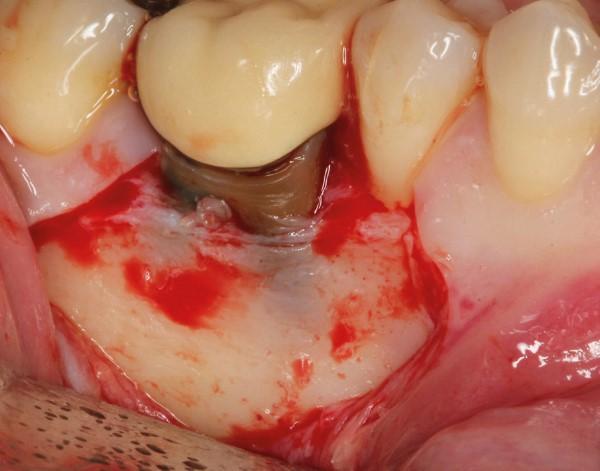
Фото 1b. Вид рабочего поля после сепарации лоскута. Важно обеспечить максимально аккуратную сепарацию лоскута, дабы избежать повреждения подбородочного нерва.
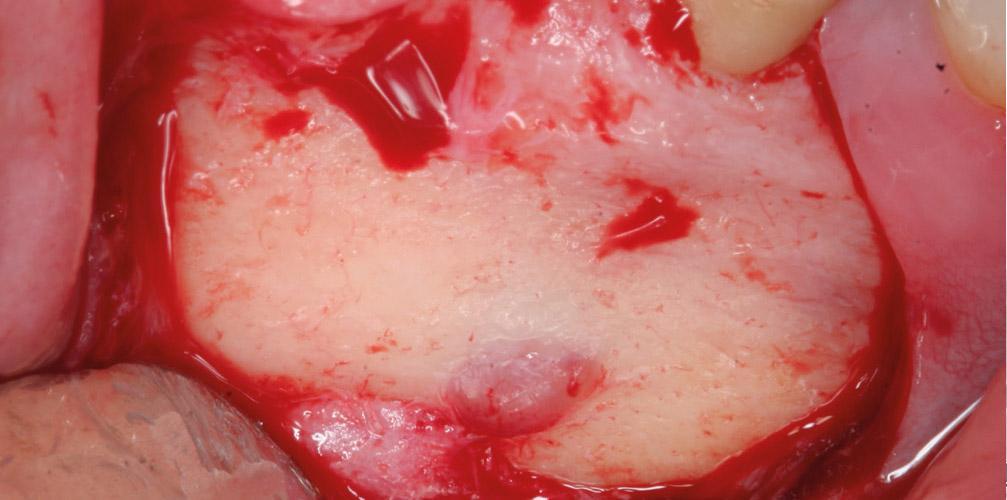
Фото 1c. Остеоэктомия выполняется с помощью твёрдосплавного бора с обильной ирригацией физиологическим раствором.
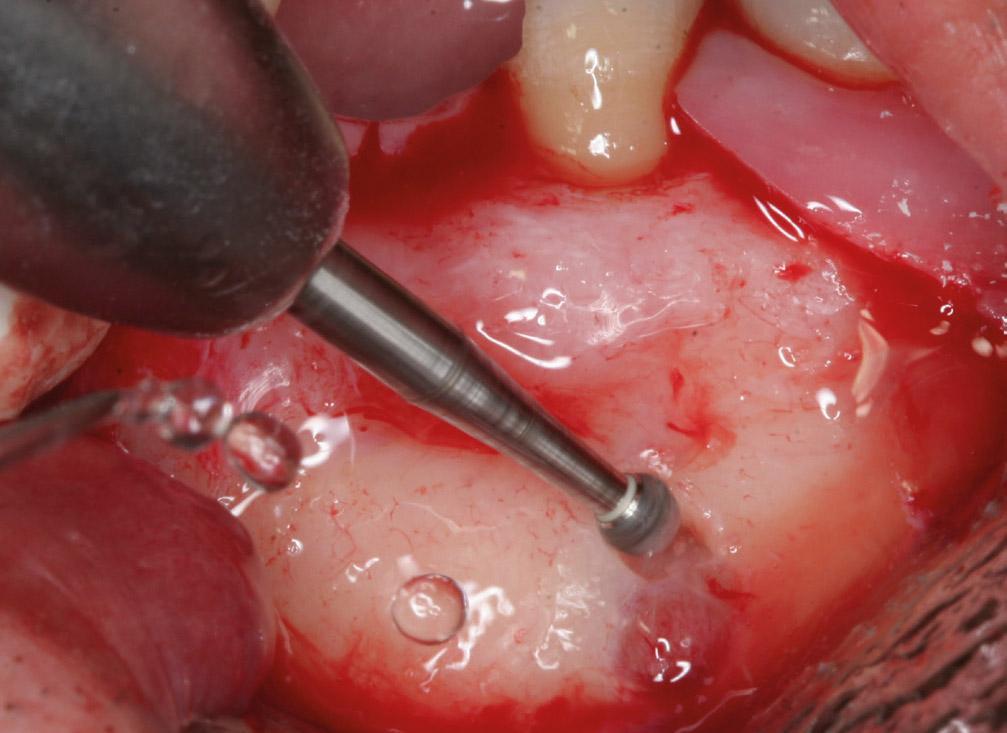
Фото 1d. Размер остеоэктомии должен составлять около 4 мм. Такой размер обеспечивает условия для свободной работы ультразвуковым наконечником.
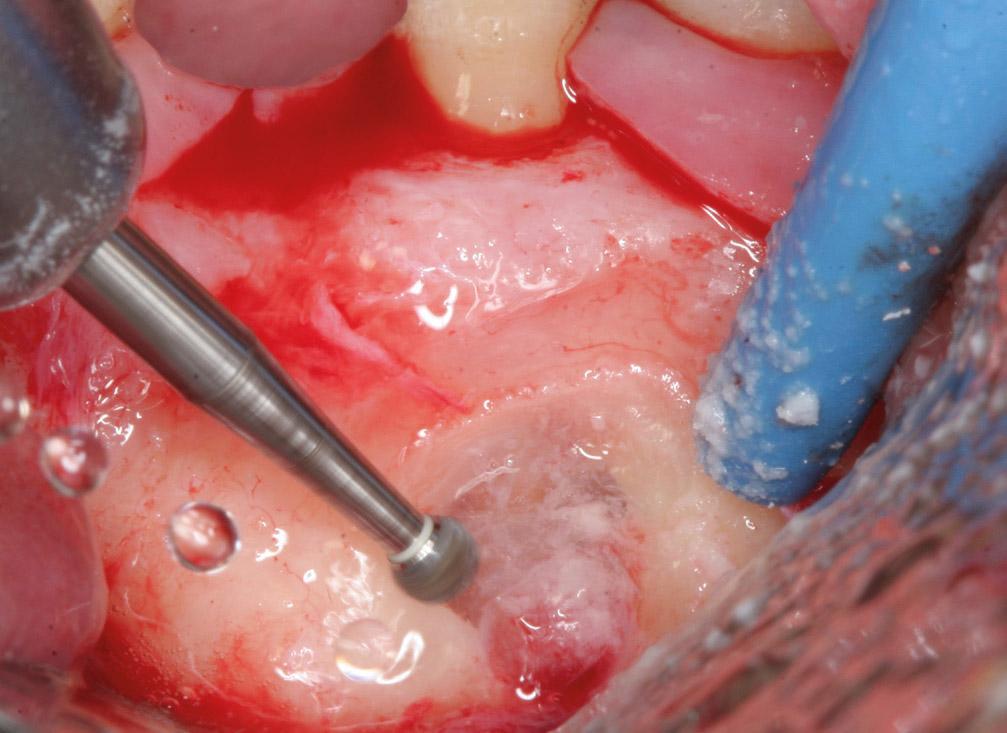
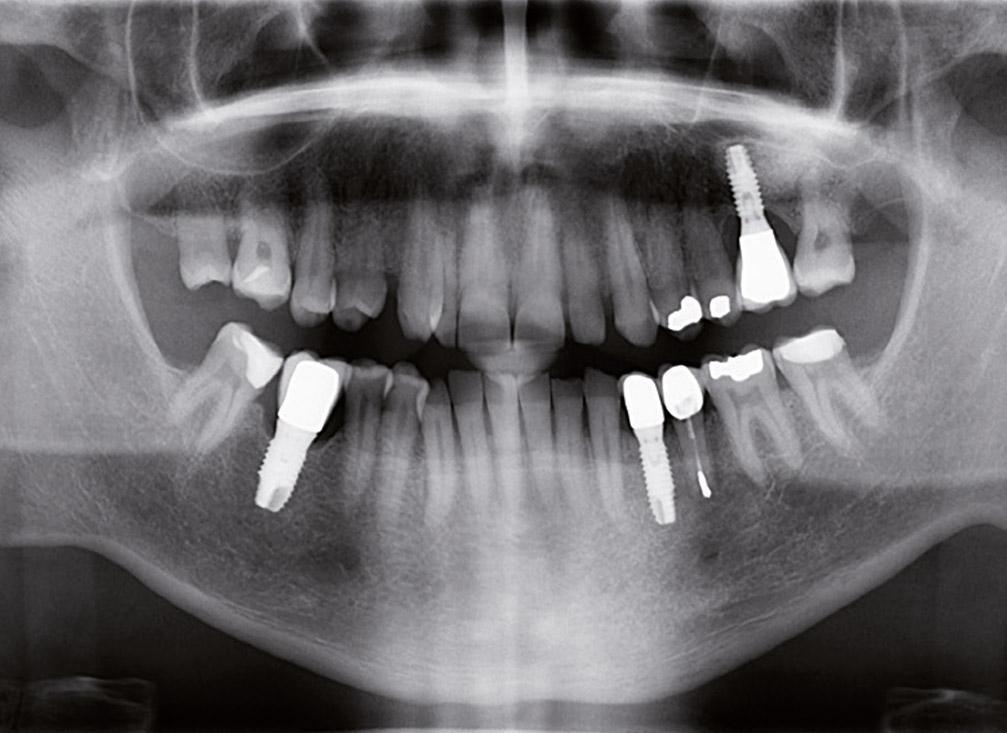
Фото 1e. Ортопантомограмма пациента через 5 лет после лечения: признаки заживления костной ткани в области левого премоляра нижней челюсти.
Совсем недавно на рынке появился новый тип углового наконечника (45°), который обеспечивает подачу только воды без воздуха, таким образом, минимизируя риск развития эмфиземы. Доступ формируют в проекции 2-4 мм от апекса, а доступ выполняют перпендикулярно длинной оси зуба до момента достижения собственно тканей корня. После этого остеоэктомию заканчивают небольшими движениями бора для удаления костной ткани вокруг цемента корня. В области моляров нижней челюсти наружная костная пластинка характеризуется значительной плотностью, а сам доступ к апексу корней является топографически осложненным. Поэтому в таких случаях объем входного отверстия приходиться значительно увеличивать, для того чтобы обеспечить достаточный контроль области рабочего поля. В результате подобных вмешательств, конечно же, остаются огромные костные дефекты, которые после можно заполнить материалом костного заменителя, перекрыв его объем наиболее подходящей мембраной.
В 1961 году Boyne и соавторы изучили уровень деструкции вестибулярной костной пластинки после выполнения остеоэктомии и периапикального кюретажа. Они установили, что после незначительных ятрогенных костных дефектов размеров 5-8 мм наблюдается почти полная регенерация костной ткани, в то время как дефекты размером в 9-12 мм характеризуются замещением в большинстве случаев соединительной тканью. Десять лет спустя Hjorting-Hansen и Andreasen изучали постостеоэктомичесике дефекты размером 5, 6 и 8 мм, сформированные через вестибулярную или язычную костную пластинку на нижней челюсти у собак. Авторы обнаружили, что паттерн заживления костной ткани зависит от размера полости и факта повреждения одновременно одной или двух кортикальных пластинок.
Rubinstein и Kim также установили, что существует прямая связь между заживлением костной ткани и размером остеоэктомии: небольшие дефекты в 0-5 мм восстанавливаются на протяжении в среднем 6,40 месяцев, в то время как для заживления дефектов среднего размера 6-10 мм требуется уже 7,25 месяцев, а для заживления дефектов размером более 10 мм – уже 11 месяцев. Учитывая этот факт, в случаях необходимости проведения остеоэктомии в области двух корней нижнего моляра, которые разделены интактной костной перегородкой без наличия воспалительного инфильтрата, можно провести две отдельные остеоэктомии в области каждого из корней, не соединяя их между собой. Таким образом, размер послеоперационных дефектов будет значительно меньше, а общее время заживления удастся заметно сократить (фото 2).
Фото 2а. Для формирования доступа к моляру нижней челюсти был сепарирован трапециевидный лоскут.
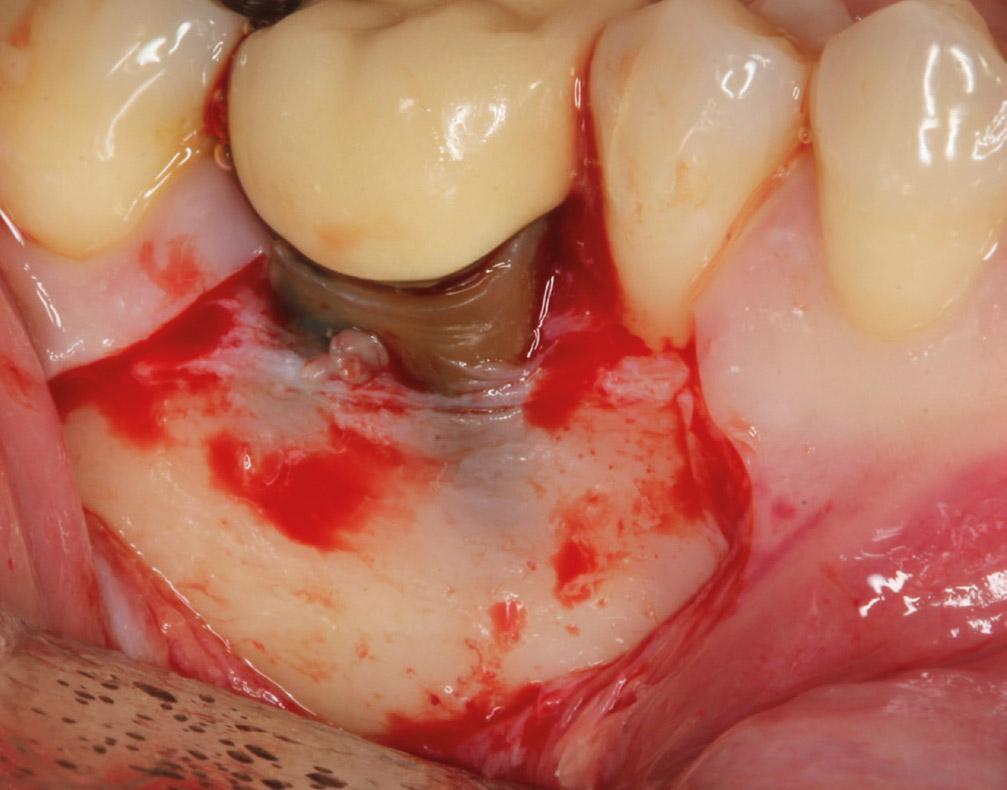
Фото 2b. Два отдельных участка остеоэктомии для формирования доступа к мезиальному и дистальному корням.
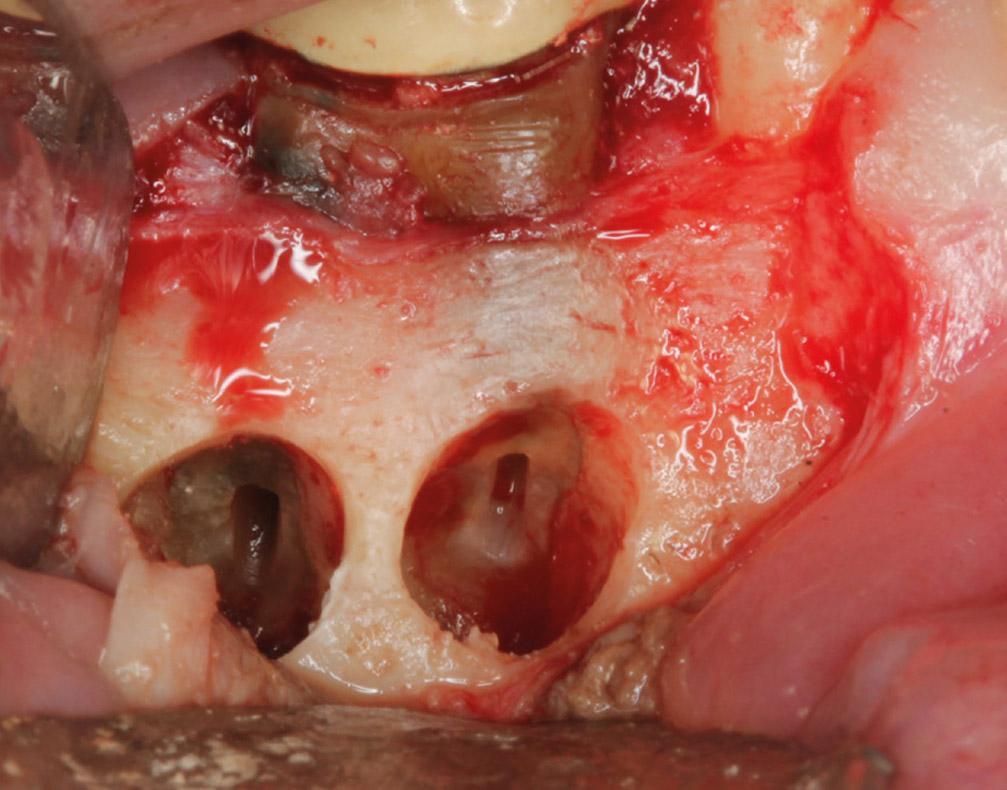
Фото 2с. Ретроградное пломбирование посредством МТА.
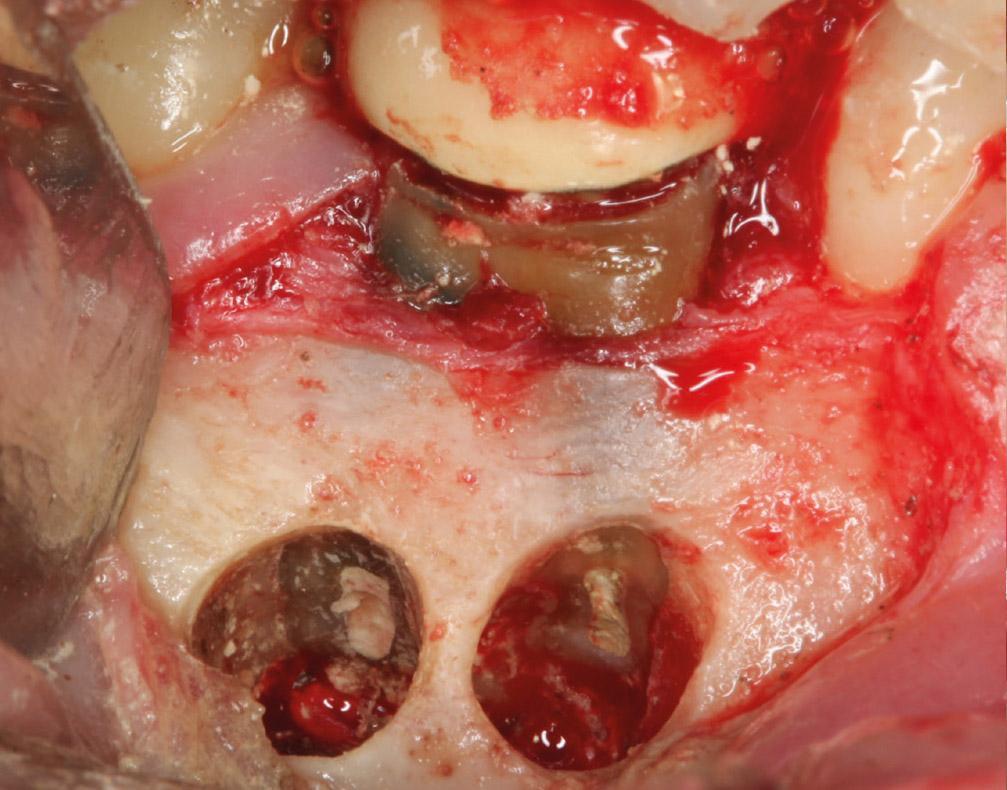
Фото 2d. Периапикальная рентгенограмма через год после лечения.
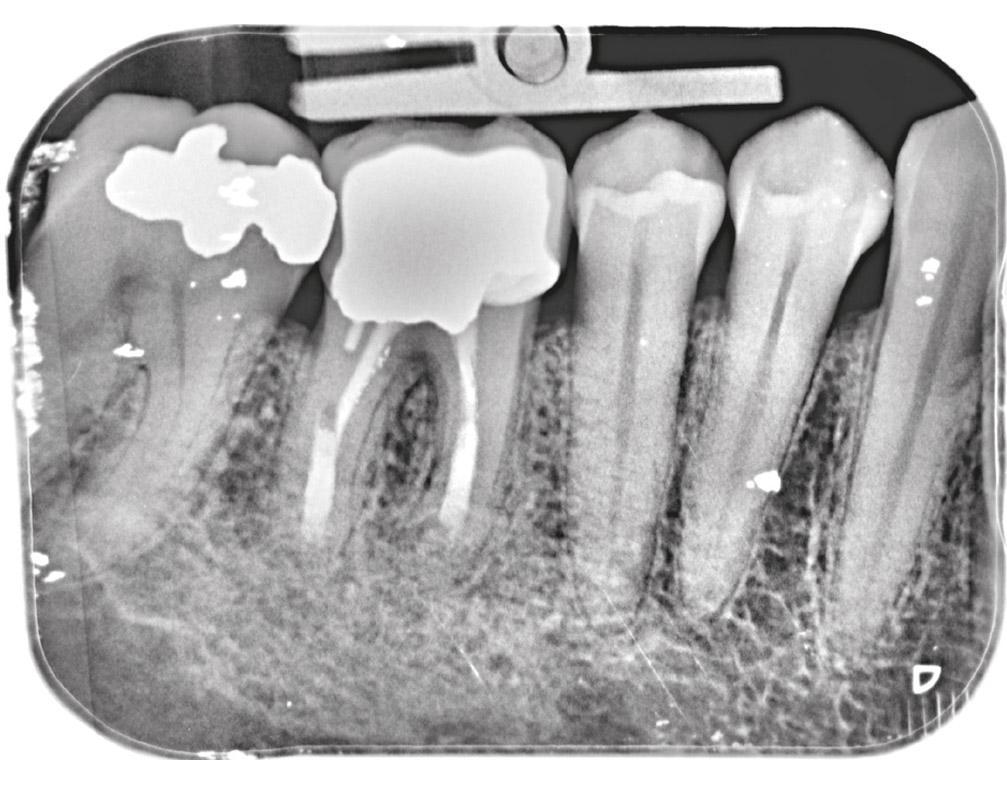
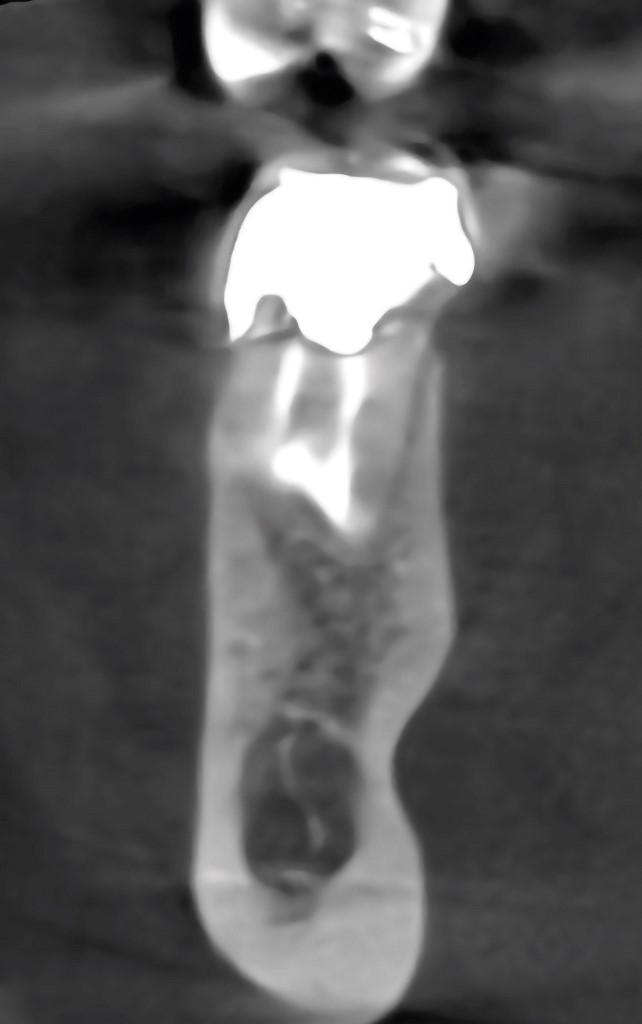
Фото 2e. КЛКТ-срез, который демонстрирует качество ретроградного пломбирования и заживления костной ткани в периапикальной области.
Микрохирургические техники оперативных вмешательств еще в большей мере позволяют уменьшить размер остеоэктомии до 4 мм в диаметре. Такой диаметр несколько больше длины ультразвуковой насадки в 3 мм, что обеспечивает достаточные условия для ее манипуляции в структуре костной полости (фото 3).
Фото 3a. Вид переднего зуба верхней челюсти со здоровым состоянием мягких тканей. Пациент обратился за помощью по поводу спонтанных болевых ощущений, возникших в данном участке.
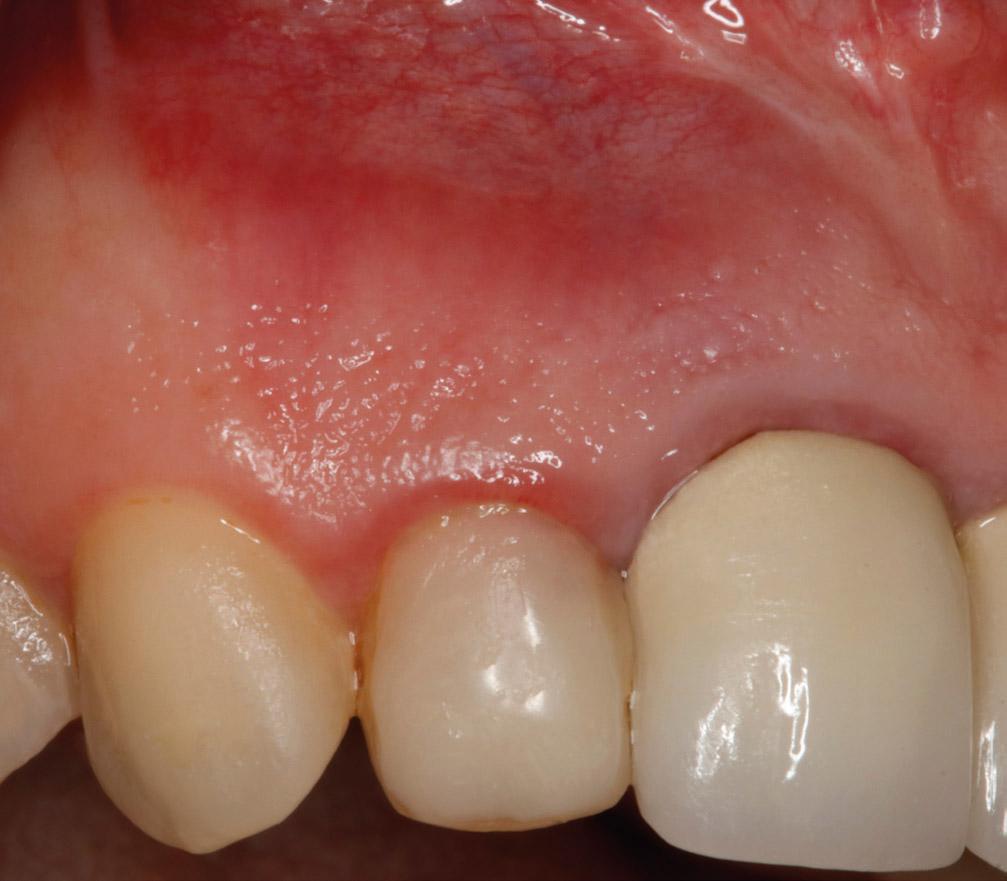
Фото 3b. На рентгенограмме визуализируется область периапикального поражения бокового резца, который ранее уже был эндодонтически пролечен.
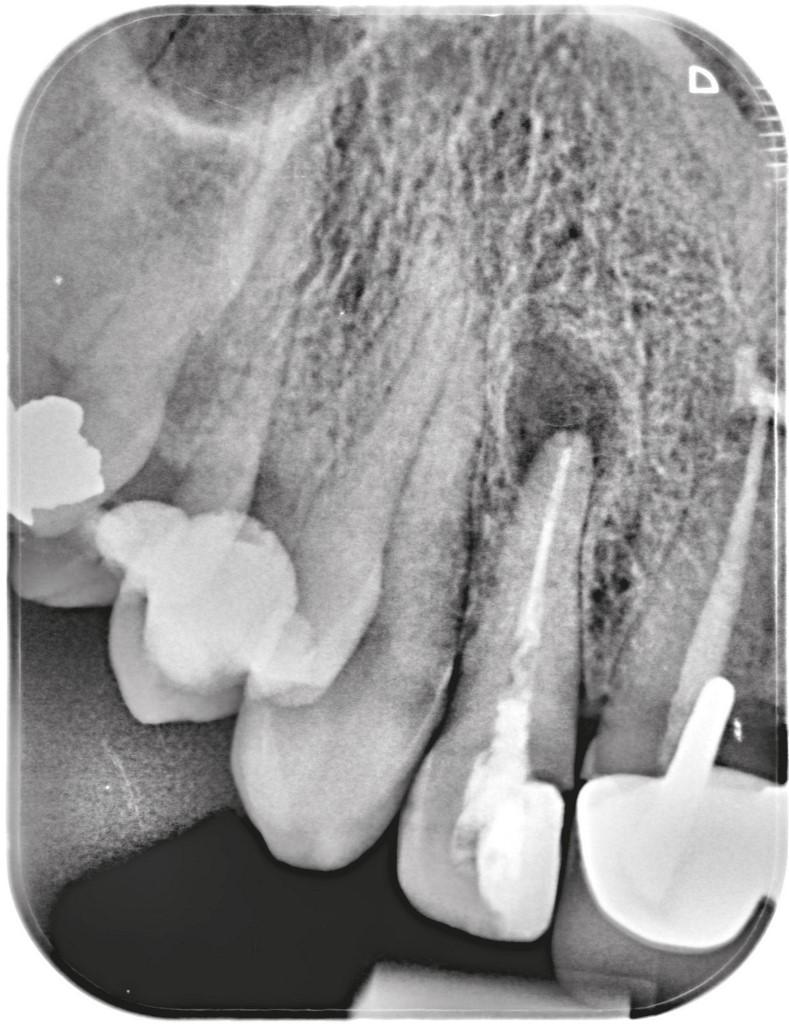
Фото 3c. КЛКТ-срез демонстрирует признаки апикального поражения, распространяющегося и на кортикальную пластинку в области бокового резца верхней челюсти.
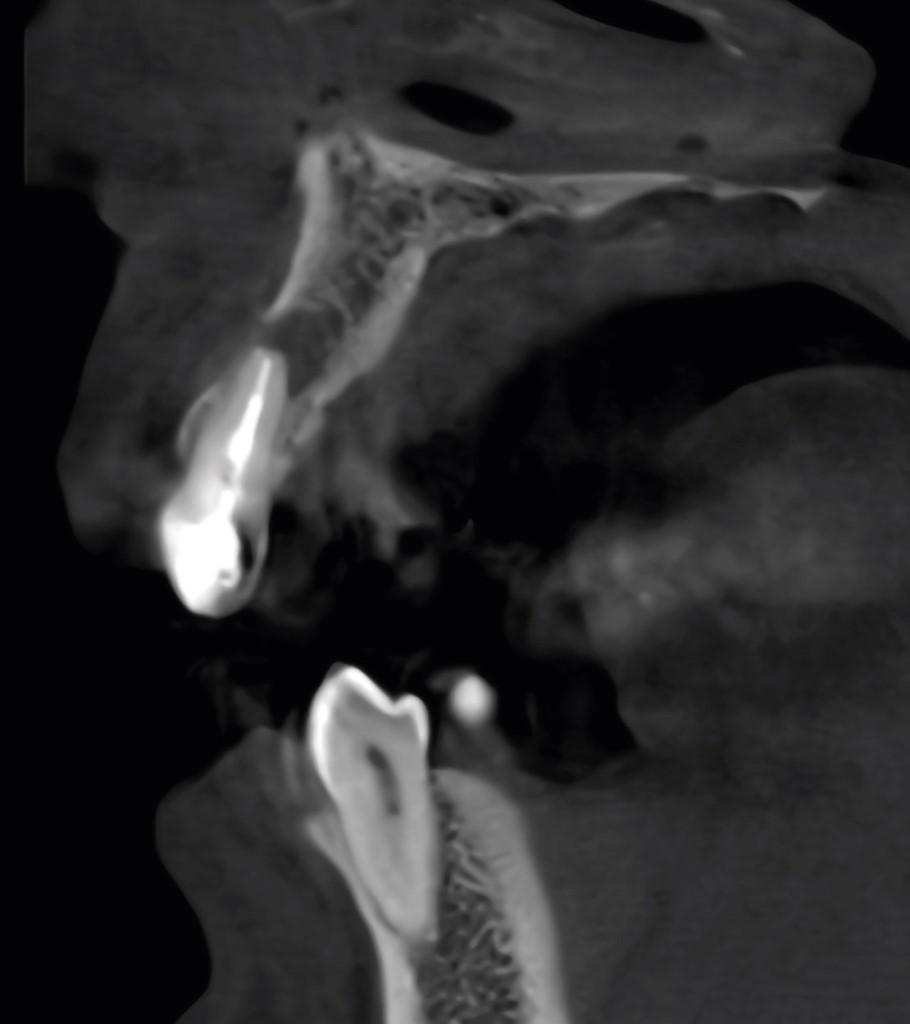
Фото 3d. Для проверки размера остеоэктомии использовали пародонтальный зонд.
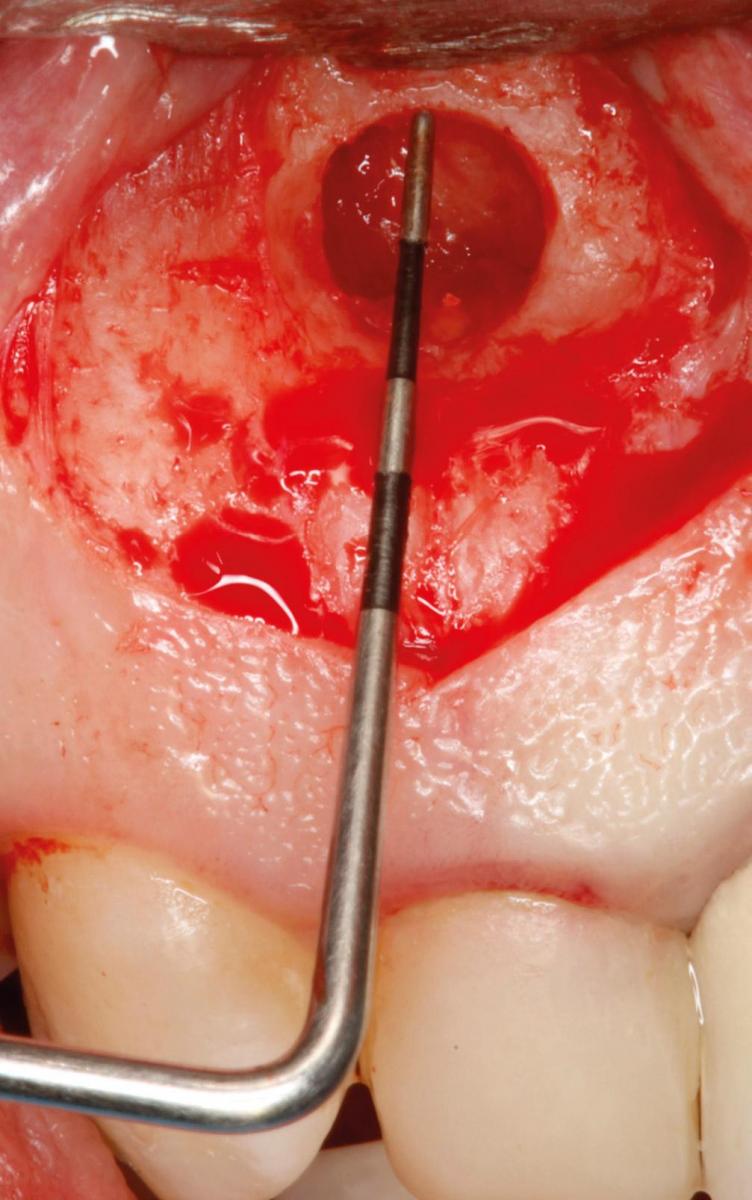
Фото 3e. Подготовка полости для ретроградного пломбирования с помощью ультразвукового наконечника.
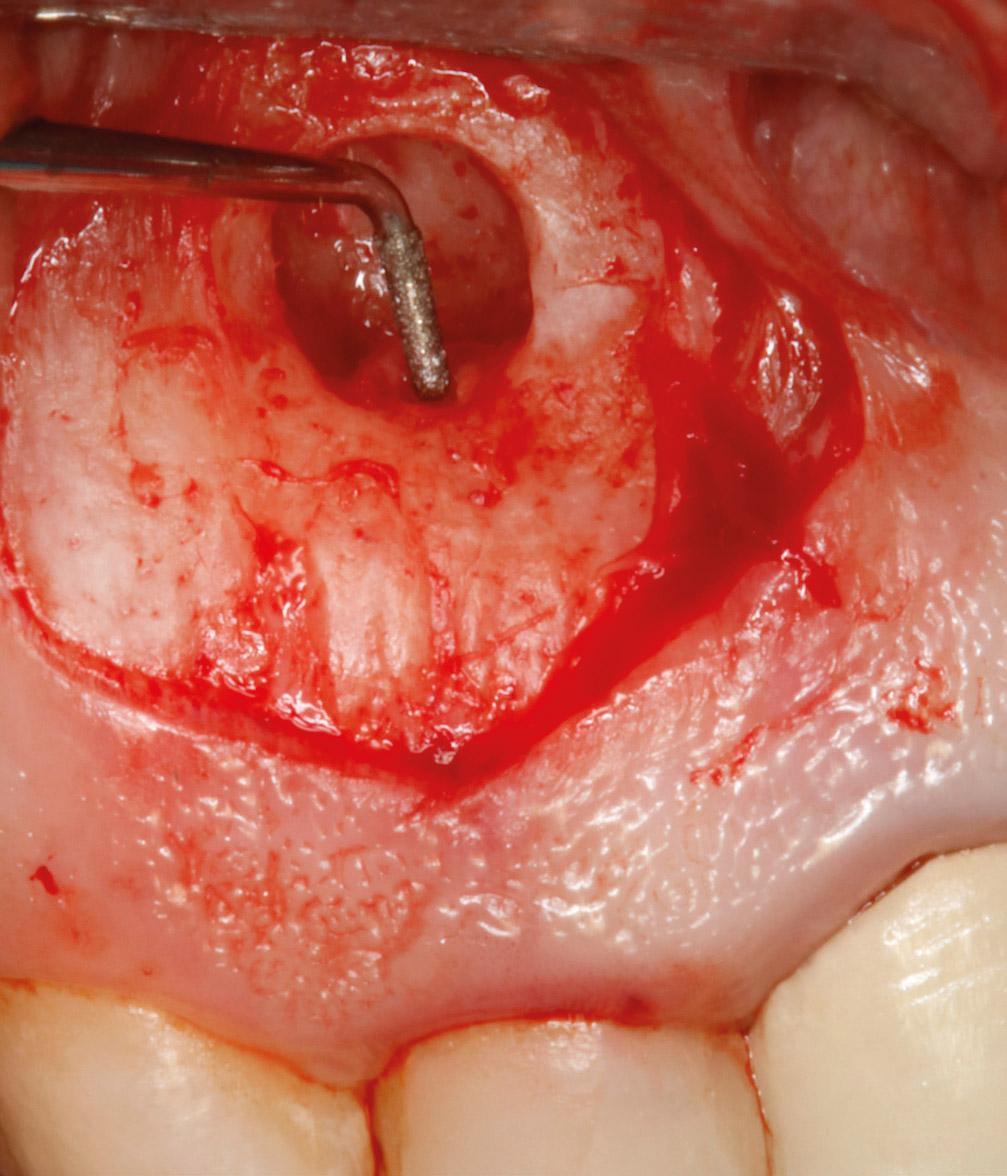
Фото 3f. Ретроградное пломбирование с применением МТА.
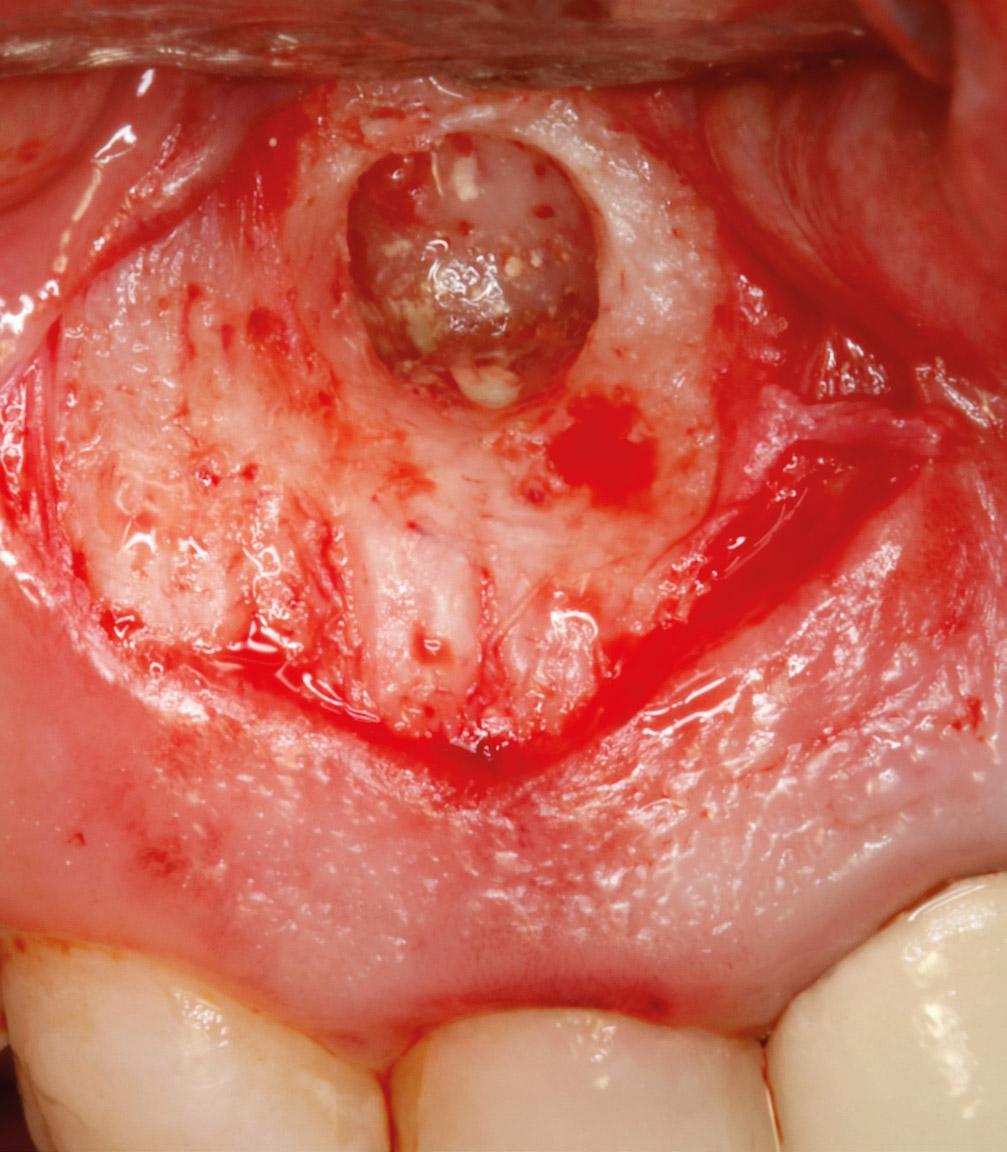
Фото 3g. Для выполнения костного дефекта использовали плазму крови, обогащенную тромбоцитами.
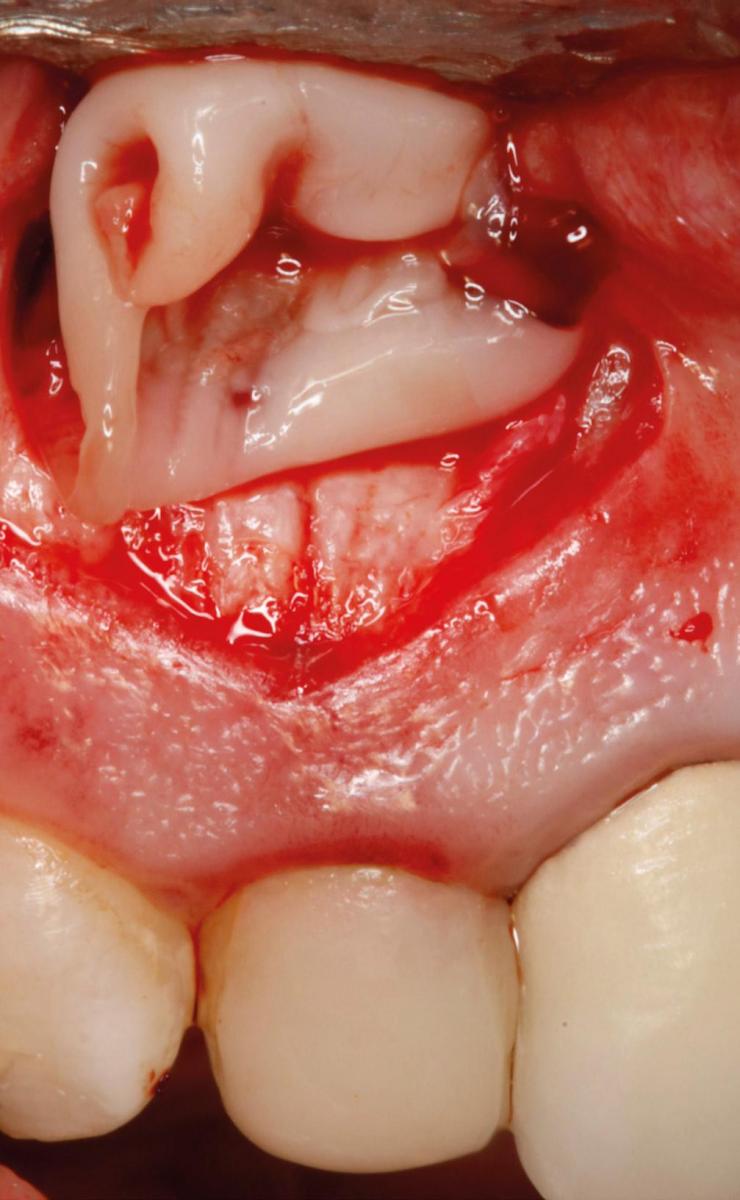
Фото 3h. Вид мягких тканей после ушивания.
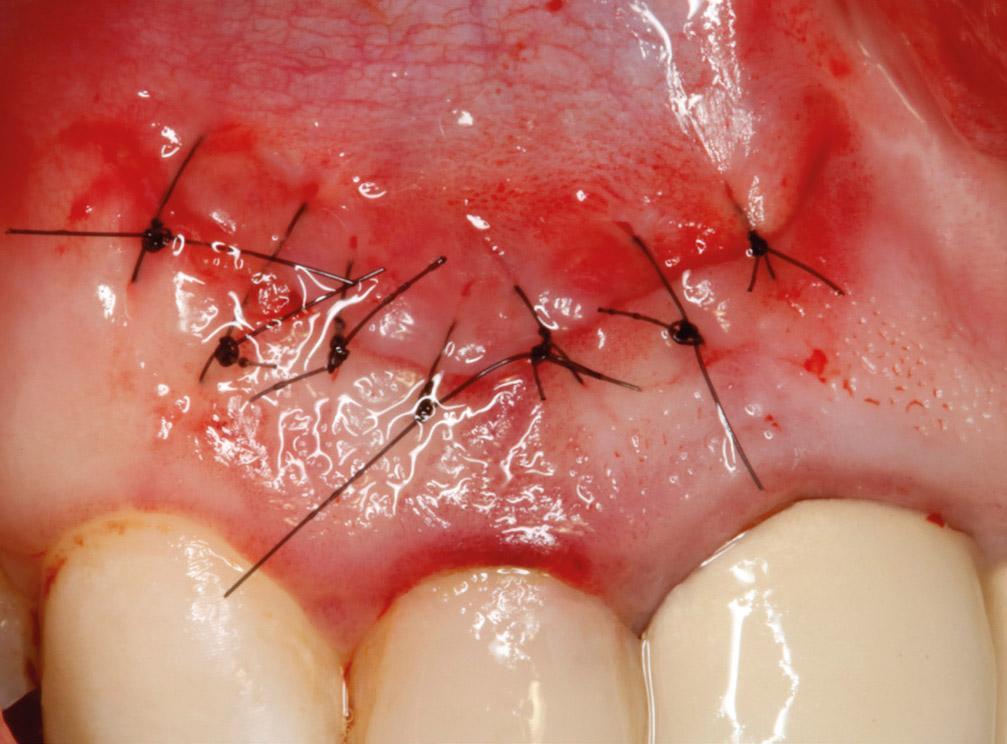
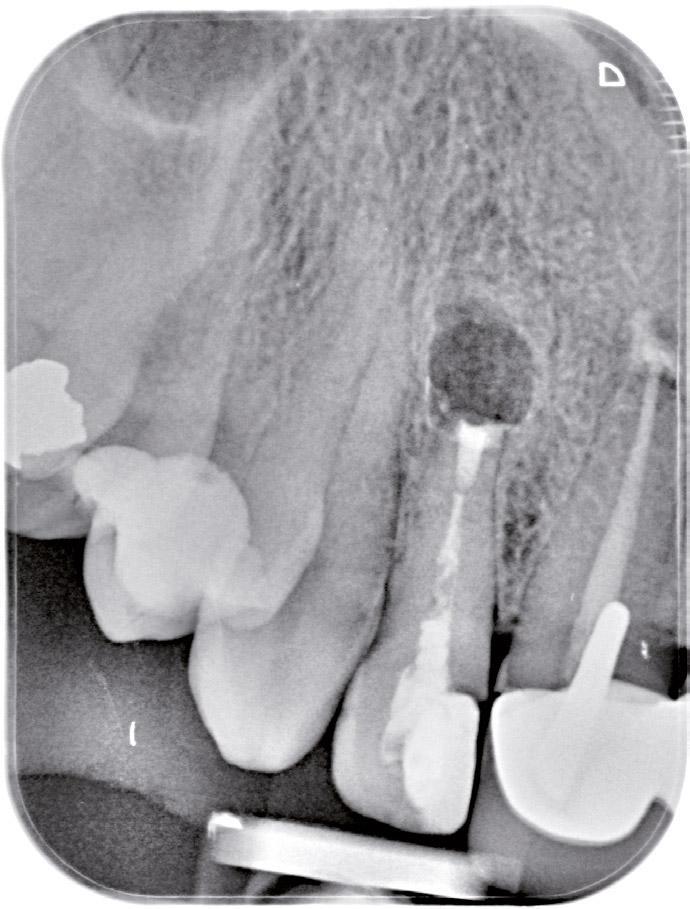
Фото 3i. Рентгенограмма после хирургического вмешательства.
Остеотомия является альтернативной хирургической манипуляцией, позволяющей сохранить целостность внешней кортикальной пластинки. Peñarrocha и Sanchis использовали технику так называемой оконной остеотомии, формирование доступа в процессе которой обеспечивали за счет полых цилиндрических трепанов разного диаметра. Остеотомия кортикальной пластинки начинается с применения трепана адекватного диаметра с сопутствующей адекватной ирригацией до достижения структуры губчатой кости. После формирования окна доступа применяют тонкое долото для поднятия костного блока. В ходе выполнения хирургического вмешательства костный блок содержат в физиологическом растворе и снова позиционируют его на место после очистки периапикального участка (фото 4). Согласно Abella, пьезохиругический подход обеспечивает лучшие условия для защиты мягких тканей, оптимальной визуализации рабочего поля, уменьшения кровопотери, редукции эффектов вибрации и шума и обеспечения лучшего комфорта для самого пациента (фото 5).
Фото 4а. Цилиндрический трепан использовался для перфорации костной ткани и обнажения периапикальной области.
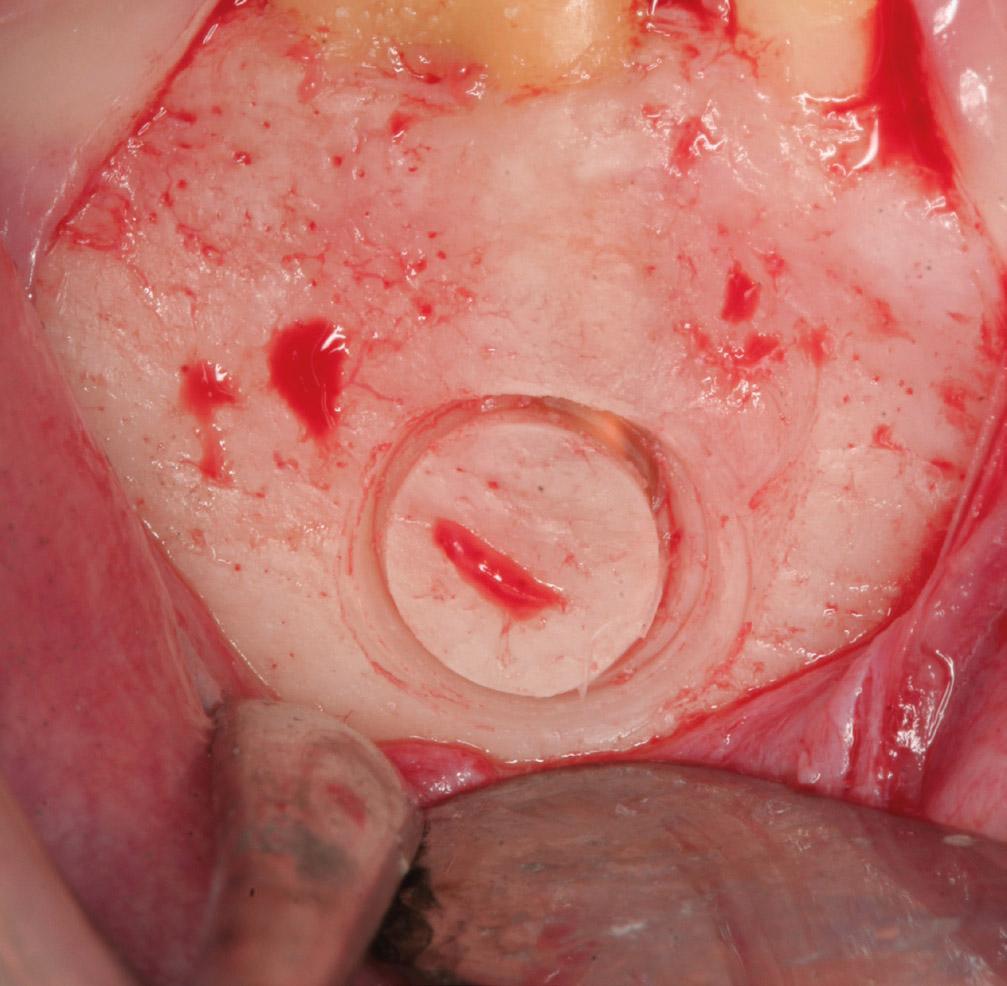
Фото 4b. Вид после пломбирования МТА.
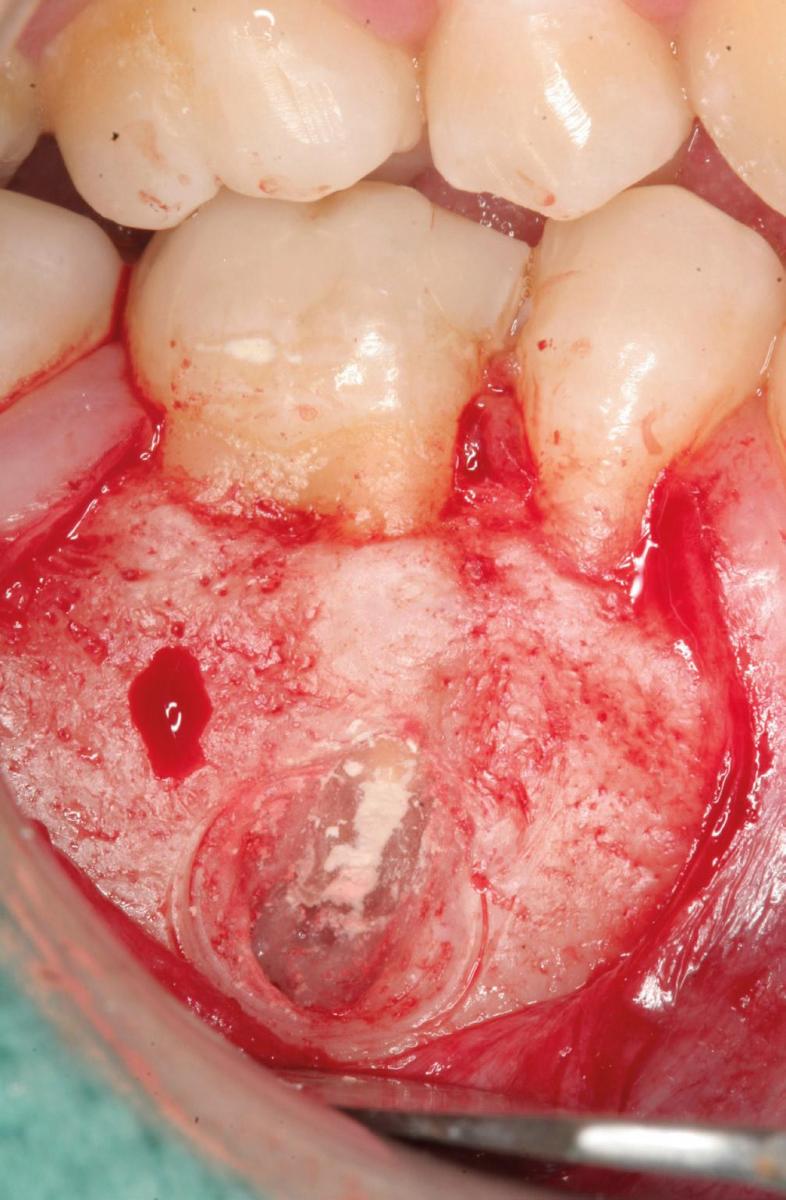
Фото 4c. Костный блок был установлен на место в конце операции.
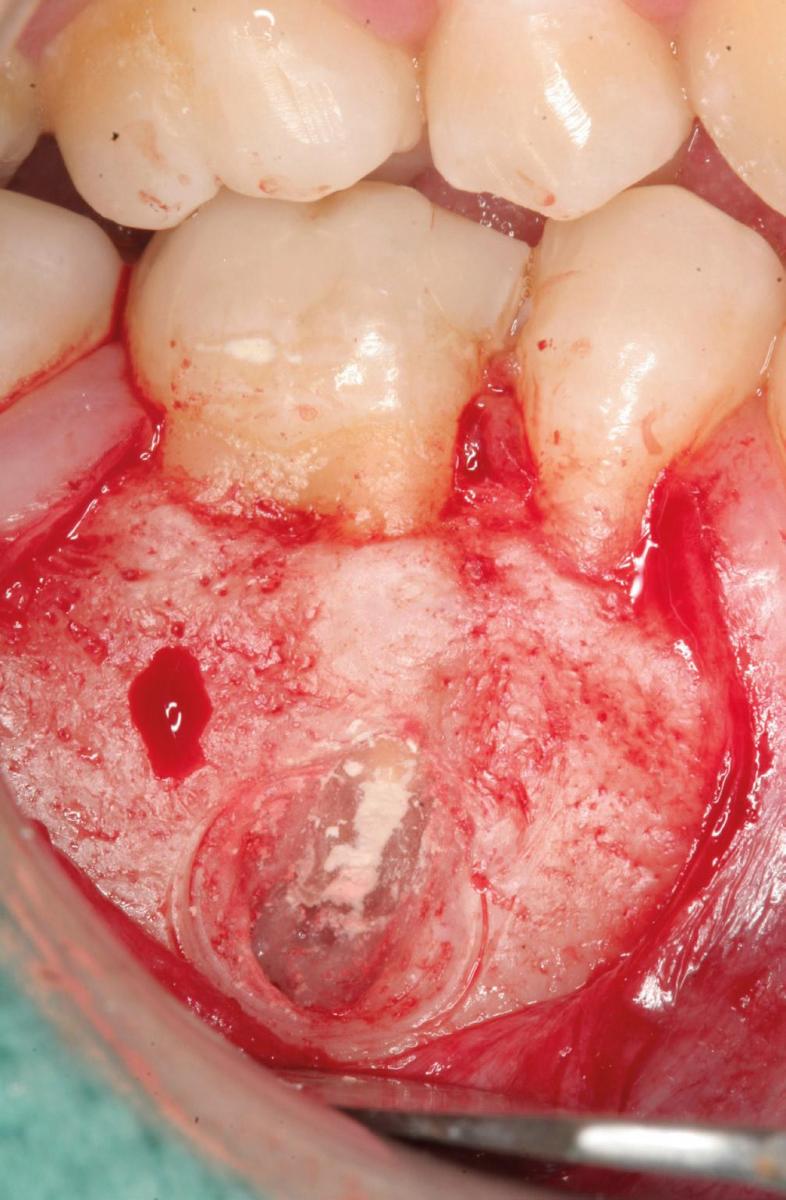
Фото 5a. Вид зуба нижней челюсти у пациента мужского пола с сильными болевыми ощущениями.
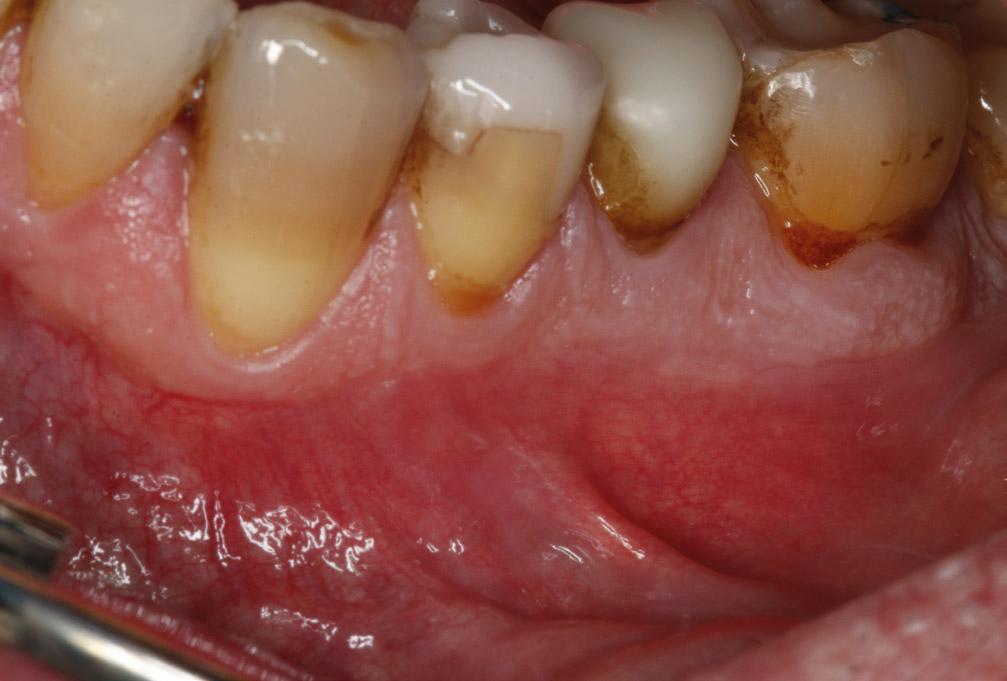
Фото 5b. На рентгенограмме было идентифицировано большое периапикальное поражение, связанное с первым премоляром, который ранее был эндодонтически пролечен, и вторым премоляром, который был восстановлен посредством штифта, но не демонстрировал рентгенологических признаков эндодонтического лечения.
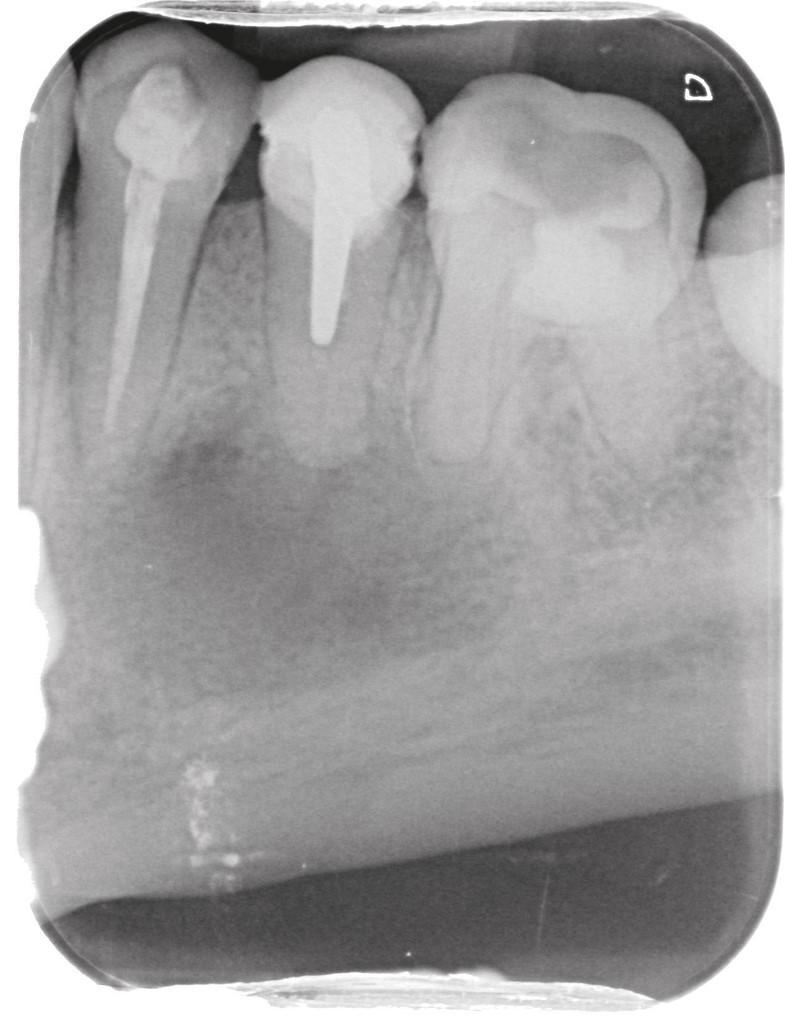
Фото. 5c, d. На КЛКТ-срезе было обнаружено близкое взаиморасположение периапикального поражения, нижнечелюстного канала и подбородочного отверстия.
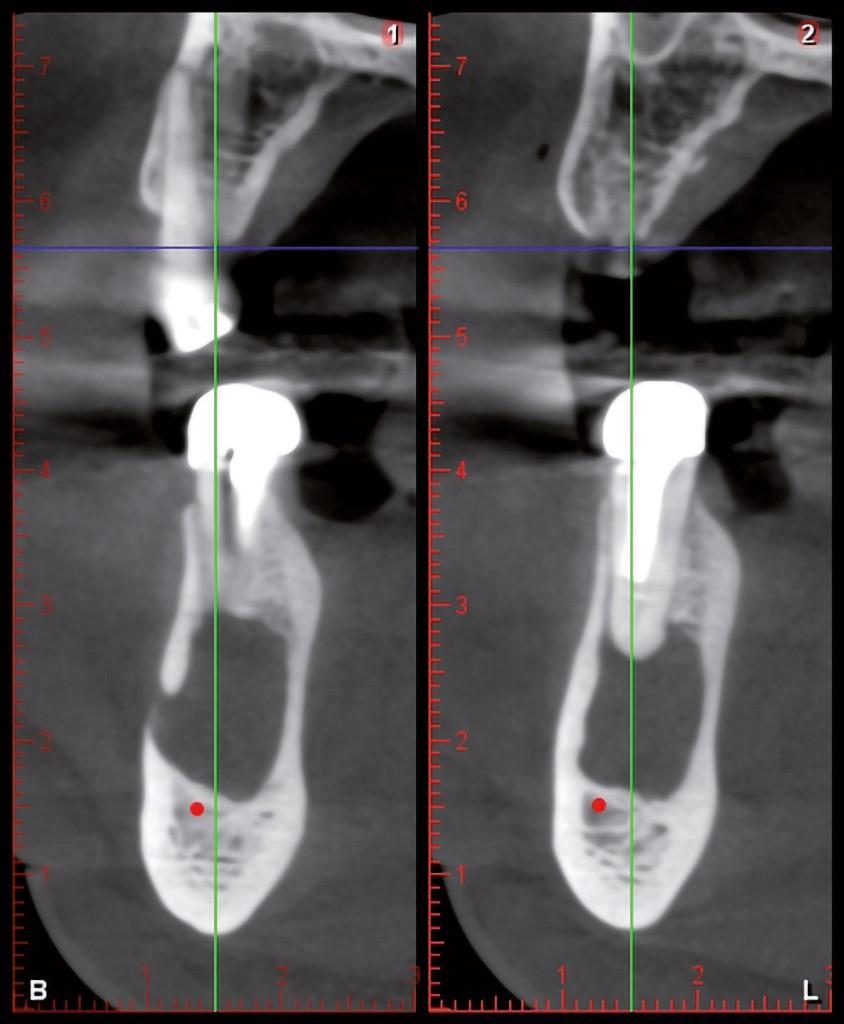
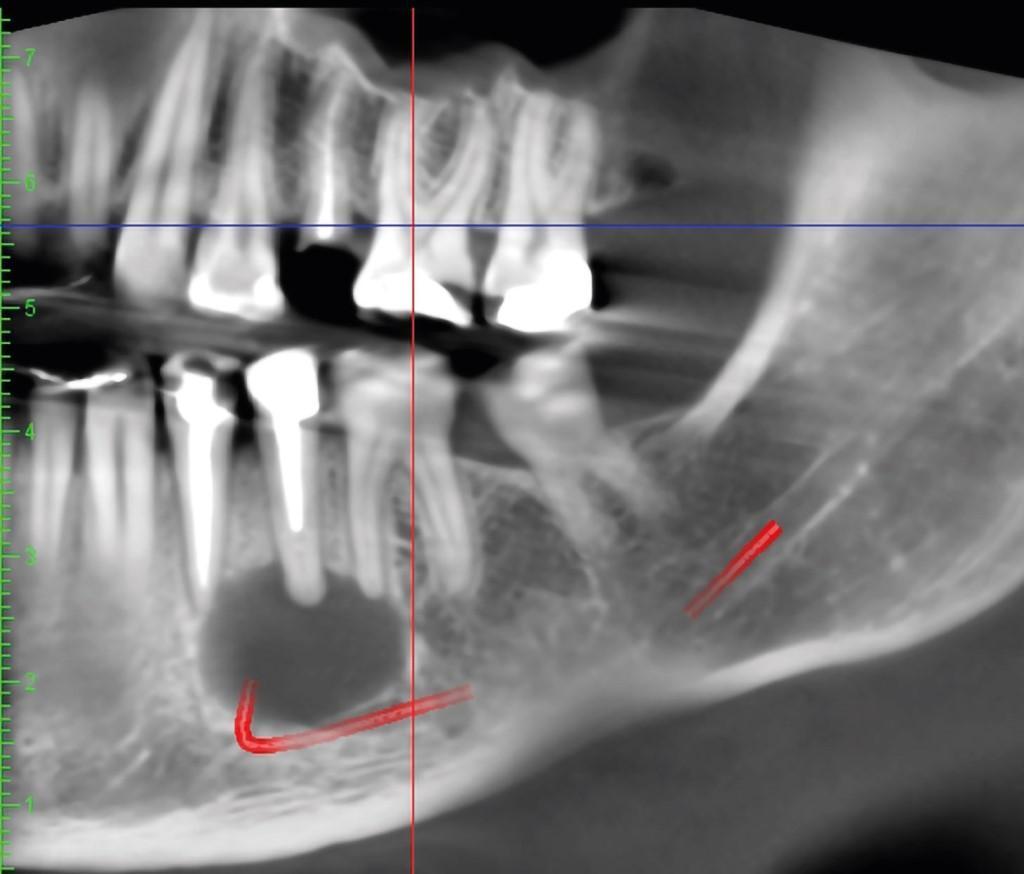
Фото 5e. Остеотомия была выполнена с помощью ультразвукового аппарата.
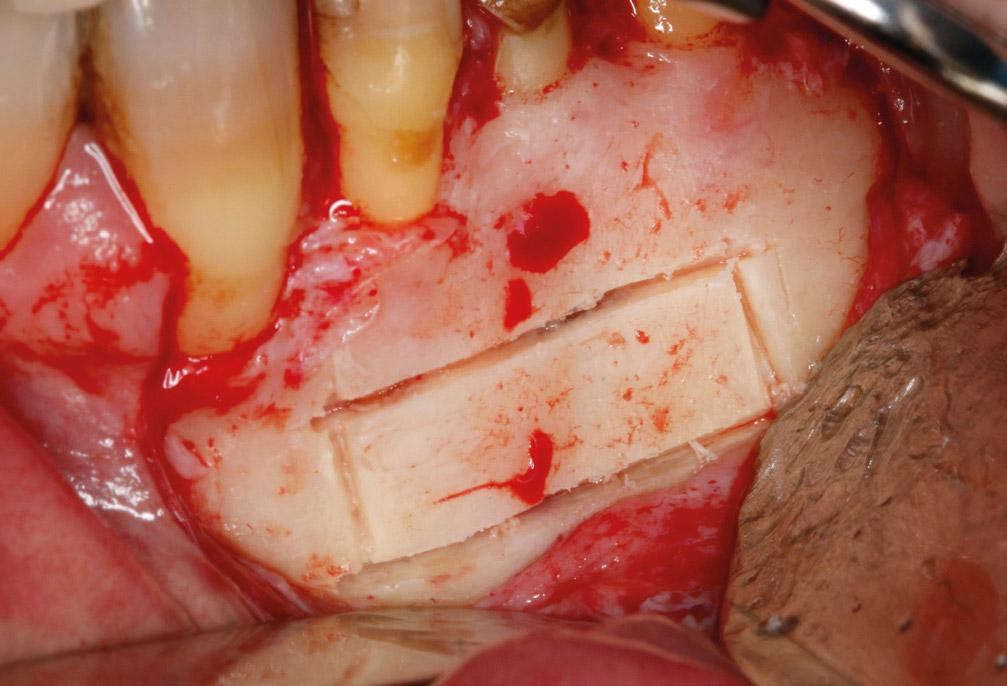
Фото 5f. Вид после удаления очага поражения и ретроградного пломбирования МТА.
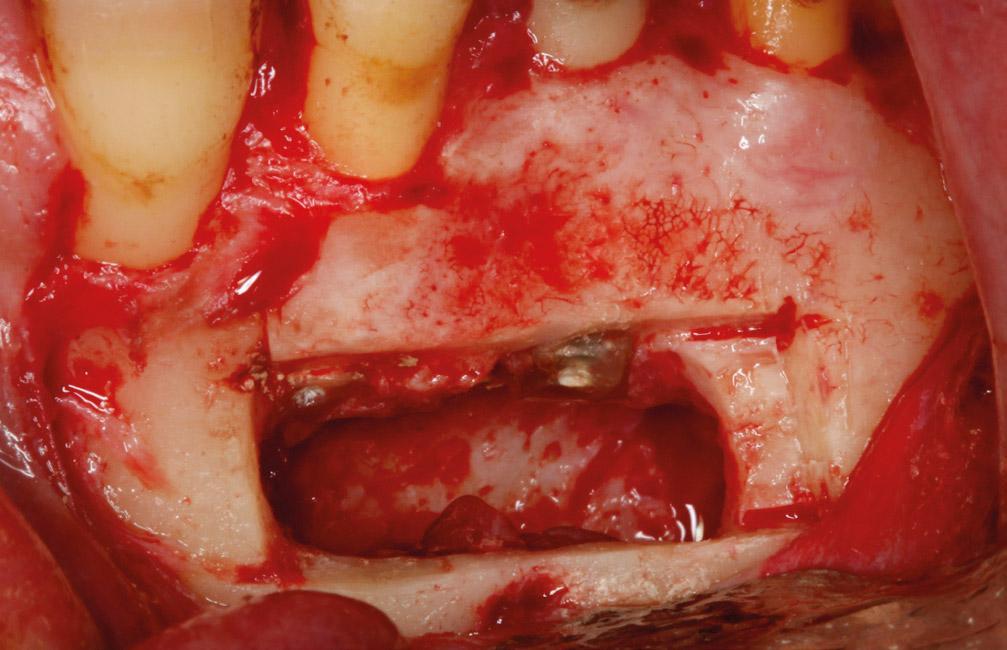
Фото 5g. Репозиционирование костного блока с помощью винта для остеосинтеза.
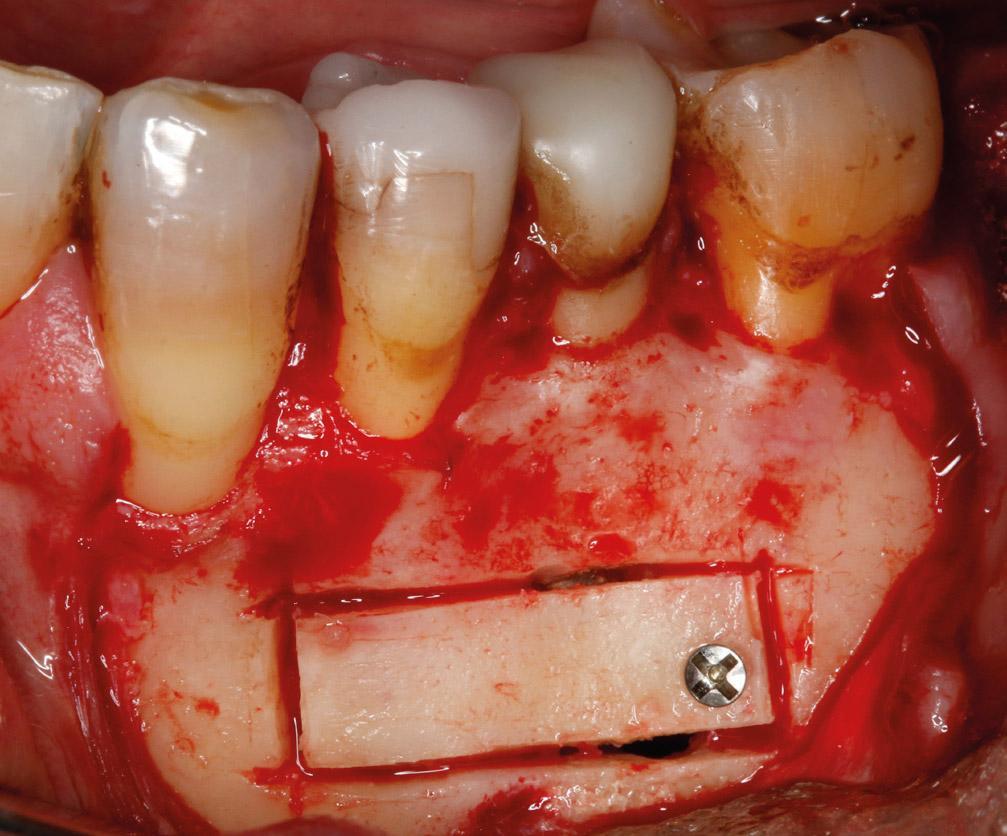
Фото 5h. Клинический вид мягких тканей через 1 год после операции.
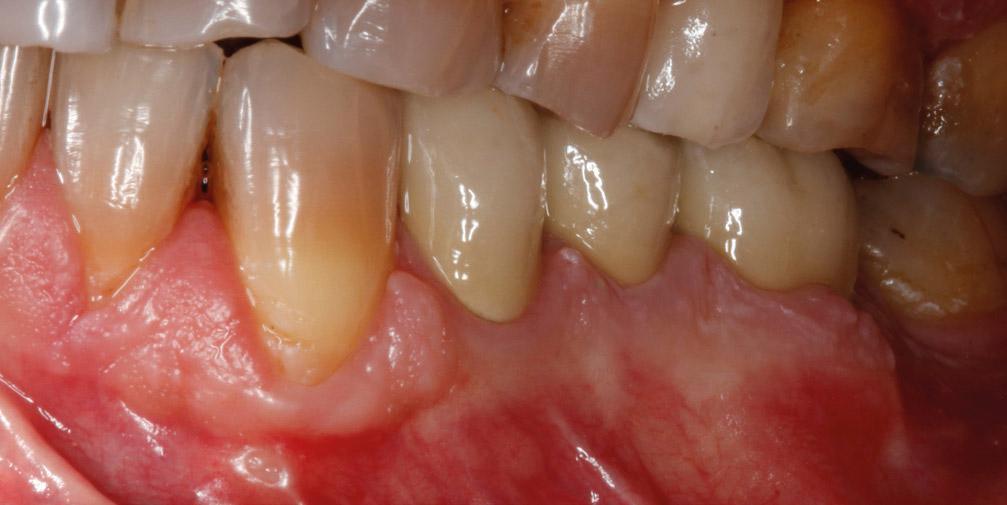
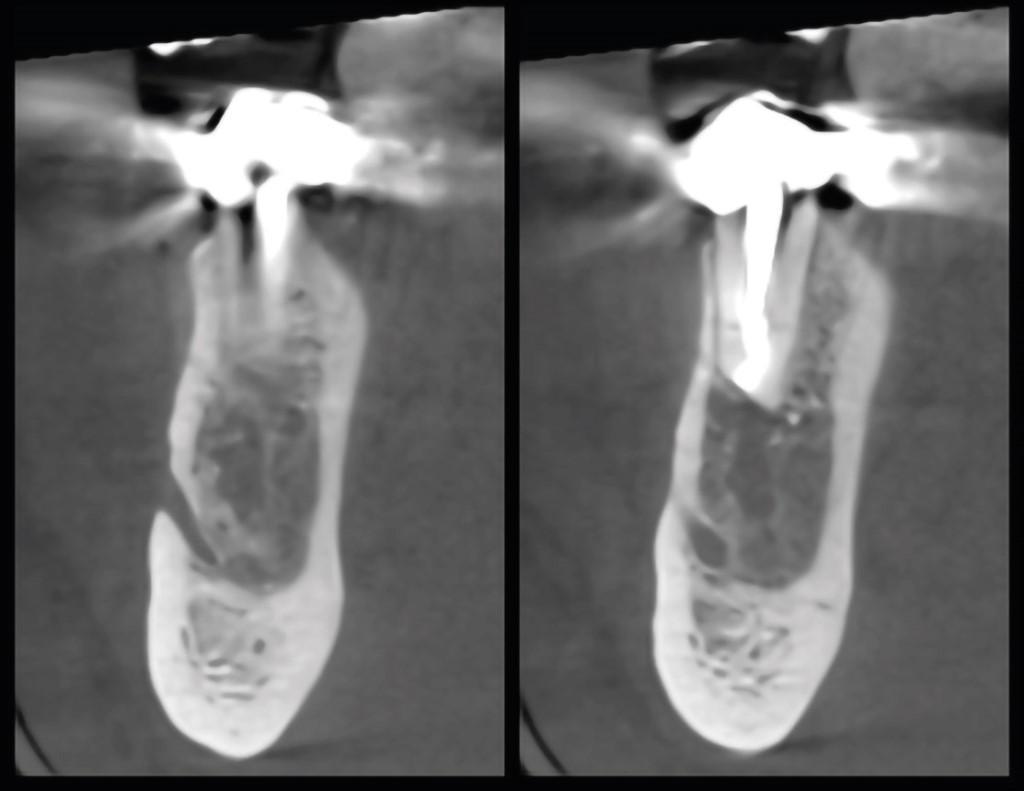
Фото 5i. Рентгенограмма, полученная через год после операции, демонстрирует регенерацию костной ткани.
García-Mira и коллеги не обнаружили никаких значительных различий в отношении постоперационных болевых ощущений и клинического прогноза при сравнении операций остеоэктомии и остеотомии. Однако у пациентов после остеоэктомии наблюдались более выраженные воспалительные реакции. Peñarrocha и Sanchis резюмировали преимущества остеотомии над остеоэктомией следующим образом:
1) возможности формирования более простого и быстрого доступа в топографически сложнодоступных участках по типу дистальных отделов нижней челюсти;
2) сохранение большего объема собственных костных тканей пациента, что способствует более быстрому заживлению. Имеющийся костный дефект кости может быть выполнен с помощью различных материалов (коллагеновой губкой или лиофилизированной бычьей тканью) перед финишным репозиционированием костного блока. Однако учитывая проведённый анализ литературы, можно резюмировать, что процедура остеотомии остается малоизученной. Основным осложнением при проведении остеотомии, особенно при использовании трепанов, остается возможность повреждения корней зубов при неучете их положения или выборе неправильного направления разреза.
Заключение
Остеоэктомия является ключевым этапом периапикальных хирургических вмешательств, позволяющим избавиться от патологического поражения в области верхушек корней зубов. С учетом возможностей микрохирургических техник лечения размер доступа для проведения остеоэктомии можно уменьшить до 5 мм, таким образом, способствуя более быстрому заживлению костной ткани в послеоперационной период. Остеотомия является альтернативной техникой хирургического лечения, которая позволяет сохранить целостность внешней кортикальной костной пластинки, однако данный метод вмешательства по имеющимся литературным данным до сих пор остается недостаточно изученным.
Авторы: Juan Cervera Ballester, Isabel Menendez Nieto, David Soto Penaloza, Maria Penarrocha Diago, David Penarrocha Oltra
Процедура периапикального хирургического вмешательства включает в себя три последовательных манипуляции: резекция верхушки корня, препарирование полости в области верхушки корня и ретроградную герметизацию. Для обеспечения успешности подобной процедуры необходимо обеспечить полное удаление патологических воспалительных тканей и максимальную очистку области верхушки корня.

В данной статье приведен анализ хирургических факторов, влияющих на эффективность процедуры остеоэктомии, и их связи с дальнейшим клиническим прогнозом.
Хирургическая техника вмешательства
Остеоэктомия предполагает удаление порции костной ткани с вестибулярной части альвеолярного гребня для формирования доступа к апексу зуба. Размер остеоэктомии определяет объем самого периапикального поражения, наличие соответствующего инструментария и близость области вмешательства к смежным анатомическим структурам (подбородочному нерву, каналу нижнечелюстного нерва и верхнечелюстному синусу). Логически, что лучше всего, если размер остеоэктомии является минимальным, однако в большинстве случаев его приходиться увеличивать для обеспечения оптимальных условий для работы кюретами и выполнения адекватного объема апикоэктомии. Остеоэктомию проводят круглыми твердосплавными борами (6-10 размера) при достаточной ирригации физиологическим раствором (фото 1).
Фото 1а. Ортопантомограмма пациента, который первично обратился за стоматологической помощью по поводу необходимости установки дентального имплантата. На снимке визуализируется периапикальное поражения левого премоляра нижней челюсти.

Фото 1b. Вид рабочего поля после сепарации лоскута. Важно обеспечить максимально аккуратную сепарацию лоскута, дабы избежать повреждения подбородочного нерва.

Фото 1c. Остеоэктомия выполняется с помощью твёрдосплавного бора с обильной ирригацией физиологическим раствором.

Фото 1d. Размер остеоэктомии должен составлять около 4 мм. Такой размер обеспечивает условия для свободной работы ультразвуковым наконечником.

Фото 1e. Ортопантомограмма пациента через 5 лет после лечения: признаки заживления костной ткани в области левого премоляра нижней челюсти.

Совсем недавно на рынке появился новый тип углового наконечника (45°), который обеспечивает подачу только воды без воздуха, таким образом, минимизируя риск развития эмфиземы. Доступ формируют в проекции 2-4 мм от апекса, а доступ выполняют перпендикулярно длинной оси зуба до момента достижения собственно тканей корня. После этого остеоэктомию заканчивают небольшими движениями бора для удаления костной ткани вокруг цемента корня. В области моляров нижней челюсти наружная костная пластинка характеризуется значительной плотностью, а сам доступ к апексу корней является топографически осложненным. Поэтому в таких случаях объем входного отверстия приходиться значительно увеличивать, для того чтобы обеспечить достаточный контроль области рабочего поля. В результате подобных вмешательств, конечно же, остаются огромные костные дефекты, которые после можно заполнить материалом костного заменителя, перекрыв его объем наиболее подходящей мембраной.
В 1961 году Boyne и соавторы изучили уровень деструкции вестибулярной костной пластинки после выполнения остеоэктомии и периапикального кюретажа. Они установили, что после незначительных ятрогенных костных дефектов размеров 5-8 мм наблюдается почти полная регенерация костной ткани, в то время как дефекты размером в 9-12 мм характеризуются замещением в большинстве случаев соединительной тканью. Десять лет спустя Hjorting-Hansen и Andreasen изучали постостеоэктомичесике дефекты размером 5, 6 и 8 мм, сформированные через вестибулярную или язычную костную пластинку на нижней челюсти у собак. Авторы обнаружили, что паттерн заживления костной ткани зависит от размера полости и факта повреждения одновременно одной или двух кортикальных пластинок.
Rubinstein и Kim также установили, что существует прямая связь между заживлением костной ткани и размером остеоэктомии: небольшие дефекты в 0-5 мм восстанавливаются на протяжении в среднем 6,40 месяцев, в то время как для заживления дефектов среднего размера 6-10 мм требуется уже 7,25 месяцев, а для заживления дефектов размером более 10 мм – уже 11 месяцев. Учитывая этот факт, в случаях необходимости проведения остеоэктомии в области двух корней нижнего моляра, которые разделены интактной костной перегородкой без наличия воспалительного инфильтрата, можно провести две отдельные остеоэктомии в области каждого из корней, не соединяя их между собой. Таким образом, размер послеоперационных дефектов будет значительно меньше, а общее время заживления удастся заметно сократить (фото 2).
Фото 2а. Для формирования доступа к моляру нижней челюсти был сепарирован трапециевидный лоскут.

Фото 2b. Два отдельных участка остеоэктомии для формирования доступа к мезиальному и дистальному корням.

Фото 2с. Ретроградное пломбирование посредством МТА.

Фото 2d. Периапикальная рентгенограмма через год после лечения.

Фото 2e. КЛКТ-срез, который демонстрирует качество ретроградного пломбирования и заживления костной ткани в периапикальной области.

Микрохирургические техники оперативных вмешательств еще в большей мере позволяют уменьшить размер остеоэктомии до 4 мм в диаметре. Такой диаметр несколько больше длины ультразвуковой насадки в 3 мм, что обеспечивает достаточные условия для ее манипуляции в структуре костной полости (фото 3).
Фото 3a. Вид переднего зуба верхней челюсти со здоровым состоянием мягких тканей. Пациент обратился за помощью по поводу спонтанных болевых ощущений, возникших в данном участке.

Фото 3b. На рентгенограмме визуализируется область периапикального поражения бокового резца, который ранее уже был эндодонтически пролечен.

Фото 3c. КЛКТ-срез демонстрирует признаки апикального поражения, распространяющегося и на кортикальную пластинку в области бокового резца верхней челюсти.

Фото 3d. Для проверки размера остеоэктомии использовали пародонтальный зонд.

Фото 3e. Подготовка полости для ретроградного пломбирования с помощью ультразвукового наконечника.

Фото 3f. Ретроградное пломбирование с применением МТА.

Фото 3g. Для выполнения костного дефекта использовали плазму крови, обогащенную тромбоцитами.

Фото 3h. Вид мягких тканей после ушивания.

Фото 3i. Рентгенограмма после хирургического вмешательства.

Остеотомия является альтернативной хирургической манипуляцией, позволяющей сохранить целостность внешней кортикальной пластинки. Peñarrocha и Sanchis использовали технику так называемой оконной остеотомии, формирование доступа в процессе которой обеспечивали за счет полых цилиндрических трепанов разного диаметра. Остеотомия кортикальной пластинки начинается с применения трепана адекватного диаметра с сопутствующей адекватной ирригацией до достижения структуры губчатой кости. После формирования окна доступа применяют тонкое долото для поднятия костного блока. В ходе выполнения хирургического вмешательства костный блок содержат в физиологическом растворе и снова позиционируют его на место после очистки периапикального участка (фото 4). Согласно Abella, пьезохиругический подход обеспечивает лучшие условия для защиты мягких тканей, оптимальной визуализации рабочего поля, уменьшения кровопотери, редукции эффектов вибрации и шума и обеспечения лучшего комфорта для самого пациента (фото 5).
Фото 4а. Цилиндрический трепан использовался для перфорации костной ткани и обнажения периапикальной области.

Фото 4b. Вид после пломбирования МТА.

Фото 4c. Костный блок был установлен на место в конце операции.

Фото 5a. Вид зуба нижней челюсти у пациента мужского пола с сильными болевыми ощущениями.

Фото 5b. На рентгенограмме было идентифицировано большое периапикальное поражение, связанное с первым премоляром, который ранее был эндодонтически пролечен, и вторым премоляром, который был восстановлен посредством штифта, но не демонстрировал рентгенологических признаков эндодонтического лечения.

Фото. 5c, d. На КЛКТ-срезе было обнаружено близкое взаиморасположение периапикального поражения, нижнечелюстного канала и подбородочного отверстия.


Фото 5e. Остеотомия была выполнена с помощью ультразвукового аппарата.

Фото 5f. Вид после удаления очага поражения и ретроградного пломбирования МТА.

Фото 5g. Репозиционирование костного блока с помощью винта для остеосинтеза.

Фото 5h. Клинический вид мягких тканей через 1 год после операции.

Фото 5i. Рентгенограмма, полученная через год после операции, демонстрирует регенерацию костной ткани.

García-Mira и коллеги не обнаружили никаких значительных различий в отношении постоперационных болевых ощущений и клинического прогноза при сравнении операций остеоэктомии и остеотомии. Однако у пациентов после остеоэктомии наблюдались более выраженные воспалительные реакции. Peñarrocha и Sanchis резюмировали преимущества остеотомии над остеоэктомией следующим образом:
1) возможности формирования более простого и быстрого доступа в топографически сложнодоступных участках по типу дистальных отделов нижней челюсти;
2) сохранение большего объема собственных костных тканей пациента, что способствует более быстрому заживлению. Имеющийся костный дефект кости может быть выполнен с помощью различных материалов (коллагеновой губкой или лиофилизированной бычьей тканью) перед финишным репозиционированием костного блока. Однако учитывая проведённый анализ литературы, можно резюмировать, что процедура остеотомии остается малоизученной. Основным осложнением при проведении остеотомии, особенно при использовании трепанов, остается возможность повреждения корней зубов при неучете их положения или выборе неправильного направления разреза.
Заключение
Остеоэктомия является ключевым этапом периапикальных хирургических вмешательств, позволяющим избавиться от патологического поражения в области верхушек корней зубов. С учетом возможностей микрохирургических техник лечения размер доступа для проведения остеоэктомии можно уменьшить до 5 мм, таким образом, способствуя более быстрому заживлению костной ткани в послеоперационной период. Остеотомия является альтернативной техникой хирургического лечения, которая позволяет сохранить целостность внешней кортикальной костной пластинки, однако данный метод вмешательства по имеющимся литературным данным до сих пор остается недостаточно изученным.
Авторы: Juan Cervera Ballester, Isabel Menendez Nieto, David Soto Penaloza, Maria Penarrocha Diago, David Penarrocha Oltra
































































































































































0 комментариев