В ходе лечения корневых каналов существует риск развития такого осложнения, как перфорация, которая непосредственно влияет на дальнейший прогноз ятрогенного вмешательства.
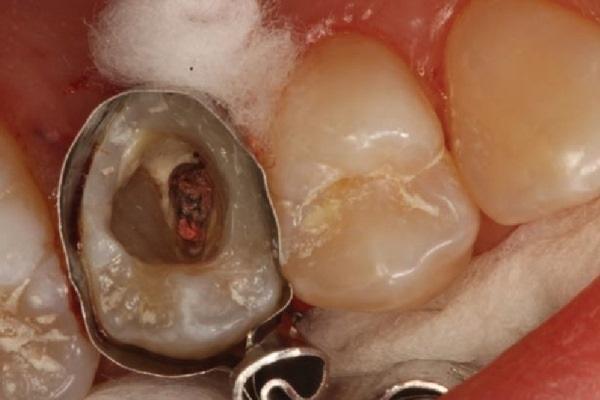
Прогноз функционирования зуба после перфорации зависит от ряда определяющих факторов:
- Тяжесть исходного поражения тканей пародонта
- Расположение и размер перфорации
- Бактериальная контаминация
- Герметизирующая способность или цитотоксичность материалов, используемых для закрытия сформировавшегося дефекта.
Даже если для лечения перфорации используется биосовместимый материал, обширная травма низлежащих тканей может привести к необратимому повреждению биологического прикрепления в области фуркации. В случаях больших перфораций полное закрытие дефекта является проблематичным, учитывая условия развития персистирующего воспаления и возможность прорастания в перфорацию бороздкового эпителия. Sinai (1977) заявил, что перфорации, расположенные в коронковой части корня, являются более проблематичными, чем те, которые формируются в срединной или апикальной трети корня. Цель данной статьи состоит в том, чтобы систематизировать и проанализировать имеющиеся научные данные относительно наиболее подходящих и эффективных методов лечения перфораций, локализированных в области фуркации.
Методы
Поиск литературы
Для первичного анализа были отобраны научные статьи из базы данных Medline, опубликованные в период с 2002 по 2015 год. Поиск данных публикаций проводился по ключевым словам «перфорации и эндодонтия», «перфорация фуркации», «корневые каналы и перфорации» и «минерал триоксид агрегат (MTA)». Дальше проводился анализ списков литературы, указанных в отобранных статьях, для определения необходимости поиска дополнительных научных источников.
Результаты
Всего было найдено 820 статей, которые были систематизированы по наборам ключевых слов: перфорация и эндодонтия – 285; перфорация фуркации – 92; корневой канал и перфорация – 299; и перфорация и минерал триоксид агрегат (MTA) – 144.
Методы закрытия перфораций и прогноз лечения
Для восстановления тканей пародонта в области сформировавшейся перфорации могут использоваться как хирургические, так и нехирургические методы лечения. При выборе одного из этих подходов следует учитывать два фактора:
- Выбор соответствующего материала
- Использование матрицы.
Выбор материала для закрытия перфорации проводится с учетом следующих критериев:
- Доступность области перфорации
- Биосовместимость (материал должен быть нетоксичным и неканцерогенным)
- Способность индуцировать процессы остеогенеза и цементогенеза
- Уровень контроля влажности
- Простота в использовании
- Эстетические соображения.
Использование матрицы
Ключевыми аспектами, определяющими успешность восстановления участка перфорации, являются контроль гемостаза и установка материала для закрытия дефекта так, чтобы он не пенетрировал в окружающие пародонтальные структуры. Контроль гемостаза является крайне важным условием для обеспечения герметичности закрытия перфорации в области фуркации. Отсроченное восстановление перфорации может привести к вытеснению слоя материала из проекции дефекта за счет разрушения низлежащих структур пародонта и их замещения грануляционной тканью. Дабы избежать подобного эффекта могут использоваться так называемые внутренние матрицы из таких материалов, как сульфат кальция, гидроксиапатит, коллаген, деминерализованная лиофилизированная кость и Gelfoam. Концепция внутренней матрицы впервые была введена Lemon (1992) для адекватного уплотнения области перфорации фуркации и предотвращения экструзии материала. Он также рекомендовал использовать гидроксиапатит в качестве матрицы под амальгамой. Сульфат кальция и гидроксид кальция также позволяют предотвратить экструзию композита, если таковой применяется в качестве материала для восстановления дефекта в участке фуркации.
В 1999 году Jantarat и коллеги продемонстрировали, что применение гипса Paris в качестве матрицы под амальгаму при восстановлении перфорации фуркации позволяет улучшить герметизирующие свойства последней. Применение хапсета (состоящий из 65% нерезорбируемого гидроксиапатита и 35% Paris-гипса) и гидроксиапатита продемонстрировало аналогичные реакции заживления при использовании их в качестве внутренних матриц под амальгамой (Rafter et al, 2002). Rafter и коллеги (2002) также сообщили, что отсутствие внутренней матрицы под амальгамой провоцировало выдавливание последней в нижележащую костную ткань, что, очевидно, было ассоциировано с тяжелой воспалительной реакцией биологических структур. Однако, применение МТА даже без внутренней матрицы характеризовалось достижением оптимальной прочности и превосходной герметичности данного материала в присутствии влаги. В 2004 году Kratchman рекомендовал пропитывать место перфорации гипохлоритом натрия после достижения гемостаза, и в случаях закрытия дефекта с помощью МТА все же нужно фиксировать какой-то физический барьер по типу коллагена или сульфата кальция.
Согласно Bargholz (2005), отличные клинические результаты были достигнуты при использовании коллагенового матрикса в качестве внутренней матрицы под МТА. Исследование Al-Daafas и Al-Nazhan (2007) показало, что сульфат кальция также позволял предотвратить экструзию восстановительного материала. При этом однако была обнаружена неблагоприятная воспалительная реакция, а именно - миграция эпителиальной ткани в область дефекта и невозможность дальнейшей регенерации низлежащеий кости. Таким образом, авторы пришли к выводу, что использование сульфата кальция в качестве внутренней матрицы под МТА все же не рекомендуется. При использовании в качестве внутреннего матрикса сульфата кальция и Collaplug (Calcitek, Carlsbad, CA) не было отмечено улучшений герметизирующих характеристик МТА, более того, эти материалы не снижали частоту возникновения случаев экструзии MTA в пародонтальные структуры. Поэтому авторы пришли к выводу, что эти два аналога также не стоит рекомендовать для применения в качестве внутренних матриц для MTA (Zou et al, 2008).
Материалы, используемые для восстановления участков перфораций в области фуркаций
В попытке восстановить перфорацию в области фуркации врачи пробовали использовать такие материалы, как амальгама, трикальцийфосфат (TCP), гидроксиапатит, гуттаперчу, гидроксид кальция, цинкооксидэвгенольный цемент, стеклоиономерный цемент, композитные аналоги, гибридные компомеры, деминерализованную лиофилизированную костную ткань, а также МТА. Тем не менее, ни один из этих материалов полностью не соответствует всем необходимым техническим и биологическим требованиям.
Balla и коллеги (1991) сообщили, что область дефекта перфорации повторно не замещалась твердыми тканями в случаях закрытия дефекта трикальций фосфатом, гидроксиапатитом, амальгамой или гидроксидом кальция (Life); вместо этого участок дефекта восполнялся эпителием и воспалительными клетками.
MTA является цементом, работающим на водной основе, полученным из портландцемента (тип I), который начали использовать в качестве эндодонтического материала в начале 1990-х годов. В результате полученных клинических материалов, было установлено, что данный цемент подходит для разных клинических ситуаций, в том числе и для перекрытия витальной пульпы, восстановления перфораций в области фуркации, а также для обтурации участка верхушки корня. При этом MTA способствует регенерации перирадикулярных тканей и отличается от других аналогов своей способностью стимулировать регенерацию цемента, таким образом, способствуя регенерации всего пародонтального комплекса. Природа его биосовместимости подтверждается способностью материала образовывать гидроксиапатит при взаимодействии с жидкостями организма человека.
На данный момент доступны две коммерческие формы MTA: Proroot MTA (Dentsply Tulsa Dental), который представлен в серой или белой форме (последняя содержит меньшее количество железа) и MTA-Angelus (Angelus). MTA-Angelus был разработан для того, чтобы решить проблему длительного времени отверждения Proroot MTA, таким образом, удалось сократить длительность данной фазы до 10 минут. MTA-Angelus содержит 80% портландцемента и 20% оксида висмута без добавок сульфата кальция, в то время как Proroot MTA состоит из 75% портландцемента, 20% оксида висмута и 5% дегидрата сульфата кальция. Сам же портландцемент содержит множество неорганических составляющих, среди которых силикат дикальция, силикат трикальция, алюминат трикальция, железоалюминат тетракальция и обезвоженный сульфат кальция. Единственным существенным различием между составами белого и серого МТА и ассоциированных с ними портландцементами является присутствие оксида висмута в структуре МТА.
Сообщалось, что герметизирующая способность MTA (Университет Лома Линда, Калифорния) является значительно лучше по сравнению с амальгамой для профилактики подтекания Fusobacterium nucleatum через перфорации в области фуркации. Результаты исследований указывают на то, что применение Proroot MTA с или без внутренней матрицы и MTA-Angelus с внутренней матрицей характеризуется наименьшим уровнем абсорбции красителя по сравнению с цинкоксидэвгенольным цементом, применяемым с или без внутренней матрицы, а также по сравнению с MTA-Angelus, используемым без внутренней матрицы. Кроме того, авторы сообщили, что IRM без внутренней матрицы имеет самую высокую поглощающую способность красителя (Hashem, Hassanien, 2008). Тем не менее, белый и серый MTA (Dentsply Tulsa Dental) практически не отличались в параметрах микроплотности при использовании с целью восстановления перфораций в области фуркации.
В одном из исследований изучали результаты закрытия перфораций с помощью Proroot grey MTA (Dentsply) и Geristore (Denmat). Geristore используется в качестве материала для пломбировки корневых каналов и восстановления дефектов зубов в поддесневой области, таких как кариес поверхности корня и ятрогенные перфорации, а также в качестве аддитивного материала в ходе процедуры направленной регенерации тканей (GTR). Geristore характеризуется лучшей уплотнительной способностью по сравнению с амальгамой. В ходе исследования авторы установили, что герметизирующие способности MTA и Geristore снижаются при использовании в качестве внутренней матрицы под ними разных вариантов биостекла.
Sluyk, Moon and Hartwell (1998) оценивали влияние времени и влажности на параметры отверждения, ретенции и адаптации MTA при его использовании с целью восстановления перфораций в области фуркации. Результаты показали, что адаптация МТА к перфорации стенок усиливается при наличии влаги. Они также предположили, что увлажненная матрица может оказаться эффективной при закрытии перфорации МТА с целью предотвращения неполного закрытия дефекта или экструзии материала в пародонт. Кроме того, Main et al (2004) также сообщили, что МТА эффективно работает и при закрытии обычных перфораций корня.
Yildirim и др. (2005) исследовали гистологический ответ на MTA и Super EBA (Bosworth Company) при использовании их с целью восстановления перфораций фуркаций у собак. При применении МТА наблюдали менее выраженный уровень воспаления и признаки образования нового цемента, в то время как закрытие перфорации Super EBA провоцировало восстановление области дефекта соединительной ткани без признаков воспаления. Аналогичные гистологические результаты наблюдались и при закрытии перфораций фуркаций такими материала как портландцемент и MTA. Результаты исследования применения МТА и трикальций фосфата с целью заполнения дефекта в области фуркаций не продемонстрировали существенных различий между материалами в плане реорганизации костной ткани или депозиции фиброзной соединительной ткани.
Таким образом, MTA считается золотым стандартом и материалом выбора для восстановления перфораций в области фуркации, который демонстрирует успешные клинические результаты. Однако у него есть и некоторые недостатки, как, например, неспособность к деградации с целью замещения естественными тканями, низкая устойчивость к сжатию в течение длительного времени, длительное время отверждения, манипуляционные сложности в работе и внесении в дефектную область. Кроме того, цемент требует наличия дополнительной влаги для его адекватного отверждения.
В литературе неоднократно сообщалось, что многие стоматологические материалы демонстрируют цитотоксические эффекты во время отверждения. В лабораторных условиях было установлено, что свежеприготовленный МТА (pH = 10,2) характеризуется гораздо меньшим уровнем миграции к его поверхности воспалительных клеток по сравнению с уже полностью отвердевшим МТА (pH = 12,5). Однако, даже при таком условии, гистологически не наблюдалось различий в регенерации костной ткани и цемента после выполнения периапикального хирургического вмешательства у собак при выполнении дефекта свежеприготовленным и предварительно отвердевшим формами Proroot MTA.
В 2006 году Asgary и коллеги представили новый цемент для применения в эндодонтии, который представлял собой кальций-обогащенный материал (CEM). Основными компонентами порошка CEM являются: 51,75% по массе оксида кальция, 9,53% по массе триоксида серы, 8,49% по массе пентоксида фосфора и 6,32% по массе диоксида кремния. Кроме того, порошок содержит также оксид алюминия, оксид натрия, оксид магния и хлор. Цемент CEM имеет аналогичный pH, но характеризуется гораздо большим уровнем текучести по сравнению с MTA. Кроме того, его рабочее время, толщина пленки и цена значительно меньше. В отличие от MTA, замешанный CEM высвобождает ионы кальция и фосфата и образует гидроксиапатит не только при взаимодействии с жидкостями организма, но и при контакте с физиологическим раствором. Хотя химический состав цемента CEM и MTA различен, они имеют сходные показания к клиническому применению. Подобно МТА, цемент CEM также обладает низким цитотоксическим действием на разные клеточные линии, но при этом он продемонстрировал лучший антибактериальный эффект, сопоставимый с гидроксидом кальция. Сходная герметизирующая способность была отмечена между Proroot MTA и CEM при их использовании с целью закрытия в области фуркации первых молочных моляров.
Нехирургический подход
При восстановлении перфорации первично необходимо оценить возможности для проведения нехирургического вмешательства, которое характеризуется меньшим риском развития травмы пародонта, а значит – и более прогнозированными шансами на успех. Как правило, перфорации, находящиеся выше уровня альвеолярного гребня, можно лечить посредством консервативного подхода. Использование хирургического микроскопа, работающего с большим увеличением и с достаточным освещением, позволяет улучшить качество процедуры восстановления перфорации. Хирургические вмешательства, в свою очередь, характеризуется риском повреждения пародонтального прикрепления, развития хронического воспаления и формирования пародонтального кармана в области дефекта. Опыт показывает, что щечные перфорации восстановить несколько легче, чем те, которые локализируются на язычной или проксимальных стенках. Лингвальное расположенные перфорации, особенно в зубах нижней челюсти, рекомендовано закрывать нехирургическим путем либо ортодонтически. Если в таких случаях достичь эффективного результата не получается, зуб должен быть удален.
Еще одни вариантом лечения является ортодонтическая экструзия зуба до уровня, когда перфорация будет находится уже над уровнем десен – в таких условиях закрыть имеющейся дефект гораздо проще. В одном из исследований даже был описан успешный результат реплантации зуба после закрытия перфорации сразу же после его удаления. В случаях больших перфораций в первую очередь нужно обеспечить контроль кровотечения за счет применения физиологического раствора. С этой же целью можно использовать кальций гидроксид, кальций сульфат или коллаген. Для контроля кровотечения следует избегать применения неспецифических внутрисосудистых свертывающих агентов, поскольку они могут привести к повреждению альвеолярного отростка и вызвать задержку в заживлении имеющегося дефекта. В случае инфицирования перфорационных отверстий можно применять ультразвуковые насадки или обычные боры для механической очистки области вмешательства. Тем не менее, ультразвуковые насадки являются более предпочтительными для данной цели, учитывая, что они менее травматичны для пародонта.
Для очистки зараженных перфораций можно применять 2,5% гипохлорит натрия, однако стерильный физиологический раствор показан при больших размерах дефектов. Чтобы избежать закупорки каналов используемым материалом, устья следует закрывать гуттаперчевыми или бумажными штифтами, ватными шариками или каким-либо другим легко удаляемым аналогом (например, Cavit). Композитный материал по типу Geristore (Denmat) рекомендуется использовать для восстановления поддесневых дефектов. Данный материал также можно использовать в качестве дополнительного при реализации процедур направленной тканевой регенерации. При этом он менее чувствителен к влаге по сравнению с обычным стеклоиономерным цементом.
Адгезивные материалы можно использовать при локализации перфорации над уровнем костной ткани, в то время как MTA подходит для перфораций, находящихся ниже уровня десен. Если дефект перфорации ассоциирован уже и с внутрикостным дефектом, для контролируемой установки восстановительного материала необходимо использовать дополнительный барьерный агент. При закрытии перфорации МТА его следует накрывать влажным ватным шариком для обеспечения адекватного отверждения материала. После закрытия перфорации окончательная реставрация может быть выполнена как через один день, так и через неделю. После закрытия перфорации врач может приступить к очистке корневых каналов и их обтурации.
Если перфорация находится в средней трети корня, проводить обработку каналов следует перед закрытием перфорации, дабы не заблокировать эндопространство. С помощью микроскопа значительно проще проводить обтурацию канала апикальнее области перфорации. Временно обтурировать область перфорации можно также с помощью обычного файла или гуттаперчевого штифта. При использовании гуттаперчи ее следует нагреть и размягчить, прижимая к стенке противоположной перфорации. Перфорации в области апикальной части зуба являются более сложными для закрытия. В отдельных случаях перфорация может быть причиной, аргументирующей необходимость проведения апикального хирургического вмешательства или даже экстракции зуба.
Хирургический подход
Хирургический подход к лечению перфораций с формированием внешнего доступа показан при неэффективности классических терапевтических алгоритмов, направленных на закрытие дефекта. Хирургический подход реализуется за счет сепарации лоскута в области перфорации, очитки зоны дефекта и упаковки в нее восстановительного материала. В ходе хирургических вмешательств происходит повреждение кортикальной костной ткани, что может компрометировать конечный успех. Техники направленной регенерации тканей, которые предусматривают использование резорбируемых или нерезорбируемых мембран, позволяют избежать подобных последствий.
Применяемые биологические барьеры способствуют тому, что область вмешательства «заселяется» популяциями клеток, необходимых для восстановления пародонтальной связки, и они же препятствуют миграции эпителиальных клеток. Если сравнивать резорбируемые и нерезорбируемые мембраны, то первые являются более предпочтительными, исключая необходимость проведения повторного хирургического вмешательства с целью их изъятия. В отдельных случаях для того, чтобы избежать коллапса тканей врачу приходиться использовать титановые мембраны, которые в конце концов приходиться удалять хирургически после полного замещения дефекта.
Регенерация цемента и роль в реконструкции пародонта
Образование цемента является крайне важным фактором для восстановления участков перфорации фуркаций. Pitt Ford и коллеги (1995), сравнивая гистологический ответ окружающих тканей на закрытие перфораций МТА и амальгамой, установили, что в случаях МТА в окружающих тканях почти отсутствует воспалительная реакция, а в отдельных участках отмечается и депозиция цемента, в то время как амальгама провоцировала развитие воспалительной реакции без каких-либо признаков депозиции цемента. Аналогичные результаты были получены при сравнении гистологических ответов тканей на закрытие перфораций МТА и Sealapex (Kerr). В 2010 году Samiee и коллеги сообщили, что после закрытия перфораций МТА и СЕМ-цементом у собак они обнаружили образование цементообразной ткани и воспалительной реакции средней степени выраженности. При этом авторы подтвердили, что оба эти материала индуцировали позитивную биологическую реакцию со стороны окружающих тканей.
Zairi и коллеги (2012) сравнивали воспалительные реакции и тканевую реакцию при закрытии перфораций фуркаций факторами роста, TGF 1, основным фактором роста фибробластов (bFGF), остеогенным белком-1 (OP-1) и IGF-I, и MTA или IRM в качестве контроля. Авторы сообщили, что факторы роста оказывают явное стимулирующее влияние на образование цемента и ингибируют образование капсул коллагена. Однако МТА при этом продемонстрировал лучшие клинические результаты по сравнению с теми, которые были зарегистрированы при использовании факторов роста. В клиническом случае, представленном Bains et al (2012), автор использовал принципы тканевой инженерии для восстановления перфорации фуркации в области дна пульповой камеры правого первого моляра нижней челюсти у 39-летнего пациента, восстанавливая дефект МТА и фибрином, обогащенном тромбоцитами (PRF). Авторы сообщили, что данная комбинация позволила эффективно восстановить дефект и способствовала регенерации утраченных тканей пародонта в области фуркации. Также был опубликован один клинический случай, описывающий успешное нехирургическое эндодонтическое лечение обширной перфорации дна пульповой камеры в первом моляре нижней челюсти у 28-летней пациентки посредством цемента CEM. Авторы сообщили, что CEM-цемент также способствует формирования твердых тканей кости и цемента.
Принципы клеточной инженерии в регенерации цемента
Один из известных подходов закрытия перфораций предусматривает забор аутологических клеток из пародонтальной связки пациента, их культивирование в лабораторных условиях с дальнейшим переносом в область дефекта и перекрытие мембраной. Однако, до сих пор неизвестно, насколько достигнутый эффект лечения был успешным. Lekic и коллеги (2005) сообщили, что клетки пародонта и костного мозга крыс способны дифференцироваться в фибробласты пародонтальной связки, остеобласты и цементобласты при трансплантации их в область пародонтального дефекта, таким образом, способствуя заживлению пародонтальных структур. Регенерация цемента, пародонтальной связки и альвеолярной кости также отмечалась при аутотрансплантации мезенхимальных клеток из костного мозга в область пораженного пародонта у собак. Тем не менее, основным недостатком «клеточных» методик лечения является сложность в проведении данных процедур. Кроме того, забор костного мозга остается довольно инвазивной и болезненной процедурой для самого пациента. Также отдельные исследования доказали тот факт, что потенциал к пролиферации и дифференцировки мезенхимальных клеток костного мозга снижается с увеличением возраста человека.
Сообщалось, что дефекты, обработанные губчатым полимером из цементобласт-биоразлагаемого полимера молочно-гликолевой кислоты (PLGA), могут полностью восстанавливаться с точки зрения костной ткани и пародонтальной связки. Стволовые клетки пародонтальной связки (PDLSC) обладают способностью дифференцироваться в цементобласты и остеобласты и демонстрируют огромный потенциал для регенерации пародонта. Проблемой остается только малое количество данных клеток в пародонтальной связке, следовательно – их приходиться культивировать для того, чтобы собрать такое количество, которого достаточно для индукции процесса регенерации пародонта. Кондиционированная среда из эмбриональных клеток, собранных из апекса зуба, является оптимальной для реализации процессов цементогенеза и цементобластной дифференциации стволовых клеток из пародонтальной связки. Клетки из Гертвиговской эпителиальной оболочки, а также секретируемые ими продукты в лабораторных условиях индуцировали процесс дифференцировки клеток пародонтальной связки в линейку цементобластов. Несколько исследований in vivo также показали потенциальную способность стволовых клеток пародонтальной связки формировать цементообразные и пародонтально-ассоциированные структуры.
Регенеративная терапия
Тканевая инженерия является междудисциплинарной отраслью, которая применяет принципы инженерии и биологии для разработки разного рода биологических заменителей, что, в свою очередь, позволяет восстановить или же улучшить функцию тканей или же целого органа. Методы тканевой инженерии направлены на стимулирование организма, самостоятельную регенерацию тканей, или же на достижение роста тканей вне тела, которые в дальнейшем могут быть имплантированы в организм.
Триада компонентов
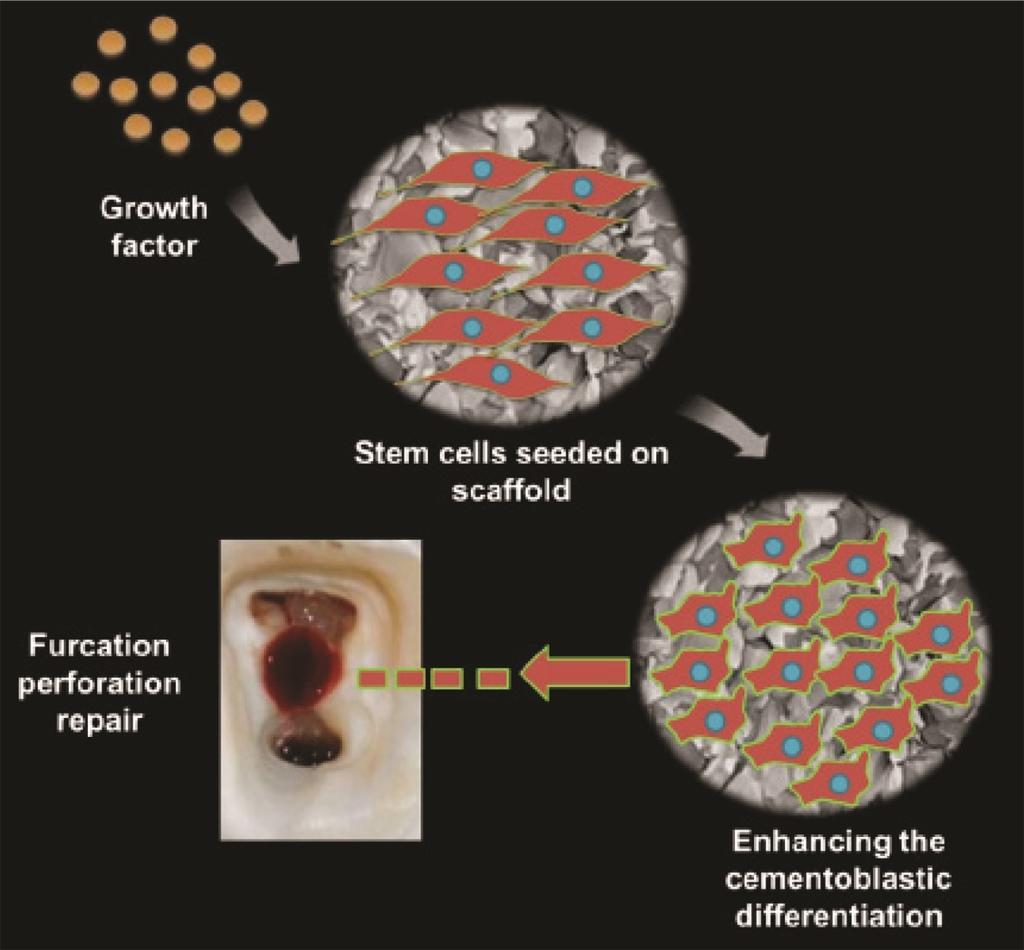
Регенеративная эндодонтия может быть определена как совокупность биологически обоснованных процедур, направленных на восстановление поврежденных структур, в том числе цемента, пародонтальной связки и костной ткани. Для реализации принципов регенеративной эндодонтии необходимо иметь три обязательных составляющих: 1) соответствующий источник клеток; 2) поддерживающий матрикс; и 3) индуктивные биологические факторы или сигналы (фото 1). Для достижения необходимого результата данные составляющие нужно комбинировать, а не использовать по отдельности.
Фото 1. Схема восстановления участка перфорации фуркации с применением стволовых клеток, биологического матрикса и факторов роста.
Перспективы восстановления перфорации
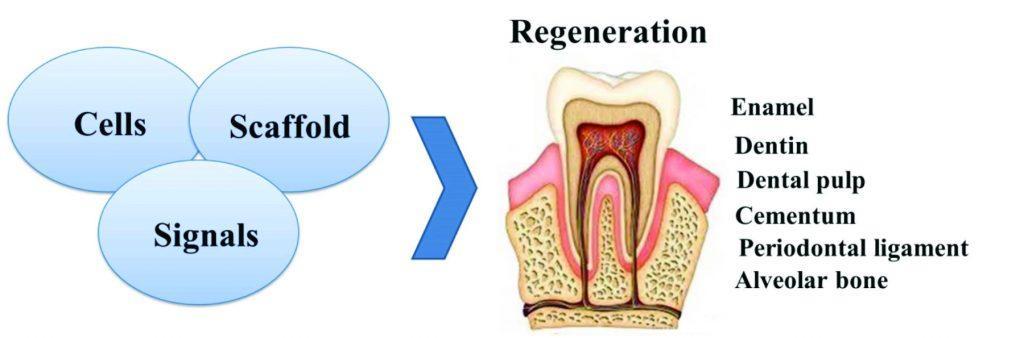
Восстановление утраченного пародонтального прикрепления путем регенерации компонентов пародонта (цемента, связки и костной ткани) имеет крайне важное значение для замещения участков перфораций в области фуркации. Цементогенез способствует повторному прикреплению волокон пародонтальной связки. В последние годы все более выражено наблюдется сдвиг парадигмы от традиционной эндодонтической терапии к регенеративной. На сегодняшний день в литературе до сих пор не опубликовано ни одного исследования, в котором бы сообщалось об эффекте применения регенеративной триады (стволовых клеток, поддерживающей матрицы и фактора роста) с целью восстановления перфорации в области фуркации, и реакции окружающих тканей на такой метод лечения. Мы предлагаем применять метод тканевой инженерии на основе стволовых клеток для восстановления перфорации фуркации посредством усиления дифференцировки стволовых клеток по линейке цементобластов. Предложенный биомиметический подход изображен на фото 2, и в дальнейшем он может сыграть значительную роль в тканевой инженерии тканей пародонта, пораженных вследствие перфорации фуркации.
Фото 2. Три основных элемента, необходимые для тканевой инженерии структур зуба.
Выводы
Перфорация дна пульповой камеры в многокорневых зубах является сложной и комплексной проблемой, требующей эффективного клинического решения. Ведь, по сути, перфорация в области фуркации – это одновременно и эндодонтическое, и пародонтальное осложнение. Воспалительная реакция пародонта, развивающаяся после перфорации, провоцирует потерю пародонтального прикрепления, что в конечном счете без адекватного лечения может привести к потере всего зуба. Для восстановления пародонтальных тканей в области перфорации могут использоваться как хирургические, так и нехирургические подходы. Кроме того, для закрытия перфораций врач имеет возможность выбрать разные виды материалов. Последний тренд в процессе восстановления пародонтальных тканей состоит в возможности реализации принципов тканевой инженерии. Данный метод, по сути, является революционным для всей эндодонтической практики. Потенциально тканевая инженерия может помочь спасти даже самые безнадежные зубы, обеспечивая при этом не только восстановление их дефектных участков, но и регенерацию окружающих тканей пародонта.
Авторы: Manal Farea, Adam Husein, Cornelis H Pameijer
Производители:
В ходе лечения корневых каналов существует риск развития такого осложнения, как перфорация, которая непосредственно влияет на дальнейший прогноз ятрогенного вмешательства.

Прогноз функционирования зуба после перфорации зависит от ряда определяющих факторов:
- Тяжесть исходного поражения тканей пародонта
- Расположение и размер перфорации
- Бактериальная контаминация
- Герметизирующая способность или цитотоксичность материалов, используемых для закрытия сформировавшегося дефекта.
Даже если для лечения перфорации используется биосовместимый материал, обширная травма низлежащих тканей может привести к необратимому повреждению биологического прикрепления в области фуркации. В случаях больших перфораций полное закрытие дефекта является проблематичным, учитывая условия развития персистирующего воспаления и возможность прорастания в перфорацию бороздкового эпителия. Sinai (1977) заявил, что перфорации, расположенные в коронковой части корня, являются более проблематичными, чем те, которые формируются в срединной или апикальной трети корня. Цель данной статьи состоит в том, чтобы систематизировать и проанализировать имеющиеся научные данные относительно наиболее подходящих и эффективных методов лечения перфораций, локализированных в области фуркации.
Методы
Поиск литературы
Для первичного анализа были отобраны научные статьи из базы данных Medline, опубликованные в период с 2002 по 2015 год. Поиск данных публикаций проводился по ключевым словам «перфорации и эндодонтия», «перфорация фуркации», «корневые каналы и перфорации» и «минерал триоксид агрегат (MTA)». Дальше проводился анализ списков литературы, указанных в отобранных статьях, для определения необходимости поиска дополнительных научных источников.
Результаты
Всего было найдено 820 статей, которые были систематизированы по наборам ключевых слов: перфорация и эндодонтия – 285; перфорация фуркации – 92; корневой канал и перфорация – 299; и перфорация и минерал триоксид агрегат (MTA) – 144.
Методы закрытия перфораций и прогноз лечения
Для восстановления тканей пародонта в области сформировавшейся перфорации могут использоваться как хирургические, так и нехирургические методы лечения. При выборе одного из этих подходов следует учитывать два фактора:
- Выбор соответствующего материала
- Использование матрицы.
Выбор материала для закрытия перфорации проводится с учетом следующих критериев:
- Доступность области перфорации
- Биосовместимость (материал должен быть нетоксичным и неканцерогенным)
- Способность индуцировать процессы остеогенеза и цементогенеза
- Уровень контроля влажности
- Простота в использовании
- Эстетические соображения.
Использование матрицы
Ключевыми аспектами, определяющими успешность восстановления участка перфорации, являются контроль гемостаза и установка материала для закрытия дефекта так, чтобы он не пенетрировал в окружающие пародонтальные структуры. Контроль гемостаза является крайне важным условием для обеспечения герметичности закрытия перфорации в области фуркации. Отсроченное восстановление перфорации может привести к вытеснению слоя материала из проекции дефекта за счет разрушения низлежащих структур пародонта и их замещения грануляционной тканью. Дабы избежать подобного эффекта могут использоваться так называемые внутренние матрицы из таких материалов, как сульфат кальция, гидроксиапатит, коллаген, деминерализованная лиофилизированная кость и Gelfoam. Концепция внутренней матрицы впервые была введена Lemon (1992) для адекватного уплотнения области перфорации фуркации и предотвращения экструзии материала. Он также рекомендовал использовать гидроксиапатит в качестве матрицы под амальгамой. Сульфат кальция и гидроксид кальция также позволяют предотвратить экструзию композита, если таковой применяется в качестве материала для восстановления дефекта в участке фуркации.
В 1999 году Jantarat и коллеги продемонстрировали, что применение гипса Paris в качестве матрицы под амальгаму при восстановлении перфорации фуркации позволяет улучшить герметизирующие свойства последней. Применение хапсета (состоящий из 65% нерезорбируемого гидроксиапатита и 35% Paris-гипса) и гидроксиапатита продемонстрировало аналогичные реакции заживления при использовании их в качестве внутренних матриц под амальгамой (Rafter et al, 2002). Rafter и коллеги (2002) также сообщили, что отсутствие внутренней матрицы под амальгамой провоцировало выдавливание последней в нижележащую костную ткань, что, очевидно, было ассоциировано с тяжелой воспалительной реакцией биологических структур. Однако, применение МТА даже без внутренней матрицы характеризовалось достижением оптимальной прочности и превосходной герметичности данного материала в присутствии влаги. В 2004 году Kratchman рекомендовал пропитывать место перфорации гипохлоритом натрия после достижения гемостаза, и в случаях закрытия дефекта с помощью МТА все же нужно фиксировать какой-то физический барьер по типу коллагена или сульфата кальция.
Согласно Bargholz (2005), отличные клинические результаты были достигнуты при использовании коллагенового матрикса в качестве внутренней матрицы под МТА. Исследование Al-Daafas и Al-Nazhan (2007) показало, что сульфат кальция также позволял предотвратить экструзию восстановительного материала. При этом однако была обнаружена неблагоприятная воспалительная реакция, а именно - миграция эпителиальной ткани в область дефекта и невозможность дальнейшей регенерации низлежащеий кости. Таким образом, авторы пришли к выводу, что использование сульфата кальция в качестве внутренней матрицы под МТА все же не рекомендуется. При использовании в качестве внутреннего матрикса сульфата кальция и Collaplug (Calcitek, Carlsbad, CA) не было отмечено улучшений герметизирующих характеристик МТА, более того, эти материалы не снижали частоту возникновения случаев экструзии MTA в пародонтальные структуры. Поэтому авторы пришли к выводу, что эти два аналога также не стоит рекомендовать для применения в качестве внутренних матриц для MTA (Zou et al, 2008).
Материалы, используемые для восстановления участков перфораций в области фуркаций
В попытке восстановить перфорацию в области фуркации врачи пробовали использовать такие материалы, как амальгама, трикальцийфосфат (TCP), гидроксиапатит, гуттаперчу, гидроксид кальция, цинкооксидэвгенольный цемент, стеклоиономерный цемент, композитные аналоги, гибридные компомеры, деминерализованную лиофилизированную костную ткань, а также МТА. Тем не менее, ни один из этих материалов полностью не соответствует всем необходимым техническим и биологическим требованиям.
Balla и коллеги (1991) сообщили, что область дефекта перфорации повторно не замещалась твердыми тканями в случаях закрытия дефекта трикальций фосфатом, гидроксиапатитом, амальгамой или гидроксидом кальция (Life); вместо этого участок дефекта восполнялся эпителием и воспалительными клетками.
MTA является цементом, работающим на водной основе, полученным из портландцемента (тип I), который начали использовать в качестве эндодонтического материала в начале 1990-х годов. В результате полученных клинических материалов, было установлено, что данный цемент подходит для разных клинических ситуаций, в том числе и для перекрытия витальной пульпы, восстановления перфораций в области фуркации, а также для обтурации участка верхушки корня. При этом MTA способствует регенерации перирадикулярных тканей и отличается от других аналогов своей способностью стимулировать регенерацию цемента, таким образом, способствуя регенерации всего пародонтального комплекса. Природа его биосовместимости подтверждается способностью материала образовывать гидроксиапатит при взаимодействии с жидкостями организма человека.
На данный момент доступны две коммерческие формы MTA: Proroot MTA (Dentsply Tulsa Dental), который представлен в серой или белой форме (последняя содержит меньшее количество железа) и MTA-Angelus (Angelus). MTA-Angelus был разработан для того, чтобы решить проблему длительного времени отверждения Proroot MTA, таким образом, удалось сократить длительность данной фазы до 10 минут. MTA-Angelus содержит 80% портландцемента и 20% оксида висмута без добавок сульфата кальция, в то время как Proroot MTA состоит из 75% портландцемента, 20% оксида висмута и 5% дегидрата сульфата кальция. Сам же портландцемент содержит множество неорганических составляющих, среди которых силикат дикальция, силикат трикальция, алюминат трикальция, железоалюминат тетракальция и обезвоженный сульфат кальция. Единственным существенным различием между составами белого и серого МТА и ассоциированных с ними портландцементами является присутствие оксида висмута в структуре МТА.
Сообщалось, что герметизирующая способность MTA (Университет Лома Линда, Калифорния) является значительно лучше по сравнению с амальгамой для профилактики подтекания Fusobacterium nucleatum через перфорации в области фуркации. Результаты исследований указывают на то, что применение Proroot MTA с или без внутренней матрицы и MTA-Angelus с внутренней матрицей характеризуется наименьшим уровнем абсорбции красителя по сравнению с цинкоксидэвгенольным цементом, применяемым с или без внутренней матрицы, а также по сравнению с MTA-Angelus, используемым без внутренней матрицы. Кроме того, авторы сообщили, что IRM без внутренней матрицы имеет самую высокую поглощающую способность красителя (Hashem, Hassanien, 2008). Тем не менее, белый и серый MTA (Dentsply Tulsa Dental) практически не отличались в параметрах микроплотности при использовании с целью восстановления перфораций в области фуркации.
В одном из исследований изучали результаты закрытия перфораций с помощью Proroot grey MTA (Dentsply) и Geristore (Denmat). Geristore используется в качестве материала для пломбировки корневых каналов и восстановления дефектов зубов в поддесневой области, таких как кариес поверхности корня и ятрогенные перфорации, а также в качестве аддитивного материала в ходе процедуры направленной регенерации тканей (GTR). Geristore характеризуется лучшей уплотнительной способностью по сравнению с амальгамой. В ходе исследования авторы установили, что герметизирующие способности MTA и Geristore снижаются при использовании в качестве внутренней матрицы под ними разных вариантов биостекла.
Sluyk, Moon and Hartwell (1998) оценивали влияние времени и влажности на параметры отверждения, ретенции и адаптации MTA при его использовании с целью восстановления перфораций в области фуркации. Результаты показали, что адаптация МТА к перфорации стенок усиливается при наличии влаги. Они также предположили, что увлажненная матрица может оказаться эффективной при закрытии перфорации МТА с целью предотвращения неполного закрытия дефекта или экструзии материала в пародонт. Кроме того, Main et al (2004) также сообщили, что МТА эффективно работает и при закрытии обычных перфораций корня.
Yildirim и др. (2005) исследовали гистологический ответ на MTA и Super EBA (Bosworth Company) при использовании их с целью восстановления перфораций фуркаций у собак. При применении МТА наблюдали менее выраженный уровень воспаления и признаки образования нового цемента, в то время как закрытие перфорации Super EBA провоцировало восстановление области дефекта соединительной ткани без признаков воспаления. Аналогичные гистологические результаты наблюдались и при закрытии перфораций фуркаций такими материала как портландцемент и MTA. Результаты исследования применения МТА и трикальций фосфата с целью заполнения дефекта в области фуркаций не продемонстрировали существенных различий между материалами в плане реорганизации костной ткани или депозиции фиброзной соединительной ткани.
Таким образом, MTA считается золотым стандартом и материалом выбора для восстановления перфораций в области фуркации, который демонстрирует успешные клинические результаты. Однако у него есть и некоторые недостатки, как, например, неспособность к деградации с целью замещения естественными тканями, низкая устойчивость к сжатию в течение длительного времени, длительное время отверждения, манипуляционные сложности в работе и внесении в дефектную область. Кроме того, цемент требует наличия дополнительной влаги для его адекватного отверждения.
В литературе неоднократно сообщалось, что многие стоматологические материалы демонстрируют цитотоксические эффекты во время отверждения. В лабораторных условиях было установлено, что свежеприготовленный МТА (pH = 10,2) характеризуется гораздо меньшим уровнем миграции к его поверхности воспалительных клеток по сравнению с уже полностью отвердевшим МТА (pH = 12,5). Однако, даже при таком условии, гистологически не наблюдалось различий в регенерации костной ткани и цемента после выполнения периапикального хирургического вмешательства у собак при выполнении дефекта свежеприготовленным и предварительно отвердевшим формами Proroot MTA.
В 2006 году Asgary и коллеги представили новый цемент для применения в эндодонтии, который представлял собой кальций-обогащенный материал (CEM). Основными компонентами порошка CEM являются: 51,75% по массе оксида кальция, 9,53% по массе триоксида серы, 8,49% по массе пентоксида фосфора и 6,32% по массе диоксида кремния. Кроме того, порошок содержит также оксид алюминия, оксид натрия, оксид магния и хлор. Цемент CEM имеет аналогичный pH, но характеризуется гораздо большим уровнем текучести по сравнению с MTA. Кроме того, его рабочее время, толщина пленки и цена значительно меньше. В отличие от MTA, замешанный CEM высвобождает ионы кальция и фосфата и образует гидроксиапатит не только при взаимодействии с жидкостями организма, но и при контакте с физиологическим раствором. Хотя химический состав цемента CEM и MTA различен, они имеют сходные показания к клиническому применению. Подобно МТА, цемент CEM также обладает низким цитотоксическим действием на разные клеточные линии, но при этом он продемонстрировал лучший антибактериальный эффект, сопоставимый с гидроксидом кальция. Сходная герметизирующая способность была отмечена между Proroot MTA и CEM при их использовании с целью закрытия в области фуркации первых молочных моляров.
Нехирургический подход
При восстановлении перфорации первично необходимо оценить возможности для проведения нехирургического вмешательства, которое характеризуется меньшим риском развития травмы пародонта, а значит – и более прогнозированными шансами на успех. Как правило, перфорации, находящиеся выше уровня альвеолярного гребня, можно лечить посредством консервативного подхода. Использование хирургического микроскопа, работающего с большим увеличением и с достаточным освещением, позволяет улучшить качество процедуры восстановления перфорации. Хирургические вмешательства, в свою очередь, характеризуется риском повреждения пародонтального прикрепления, развития хронического воспаления и формирования пародонтального кармана в области дефекта. Опыт показывает, что щечные перфорации восстановить несколько легче, чем те, которые локализируются на язычной или проксимальных стенках. Лингвальное расположенные перфорации, особенно в зубах нижней челюсти, рекомендовано закрывать нехирургическим путем либо ортодонтически. Если в таких случаях достичь эффективного результата не получается, зуб должен быть удален.
Еще одни вариантом лечения является ортодонтическая экструзия зуба до уровня, когда перфорация будет находится уже над уровнем десен – в таких условиях закрыть имеющейся дефект гораздо проще. В одном из исследований даже был описан успешный результат реплантации зуба после закрытия перфорации сразу же после его удаления. В случаях больших перфораций в первую очередь нужно обеспечить контроль кровотечения за счет применения физиологического раствора. С этой же целью можно использовать кальций гидроксид, кальций сульфат или коллаген. Для контроля кровотечения следует избегать применения неспецифических внутрисосудистых свертывающих агентов, поскольку они могут привести к повреждению альвеолярного отростка и вызвать задержку в заживлении имеющегося дефекта. В случае инфицирования перфорационных отверстий можно применять ультразвуковые насадки или обычные боры для механической очистки области вмешательства. Тем не менее, ультразвуковые насадки являются более предпочтительными для данной цели, учитывая, что они менее травматичны для пародонта.
Для очистки зараженных перфораций можно применять 2,5% гипохлорит натрия, однако стерильный физиологический раствор показан при больших размерах дефектов. Чтобы избежать закупорки каналов используемым материалом, устья следует закрывать гуттаперчевыми или бумажными штифтами, ватными шариками или каким-либо другим легко удаляемым аналогом (например, Cavit). Композитный материал по типу Geristore (Denmat) рекомендуется использовать для восстановления поддесневых дефектов. Данный материал также можно использовать в качестве дополнительного при реализации процедур направленной тканевой регенерации. При этом он менее чувствителен к влаге по сравнению с обычным стеклоиономерным цементом.
Адгезивные материалы можно использовать при локализации перфорации над уровнем костной ткани, в то время как MTA подходит для перфораций, находящихся ниже уровня десен. Если дефект перфорации ассоциирован уже и с внутрикостным дефектом, для контролируемой установки восстановительного материала необходимо использовать дополнительный барьерный агент. При закрытии перфорации МТА его следует накрывать влажным ватным шариком для обеспечения адекватного отверждения материала. После закрытия перфорации окончательная реставрация может быть выполнена как через один день, так и через неделю. После закрытия перфорации врач может приступить к очистке корневых каналов и их обтурации.
Если перфорация находится в средней трети корня, проводить обработку каналов следует перед закрытием перфорации, дабы не заблокировать эндопространство. С помощью микроскопа значительно проще проводить обтурацию канала апикальнее области перфорации. Временно обтурировать область перфорации можно также с помощью обычного файла или гуттаперчевого штифта. При использовании гуттаперчи ее следует нагреть и размягчить, прижимая к стенке противоположной перфорации. Перфорации в области апикальной части зуба являются более сложными для закрытия. В отдельных случаях перфорация может быть причиной, аргументирующей необходимость проведения апикального хирургического вмешательства или даже экстракции зуба.
Хирургический подход
Хирургический подход к лечению перфораций с формированием внешнего доступа показан при неэффективности классических терапевтических алгоритмов, направленных на закрытие дефекта. Хирургический подход реализуется за счет сепарации лоскута в области перфорации, очитки зоны дефекта и упаковки в нее восстановительного материала. В ходе хирургических вмешательств происходит повреждение кортикальной костной ткани, что может компрометировать конечный успех. Техники направленной регенерации тканей, которые предусматривают использование резорбируемых или нерезорбируемых мембран, позволяют избежать подобных последствий.
Применяемые биологические барьеры способствуют тому, что область вмешательства «заселяется» популяциями клеток, необходимых для восстановления пародонтальной связки, и они же препятствуют миграции эпителиальных клеток. Если сравнивать резорбируемые и нерезорбируемые мембраны, то первые являются более предпочтительными, исключая необходимость проведения повторного хирургического вмешательства с целью их изъятия. В отдельных случаях для того, чтобы избежать коллапса тканей врачу приходиться использовать титановые мембраны, которые в конце концов приходиться удалять хирургически после полного замещения дефекта.
Регенерация цемента и роль в реконструкции пародонта
Образование цемента является крайне важным фактором для восстановления участков перфорации фуркаций. Pitt Ford и коллеги (1995), сравнивая гистологический ответ окружающих тканей на закрытие перфораций МТА и амальгамой, установили, что в случаях МТА в окружающих тканях почти отсутствует воспалительная реакция, а в отдельных участках отмечается и депозиция цемента, в то время как амальгама провоцировала развитие воспалительной реакции без каких-либо признаков депозиции цемента. Аналогичные результаты были получены при сравнении гистологических ответов тканей на закрытие перфораций МТА и Sealapex (Kerr). В 2010 году Samiee и коллеги сообщили, что после закрытия перфораций МТА и СЕМ-цементом у собак они обнаружили образование цементообразной ткани и воспалительной реакции средней степени выраженности. При этом авторы подтвердили, что оба эти материала индуцировали позитивную биологическую реакцию со стороны окружающих тканей.
Zairi и коллеги (2012) сравнивали воспалительные реакции и тканевую реакцию при закрытии перфораций фуркаций факторами роста, TGF 1, основным фактором роста фибробластов (bFGF), остеогенным белком-1 (OP-1) и IGF-I, и MTA или IRM в качестве контроля. Авторы сообщили, что факторы роста оказывают явное стимулирующее влияние на образование цемента и ингибируют образование капсул коллагена. Однако МТА при этом продемонстрировал лучшие клинические результаты по сравнению с теми, которые были зарегистрированы при использовании факторов роста. В клиническом случае, представленном Bains et al (2012), автор использовал принципы тканевой инженерии для восстановления перфорации фуркации в области дна пульповой камеры правого первого моляра нижней челюсти у 39-летнего пациента, восстанавливая дефект МТА и фибрином, обогащенном тромбоцитами (PRF). Авторы сообщили, что данная комбинация позволила эффективно восстановить дефект и способствовала регенерации утраченных тканей пародонта в области фуркации. Также был опубликован один клинический случай, описывающий успешное нехирургическое эндодонтическое лечение обширной перфорации дна пульповой камеры в первом моляре нижней челюсти у 28-летней пациентки посредством цемента CEM. Авторы сообщили, что CEM-цемент также способствует формирования твердых тканей кости и цемента.
Принципы клеточной инженерии в регенерации цемента
Один из известных подходов закрытия перфораций предусматривает забор аутологических клеток из пародонтальной связки пациента, их культивирование в лабораторных условиях с дальнейшим переносом в область дефекта и перекрытие мембраной. Однако, до сих пор неизвестно, насколько достигнутый эффект лечения был успешным. Lekic и коллеги (2005) сообщили, что клетки пародонта и костного мозга крыс способны дифференцироваться в фибробласты пародонтальной связки, остеобласты и цементобласты при трансплантации их в область пародонтального дефекта, таким образом, способствуя заживлению пародонтальных структур. Регенерация цемента, пародонтальной связки и альвеолярной кости также отмечалась при аутотрансплантации мезенхимальных клеток из костного мозга в область пораженного пародонта у собак. Тем не менее, основным недостатком «клеточных» методик лечения является сложность в проведении данных процедур. Кроме того, забор костного мозга остается довольно инвазивной и болезненной процедурой для самого пациента. Также отдельные исследования доказали тот факт, что потенциал к пролиферации и дифференцировки мезенхимальных клеток костного мозга снижается с увеличением возраста человека.
Сообщалось, что дефекты, обработанные губчатым полимером из цементобласт-биоразлагаемого полимера молочно-гликолевой кислоты (PLGA), могут полностью восстанавливаться с точки зрения костной ткани и пародонтальной связки. Стволовые клетки пародонтальной связки (PDLSC) обладают способностью дифференцироваться в цементобласты и остеобласты и демонстрируют огромный потенциал для регенерации пародонта. Проблемой остается только малое количество данных клеток в пародонтальной связке, следовательно – их приходиться культивировать для того, чтобы собрать такое количество, которого достаточно для индукции процесса регенерации пародонта. Кондиционированная среда из эмбриональных клеток, собранных из апекса зуба, является оптимальной для реализации процессов цементогенеза и цементобластной дифференциации стволовых клеток из пародонтальной связки. Клетки из Гертвиговской эпителиальной оболочки, а также секретируемые ими продукты в лабораторных условиях индуцировали процесс дифференцировки клеток пародонтальной связки в линейку цементобластов. Несколько исследований in vivo также показали потенциальную способность стволовых клеток пародонтальной связки формировать цементообразные и пародонтально-ассоциированные структуры.
Регенеративная терапия
Тканевая инженерия является междудисциплинарной отраслью, которая применяет принципы инженерии и биологии для разработки разного рода биологических заменителей, что, в свою очередь, позволяет восстановить или же улучшить функцию тканей или же целого органа. Методы тканевой инженерии направлены на стимулирование организма, самостоятельную регенерацию тканей, или же на достижение роста тканей вне тела, которые в дальнейшем могут быть имплантированы в организм.
Триада компонентов
Регенеративная эндодонтия может быть определена как совокупность биологически обоснованных процедур, направленных на восстановление поврежденных структур, в том числе цемента, пародонтальной связки и костной ткани. Для реализации принципов регенеративной эндодонтии необходимо иметь три обязательных составляющих: 1) соответствующий источник клеток; 2) поддерживающий матрикс; и 3) индуктивные биологические факторы или сигналы (фото 1). Для достижения необходимого результата данные составляющие нужно комбинировать, а не использовать по отдельности.
Фото 1. Схема восстановления участка перфорации фуркации с применением стволовых клеток, биологического матрикса и факторов роста.

Перспективы восстановления перфорации
Восстановление утраченного пародонтального прикрепления путем регенерации компонентов пародонта (цемента, связки и костной ткани) имеет крайне важное значение для замещения участков перфораций в области фуркации. Цементогенез способствует повторному прикреплению волокон пародонтальной связки. В последние годы все более выражено наблюдется сдвиг парадигмы от традиционной эндодонтической терапии к регенеративной. На сегодняшний день в литературе до сих пор не опубликовано ни одного исследования, в котором бы сообщалось об эффекте применения регенеративной триады (стволовых клеток, поддерживающей матрицы и фактора роста) с целью восстановления перфорации в области фуркации, и реакции окружающих тканей на такой метод лечения. Мы предлагаем применять метод тканевой инженерии на основе стволовых клеток для восстановления перфорации фуркации посредством усиления дифференцировки стволовых клеток по линейке цементобластов. Предложенный биомиметический подход изображен на фото 2, и в дальнейшем он может сыграть значительную роль в тканевой инженерии тканей пародонта, пораженных вследствие перфорации фуркации.
Фото 2. Три основных элемента, необходимые для тканевой инженерии структур зуба.

Выводы
Перфорация дна пульповой камеры в многокорневых зубах является сложной и комплексной проблемой, требующей эффективного клинического решения. Ведь, по сути, перфорация в области фуркации – это одновременно и эндодонтическое, и пародонтальное осложнение. Воспалительная реакция пародонта, развивающаяся после перфорации, провоцирует потерю пародонтального прикрепления, что в конечном счете без адекватного лечения может привести к потере всего зуба. Для восстановления пародонтальных тканей в области перфорации могут использоваться как хирургические, так и нехирургические подходы. Кроме того, для закрытия перфораций врач имеет возможность выбрать разные виды материалов. Последний тренд в процессе восстановления пародонтальных тканей состоит в возможности реализации принципов тканевой инженерии. Данный метод, по сути, является революционным для всей эндодонтической практики. Потенциально тканевая инженерия может помочь спасти даже самые безнадежные зубы, обеспечивая при этом не только восстановление их дефектных участков, но и регенерацию окружающих тканей пародонта.
Авторы: Manal Farea, Adam Husein, Cornelis H Pameijer






























































































































































0 комментариев