Профилактика кариеса и реминерализация эмали — два важнейших аспекта здоровья полости рта, требующие комплексного подхода. Стратегии профилактики снижают риск возникновения новых кариозных поражений, тогда как методы реминерализации направлены на восстановление минерального состава уже пораженных твердых тканей на ранних стадиях. Фториды в различных формах (фторирование воды, зубные пасты, ополаскиватели, лаки и каппы) способны предотвращать кариес и реминерализировать пораженные ткани, однако их избыточное применение может иметь негативные последствия для здоровья. Доказательства эффективности гидроксиапатита, добавляемого в некоторые зубные пасты, ограничены, он он может обладать свойствами, способствующими реминерализации. Кроме того, антимикробные средства снижают количество кариесогенных бактерий, что может замедлять развитие и прогрессирование кариеса. Неинвазивные методы реминерализации или восстановления начальных поражений предлагают консервативные варианты лечения.

Фториды для профилактики кариеса
Фториды помогают предотвращать развитие кариеса, повышая устойчивость эмали к потере минералов в кислой среде. Эмаль состоит из минерала гидроксиапатита — Ca10(PO4)6(OH)2. В присутствии фторидов при реминерализации ионы фтора могут включаться в структуру этого минерала, образуя фторапатит (Ca10(PO4)6(OH)(2-x)F) в твердых тканях зуба. Замена гидроксильных групп (-OH) в гидроксиапатите на меньшие по размеру ионы фтора во фторапатите приводит к образованию более плотной кристаллической решетки. Эти более компактные кристаллы обладают повышенной устойчивостью к деминерализации в условиях низкого значения pH. Электростатические силы между противоположно заряженными ионами усиливаются на меньших расстояниях, поэтому фторапатит имеет более высокую силу притяжения между ионами и меньшую растворимость.
В начале 20 века в Колорадо-Спрингс, штат Колорадо, было замечено, что люди, пившие воду с природным фтором, реже страдали от кариеса. Это стало первым открытием положительного влияния фторидов на устойчивость зубов к кариесу. Доказательства целенаправленного использования фторидов для профилактики кариеса относятся к 1940-м годам, когда в Гранд-Рапидс, штат Мичиган, была запущена программа фторирования питьевой воды. та инициатива привела к значительному снижению индекса КПУ (количество пораженных, отсутствующих и запломбированных зубов) у детей через 10 лет после внедрения программы. После внедрения фторирования питьевой воды (ФПВ) его польза была поставлена под сомнение из-за широкого распространения фторсодержащих средств гигиены полости рта, появившихся около 1975 года. Обновленный обзор Кохрейна показал, что улучшение индекса КПУ после введения ФПВ в исследованиях после 1975 года было менее выраженным, чем в исследованиях до 1975 года. Предполагается, что ФПВ по-прежнему полезно для людей, не имеющих доступа к фторсодержащим гигиеническим средствам. Однако в обзоре не было обнаружено достаточных доказательств того, что отмена ФПВ увеличивает разрыв в уровнях кариеса между социально-экономическими группами. Тем не менее, результаты свидетельствуют, что ФПВ сохраняет пользу для общественного здоровья, несмотря на снижение эффекта после распространения фторсодержащих зубных паст.
Фторид содержится в безрецептурных зубных пастах в концентрации 1000 частей на миллион (ppm) и в рецептурных пастах — до 5000 ppm, тогда как в питьевой воде его концентрация составляет 0,7–1 ppm. Использование паст с высокой концентрацией фторида приводит к увеличению его уровня в слюне в течение нескольких часов после чистки. Помимо зубных паст, фторид присутствует в других профилактических продуктах, таких как ополаскиватели, лаки и каппы.
Фторид может входить в состав безрецептурных ополаскивателей в форме 0,02–0,05% фторида натрия (92–230 ppm) или в состав рецептурных ополаскивателей — 0,2% фторида натрия (900 ppm). Согласно Кохрейновскому обзору, использование фторсодержащих ополаскивателей снижает индекс КПУ на 23% (при этом разницы между концентрациями 0,05% и 0,2% не выявлено). Однако они отметили, что это утверждение не основано на исследованиях, сравнивающих использование фторсодержащих зубных паст и ополаскивателей в рамках одного исследования, а классификация исследований с учетом фонового воздействия фторидов часто основывалась на рыночных предположениях. Клинические испытания, в которых сравнивали ополаскиватель с 0,05% фторида натрия и зубную пасту в одном исследовании, показали, что дополнительной пользы в профилактике кариеса при совместном использовании ополаскивателя и пасты не наблюдается. Однако ополаскиватель снижал частоту кариеса, если фторсодержащая зубная паста не использовалась. Таким образом, фторсодержащие ополаскиватели могут быть полезны для пациентов, которые не могут качественно чистить зубы из-за недостаточной мотивации или моторных навыков. Еще одним фактором является то, что концентрация фторидов в ополаскивателях ниже, чем в зубных пастах. Использование ополаскивателя без фторидов после чистки зубов пастой с 1000 ppm фторидов или ополаскивателя с 230 ppm фторидов после пасты с 5000 ppm фторидов снижает концентрацию фторидов в слюне. Поэтому таким пациентам рекомендуется сначала использовать ополаскиватель, а затем чистить зубы.
Фторидные лаки обычно содержат 5% фторида натрия (22 600 ppm). В крупном систематическом обзоре и метаанализе 13 исследований было показано, что использование фторидного лака снижает индекс КПУ на 43% у подростков с постоянными зубами. Исследования на взрослых не проводились, однако предполагается, что фторидные лаки также эффективны для профилактики кариеса у взрослых. Механизм действия высоких концентраций фторидов заключается в образовании глобул фторида кальция на поверхности эмали после применения. Эти глобулы относительно нерастворимы при нейтральном pH и могут оставаться на зубах в течение нескольких месяцев после нанесения. При снижении pH фторид кальция растворяется и способствует реминерализации тканей зуба фторапатитом.
Фторидные каппы стали стандартным методом лечения пациентов с ксеростомией после лучевой терапии. Рекомендуется использовать 0,4% фторид олова (1000 ppm) в каппах ежедневно в течение 5 минут. Этот метод основан на клиническом исследовании 1977 года, в котором сообщалось о частоте возникновения кариеса 0,16 КПУ/месяц при использовании капп и 2,51 КПУ/месяц — без них у пациентов с лучевой ксеростомией. Помимо повышения воздействия фторидов, пациенты с ксеростомией могут также получить пользу от использования буферных агентов, так как у них отсутствует бикарбонатный буфер, содержащийся в слюне. Для повышения pH слюны можно использовать воду с пищевой содой или другие продукты, содержащие бикарбонат натрия.
Проблемы здоровья, связанные с употреблением фторидов
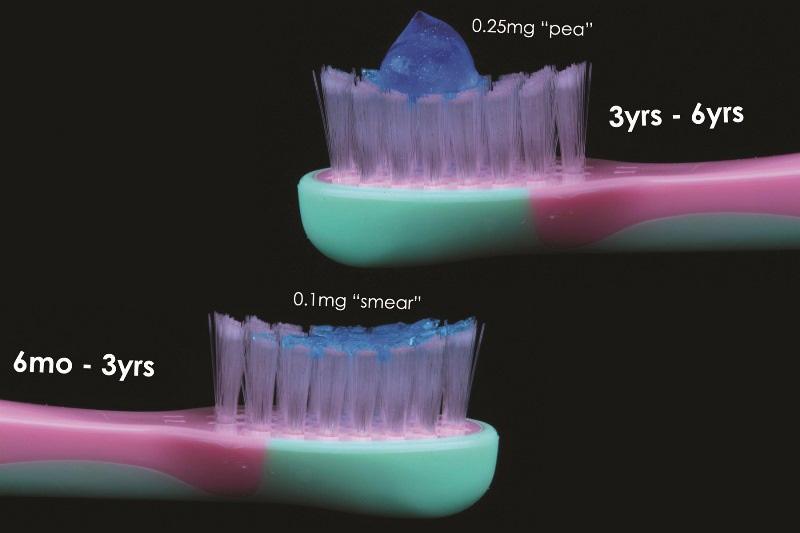
При фторировании воды на уровне 0,7 ppm частота заметного флюороза составляет 12%, а флюороза любой степени — 40%. Рекомендуемая доза общего потребляемого фторида составляет менее 0,05 мг/кг массы тела, так как это снижает риск флюороза. Концентрация фторидов в детских зубных пастах в США такая же, как и во взрослых. Поэтому для маленьких детей рекомендуется использовать меньшее количество пасты из-за их небольшого веса и неспособности полностью выплевывать пасту после чистки. Таким образом, для детей в возрасте от 6 месяцев до 3 лет рекомендуется количество пасты размером с рисовое зерно (0,10 мг), а для детей от 3 до 6 лет — размером с горошину (0,25 мг) (Фото 1).
Фото 1: Рекомендуемые дозы фторсодержащей зубной пасты для детей до 6 лет.
При более высоких дозах фторидов возникают опасения по поводу токсичности. К распространенным симптомам острой фторидной токсичности относятся боль в животе, рвота, диарея и головная боль. Более высокие дозы могут вызвать проблемы с центральной нервной системой, включая судороги и тетанию. Доза 5 мг/кг считается потенциально токсичной, а 15 мг/кг — смертельной. Точная смертельная доза трудно определима, так как она основана на трех случаях, где летальная доза варьировалась от 3,1 мг/кг до 35 мг/кг.
Другие возможные негативные системные эффекты фторидов включают скелетный флюороз (из-за связывания фторидов с кальцием в костях) и снижение коэффициента интеллекта (IQ). Однако такие последствия наблюдаются в регионах с очень высоким содержанием фторидов в питьевой воде. Недавний отчет Национальной программы по токсикологии (NTP) оценил связь между IQ и уровнем фторидов в воде в сообществах за пределами США с естественно повышенным содержанием фторидов. В отчете указано, что фторированная вода с концентрацией более 1,5 ppm ассоциировалась с более низким IQ у детей. Метаанализ исследований, где уровни фторидов соответствовали общепринятым нормам, а не эндемическим, не выявил связи с IQ детей. Совсем недавно был опубликован метаанализ из отчета NTP, который заключил, что фторированная вода не ассоциировалась со снижением IQ при уровнях ниже 1,5 ppm, за исключением случаев, когда рассматривались только исследования с низким риском систематической ошибки (n = 3). Исследования с низким риском ошибки подразумевали уверенность в способности измерять влияние мешающих факторов (например, других экологических факторов), точность измерений уровня фторидов и результатов. Для определения причинно-следственной связи между воздействием фторидов и IQ необходимы интервенционные исследования, которые позволят лучше контролировать мешающие факторы. Еще одним важным моментом является то, что величина снижения IQ, предложенная в анализе исследований с низким риском ошибки, составляла 1,14 пункта на каждые 1 мг/л увеличения концентрации фторидов в моче. Для справки, концентрация фторидов в моче 0,28 мг/л соответствует концентрации фторидов в воде 0,7 ppm.
Доказательства эффективности зубных паст с гидроксиапатитом
В настоящее время единственными соединениями, упомянутыми в монографии Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) США в отношении антикариесных препаратов и имеющих право на маркировку «антикариес» с печатью Американской стоматологической ассоциации, являются монофторфосфат натрия, фторид натрия и фторид олова. В Японии бывшее Министерство здравоохранения и благосостояния одобрило «медицинский гидроксиапатит» из-за его антикариозных эффектов, включая: (1) удаление зубного налета, (2) заполнение поверхностных дефектов зуба и (3) реминерализацию подповерхностных поражений. Утверждение о заполнении поверхностных дефектов подтверждается лабораторными исследованиями, в которых с помощью сканирующей электронной микроскопии (СЭМ) было показано заполнение пор в эмали Реминерализация подповерхностных поражений демонстрируется в лабораторных и in situ исследованиях с использованием микротвердости, поляризационной микроскопии или микрорентгенографии.
Хотя лабораторные исследования показали пользу гидроксиапатита для реминерализации, лишь несколько клинических испытаний оценили эффективность зубных паст с гидроксиапатитом для лечения кариеса. Недавние систематические обзоры обобщили клинические испытания зубных паст с гидроксиапатитом в отношении кариеса. Некоторые исследования изучали профилактику кариеса (частоту новых кариозных поражений), а другие — реминерализацию (улучшение состояния имеющихся поражений). В обзоре три исследования сравнивали профилактическую эффективность гидроксиапатитной зубной пасты с фторсодержащей пастой (контроль). Исследования оценивали прогрессирование кариеса в течение 6, 12 или 18 месяцев и пришли к выводу, что статистически значимых различий между гидроксиапатитной и фторсодержащей пастой не обнаружено. Другое исследование показало улучшение прогрессирования кариеса по сравнению с плацебо без фторидов. В пяти других исследованиях сообщили о реминерализации начальных поражений с использованием гидроксиапатитной пасты, причем в четырех из них она была более эффективна, чем фторсодержащий контроль. Результаты исследований, представленных в обзорах, указывают на то, что нет доказательств превосходства гидроксиапатита над фторидами в профилактике новых кариозных поражений. Небольшой срок наблюдения и ограниченное количество исследований с гидроксиапатитными пастами свидетельствуют о необходимости дальнейших исследований, прежде чем можно будет утверждать об их эквивалентной профилактической эффективности. Гидроксиапатитные пасты не способны снижать растворимость кристаллов твердых тканей зуба, как фториды, что может ограничивать их способность предотвращать новые кариозные поражения. Их основное преимущество может заключаться в реминерализации начальных поражений.
Гидроксиапатит в зубных пастах классифицируется как микрогидроксиапатит или наногидроксиапатит. Исследование in vitro показало, что наногидроксиапатит более эффективен в высвобождении кальция и фосфатов, а также в восстановлении поверхностной твердости деминерализованной эмали, чем микрогидроксиапатит. Меньший размер наногидроксиапатита позволяет ему лучше проникать в дефекты эмали по сравнению с более крупным микрогидроксиапатитом. Однако клинические испытания, показавшие эквивалентность фторсодержащим пастам, использовали микрогидроксиапатитные пасты. Концентрация гидроксиапатита — еще один фактор, отличающий зубные пасты. Одно лабораторное исследование показало, что 10% раствор наногидроксиапатита реминерализировал коровьи зубы лучше, чем 1% или 5% растворы. Это исследование стало основанием для некоторых производителей утверждать, что эффективной дозой является содержание наногидроксиапатита в 10%. Распространенным источником наногидроксиапатита для паст является производитель, поставляющий его в виде 15% водной суспензии. . Внутреннее исследование этого производителя показало, что суспензия с 12% обеспечивает оптимальное покрытие поверхностных пор эмали, что соответствует конечной концентрации 1,8% наногидроксиапатита.
Из-за малого размера кристаллов наногидроксиапатита (<100 нм) возникают опасения по поводу безопасности. Европейский научный комитет по безопасности потребителей оценил наногидроксиапатит, используемый в 15% водном растворе. В отчете комитета за 2022 год указано, что стержнеобразный наногидроксиапатит проникает только в самый внешний слой клеток буккального эпителия и растворяется в желудке, поэтому не ожидается его системного распространения. Он не является цитотоксичным для эпителиальных или слизистых клеток, имеет минимальное поглощение клетками и не вызывает мутаций генов. В отчете особо подчеркивается, что эти результаты не применимы к игольчатому наногидроксиапатиту, который показал системные эффекты после кожного нанесения, а также клеточное поглощение, повреждение клеток и генотоксический потенциал.
Гидроксиапатные пасты обычно представлены в виде продуктов без фторидов для пациентов, избегающих фторидов, или детей с риском флюороза из-за проглатывания пасты. Однако некоторые бренды паст содержат и гидроксиапатит, и фториды. Систематический обзор сравнил четыре клинических испытания и одно in situ исследование, оценивавшие способность паст с гидроксиапатитом и фторидами реминерализировать существующие поражения. Из клинических испытаний только одно сравнивало чистку зубов пастой с гидроксиапатитом и фторидами с пастой, содержащей только фториды. Это исследование не выявило различий в способности к реминерализации между пастой с гидроксиапатитом и фторидами и пастой только с фторидами. Исследование in situ показало, что паста с гидроксиапатитом и фторидами реминерализировала удаленные зубы лучше, чем паста только с фторидами. Эти результаты позволяют предположить, что в настоящее время нет достаточных доказательств пользы добавления гидроксиапатита к фторсодержащим пастам.
Антимикробные средства для лечения кариеса
Для лечения кариеса предлагалось несколько антимикробных агентов, включая ксилит, повидон-йод, хлоргексидин, серебро, гипохлорит натрия и цетилпиридиния хлорид.
Ксилит — это неферментируемый сахарный спирт, который может использоваться в качестве заменителя сахара. Он также обладает механизмами антикариозного действия. Streptococcus mutans метаболизирует ксилит в ксилит-5-фосфат, что снижает количество глюкозы, которую бактерии могут превращать в молочную кислоту. Этот процесс также заставляет S. mutans тратить энергию впустую, что тормозит его рост. Хотя могут развиваться устойчивые к ксилиту штаммы S. mutans, они могут иметь сниженную способность прикрепляться к тканям зуба.
Политика Американской академии детской стоматологии 2024 года в отношении ксилита указывает на отсутствие доказательств его профилактического действия против кариеса и озабоченность по поводу необходимой дозы/частоты применения. Кокрейновский обзор использования ксилита для профилактики кариеса позволяет сделать вывод, что недостаточно доказательств для определения, могут ли продукты с ксилитом предотвращать кариес у детей или взрослых. Несмотря на это, клинические испытания показали пользу ксилита для профилактики кариеса. Систематический обзор 10 клинических испытаний показал, что в четырех исследованиях, где использовался ксилит в дозе 4,3–10,7 г/день, наблюдалось значительное снижение кариеса, тогда как в трех исследованиях с дозой 2,5–2,9 г/день значительных различий не было. Два исследования показали, что добавление 10% ксилита в зубную пасту снижает частоту возникновения новых кариозных поражений. Эти исследования позволяют предположить, что эффективность ксилита зависит от дозы, и для антикариесного эффекта рекомендуется доза 5–6 г/день. Жевательная резинка и леденцы — распространенные способы доставки ксилита, причем некоторые бренды содержат около 1 г/штуку. Однако некоторые жевательные резинки с ксилитом содержат всего 0,06–0,17 г/штуку (Фото 2).
Фото 2: Количество жевательных резинок с разной концентрацией ксилита, необходимых для достижения 5 г ксилита.

С ксилитом связаны некоторые проблемы со здоровьем. Доза 20–70 г/день может вызвать осмотическую диарею. Недавнее исследование показало повышенный риск сердечно-сосудистых событий у пациентов с повышенным уровнем ксилита в плазме. Исследование измеряло уровень ксилита в плазме натощак, что предполагает связь сердечно-сосудистого риска с эндогенным ксилитом, а не с пищевым. Также было указано, что потребление 30 г ксилита увеличивает свертываемость крови на несколько часов, однако эта доза значительно превышает рекомендуемую для контроля кариеса. Стоит отметить, что ксилит может быть смертельно опасен для собак: дозы >0,1 г/кг могут вызвать гипогликемию, а >0,5 г/кг — острую печеночную недостаточность.
Повидон-йод вызывает лизис клеточной стенки и инактивацию белков и нуклеотидов у кариесогенных бактерий. Кроме того, он ингибирует синтез глюканов — липких полимеров, которые помогают бактериям прикрепляться к зубам. Клинические испытания показали, что нанесение повидон-йода на зубы может снижать количество S. mutans в слюне, на проксимальных и окклюзионных поверхностях зубов в течение до 24 недель. Использование повидон-йода перед нанесением фторидного лака в клинических испытаниях у детей младшего возраста показало значительное снижение нового кариеса по сравнению с одним фторидным лаком. В клинической практике рекомендуется наносить 8 капель (около 0,45 мл) 10% повидон-йода на сухие зубы каждые 2–3 месяца (Фото 3). Эту процедуру пациент может выполнять дома, доступен коммерческий продукт — флаконы с 0,45 мл 10% повидон-йода.
Фото 3: Протокол нанесения повидон-йода.

Хлоргексидин — это антимикробный агент, который убивает бактерии, разрушая их клеточные стенки. Хотя хлоргексидин может снижать уровень S. mutans в слюне, несколько исследований не показали снижения частоты кариеса при использовании 0,12% ополаскивателя с хлоргексидином, который доступен по рецепту в США. Существуют опасения по поводу 0,12% ополаскивателей с хлоргексидином, так как они могут снижать количество нитратредуцирующих бактерий, которые уменьшают уровень молочной кислоты (улучшают pH полости рта) и производят оксид азота (улучшают здоровье сердечно-сосудистой системы). В ополаскиватели могут включаться и другие антимикробные агенты, такие как серебро, гипохлорит натрия и цетилпиридиния хлорид. Хотя эти агенты демонстрируют антибактериальную активность против S. mutans, клинических доказательств их антикариесного действия в настоящее время недостаточно.
Диагностика начальных поражений
Когда профилактика кариозных поражений оказывается неудачной и образуются начальные поражения, минимально инвазивное лечение может помочь продлить срок службы зуба и избежать более инвазивных методов восстановления. Выявление таких поражений требует тщательного осмотра зубов, и для их обнаружения могут использоваться несколько диагностических инструментов. Инструменты для диагностики кариеса можно разделить на те, которые используют излучение, и те, которые используют свет.
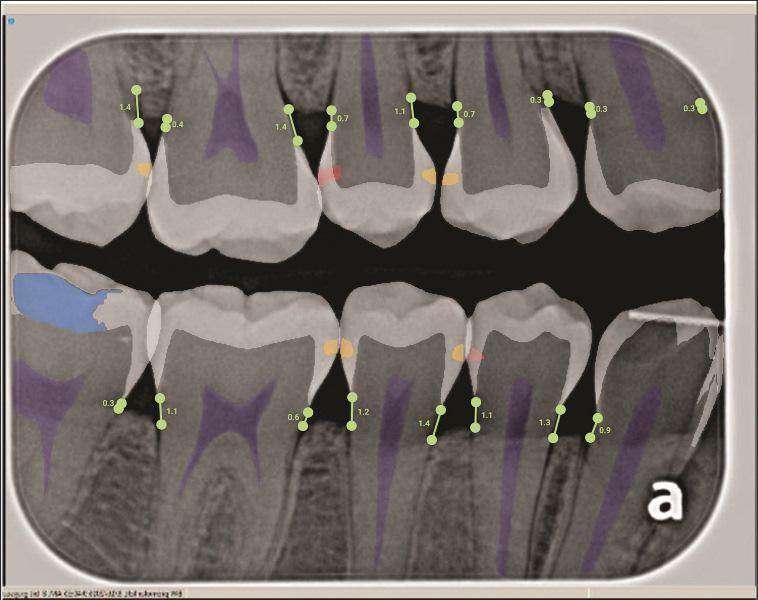
Радиационные методы диагностики кариеса (например, рентген) являются стандартом в стоматологической практике. Новшеством в радиационной диагностике является программное обеспечение на основе искусственного интеллекта (ИИ), которое может накладывать цветовые маркеры на цифровые рентгеновские снимки, указывая на участки рентгенопрозрачности, характерные для деминерализации и кариеса (Фото 4). Чувствительность (истинно положительные результаты) ИИ по сравнению с заключением экспертов составляет 73–90%, а специфичность (истинно отрицательные результаты) — 61,5–93%. Таким образом, ИИ — это лишь инструмент, помогающий стоматологу выявить потенциальные поражения. Анализ ИИ наиболее полезен для повышения чувствительности при выявлении кариеса эмали. Исследование показало, что использование ИИ для диагностики кариеса эмали увеличивает применение профилактических методов, но также повышает частоту инвазивного лечения.
Фото 4: Обнаружение кариеса с помощью искусственного интеллекта (ИИ), демонстрирующее несколько начальных поражений эмали.
Методы диагностики кариеса, использующие свет, можно разделить на те, которые применяют трансиллюминацию, светоиндуцированную флуоресценцию или лазероиндуцированную флуоресценцию. Трансиллюминация ближним инфракрасным светом работает за счет того, что более пористая кариозная эмаль поглощает больше света и выглядит темнее. Эта технология хорошо визуализирует кариес по всему зубу, но не может различить кариозные поражения и изменения контраста минерализованных тканей, вызванные другими причинами (например, флюорозом). Кариозные ткани зуба обладают иными флуоресцентными свойствами, чем здоровые. Светоиндуцированная флуоресценция основана на том, что кариозные поражения поглощают свет коротких волн и переизлучают свет с большей длиной волны. Эта технология не визуализирует проксимальные поверхности зубов и не дифференцирует активность кариозных поражений. Лазероиндуцированная флуоресценция возникает при активации протопорфирина — фотосенситивного пигмента, который является метаболическим продуктом кариесогенных бактерий. Таким образом, эта технология, как утверждается, определяет активность кариеса. Она не предоставляет визуальной карты кариеса, как другие методы, а генерирует число, указывающее на его тяжесть.
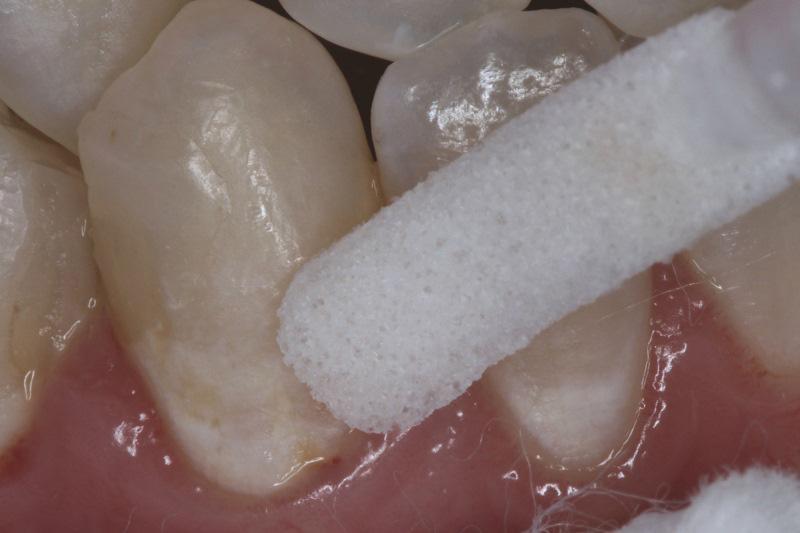
Малые молекулы также могут использоваться для визуального выявления начальных поражений. Один коммерческий продукт содержит отрицательно заряженные наночастицы крахмала (100 нм), которые избирательно связываются с кариозной эмалью. Они помечены флуоресцентным маркером, который светится при освещении стоматологической лампой (Фото 5). Другой продукт содержит краситель на основе гемоглобина, который связывается с обнаженным гидроксиапатитом в порах подповерхностной эмали. Окрашивание видно при обычном освещении.
Фото 5: Флуоресцентные заряженные наночастицы крахмала для выявления начальных поражений.

Минимально инвазивное лечение начальных поражений
Современные стратегии реминерализации или восстановления начальных поражений включают самособирающиеся пептиды, пасты с казеинфосфопептидом-аморфным фосфатом кальция и инфильтрацию композитом. Использование серебра диаминфторида (СДФ) — еще один минимально инвазивный метод остановки кариеса, который обычно используется для поражений с образовавшейся полостью. Однако есть некоторые доказательства того, что СДФ может замедлять прогрессирование начальных, межзубных и окклюзионных поражений без полости.
Матрикс эмали присутствует во время одонтогенеза, способствуя формированию кристаллов гидроксиапатита, но отсутствует в зрелом зубе. Новый подход к реминерализации начальных поражений заключается в создании искусственного самособирающегося пептида, который служит каркасом, имитирующим функцию матрикса эмали (Фото 6). P11-4 — это пептид, способный самособираться в ленты с участками связывания ионов кальция. Расстояние между этими участками соответствует межатомному расстоянию между столбцами кальция в кристалле гидроксиапатита. Было показано, что эти пептиды проникают в подповерхностную деминерализацию и индуцируют реминерализацию. Клинические испытания коммерческого продукта с самособирающимися пептидами P11-4 показали эффективность в остановке поражений и уменьшении их размера. Лечение показало положительные результаты как для гладких поверхностей, так и для межзубных поражений.
Фото 6: Препарат с самособирающимися пептидами P11-4, используемый для лечения начального поражения на вестибулярной поверхности.
Другая стратегия лечения — обеспечение биодоступного кальция и фосфатов для реминерализации дефектов эмали и подповерхностных поражений. Проблема реминерализации кальций-фосфатными препаратами заключается в их низкой растворимости в слюне. Если кальций и фосфаты находятся в твердой фазе, они не биодоступны для реминерализации. Кальций-фосфатные соединения могут добавляться в кристаллической форме (например, трикальцийфосфат или биоактивное стекло) или в аморфной форме (например, аморфный фосфат кальция [АФК]). Аморфная форма, обладая менее упорядоченной структурой, более растворима, чем кристаллическая. Для повышения растворимости и биодоступности АФК его можно связать со стабилизирующим белком, например, казеином из молока. Фосфопептиды в казеине содержат участки, способные слабо связываться с кальцием и фосфатами, предотвращая их кристаллизацию и осаждение. Кроме того, эти участки могут связываться с кальцием в поврежденной эмали, поэтому пептиды могут "доставлять" кальций и фосфаты из слюны к зубу. В продаже имеются коммерческие продукты, содержащие комплексы казеинфосфопептида со стабилизированным аморфным фосфатом кальция (КФП-АФК), а также казеинфосфопептида со стабилизированным аморфным фторидом фосфата кальция (КФП-АФФК) в виде паст, жевательных резинок и лаков. Доказательства клинической пользы паст с КФП-АФК по сравнению с фторсодержащими пастами для профилактики новых поражений сомнительны, однако есть некоторые данные о пользе КФП-АФК для реминерализации начальных поражений. КФП-АФФК не показал клинических преимуществ перед КФП-АФК или фторсодержащими пастами для реминерализации.
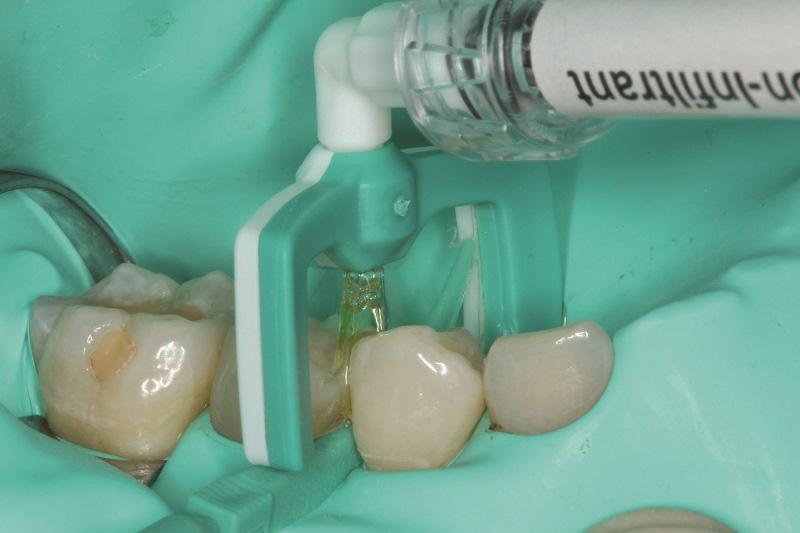
Инфильтрация композитом — это метод лечения начального кариеса путем проникновения ненаполненного композитного материала через поверхностные поры в подповерхностные поражения на вестибулярных и межзубных поверхностях (Фото 7). Хотя эта методика не является формой реминерализации, клинические испытания показали, что инфильтрация смолой может останавливать некавитированные кариозные поражения.
Фото 7: Инфильтрация композитом, используемая для лечения начального межзубного поражения.
Вывод
Фториды остаются основой профилактики, так как их включение в кристаллы апатита обеспечивает устойчивость к последующему кислотному разрушению. Пациенты, обеспокоенные флюорозом или потенциальными проблемами со здоровьем, связанными с фторидами, могут рассмотреть зубные пасты с гидроксиапатитом, хотя доказательств их способности предотвращать новые кариозные поражения недостаточно. Инновации в диагностике кариеса, включая ИИ, световые методы и малые молекулы, помогают в раннем выявлении начальных поражений. Стратегии реминерализации, такие как гидроксиапатит, самособирающиеся пептиды или КФП-АФК, предлагают перспективные варианты для начальных поражений. Антибактериальные продукты могут помочь в лечении пациентов с факторами риска кариеса. Наконец, план управления риском кариеса должен учитывать готовность пациента участвовать в снижении факторов риска, изменяя диету и гигиенические привычки.
Автор: Nathaniel C. Lawson, DMD, PhD
Профилактика кариеса и реминерализация эмали — два важнейших аспекта здоровья полости рта, требующие комплексного подхода. Стратегии профилактики снижают риск возникновения новых кариозных поражений, тогда как методы реминерализации направлены на восстановление минерального состава уже пораженных твердых тканей на ранних стадиях. Фториды в различных формах (фторирование воды, зубные пасты, ополаскиватели, лаки и каппы) способны предотвращать кариес и реминерализировать пораженные ткани, однако их избыточное применение может иметь негативные последствия для здоровья. Доказательства эффективности гидроксиапатита, добавляемого в некоторые зубные пасты, ограничены, он он может обладать свойствами, способствующими реминерализации. Кроме того, антимикробные средства снижают количество кариесогенных бактерий, что может замедлять развитие и прогрессирование кариеса. Неинвазивные методы реминерализации или восстановления начальных поражений предлагают консервативные варианты лечения.

Фториды для профилактики кариеса
Фториды помогают предотвращать развитие кариеса, повышая устойчивость эмали к потере минералов в кислой среде. Эмаль состоит из минерала гидроксиапатита — Ca10(PO4)6(OH)2. В присутствии фторидов при реминерализации ионы фтора могут включаться в структуру этого минерала, образуя фторапатит (Ca10(PO4)6(OH)(2-x)F) в твердых тканях зуба. Замена гидроксильных групп (-OH) в гидроксиапатите на меньшие по размеру ионы фтора во фторапатите приводит к образованию более плотной кристаллической решетки. Эти более компактные кристаллы обладают повышенной устойчивостью к деминерализации в условиях низкого значения pH. Электростатические силы между противоположно заряженными ионами усиливаются на меньших расстояниях, поэтому фторапатит имеет более высокую силу притяжения между ионами и меньшую растворимость.
В начале 20 века в Колорадо-Спрингс, штат Колорадо, было замечено, что люди, пившие воду с природным фтором, реже страдали от кариеса. Это стало первым открытием положительного влияния фторидов на устойчивость зубов к кариесу. Доказательства целенаправленного использования фторидов для профилактики кариеса относятся к 1940-м годам, когда в Гранд-Рапидс, штат Мичиган, была запущена программа фторирования питьевой воды. та инициатива привела к значительному снижению индекса КПУ (количество пораженных, отсутствующих и запломбированных зубов) у детей через 10 лет после внедрения программы. После внедрения фторирования питьевой воды (ФПВ) его польза была поставлена под сомнение из-за широкого распространения фторсодержащих средств гигиены полости рта, появившихся около 1975 года. Обновленный обзор Кохрейна показал, что улучшение индекса КПУ после введения ФПВ в исследованиях после 1975 года было менее выраженным, чем в исследованиях до 1975 года. Предполагается, что ФПВ по-прежнему полезно для людей, не имеющих доступа к фторсодержащим гигиеническим средствам. Однако в обзоре не было обнаружено достаточных доказательств того, что отмена ФПВ увеличивает разрыв в уровнях кариеса между социально-экономическими группами. Тем не менее, результаты свидетельствуют, что ФПВ сохраняет пользу для общественного здоровья, несмотря на снижение эффекта после распространения фторсодержащих зубных паст.
Фторид содержится в безрецептурных зубных пастах в концентрации 1000 частей на миллион (ppm) и в рецептурных пастах — до 5000 ppm, тогда как в питьевой воде его концентрация составляет 0,7–1 ppm. Использование паст с высокой концентрацией фторида приводит к увеличению его уровня в слюне в течение нескольких часов после чистки. Помимо зубных паст, фторид присутствует в других профилактических продуктах, таких как ополаскиватели, лаки и каппы.
Фторид может входить в состав безрецептурных ополаскивателей в форме 0,02–0,05% фторида натрия (92–230 ppm) или в состав рецептурных ополаскивателей — 0,2% фторида натрия (900 ppm). Согласно Кохрейновскому обзору, использование фторсодержащих ополаскивателей снижает индекс КПУ на 23% (при этом разницы между концентрациями 0,05% и 0,2% не выявлено). Однако они отметили, что это утверждение не основано на исследованиях, сравнивающих использование фторсодержащих зубных паст и ополаскивателей в рамках одного исследования, а классификация исследований с учетом фонового воздействия фторидов часто основывалась на рыночных предположениях. Клинические испытания, в которых сравнивали ополаскиватель с 0,05% фторида натрия и зубную пасту в одном исследовании, показали, что дополнительной пользы в профилактике кариеса при совместном использовании ополаскивателя и пасты не наблюдается. Однако ополаскиватель снижал частоту кариеса, если фторсодержащая зубная паста не использовалась. Таким образом, фторсодержащие ополаскиватели могут быть полезны для пациентов, которые не могут качественно чистить зубы из-за недостаточной мотивации или моторных навыков. Еще одним фактором является то, что концентрация фторидов в ополаскивателях ниже, чем в зубных пастах. Использование ополаскивателя без фторидов после чистки зубов пастой с 1000 ppm фторидов или ополаскивателя с 230 ppm фторидов после пасты с 5000 ppm фторидов снижает концентрацию фторидов в слюне. Поэтому таким пациентам рекомендуется сначала использовать ополаскиватель, а затем чистить зубы.
Фторидные лаки обычно содержат 5% фторида натрия (22 600 ppm). В крупном систематическом обзоре и метаанализе 13 исследований было показано, что использование фторидного лака снижает индекс КПУ на 43% у подростков с постоянными зубами. Исследования на взрослых не проводились, однако предполагается, что фторидные лаки также эффективны для профилактики кариеса у взрослых. Механизм действия высоких концентраций фторидов заключается в образовании глобул фторида кальция на поверхности эмали после применения. Эти глобулы относительно нерастворимы при нейтральном pH и могут оставаться на зубах в течение нескольких месяцев после нанесения. При снижении pH фторид кальция растворяется и способствует реминерализации тканей зуба фторапатитом.
Фторидные каппы стали стандартным методом лечения пациентов с ксеростомией после лучевой терапии. Рекомендуется использовать 0,4% фторид олова (1000 ppm) в каппах ежедневно в течение 5 минут. Этот метод основан на клиническом исследовании 1977 года, в котором сообщалось о частоте возникновения кариеса 0,16 КПУ/месяц при использовании капп и 2,51 КПУ/месяц — без них у пациентов с лучевой ксеростомией. Помимо повышения воздействия фторидов, пациенты с ксеростомией могут также получить пользу от использования буферных агентов, так как у них отсутствует бикарбонатный буфер, содержащийся в слюне. Для повышения pH слюны можно использовать воду с пищевой содой или другие продукты, содержащие бикарбонат натрия.
Проблемы здоровья, связанные с употреблением фторидов
При фторировании воды на уровне 0,7 ppm частота заметного флюороза составляет 12%, а флюороза любой степени — 40%. Рекомендуемая доза общего потребляемого фторида составляет менее 0,05 мг/кг массы тела, так как это снижает риск флюороза. Концентрация фторидов в детских зубных пастах в США такая же, как и во взрослых. Поэтому для маленьких детей рекомендуется использовать меньшее количество пасты из-за их небольшого веса и неспособности полностью выплевывать пасту после чистки. Таким образом, для детей в возрасте от 6 месяцев до 3 лет рекомендуется количество пасты размером с рисовое зерно (0,10 мг), а для детей от 3 до 6 лет — размером с горошину (0,25 мг) (Фото 1).
Фото 1: Рекомендуемые дозы фторсодержащей зубной пасты для детей до 6 лет.

При более высоких дозах фторидов возникают опасения по поводу токсичности. К распространенным симптомам острой фторидной токсичности относятся боль в животе, рвота, диарея и головная боль. Более высокие дозы могут вызвать проблемы с центральной нервной системой, включая судороги и тетанию. Доза 5 мг/кг считается потенциально токсичной, а 15 мг/кг — смертельной. Точная смертельная доза трудно определима, так как она основана на трех случаях, где летальная доза варьировалась от 3,1 мг/кг до 35 мг/кг.
Другие возможные негативные системные эффекты фторидов включают скелетный флюороз (из-за связывания фторидов с кальцием в костях) и снижение коэффициента интеллекта (IQ). Однако такие последствия наблюдаются в регионах с очень высоким содержанием фторидов в питьевой воде. Недавний отчет Национальной программы по токсикологии (NTP) оценил связь между IQ и уровнем фторидов в воде в сообществах за пределами США с естественно повышенным содержанием фторидов. В отчете указано, что фторированная вода с концентрацией более 1,5 ppm ассоциировалась с более низким IQ у детей. Метаанализ исследований, где уровни фторидов соответствовали общепринятым нормам, а не эндемическим, не выявил связи с IQ детей. Совсем недавно был опубликован метаанализ из отчета NTP, который заключил, что фторированная вода не ассоциировалась со снижением IQ при уровнях ниже 1,5 ppm, за исключением случаев, когда рассматривались только исследования с низким риском систематической ошибки (n = 3). Исследования с низким риском ошибки подразумевали уверенность в способности измерять влияние мешающих факторов (например, других экологических факторов), точность измерений уровня фторидов и результатов. Для определения причинно-следственной связи между воздействием фторидов и IQ необходимы интервенционные исследования, которые позволят лучше контролировать мешающие факторы. Еще одним важным моментом является то, что величина снижения IQ, предложенная в анализе исследований с низким риском ошибки, составляла 1,14 пункта на каждые 1 мг/л увеличения концентрации фторидов в моче. Для справки, концентрация фторидов в моче 0,28 мг/л соответствует концентрации фторидов в воде 0,7 ppm.
Доказательства эффективности зубных паст с гидроксиапатитом
В настоящее время единственными соединениями, упомянутыми в монографии Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) США в отношении антикариесных препаратов и имеющих право на маркировку «антикариес» с печатью Американской стоматологической ассоциации, являются монофторфосфат натрия, фторид натрия и фторид олова. В Японии бывшее Министерство здравоохранения и благосостояния одобрило «медицинский гидроксиапатит» из-за его антикариозных эффектов, включая: (1) удаление зубного налета, (2) заполнение поверхностных дефектов зуба и (3) реминерализацию подповерхностных поражений. Утверждение о заполнении поверхностных дефектов подтверждается лабораторными исследованиями, в которых с помощью сканирующей электронной микроскопии (СЭМ) было показано заполнение пор в эмали Реминерализация подповерхностных поражений демонстрируется в лабораторных и in situ исследованиях с использованием микротвердости, поляризационной микроскопии или микрорентгенографии.
Хотя лабораторные исследования показали пользу гидроксиапатита для реминерализации, лишь несколько клинических испытаний оценили эффективность зубных паст с гидроксиапатитом для лечения кариеса. Недавние систематические обзоры обобщили клинические испытания зубных паст с гидроксиапатитом в отношении кариеса. Некоторые исследования изучали профилактику кариеса (частоту новых кариозных поражений), а другие — реминерализацию (улучшение состояния имеющихся поражений). В обзоре три исследования сравнивали профилактическую эффективность гидроксиапатитной зубной пасты с фторсодержащей пастой (контроль). Исследования оценивали прогрессирование кариеса в течение 6, 12 или 18 месяцев и пришли к выводу, что статистически значимых различий между гидроксиапатитной и фторсодержащей пастой не обнаружено. Другое исследование показало улучшение прогрессирования кариеса по сравнению с плацебо без фторидов. В пяти других исследованиях сообщили о реминерализации начальных поражений с использованием гидроксиапатитной пасты, причем в четырех из них она была более эффективна, чем фторсодержащий контроль. Результаты исследований, представленных в обзорах, указывают на то, что нет доказательств превосходства гидроксиапатита над фторидами в профилактике новых кариозных поражений. Небольшой срок наблюдения и ограниченное количество исследований с гидроксиапатитными пастами свидетельствуют о необходимости дальнейших исследований, прежде чем можно будет утверждать об их эквивалентной профилактической эффективности. Гидроксиапатитные пасты не способны снижать растворимость кристаллов твердых тканей зуба, как фториды, что может ограничивать их способность предотвращать новые кариозные поражения. Их основное преимущество может заключаться в реминерализации начальных поражений.
Гидроксиапатит в зубных пастах классифицируется как микрогидроксиапатит или наногидроксиапатит. Исследование in vitro показало, что наногидроксиапатит более эффективен в высвобождении кальция и фосфатов, а также в восстановлении поверхностной твердости деминерализованной эмали, чем микрогидроксиапатит. Меньший размер наногидроксиапатита позволяет ему лучше проникать в дефекты эмали по сравнению с более крупным микрогидроксиапатитом. Однако клинические испытания, показавшие эквивалентность фторсодержащим пастам, использовали микрогидроксиапатитные пасты. Концентрация гидроксиапатита — еще один фактор, отличающий зубные пасты. Одно лабораторное исследование показало, что 10% раствор наногидроксиапатита реминерализировал коровьи зубы лучше, чем 1% или 5% растворы. Это исследование стало основанием для некоторых производителей утверждать, что эффективной дозой является содержание наногидроксиапатита в 10%. Распространенным источником наногидроксиапатита для паст является производитель, поставляющий его в виде 15% водной суспензии. . Внутреннее исследование этого производителя показало, что суспензия с 12% обеспечивает оптимальное покрытие поверхностных пор эмали, что соответствует конечной концентрации 1,8% наногидроксиапатита.
Из-за малого размера кристаллов наногидроксиапатита (<100 нм) возникают опасения по поводу безопасности. Европейский научный комитет по безопасности потребителей оценил наногидроксиапатит, используемый в 15% водном растворе. В отчете комитета за 2022 год указано, что стержнеобразный наногидроксиапатит проникает только в самый внешний слой клеток буккального эпителия и растворяется в желудке, поэтому не ожидается его системного распространения. Он не является цитотоксичным для эпителиальных или слизистых клеток, имеет минимальное поглощение клетками и не вызывает мутаций генов. В отчете особо подчеркивается, что эти результаты не применимы к игольчатому наногидроксиапатиту, который показал системные эффекты после кожного нанесения, а также клеточное поглощение, повреждение клеток и генотоксический потенциал.
Гидроксиапатные пасты обычно представлены в виде продуктов без фторидов для пациентов, избегающих фторидов, или детей с риском флюороза из-за проглатывания пасты. Однако некоторые бренды паст содержат и гидроксиапатит, и фториды. Систематический обзор сравнил четыре клинических испытания и одно in situ исследование, оценивавшие способность паст с гидроксиапатитом и фторидами реминерализировать существующие поражения. Из клинических испытаний только одно сравнивало чистку зубов пастой с гидроксиапатитом и фторидами с пастой, содержащей только фториды. Это исследование не выявило различий в способности к реминерализации между пастой с гидроксиапатитом и фторидами и пастой только с фторидами. Исследование in situ показало, что паста с гидроксиапатитом и фторидами реминерализировала удаленные зубы лучше, чем паста только с фторидами. Эти результаты позволяют предположить, что в настоящее время нет достаточных доказательств пользы добавления гидроксиапатита к фторсодержащим пастам.
Антимикробные средства для лечения кариеса
Для лечения кариеса предлагалось несколько антимикробных агентов, включая ксилит, повидон-йод, хлоргексидин, серебро, гипохлорит натрия и цетилпиридиния хлорид.
Ксилит — это неферментируемый сахарный спирт, который может использоваться в качестве заменителя сахара. Он также обладает механизмами антикариозного действия. Streptococcus mutans метаболизирует ксилит в ксилит-5-фосфат, что снижает количество глюкозы, которую бактерии могут превращать в молочную кислоту. Этот процесс также заставляет S. mutans тратить энергию впустую, что тормозит его рост. Хотя могут развиваться устойчивые к ксилиту штаммы S. mutans, они могут иметь сниженную способность прикрепляться к тканям зуба.
Политика Американской академии детской стоматологии 2024 года в отношении ксилита указывает на отсутствие доказательств его профилактического действия против кариеса и озабоченность по поводу необходимой дозы/частоты применения. Кокрейновский обзор использования ксилита для профилактики кариеса позволяет сделать вывод, что недостаточно доказательств для определения, могут ли продукты с ксилитом предотвращать кариес у детей или взрослых. Несмотря на это, клинические испытания показали пользу ксилита для профилактики кариеса. Систематический обзор 10 клинических испытаний показал, что в четырех исследованиях, где использовался ксилит в дозе 4,3–10,7 г/день, наблюдалось значительное снижение кариеса, тогда как в трех исследованиях с дозой 2,5–2,9 г/день значительных различий не было. Два исследования показали, что добавление 10% ксилита в зубную пасту снижает частоту возникновения новых кариозных поражений. Эти исследования позволяют предположить, что эффективность ксилита зависит от дозы, и для антикариесного эффекта рекомендуется доза 5–6 г/день. Жевательная резинка и леденцы — распространенные способы доставки ксилита, причем некоторые бренды содержат около 1 г/штуку. Однако некоторые жевательные резинки с ксилитом содержат всего 0,06–0,17 г/штуку (Фото 2).
Фото 2: Количество жевательных резинок с разной концентрацией ксилита, необходимых для достижения 5 г ксилита.

С ксилитом связаны некоторые проблемы со здоровьем. Доза 20–70 г/день может вызвать осмотическую диарею. Недавнее исследование показало повышенный риск сердечно-сосудистых событий у пациентов с повышенным уровнем ксилита в плазме. Исследование измеряло уровень ксилита в плазме натощак, что предполагает связь сердечно-сосудистого риска с эндогенным ксилитом, а не с пищевым. Также было указано, что потребление 30 г ксилита увеличивает свертываемость крови на несколько часов, однако эта доза значительно превышает рекомендуемую для контроля кариеса. Стоит отметить, что ксилит может быть смертельно опасен для собак: дозы >0,1 г/кг могут вызвать гипогликемию, а >0,5 г/кг — острую печеночную недостаточность.
Повидон-йод вызывает лизис клеточной стенки и инактивацию белков и нуклеотидов у кариесогенных бактерий. Кроме того, он ингибирует синтез глюканов — липких полимеров, которые помогают бактериям прикрепляться к зубам. Клинические испытания показали, что нанесение повидон-йода на зубы может снижать количество S. mutans в слюне, на проксимальных и окклюзионных поверхностях зубов в течение до 24 недель. Использование повидон-йода перед нанесением фторидного лака в клинических испытаниях у детей младшего возраста показало значительное снижение нового кариеса по сравнению с одним фторидным лаком. В клинической практике рекомендуется наносить 8 капель (около 0,45 мл) 10% повидон-йода на сухие зубы каждые 2–3 месяца (Фото 3). Эту процедуру пациент может выполнять дома, доступен коммерческий продукт — флаконы с 0,45 мл 10% повидон-йода.
Фото 3: Протокол нанесения повидон-йода.

Хлоргексидин — это антимикробный агент, который убивает бактерии, разрушая их клеточные стенки. Хотя хлоргексидин может снижать уровень S. mutans в слюне, несколько исследований не показали снижения частоты кариеса при использовании 0,12% ополаскивателя с хлоргексидином, который доступен по рецепту в США. Существуют опасения по поводу 0,12% ополаскивателей с хлоргексидином, так как они могут снижать количество нитратредуцирующих бактерий, которые уменьшают уровень молочной кислоты (улучшают pH полости рта) и производят оксид азота (улучшают здоровье сердечно-сосудистой системы). В ополаскиватели могут включаться и другие антимикробные агенты, такие как серебро, гипохлорит натрия и цетилпиридиния хлорид. Хотя эти агенты демонстрируют антибактериальную активность против S. mutans, клинических доказательств их антикариесного действия в настоящее время недостаточно.
Диагностика начальных поражений
Когда профилактика кариозных поражений оказывается неудачной и образуются начальные поражения, минимально инвазивное лечение может помочь продлить срок службы зуба и избежать более инвазивных методов восстановления. Выявление таких поражений требует тщательного осмотра зубов, и для их обнаружения могут использоваться несколько диагностических инструментов. Инструменты для диагностики кариеса можно разделить на те, которые используют излучение, и те, которые используют свет.
Радиационные методы диагностики кариеса (например, рентген) являются стандартом в стоматологической практике. Новшеством в радиационной диагностике является программное обеспечение на основе искусственного интеллекта (ИИ), которое может накладывать цветовые маркеры на цифровые рентгеновские снимки, указывая на участки рентгенопрозрачности, характерные для деминерализации и кариеса (Фото 4). Чувствительность (истинно положительные результаты) ИИ по сравнению с заключением экспертов составляет 73–90%, а специфичность (истинно отрицательные результаты) — 61,5–93%. Таким образом, ИИ — это лишь инструмент, помогающий стоматологу выявить потенциальные поражения. Анализ ИИ наиболее полезен для повышения чувствительности при выявлении кариеса эмали. Исследование показало, что использование ИИ для диагностики кариеса эмали увеличивает применение профилактических методов, но также повышает частоту инвазивного лечения.
Фото 4: Обнаружение кариеса с помощью искусственного интеллекта (ИИ), демонстрирующее несколько начальных поражений эмали.

Методы диагностики кариеса, использующие свет, можно разделить на те, которые применяют трансиллюминацию, светоиндуцированную флуоресценцию или лазероиндуцированную флуоресценцию. Трансиллюминация ближним инфракрасным светом работает за счет того, что более пористая кариозная эмаль поглощает больше света и выглядит темнее. Эта технология хорошо визуализирует кариес по всему зубу, но не может различить кариозные поражения и изменения контраста минерализованных тканей, вызванные другими причинами (например, флюорозом). Кариозные ткани зуба обладают иными флуоресцентными свойствами, чем здоровые. Светоиндуцированная флуоресценция основана на том, что кариозные поражения поглощают свет коротких волн и переизлучают свет с большей длиной волны. Эта технология не визуализирует проксимальные поверхности зубов и не дифференцирует активность кариозных поражений. Лазероиндуцированная флуоресценция возникает при активации протопорфирина — фотосенситивного пигмента, который является метаболическим продуктом кариесогенных бактерий. Таким образом, эта технология, как утверждается, определяет активность кариеса. Она не предоставляет визуальной карты кариеса, как другие методы, а генерирует число, указывающее на его тяжесть.
Малые молекулы также могут использоваться для визуального выявления начальных поражений. Один коммерческий продукт содержит отрицательно заряженные наночастицы крахмала (100 нм), которые избирательно связываются с кариозной эмалью. Они помечены флуоресцентным маркером, который светится при освещении стоматологической лампой (Фото 5). Другой продукт содержит краситель на основе гемоглобина, который связывается с обнаженным гидроксиапатитом в порах подповерхностной эмали. Окрашивание видно при обычном освещении.
Фото 5: Флуоресцентные заряженные наночастицы крахмала для выявления начальных поражений.

Минимально инвазивное лечение начальных поражений
Современные стратегии реминерализации или восстановления начальных поражений включают самособирающиеся пептиды, пасты с казеинфосфопептидом-аморфным фосфатом кальция и инфильтрацию композитом. Использование серебра диаминфторида (СДФ) — еще один минимально инвазивный метод остановки кариеса, который обычно используется для поражений с образовавшейся полостью. Однако есть некоторые доказательства того, что СДФ может замедлять прогрессирование начальных, межзубных и окклюзионных поражений без полости.
Матрикс эмали присутствует во время одонтогенеза, способствуя формированию кристаллов гидроксиапатита, но отсутствует в зрелом зубе. Новый подход к реминерализации начальных поражений заключается в создании искусственного самособирающегося пептида, который служит каркасом, имитирующим функцию матрикса эмали (Фото 6). P11-4 — это пептид, способный самособираться в ленты с участками связывания ионов кальция. Расстояние между этими участками соответствует межатомному расстоянию между столбцами кальция в кристалле гидроксиапатита. Было показано, что эти пептиды проникают в подповерхностную деминерализацию и индуцируют реминерализацию. Клинические испытания коммерческого продукта с самособирающимися пептидами P11-4 показали эффективность в остановке поражений и уменьшении их размера. Лечение показало положительные результаты как для гладких поверхностей, так и для межзубных поражений.
Фото 6: Препарат с самособирающимися пептидами P11-4, используемый для лечения начального поражения на вестибулярной поверхности.

Другая стратегия лечения — обеспечение биодоступного кальция и фосфатов для реминерализации дефектов эмали и подповерхностных поражений. Проблема реминерализации кальций-фосфатными препаратами заключается в их низкой растворимости в слюне. Если кальций и фосфаты находятся в твердой фазе, они не биодоступны для реминерализации. Кальций-фосфатные соединения могут добавляться в кристаллической форме (например, трикальцийфосфат или биоактивное стекло) или в аморфной форме (например, аморфный фосфат кальция [АФК]). Аморфная форма, обладая менее упорядоченной структурой, более растворима, чем кристаллическая. Для повышения растворимости и биодоступности АФК его можно связать со стабилизирующим белком, например, казеином из молока. Фосфопептиды в казеине содержат участки, способные слабо связываться с кальцием и фосфатами, предотвращая их кристаллизацию и осаждение. Кроме того, эти участки могут связываться с кальцием в поврежденной эмали, поэтому пептиды могут "доставлять" кальций и фосфаты из слюны к зубу. В продаже имеются коммерческие продукты, содержащие комплексы казеинфосфопептида со стабилизированным аморфным фосфатом кальция (КФП-АФК), а также казеинфосфопептида со стабилизированным аморфным фторидом фосфата кальция (КФП-АФФК) в виде паст, жевательных резинок и лаков. Доказательства клинической пользы паст с КФП-АФК по сравнению с фторсодержащими пастами для профилактики новых поражений сомнительны, однако есть некоторые данные о пользе КФП-АФК для реминерализации начальных поражений. КФП-АФФК не показал клинических преимуществ перед КФП-АФК или фторсодержащими пастами для реминерализации.
Инфильтрация композитом — это метод лечения начального кариеса путем проникновения ненаполненного композитного материала через поверхностные поры в подповерхностные поражения на вестибулярных и межзубных поверхностях (Фото 7). Хотя эта методика не является формой реминерализации, клинические испытания показали, что инфильтрация смолой может останавливать некавитированные кариозные поражения.
Фото 7: Инфильтрация композитом, используемая для лечения начального межзубного поражения.

Вывод
Фториды остаются основой профилактики, так как их включение в кристаллы апатита обеспечивает устойчивость к последующему кислотному разрушению. Пациенты, обеспокоенные флюорозом или потенциальными проблемами со здоровьем, связанными с фторидами, могут рассмотреть зубные пасты с гидроксиапатитом, хотя доказательств их способности предотвращать новые кариозные поражения недостаточно. Инновации в диагностике кариеса, включая ИИ, световые методы и малые молекулы, помогают в раннем выявлении начальных поражений. Стратегии реминерализации, такие как гидроксиапатит, самособирающиеся пептиды или КФП-АФК, предлагают перспективные варианты для начальных поражений. Антибактериальные продукты могут помочь в лечении пациентов с факторами риска кариеса. Наконец, план управления риском кариеса должен учитывать готовность пациента участвовать в снижении факторов риска, изменяя диету и гигиенические привычки.
Автор: Nathaniel C. Lawson, DMD, PhD































































































































































0 комментариев