Хирургическое удаление пораженных третьих моляров нижней челюсти провоцирует развитие ятрогенной травмы, объем которой зависит от положения и наклона зуба, и анатомических особенностей данного участка. В отдельных случаях экстракция третьего моляра может вызвать резорбцию дистального корня второго моляра и формирование огромного костного дефекта. Процедура удаления третьих моляров предусматривает сепарацию полнотканного слизистопериостального лоскута, удаление костной ткани в ходе остеотомии для формирования доступа, сегментирование проблемного зуба и его дальнейшую экстракцию. Совокупность данных манипуляций приводит к формированию костного дефекта дистальнее второго моляра. Данный дефект уменьшает прочность челюсти, делает процесс заживления более длительным, а также может быть ассоциирован с развитием пародонтита или остеопороза.
В 1967 году Yeomans и Urist установили, что дентин содержит костные морфогенетические белки (BMPs), которые способствуют дифференцировке мезенхимальных стволовых клеток в хондроциты и, таким образом, улучшают образование кости. Кроме того, альвеолярная кость, как и зубы, развивается из клеток нервного гребешка.
В 2003 году Murata и соавторы впервые использовали аутогенный дентин с целью НКР в ходе проведения процедуры синус-лифта. Для получения АДА с размером части от 300 до 1200 мкм, который может быть изготовлен и продезинфицирован на протяжении всего 8 минут, можно использовать несколько коммерческих систем. В данной статье мы опишем результаты аугментации костного дефекта дистальнее второго моляра посредством АДА и проведем сравнение полученных данных с теми, которые были зарегистрированы в группе контроля, пациентам которой после экстракции третьих моляров не проводилось никаких НКР-процедур.
Материал и методы
Исследование было спланировано в форме рандомизированного по типу «split-mouth». В группу исследования были включены 13 пациентов (трое мужчин и десять женщин) в возрасте от 18 до 27 лет (средний возраст 22,61 года). Каждый пациент имел хотя бы один ретинированный третий моляр на нижней челюсти, который был горизонтально дистопирован ниже цементоэмалевой границы второго моляра. Пародонтологический статус всех пациентов до начала лечения был отличным. АДА получали с использованием системы Smart Dentin Grinder, которая в США доступна от таких фирм-производителей как KometaBio, IDS-Integrated Dental Systems и GoldenDent.
Критерии включения
Чтобы быть включенным в исследование, пациент должен был:
- быть готовым участвовать в исследовании,
- быть не моложе 18 лет,
- характеризоваться отличным соматическим состоянием здоровья и отсутствием пародонтальных патологий,
- иметь по меньшей мере один дистопированный третий моляр, горизонтально наклоненный относительно второго моляра.
Критерий исключения
Пациенты были исключены из исследования, если:
- у них отмечалось активное пародонтальное поражение,
- они были несовершеннолетними (<18 лет),
- характеризовались наличием системных заболеваний, которые ограничивали возможности для проведения хирургического вмешательства,
- или они принимали алкоголь, наркотиками или другие вещества, которые компрометировали их состояние.
Лечение до начала исследования
После отбора пациентов и получения от них информированного согласия, им было проведено полное обследование пародонта с заполнением пародонтальной карты. Это было сделано для того, чтобы объективно оценить состояние пародонта и установить потребность в проведении профессиональной гигиены полости рта.
Предоперационные процедуры
Перед проведением операции экстракции были проведены тщательный анализ всех данных анамнеза пациента, ортопантомография для верификации угла наклона моляра, а также обследование на предмет наличия каких-либо инфекционных поражений ротовой полости. Пациенты основной и контрольной групп были распределены рандомизировано.
Хирургическое удаление третьего моляра
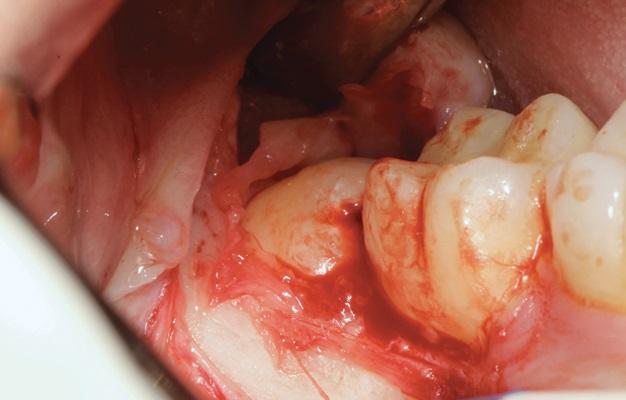
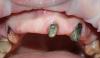
Дооперационную ирригацию ротовой полости проводили 0,2% раствором хлоргексидина (ХГ) с последующим выполнением анестезии 4% артикаином с раствором адреналина. Крестальный разрез формировали с послабляющим вертикальным с мезиальной стороны области вмешательства, после чего проводили сепарирование полнотканного слизистопериостального лоскута (фото 1).
Фото 1. Дистопированный третий моляр: вид после сепарации лоскута.
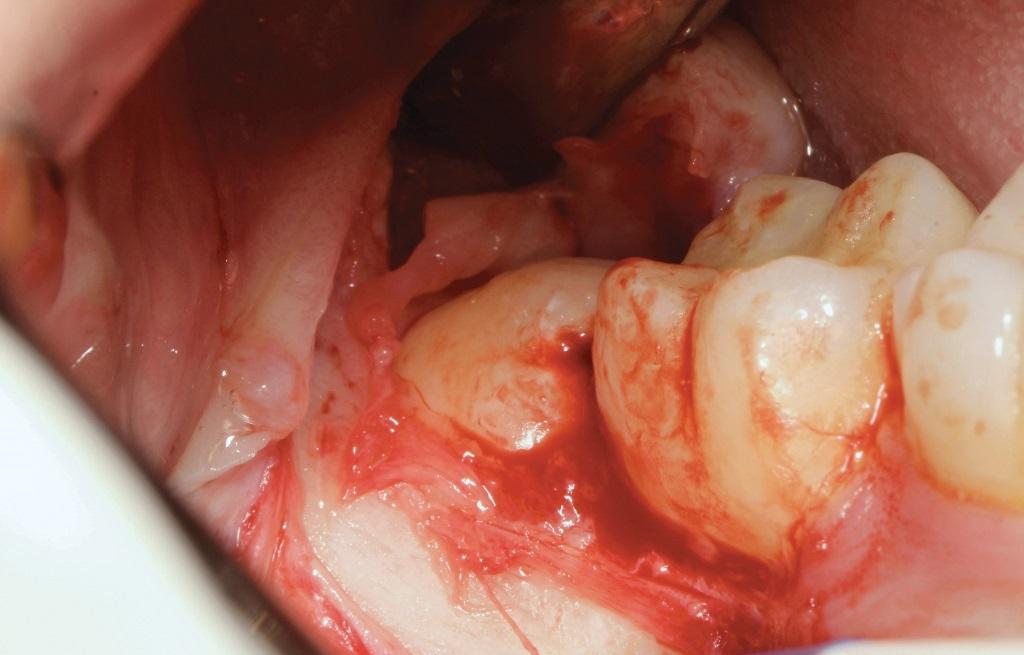
Остеотомию выполняли при помощи круглого карбидного бора и прямого наконечника. При необходимости проводили сегментацию зуба с дальнейшей его экстракцией (фото 2).
Фото 2. Сегментирование зуба для удаления.
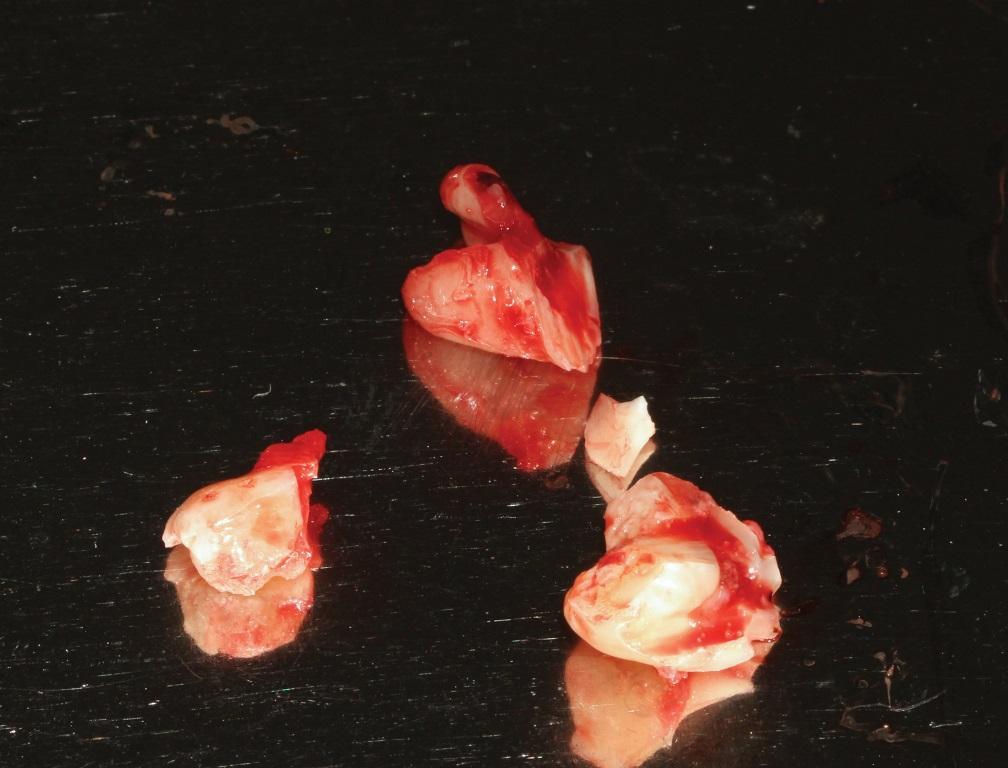
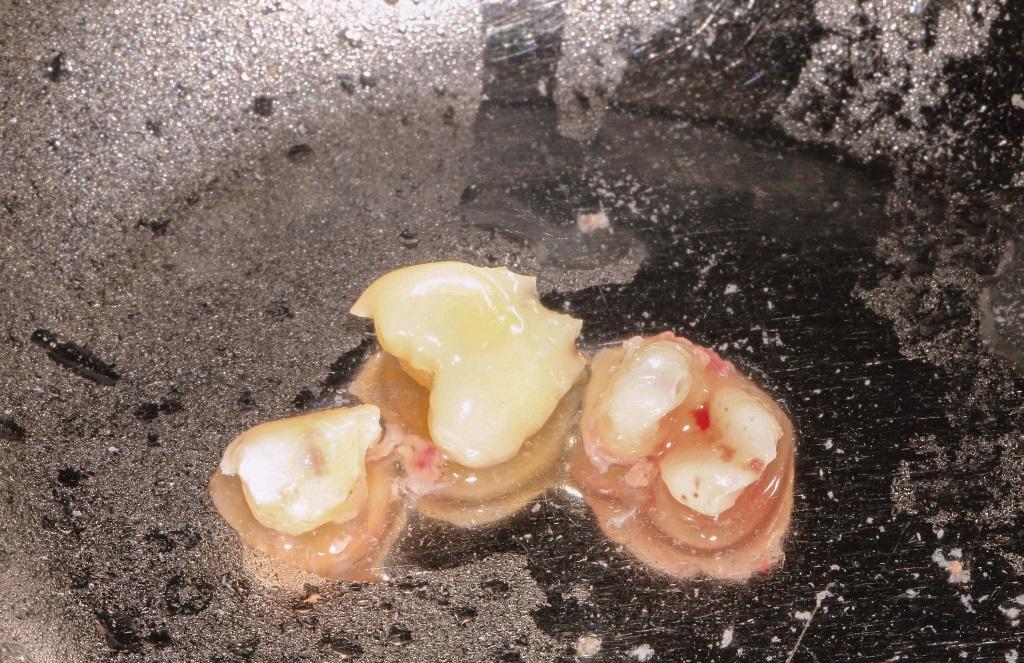
В ходе удаления старались не повредить ни соседний второй моляр, ни опорную альвеолярную кость. Постэкстракционная лунка была тщательно очищена и промыта 0,2%-ным раствором ХГ для снижения уровня бактериальной нагрузки (фото 3). Удаленные фрагменты зубов были очищены от кариеса и остатков пародонтальной связки (фото 4) и измельчены посредством аппарата.
Фото 3. Вид постэкстракционной лунки.
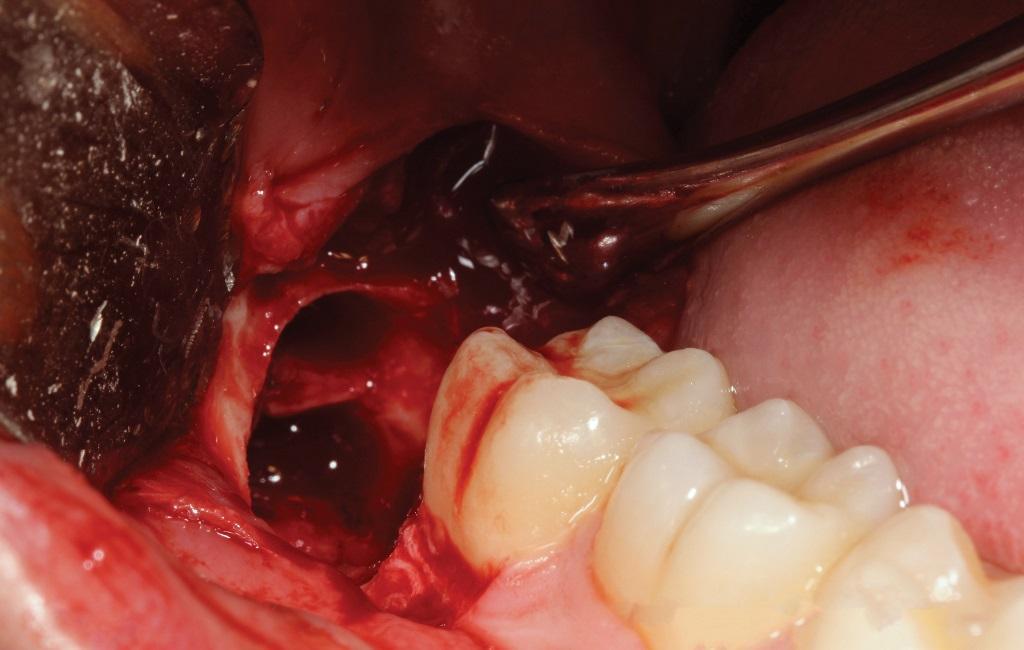
Фото 4. Удаление остатков пародонтальной связки и пломбировочного материала перед обработкой зуба в системе для дробления.
После этого аугментат замачивали на 10 минут в растворе гидроксида натрия, смешанного с 20% этанолом. Затем трансплантат промывали фосфатным солевым раствором, благодаря чему его удавалось полностью дезинфицировать (фото 5). АДА упаковывали в сформировавшейся костный дефект и ждали пока он смочиться кровью пациента. Для удаления чрезмерной влаги использовали стерильный марлевый тампон (фото 6). Поверх АДА устанавливали резорбируемую гемостатическую желатиновую губку и ушивали рану викриловыми швами 4-0 (фото 7).
Фото 5. Вид полученного материала после обработки.

Фото 6. Вид лунки после ее заполнения аутогенным дентином.
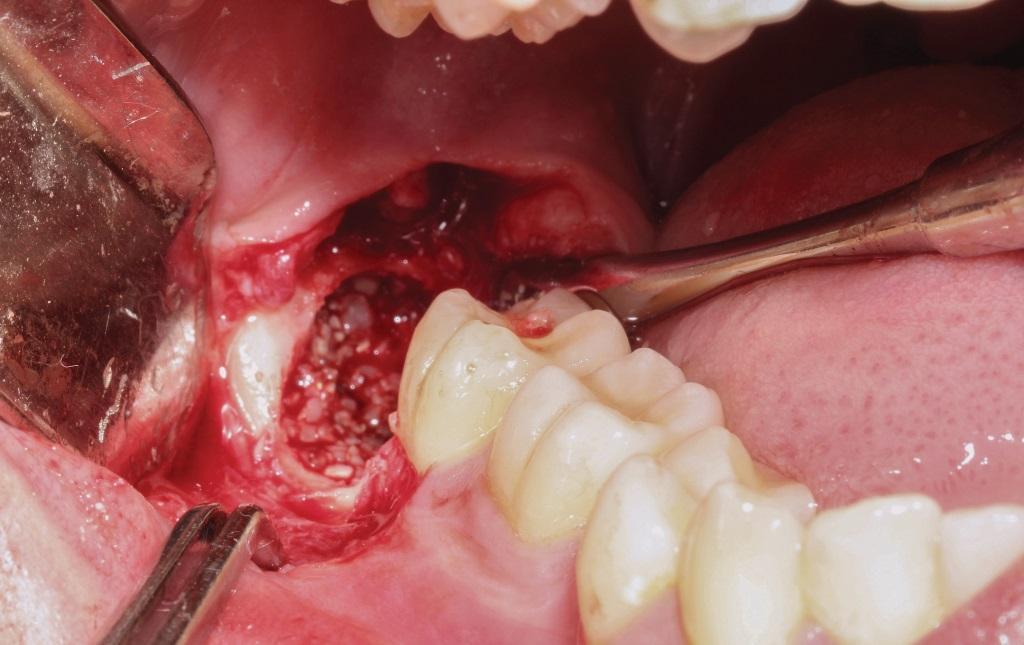
Фото 7. Вид лунки после ушивания лоскута.
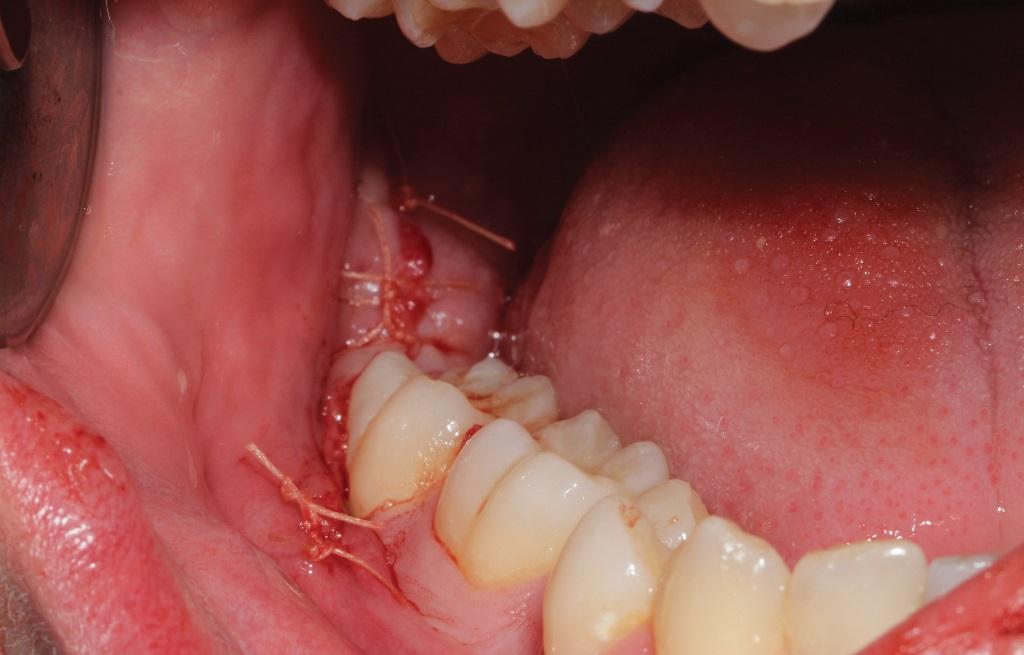
Для контрольной группы пациентов использовался тот же хирургический протокол, за исключением аугментации АДА; постэкстракционную лунку выполняли попросту гемостатической губкой. Сгусток крови формировали с использованием хирургической кюретки, а лоскут также ушивали викриловыми швами 4-0.
Послеоперационные процедуры
Все пациенты после операции проходили 5-дневный курс профилактической антибиотикотерапии амоксициллином по 1000 мг два раза в день, а также принимали нестероидные противовоспалительные препараты (НПВП), которые назначались в соответствии с индивидуальными потребностями. Пациентам было предписано проводить ирригацию ротовой полости 0,12% раствором на основе ХГ два раза в день в течение 14 дней. Швы снимали через 10 дней после операции.
Оценка и клиническое обследование
Клинические осмотры и операции выполнялись резидентом отделения хирургической стоматологии и челюстно-лицевой хирургии Литовского университета наук о здоровье в Каунасе, Литва. Глубину дефекта дистальнее второго моляра измеряли при помощи пародонтального зонда со щечной и язычной сторон.
Рентгенографическое исследование
Ортопантомограммы получали через 3 месяца и 12 месяцев после выполнения операции для оценки состояния костной ткани в области дефекта и исключения патологий, которые могли возникнуть в результате экстракции. Для изменения уровня альвеолярного гребня анализ ортопантомограмм проводили в программном обеспечении Kodak Dental Imaging Software 6.12.32.0 (Carestream Dental).
Потенциал заживления послеоперационной раны и его влияние на пациента
Пациенты были осмотрены через 10 дней, 3 месяца и 12 месяцев после операции для оценки процесса заживления раны. В ходе данных осмотров пациента заполняли опросник для оценки имеющихся послеопераицонных ощущений, боли, отека, факта использования НПВП, ограничений в приеме пищи и общего влияния проведенной операции на качество повседневной жизни. При снятии швов область вмешательства осматривали на предмет наличия патологии «сухой лунки» (альвеолярного остеита). Пациенты интерпретовали степень тяжести своего состояния от 1 до 5, при котором 1 свидетельствовало об отсутствии дискомфорта / боли, а 5 – о наличие сильного дискомфорта/боли. Влияние хирургического вмешательства на повседневную жизнь пациента также оценивалось по шкале от 1 до 5, при этом 1 указывало на отсутствие влияния проведенной операции, а 5 - на значительные изменения повседневной жизни. Пациенты могли добавлять свои комментарии для описания степени негативного или положительного воздействия, которое они испытали в своей повседневной жизни. Тест Манна-Уитни использовался для определения статистической значимости результатов с использованием SPSS Statistics версии 23.0 (IBM). Уровень значимости был установлен на P < 0,05.
Результаты
В общей сложности была проведена оценка 24 клинических случаев (N = 11 в контрольной группе и N = 13 в основной группе). Зондирование через 3 месяца после выполнения операции проводили под очень легким давлением, дабы не нарушить процесс заживления раны. Через 3 месяца в группе исследования средняя глубина зондирования составляла 1,31 мм (стандартное отклонение [СО] 0,751 мм), а в контрольной - 4 мм (СО 0,853 мм). Через 12 месяцев в группе исследования глубина зондирования составляла уже 1,15 мм (СО 0,801 мм), а в контрольной - 4,45 мм (СО 0,934 мм). Значения глубины зондирования, зарегистрированные как в группе исследования, так и в группе контроля через 3 и 12 месяцев после проведения операции, статистически не отличались, однако статистически значимая разница была зарегистрирована при использовании теста Манна-Уитни в ходе сравнения двух групп (P <.001). В группе исследования также были зарегистрированы рентгенологические признаки конверсии АДА в костную ткань челюсти, что позволяло почти полностью восстановить имеющийся дефект (фото 9).
Фото 8. Оценка глубины зондирования через 3 и 12 месяцев.
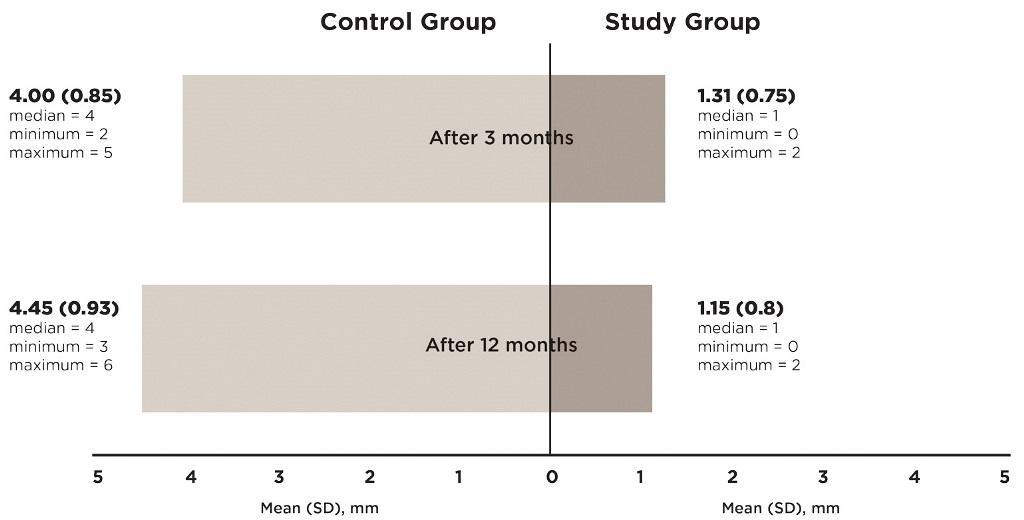
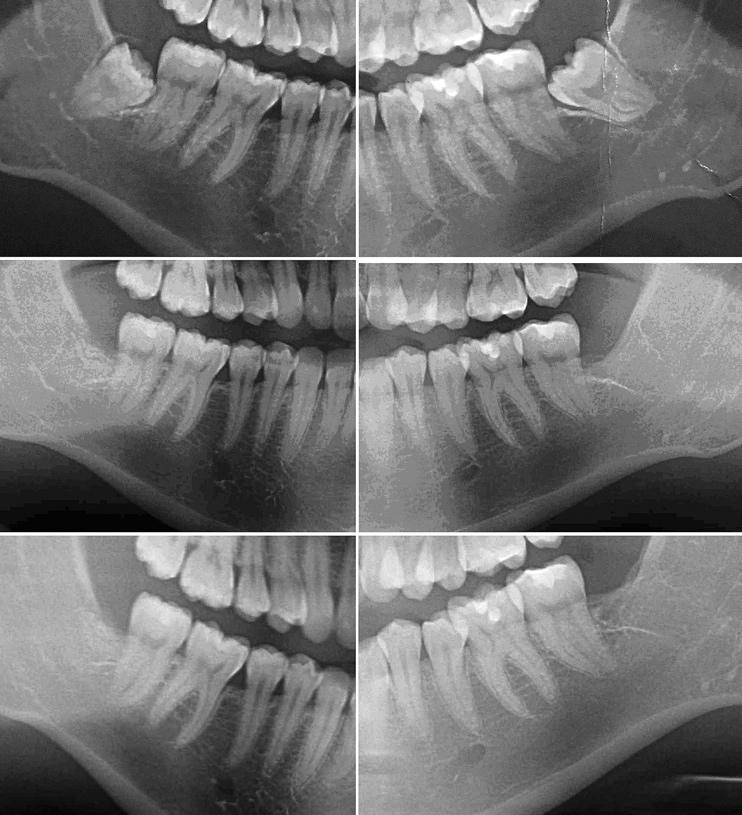
Фото 9. Ортопантомограмма до вмешательства (вверху); ортопантомограмма через 3 месяца после аугментации лунок с помощью АДА (посредине); ортопантомограмма через 12 месяцев после вмешательства (внизу).
Согласно результатам опросника 5 из 11 пациентов контрольной группы жаловались на застревание пищи в области вмешательства через 3 месяца после операции, что свидетельствует о необходимости контроля уровня гигиены ротовой полости. В группе исследования подобных жалоб зарегистрировано не было. Ни в группе контроля, ни в группе исследования пациенты не сообщали о каких-то значительных изменениях в процессе заживления оперированного участка. Ортопантомография также позволила обнаружить статистически более значимую потерю уровня костной ткани в группе контроля, где она составляла 4,2 мм (СО 1,2 мм), по сравнению с группой исследования – 1,05 (СО 0,91).
Обсуждение
Обычно пациенты, которым проводиться удаление третьих дистопированных моляров, являются реферативными, и после заживления области вмешательства они возвращаются к своему лечащему стоматологу, поэтому мониторинг со стороны хирурга за ними является ограниченным. Kugelberg и коллеги отметили, что стабильность пародонтальных тканей дистальнее второго моляра после удаления дистопированного зуба мудрости является компрометированной без проведения процедур аугментации лунки. Таковую можно выполнить посредством костного трансплантата, однако параллельно с этим и увеличивается стоимость лечения. В свою очередь, АДА является достаточно успешным материалом для проведения аугментации, который обеспечивает формирование достаточного количества грубоволокнистой кости через 60 дней заживления, и небольшое количество пластинчатой кости через 90 дней. Успешность АДА было даже доказано при применении материала в ходе дентальной имплантации с регистрацией достаточной стабильности интраоссальной опоры через два года после проведения операции. Таким образом, АДА может рассматриваться как эффективная альтернатива классическим костным заменителям. Поскольку сам по себе материал является аутогенным, он содержит сигнальные клетки, которые отвечают за миграцию костных морфологических протеинов, и играет роль остова для дальнейшего формирования кости. Ведь по данным Urist от 1967 года, клетки, которые вступают в контакт с костными морфологическими протеинами, изменяют паттерн своей дифференциации, и начинают видоизменятся в клетки костной ткани. Позже этот же автор подтвердил наличие данных протеинов в структуре самого дентина. Экстрагированные из дентина протеины индуцируют формирование костной ткани уже через 3 недели после их имплантации, и хоть они несколько отличаются от аналогичных костных белков, однако обеспечивают реализацию одного и того же процесса. Резорбция АДА протекает очень медленно, что, в свою очередь, сопутствует образованию пластинчатой кости. Результаты исследований свидетельствуют о стабильности такой кости вокруг имплантатов на протяжении как минимум 5 лет наблюдения. Можно отметить, что пациенты в данном исследовании являются весьма молодыми, и в таком возрасте процесс заживления обычно проходит и так без каких-либо осложнений. Но, как правило, именно такие молодые люди и обращаются за помощью по поводу экстракции третьих моляров. Данное хирургическое вмешательство является достаточно агрессивным, поскольку предполагает выполнение остеотомии для формирования доступа к проблемному зубу. Из наблюдений автора можно отметить, что АДА аналогично эффективно и среди пациентов старшего возраста, которым проводили экстракцию зубов мудрости.
Выводы
Аугментация постэктсракционной лунки третьего моляра позволяет минимизировать уровень резорбции области вмешательства и обеспечить стабильность пародонтальных структур в области дистального корня второго моляра. Для этой цели на рынке доступно огромное количество материалов, которые являются достаточно дорогостоящими. Как было показано в данном исследовании, АДА является биологически подходящим материалом для проведения НКР в случаях экстракции дистопированных зубов мудрости. Кроме того, применение АДА не является таким дорогостоящим, а сам материалов по своей природе – полностью аутогенный, что, в свою очередь, позволяет исключить риск развития иммунологических реакций.
Авторы:
Avi Kuperschlag, DDS, MSc
Greta Keršytė
Gregori M. Kurtzman, DDS
Robert A. Horowitz, DDS
Хирургическое удаление пораженных третьих моляров нижней челюсти провоцирует развитие ятрогенной травмы, объем которой зависит от положения и наклона зуба, и анатомических особенностей данного участка. В отдельных случаях экстракция третьего моляра может вызвать резорбцию дистального корня второго моляра и формирование огромного костного дефекта. Процедура удаления третьих моляров предусматривает сепарацию полнотканного слизистопериостального лоскута, удаление костной ткани в ходе остеотомии для формирования доступа, сегментирование проблемного зуба и его дальнейшую экстракцию. Совокупность данных манипуляций приводит к формированию костного дефекта дистальнее второго моляра. Данный дефект уменьшает прочность челюсти, делает процесс заживления более длительным, а также может быть ассоциирован с развитием пародонтита или остеопороза.

В 1967 году Yeomans и Urist установили, что дентин содержит костные морфогенетические белки (BMPs), которые способствуют дифференцировке мезенхимальных стволовых клеток в хондроциты и, таким образом, улучшают образование кости. Кроме того, альвеолярная кость, как и зубы, развивается из клеток нервного гребешка.
В 2003 году Murata и соавторы впервые использовали аутогенный дентин с целью НКР в ходе проведения процедуры синус-лифта. Для получения АДА с размером части от 300 до 1200 мкм, который может быть изготовлен и продезинфицирован на протяжении всего 8 минут, можно использовать несколько коммерческих систем. В данной статье мы опишем результаты аугментации костного дефекта дистальнее второго моляра посредством АДА и проведем сравнение полученных данных с теми, которые были зарегистрированы в группе контроля, пациентам которой после экстракции третьих моляров не проводилось никаких НКР-процедур.
Материал и методы
Исследование было спланировано в форме рандомизированного по типу «split-mouth». В группу исследования были включены 13 пациентов (трое мужчин и десять женщин) в возрасте от 18 до 27 лет (средний возраст 22,61 года). Каждый пациент имел хотя бы один ретинированный третий моляр на нижней челюсти, который был горизонтально дистопирован ниже цементоэмалевой границы второго моляра. Пародонтологический статус всех пациентов до начала лечения был отличным. АДА получали с использованием системы Smart Dentin Grinder, которая в США доступна от таких фирм-производителей как KometaBio, IDS-Integrated Dental Systems и GoldenDent.
Критерии включения
Чтобы быть включенным в исследование, пациент должен был:
- быть готовым участвовать в исследовании,
- быть не моложе 18 лет,
- характеризоваться отличным соматическим состоянием здоровья и отсутствием пародонтальных патологий,
- иметь по меньшей мере один дистопированный третий моляр, горизонтально наклоненный относительно второго моляра.
Критерий исключения
Пациенты были исключены из исследования, если:
- у них отмечалось активное пародонтальное поражение,
- они были несовершеннолетними (<18 лет),
- характеризовались наличием системных заболеваний, которые ограничивали возможности для проведения хирургического вмешательства,
- или они принимали алкоголь, наркотиками или другие вещества, которые компрометировали их состояние.
Лечение до начала исследования
После отбора пациентов и получения от них информированного согласия, им было проведено полное обследование пародонта с заполнением пародонтальной карты. Это было сделано для того, чтобы объективно оценить состояние пародонта и установить потребность в проведении профессиональной гигиены полости рта.
Предоперационные процедуры
Перед проведением операции экстракции были проведены тщательный анализ всех данных анамнеза пациента, ортопантомография для верификации угла наклона моляра, а также обследование на предмет наличия каких-либо инфекционных поражений ротовой полости. Пациенты основной и контрольной групп были распределены рандомизировано.
Хирургическое удаление третьего моляра
Дооперационную ирригацию ротовой полости проводили 0,2% раствором хлоргексидина (ХГ) с последующим выполнением анестезии 4% артикаином с раствором адреналина. Крестальный разрез формировали с послабляющим вертикальным с мезиальной стороны области вмешательства, после чего проводили сепарирование полнотканного слизистопериостального лоскута (фото 1).
Фото 1. Дистопированный третий моляр: вид после сепарации лоскута.

Остеотомию выполняли при помощи круглого карбидного бора и прямого наконечника. При необходимости проводили сегментацию зуба с дальнейшей его экстракцией (фото 2).
Фото 2. Сегментирование зуба для удаления.

В ходе удаления старались не повредить ни соседний второй моляр, ни опорную альвеолярную кость. Постэкстракционная лунка была тщательно очищена и промыта 0,2%-ным раствором ХГ для снижения уровня бактериальной нагрузки (фото 3). Удаленные фрагменты зубов были очищены от кариеса и остатков пародонтальной связки (фото 4) и измельчены посредством аппарата.
Фото 3. Вид постэкстракционной лунки.

Фото 4. Удаление остатков пародонтальной связки и пломбировочного материала перед обработкой зуба в системе для дробления.

После этого аугментат замачивали на 10 минут в растворе гидроксида натрия, смешанного с 20% этанолом. Затем трансплантат промывали фосфатным солевым раствором, благодаря чему его удавалось полностью дезинфицировать (фото 5). АДА упаковывали в сформировавшейся костный дефект и ждали пока он смочиться кровью пациента. Для удаления чрезмерной влаги использовали стерильный марлевый тампон (фото 6). Поверх АДА устанавливали резорбируемую гемостатическую желатиновую губку и ушивали рану викриловыми швами 4-0 (фото 7).
Фото 5. Вид полученного материала после обработки.

Фото 6. Вид лунки после ее заполнения аутогенным дентином.

Фото 7. Вид лунки после ушивания лоскута.

Для контрольной группы пациентов использовался тот же хирургический протокол, за исключением аугментации АДА; постэкстракционную лунку выполняли попросту гемостатической губкой. Сгусток крови формировали с использованием хирургической кюретки, а лоскут также ушивали викриловыми швами 4-0.
Послеоперационные процедуры
Все пациенты после операции проходили 5-дневный курс профилактической антибиотикотерапии амоксициллином по 1000 мг два раза в день, а также принимали нестероидные противовоспалительные препараты (НПВП), которые назначались в соответствии с индивидуальными потребностями. Пациентам было предписано проводить ирригацию ротовой полости 0,12% раствором на основе ХГ два раза в день в течение 14 дней. Швы снимали через 10 дней после операции.
Оценка и клиническое обследование
Клинические осмотры и операции выполнялись резидентом отделения хирургической стоматологии и челюстно-лицевой хирургии Литовского университета наук о здоровье в Каунасе, Литва. Глубину дефекта дистальнее второго моляра измеряли при помощи пародонтального зонда со щечной и язычной сторон.
Рентгенографическое исследование
Ортопантомограммы получали через 3 месяца и 12 месяцев после выполнения операции для оценки состояния костной ткани в области дефекта и исключения патологий, которые могли возникнуть в результате экстракции. Для изменения уровня альвеолярного гребня анализ ортопантомограмм проводили в программном обеспечении Kodak Dental Imaging Software 6.12.32.0 (Carestream Dental).
Потенциал заживления послеоперационной раны и его влияние на пациента
Пациенты были осмотрены через 10 дней, 3 месяца и 12 месяцев после операции для оценки процесса заживления раны. В ходе данных осмотров пациента заполняли опросник для оценки имеющихся послеопераицонных ощущений, боли, отека, факта использования НПВП, ограничений в приеме пищи и общего влияния проведенной операции на качество повседневной жизни. При снятии швов область вмешательства осматривали на предмет наличия патологии «сухой лунки» (альвеолярного остеита). Пациенты интерпретовали степень тяжести своего состояния от 1 до 5, при котором 1 свидетельствовало об отсутствии дискомфорта / боли, а 5 – о наличие сильного дискомфорта/боли. Влияние хирургического вмешательства на повседневную жизнь пациента также оценивалось по шкале от 1 до 5, при этом 1 указывало на отсутствие влияния проведенной операции, а 5 - на значительные изменения повседневной жизни. Пациенты могли добавлять свои комментарии для описания степени негативного или положительного воздействия, которое они испытали в своей повседневной жизни. Тест Манна-Уитни использовался для определения статистической значимости результатов с использованием SPSS Statistics версии 23.0 (IBM). Уровень значимости был установлен на P < 0,05.
Результаты
В общей сложности была проведена оценка 24 клинических случаев (N = 11 в контрольной группе и N = 13 в основной группе). Зондирование через 3 месяца после выполнения операции проводили под очень легким давлением, дабы не нарушить процесс заживления раны. Через 3 месяца в группе исследования средняя глубина зондирования составляла 1,31 мм (стандартное отклонение [СО] 0,751 мм), а в контрольной - 4 мм (СО 0,853 мм). Через 12 месяцев в группе исследования глубина зондирования составляла уже 1,15 мм (СО 0,801 мм), а в контрольной - 4,45 мм (СО 0,934 мм). Значения глубины зондирования, зарегистрированные как в группе исследования, так и в группе контроля через 3 и 12 месяцев после проведения операции, статистически не отличались, однако статистически значимая разница была зарегистрирована при использовании теста Манна-Уитни в ходе сравнения двух групп (P <.001). В группе исследования также были зарегистрированы рентгенологические признаки конверсии АДА в костную ткань челюсти, что позволяло почти полностью восстановить имеющийся дефект (фото 9).
Фото 8. Оценка глубины зондирования через 3 и 12 месяцев.

Фото 9. Ортопантомограмма до вмешательства (вверху); ортопантомограмма через 3 месяца после аугментации лунок с помощью АДА (посредине); ортопантомограмма через 12 месяцев после вмешательства (внизу).

Согласно результатам опросника 5 из 11 пациентов контрольной группы жаловались на застревание пищи в области вмешательства через 3 месяца после операции, что свидетельствует о необходимости контроля уровня гигиены ротовой полости. В группе исследования подобных жалоб зарегистрировано не было. Ни в группе контроля, ни в группе исследования пациенты не сообщали о каких-то значительных изменениях в процессе заживления оперированного участка. Ортопантомография также позволила обнаружить статистически более значимую потерю уровня костной ткани в группе контроля, где она составляла 4,2 мм (СО 1,2 мм), по сравнению с группой исследования – 1,05 (СО 0,91).
Обсуждение
Обычно пациенты, которым проводиться удаление третьих дистопированных моляров, являются реферативными, и после заживления области вмешательства они возвращаются к своему лечащему стоматологу, поэтому мониторинг со стороны хирурга за ними является ограниченным. Kugelberg и коллеги отметили, что стабильность пародонтальных тканей дистальнее второго моляра после удаления дистопированного зуба мудрости является компрометированной без проведения процедур аугментации лунки. Таковую можно выполнить посредством костного трансплантата, однако параллельно с этим и увеличивается стоимость лечения. В свою очередь, АДА является достаточно успешным материалом для проведения аугментации, который обеспечивает формирование достаточного количества грубоволокнистой кости через 60 дней заживления, и небольшое количество пластинчатой кости через 90 дней. Успешность АДА было даже доказано при применении материала в ходе дентальной имплантации с регистрацией достаточной стабильности интраоссальной опоры через два года после проведения операции. Таким образом, АДА может рассматриваться как эффективная альтернатива классическим костным заменителям. Поскольку сам по себе материал является аутогенным, он содержит сигнальные клетки, которые отвечают за миграцию костных морфологических протеинов, и играет роль остова для дальнейшего формирования кости. Ведь по данным Urist от 1967 года, клетки, которые вступают в контакт с костными морфологическими протеинами, изменяют паттерн своей дифференциации, и начинают видоизменятся в клетки костной ткани. Позже этот же автор подтвердил наличие данных протеинов в структуре самого дентина. Экстрагированные из дентина протеины индуцируют формирование костной ткани уже через 3 недели после их имплантации, и хоть они несколько отличаются от аналогичных костных белков, однако обеспечивают реализацию одного и того же процесса. Резорбция АДА протекает очень медленно, что, в свою очередь, сопутствует образованию пластинчатой кости. Результаты исследований свидетельствуют о стабильности такой кости вокруг имплантатов на протяжении как минимум 5 лет наблюдения. Можно отметить, что пациенты в данном исследовании являются весьма молодыми, и в таком возрасте процесс заживления обычно проходит и так без каких-либо осложнений. Но, как правило, именно такие молодые люди и обращаются за помощью по поводу экстракции третьих моляров. Данное хирургическое вмешательство является достаточно агрессивным, поскольку предполагает выполнение остеотомии для формирования доступа к проблемному зубу. Из наблюдений автора можно отметить, что АДА аналогично эффективно и среди пациентов старшего возраста, которым проводили экстракцию зубов мудрости.
Выводы
Аугментация постэктсракционной лунки третьего моляра позволяет минимизировать уровень резорбции области вмешательства и обеспечить стабильность пародонтальных структур в области дистального корня второго моляра. Для этой цели на рынке доступно огромное количество материалов, которые являются достаточно дорогостоящими. Как было показано в данном исследовании, АДА является биологически подходящим материалом для проведения НКР в случаях экстракции дистопированных зубов мудрости. Кроме того, применение АДА не является таким дорогостоящим, а сам материалов по своей природе – полностью аутогенный, что, в свою очередь, позволяет исключить риск развития иммунологических реакций.
Авторы:
Avi Kuperschlag, DDS, MSc
Greta Keršytė
Gregori M. Kurtzman, DDS
Robert A. Horowitz, DDS




























































































































































0 комментариев