В данном описании клинического случая представлено использование единого резорбируемого композитного биоматериала, состоящего из бычьего коллагена и биоактивного апатита кальция, при комбинированном сложном дефекте, подчеркивая регенерацию тканей полости рта. Согласно стандартным процедурам лечения, 68-летний пациент был пролечен в условиях частной практики одним и тем же биоматериалом по двум различным терапевтическим показаниям: сохранение альвеолярного гребня в беззубом участке зуба № 2.4 и направленная тканевая регенерация на медиальной поверхности зуба № 2.5. Никакие другие биоматериалы не использовались при лечении данного комбинированного сложного дефекта. Заживление протекало без осложнений, и пациент был удовлетворен окончательным результатом лечения. Беззубый промежуток № 2.4 в дальнейшем был восстановлен с помощью реставрации с винтовой фиксацией на имплантате. На контрольном осмотре через 16 месяцев клиническая оценка выявила сохраненный объем гребня и стабильную кератинизированную мягкую ткань. Рентгенологический анализ подтвердил стабильный уровень кости вокруг имплантата № 2.4 и положительные рентгенологические изменения, свидетельствующие о регенерации тканей на медиальной поверхности зуба № 2.5, включая восстановление периодонтальной связки. В рамках ограничений данного описания случая, биоматериал продемонстрировал эффективность, удобство клинического применения и экономическую эффективность в качестве однокомпонентного подхода, уменьшая потребность в дополнительных вмешательствах.
Методы сохранения альвеолярного гребня (САГ) направлены на поддержание его объема путем заполнения лунки костным заменителем — аутогенным, аллогенным, ксеногенным трансплантатом или аллопластом — с мембраной или без нее, а также с пластикой мягких тканей для облегчения регенерации тканей полости рта. Хотя САГ имеет убедительные доказательства в сохранении размеров, эффективность биоматериалов оценивается как умеренная из-за ограниченной стандартизации и отчетности. Клиницисты должны взвешивать свойства и такие факторы, как биосовместимость, резорбция, доказательства формирования новой кости, удобство использования, послеоперационный комфорт, экономическая эффективность и предпочтения пациента. Дизайн каркаса также значительно влияет на результаты регенерации. Кроме того, взаимосвязанность пор, размер частиц и пористость влияют на поведение остеобластов, причем каркасы, богатые коллагеном, превосходят высокоминерализованные по показателям костеобразования.
Современная стоматология предлагает несколько вариантов лечения зуба, значительно пораженного пародонтологическим заболеванием, включая удаление с САГ или направленную тканевую регенерацию (НТР). При рассмотрении регенеративных методов восстановление поврежденных пародонтальных тканей так же важно, как и сохранение объема альвеолярного гребня для достижения успешной реабилитации. НТР использует мембраны для предотвращения врастания эпителиальных клеток в дефект и поддержания пространства для регенерации кости. Однако экспозиция мембраны остается частым осложнением, особенно если мембрана нерезорбируемая. Один из подходов к решению этой проблемы — использование резорбируемого ксеногенно-аллопластического биоматериала (OsteoGen Plug, Impladent Ltd.), разработанного для поддержки ключевых принципов регенерации тканей полости рта при одновременном снижении риска коллапса мембраны. Состоящий из резорбируемого апатита кальция и коллагена из бычьего ахиллова сухожилия, биоматериал имитирует органические и неорганические компоненты натуральной кости. Его форма в виде пробки предлагает простую, экономически эффективную альтернативу костным гранулам и мембранным трансплантатам, улучшая удобство клинического применения.
В данном описании клинического случая представлено использование этого резорбируемого каркаса из бычьего коллагена и биоактивного апатита кальция в качестве единственного биоматериала для САГ в беззубом участке зуба № 2.4 и для НТР на медиальной поверхности зуба № 2.5.
Клинический случай
Пациент мужского пола 68 лет был направлен эндодонтистом с диагнозом симптоматический необратимый пульпит с нормальными периапикальными тканями и значительной потерей костной ткани с вовлечением фуркации у первого премоляра верхней челюсти слева (зуб № 2.4). Из-за состояния пародонта была показана реабилитация с помощью имплантационной реставрации. Конусно-лучевая компьютерная томография (КЛКТ) выявила потерю кости с дистальной стороны пораженного зуба, размером 5 мм в ширину и 9 мм в длину соответственно, с вовлечением альвеолярного костного гребня (Фото 1 – Фото 4).
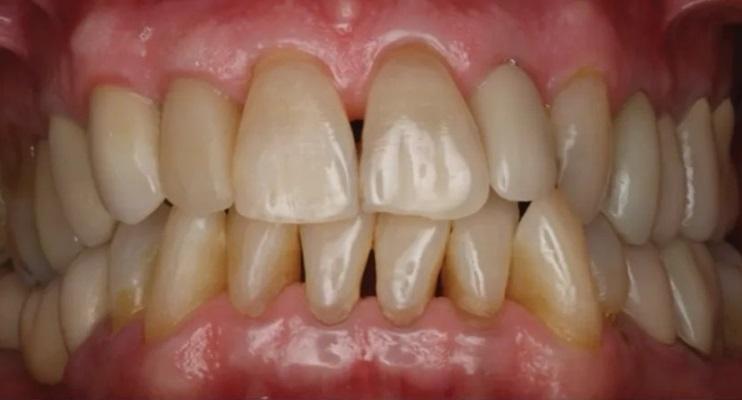
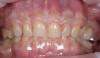
Фото 1. Предоперационный интраоральный передний вид.
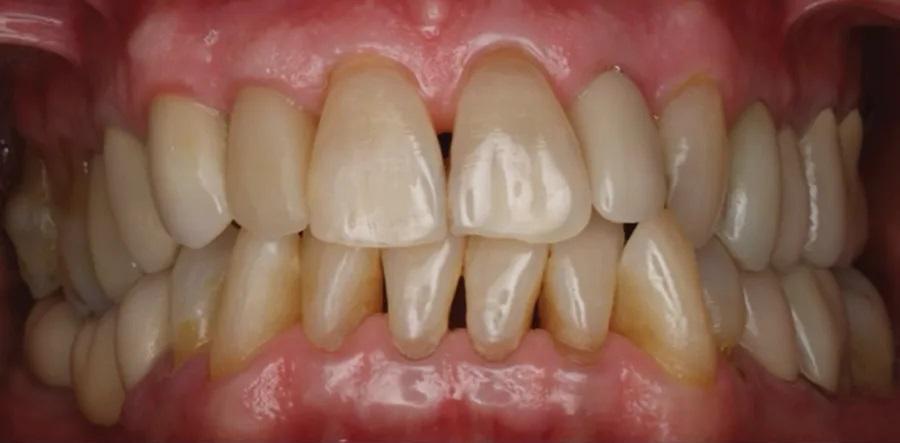
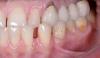
Фото 2. Предоперационный интраоральный латеральный вестибулярный вид.
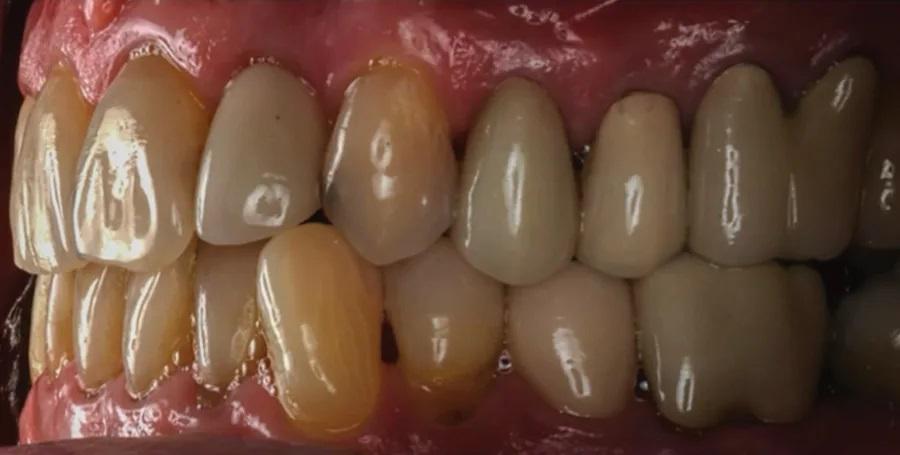
Фото 3. Предоперационный корональный срез КЛКТ первого премоляра верхней челюсти слева.
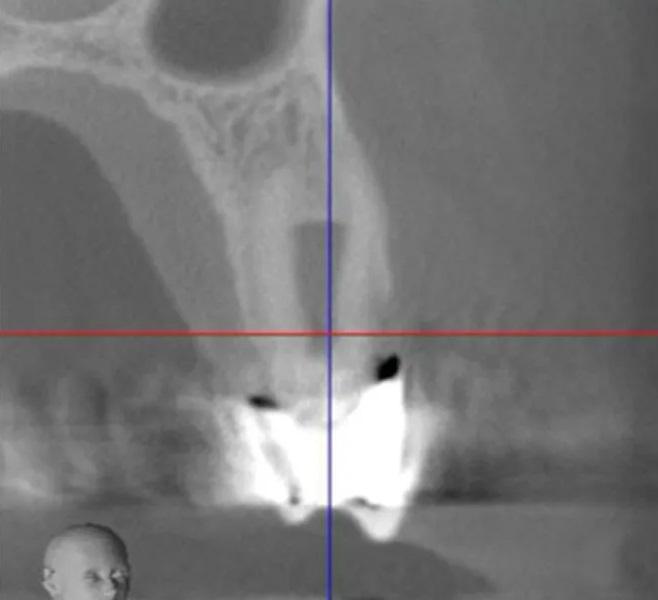
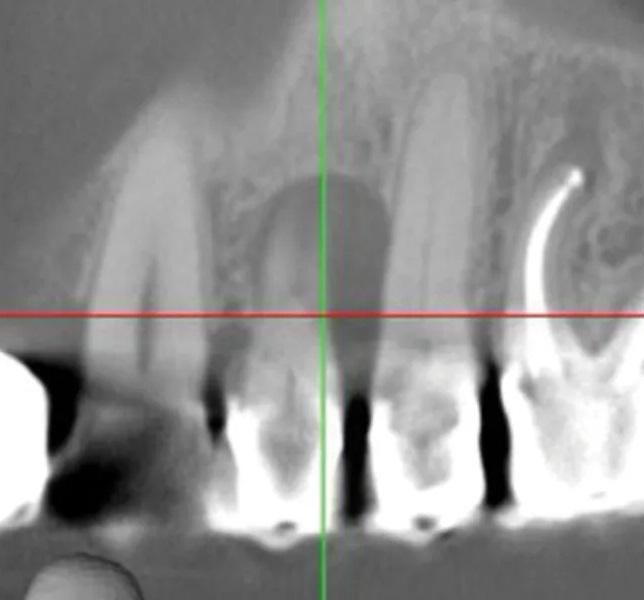
Фото 4. Предоперационный сагиттальный срез КЛКТ первого премоляра верхней челюсти слева, демонстрирующий область рентгенопрозрачности, вовлекающую более двух третей корня, включая пришеечную область и альвеолярный костный гребень.
Хирургическое удаление и регенеративные процедуры: После всестороннего изучения медицинского и стоматологического анамнеза пациента, клинического обследования и разработки индивидуального плана лечения было получено информированное согласие. За 30 минут до операции пациент получил премедикацию: амоксициллин 500 мг, ацетаминофен 500 мг и ибупрофен 600 мг. Были зафиксированы жизненные показатели и сделан периапикальный (ПА) рентгеновский снимок (Фото 5). Местная анестезия была проведена методом инфильтрации артикаина гидрохлоридом 4% с эпинефрином 1:100 000 (Septocaine, Septodont).
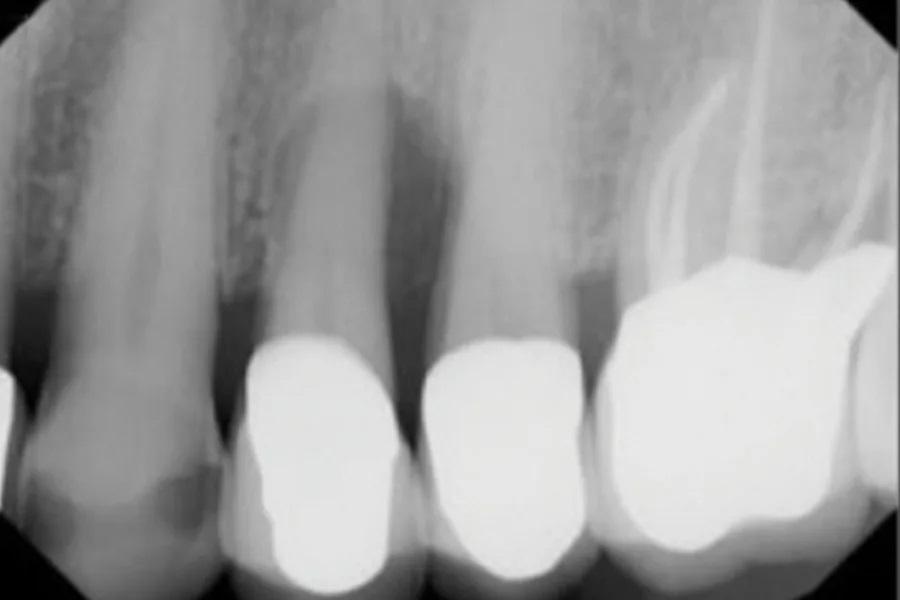
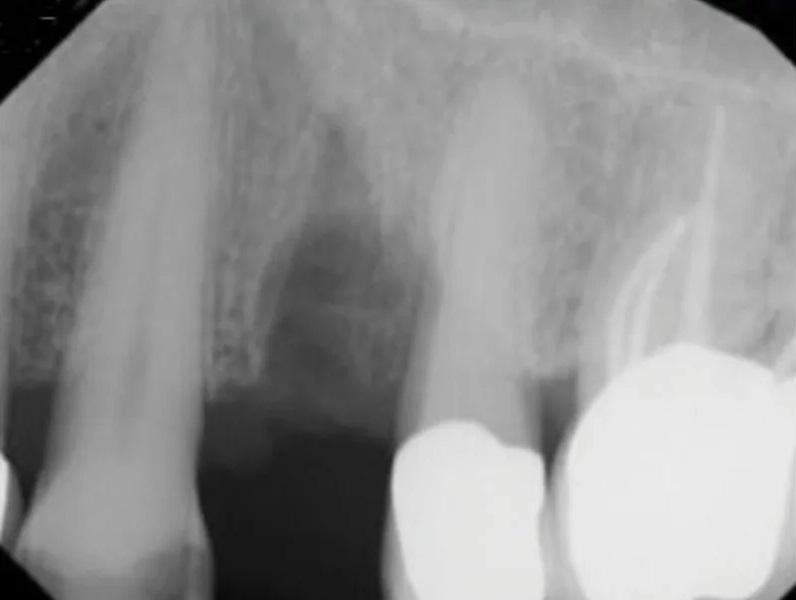
Фото 5. ПА рентгеновский снимок на исходном этапе перед удалением первого премоляра верхней челюсти слева.
Существующая реставрация (№ 2.4) была разделена для получения доступа к фуркации. Оба корня (щечный и небный) были удалены с использованием периотомов, элеваторов и щипцов. Лунка была очищена от грануляционной ткани, которая отправлена на гистопатологический анализ. ПА рентгеновский снимок подтвердил полное удаление корней. Процедура САГ была выполнена с использованием упомянутого выше резорбируемого ксеногенно-аллопластического биоматериала (OsteoGen Plug), который был адаптирован в лунку (Фото 6). ПА рентгеновский снимок подтвердил правильное размещение биоматериала. Участок был ушит швом из политетрафторэтилена (ПТФЭ) (Фото 7 – Фото 10). Пациенту были даны инструкции по гигиене полости рта и послеоперационному уходу.
Фото 6. Пробка из ксеногенно-аллопластического биоматериала была подточена для оптимальной адаптации к лунке.

Фото 7. Удаление первого премоляра верхней челюсти слева. Свежая лунка демонстрирует сохраненный контур мягких тканей.
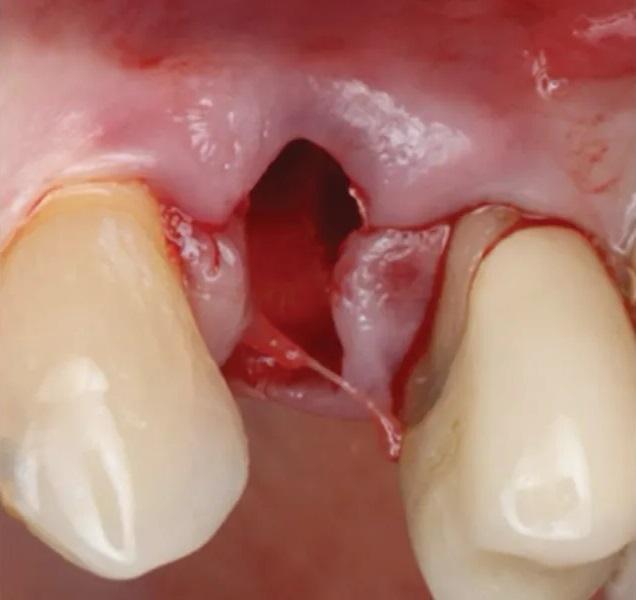
Фото 8. Вестибулярный лоскут слегка отслоен, видны хороший уровень васкуляризации и немедленное образование кровяного сгустка в лунке.
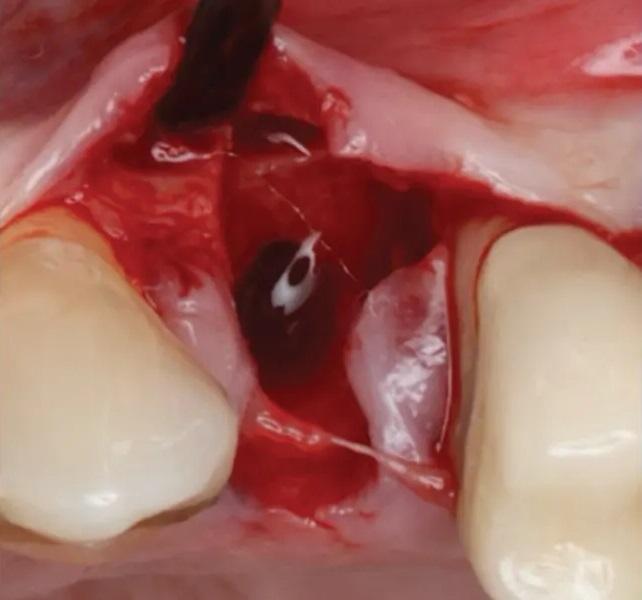
Фото 9. Пробка из ксеногенно-аллопластического биоматериала помещена в лунку, и наложен матрацный шов из ПТФЭ.
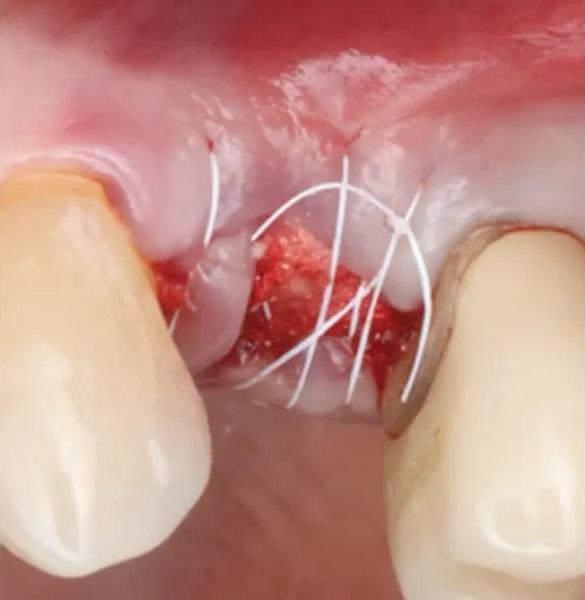
Фото 10. ПА рентгеновский снимок непосредственно после САГ.
На контрольном осмотре через 1 неделю пациент не сообщал о боли или отеке. Шов был удален, и инструкции по гигиене полости рта были повторены.
Через 5 месяцев после удаления были выполнены контрольные КЛКТ и интраоральное сканирование, а также завершено цифровое планирование имплантации (Фото 11).
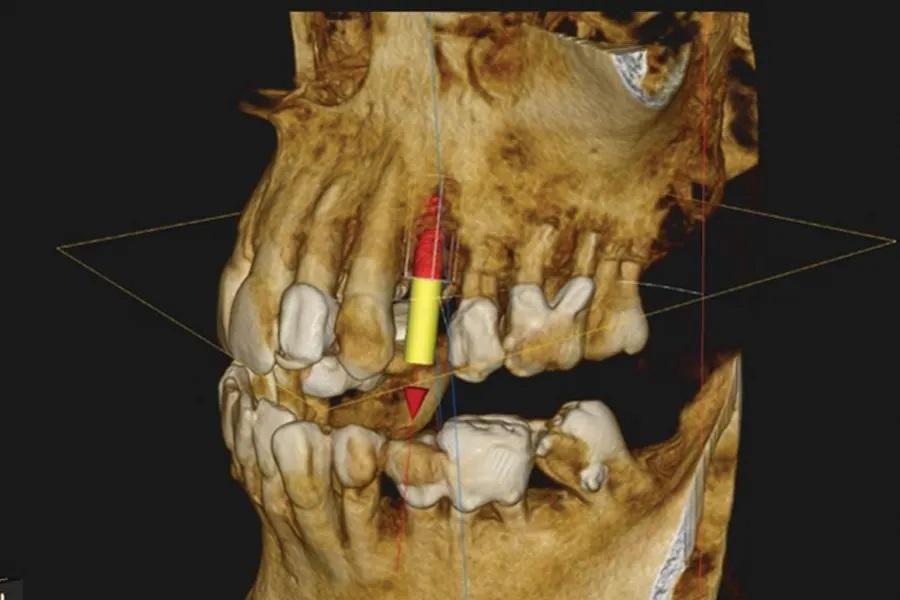
Фото 11. 3D-позиционирование имплантата при цифровом планировании.
Операция по установке имплантата: Изменений в состоянии здоровья пациента не отмечено. Форма информированного согласия была рассмотрена и подписана. За 30 минут до операции пациент получил премедикацию: амоксициллин 500 мг, ацетаминофен 500 мг и ибупрофен 600 мг. Была проведена местная инфильтрационная анестезия (Septocaine) с вестибулярной и небной сторон. Используя цифровое планирование имплантации на основе КЛКТ через 5 месяцев после удаления, был выполнен серединный гребневой разрез и отслоен полнослойный лоскут для доступа к кости. На нескольких этапах были сделаны ПА рентгеновские снимки, использовалась направляющая штанга для подтверждения глубины и угла, и был установлен конический имплантат на уровне кости диаметром 3,3 мм и длиной 10 мм (Straumann). Лоскуты были репозиционированы для увеличения толщины кератинизированной вестибулярной слизистой (Фото 12 – Фото 16).
Фото 12. Вестибулярный вид здоровых мягких тканей через 5 месяцев после удаления первого премоляра верхней челюсти слева.
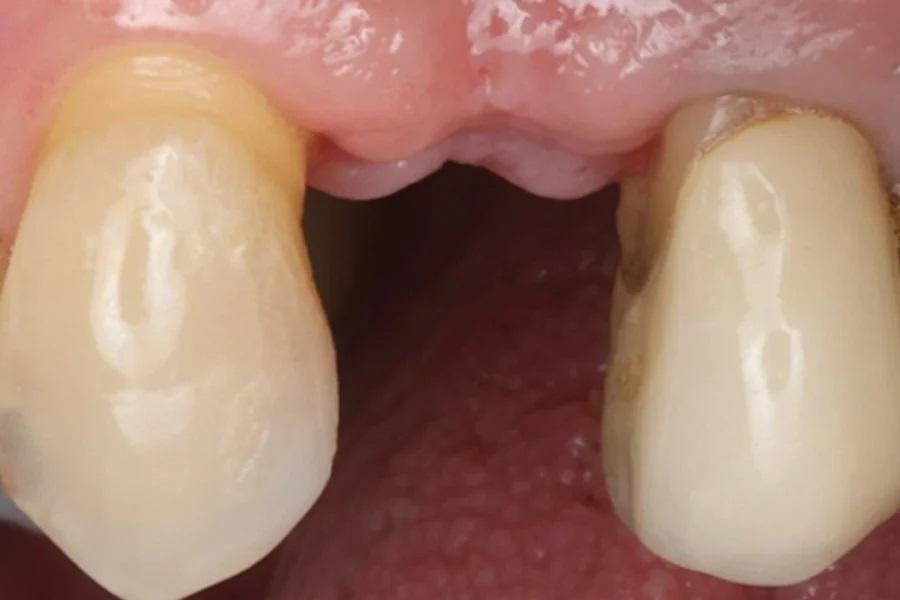
Фото 13. Окклюзионный вид сохраненного объема альвеолярного гребня после удаления.
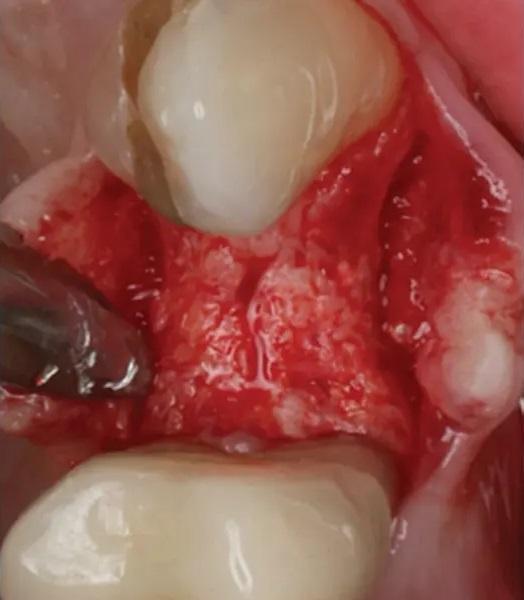
Фото 14. Окклюзионный вид ложа для установки имплантата.
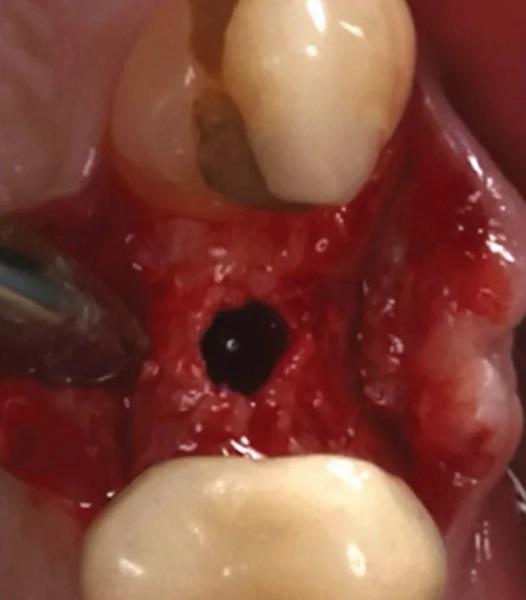
Фото 15. Окклюзионный вид гребня непосредственно после установки имплантата.
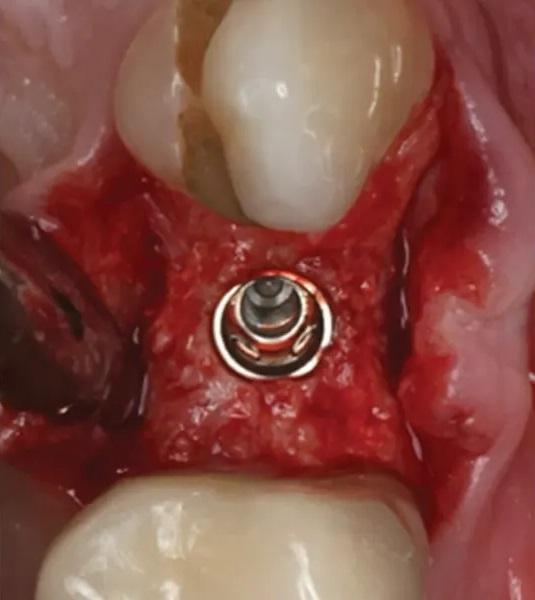
Фото 16. Окклюзионный вид шва, демонстрирующий первичное закрытие.
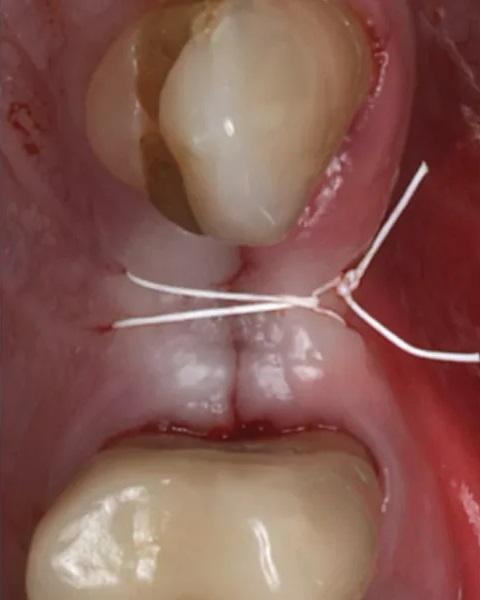
Пациенту были даны инструкции по гигиене полости рта и послеоперационному уходу. Швы были сняты через 1 неделю, и инструкции по гигиене полости рта были повторены.
Раскрытие имплантата: Через шесть месяцев после установки имплантата были выполнены оценка мягких тканей и рентгенография (Фото 17). Была проведена местная инфильтрационная анестезия препаратом Septocaine, выполнен гребневой разрез для обнажения ранее установленного имплантата. Была установлена формировательная головка (Фото 18). ПА рентгеновский снимок подтвердил краевое прилегание абатмента к имплантату (Фото 19). Участок был ушит швом ПТФЭ, и пациенту были даны инструкции по гигиене полости рта и послеоперационному уходу. Контрольный осмотр проведен через 2 недели после раскрытия имплантата, мягкие ткани выглядели здоровыми (Фото 20 и Фото 21).
Фото 17. Окклюзионный вид здоровых мягких тканей и ширины гребня через 6 месяцев после установки имплантата.
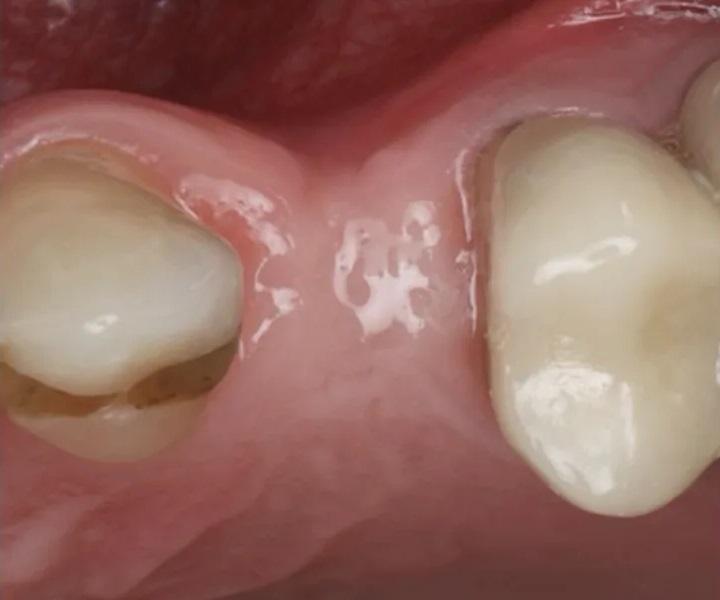
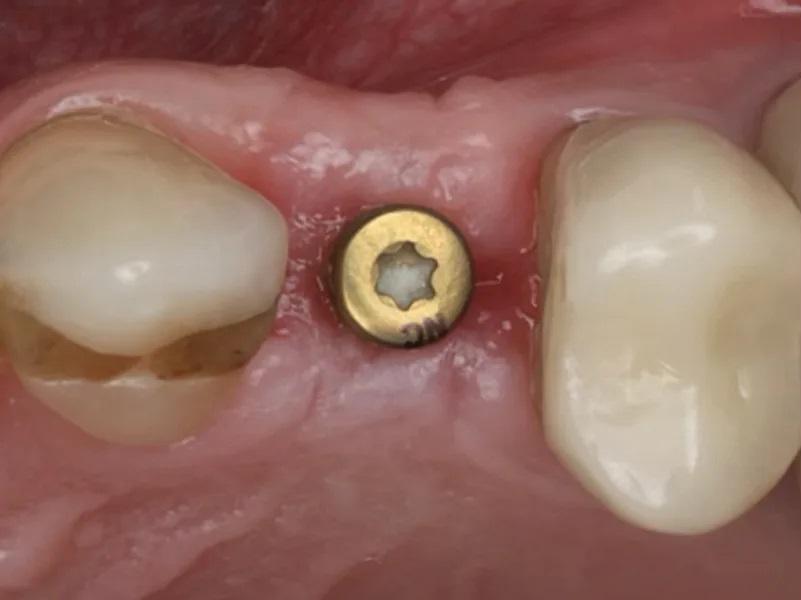
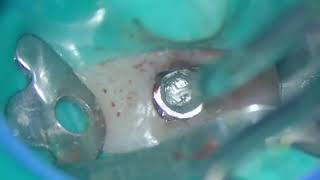
Фото 18. Вестибулярный вид непосредственно после раскрытия имплантата, установки абатмента и коррекции вестибулярной мягкой ткани.
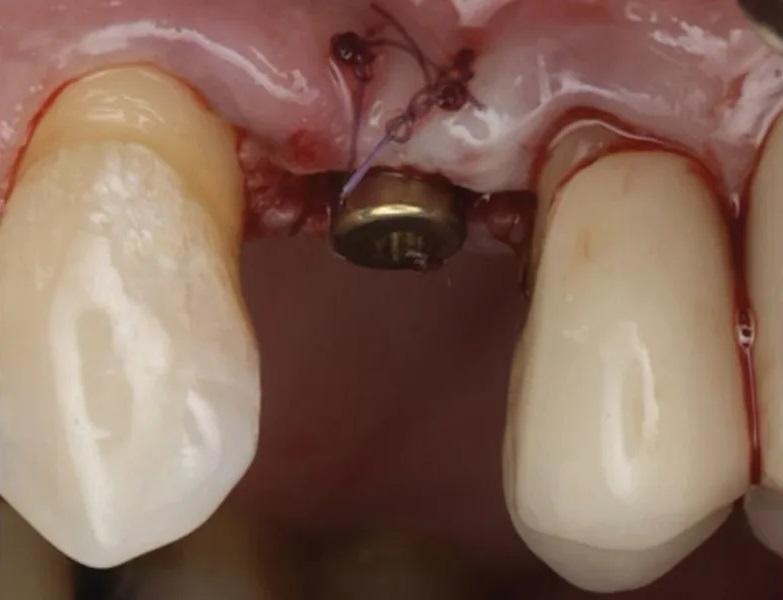
Фото 19. ПА рентгеновский снимок, подтверждающий хорошую посадку абатмента на имплантат.
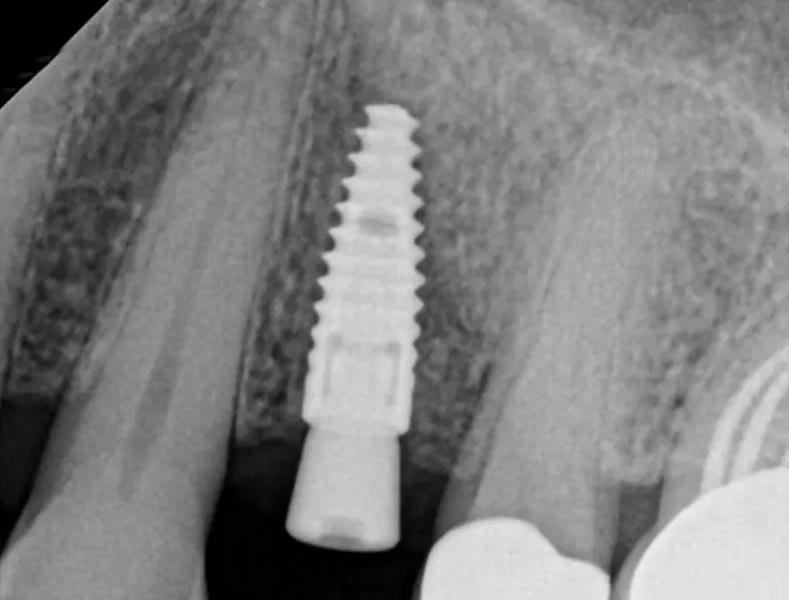
Фото 20. Через две недели после раскрытия имплантата.
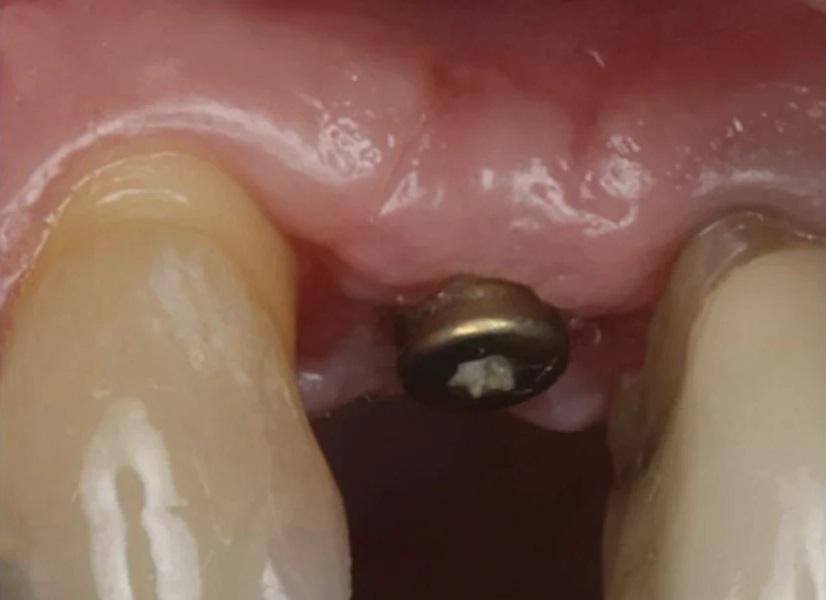
Фото 21. Окклюзионный вид ширины гребня через 2 недели после раскрытия имплантата, демонстрирующий улучшения на вестибулярной стороне мягкой ткани.
Окончательная реставрация была установлена на имплантат стоматологом-ортопедом через 4 недели после процедуры раскрытия имплантата.
Результаты
Заживление в данном случае протекало без осложнений, и в течение 5 месяцев после удаления зуба и проведения САГ были отмечены положительные клинические и рентгенологические изменения как в области удаления, так и на медиальной поверхности зуба № 2.5, включая наличие периодонтальной связки, что, возможно, указывает на регенерацию. Сохраненный объем гребня наряду с формированием плотной, хорошо интегрированной кости обеспечили оптимальное основание для установки имплантата. Кроме того, окружающая кератинизированная мягкая ткань показала стабильность и здоровую архитектуру, что способствует предсказуемым эстетическим и функциональным результатам имплантационной реставрации. Эти данные подчеркивают эффективность использованного в данном случае биоматериала.
На контрольном осмотре через 16 месяцев клиническая оценка выявила сохраненный объем гребня и стабильную кератинизированную мягкую ткань (Фото 22 и Фото 23). Рентгенологический анализ подтвердил стабильный уровень кости вокруг имплантата № 2.4 и положительные рентгенологические изменения, свидетельствующие о регенерации тканей на медиальной поверхности зуба № 2.5, включая восстановление периодонтальной связки (Фото 24).
Фото 22 и Фото 23. На контрольном осмотре через 16 месяцев: интраоральный окклюзионный вид (Фото 22) и латеральный вестибулярный вид (Фото 23) демонстрируют реставрацию на имплантате с винтовой фиксацией.
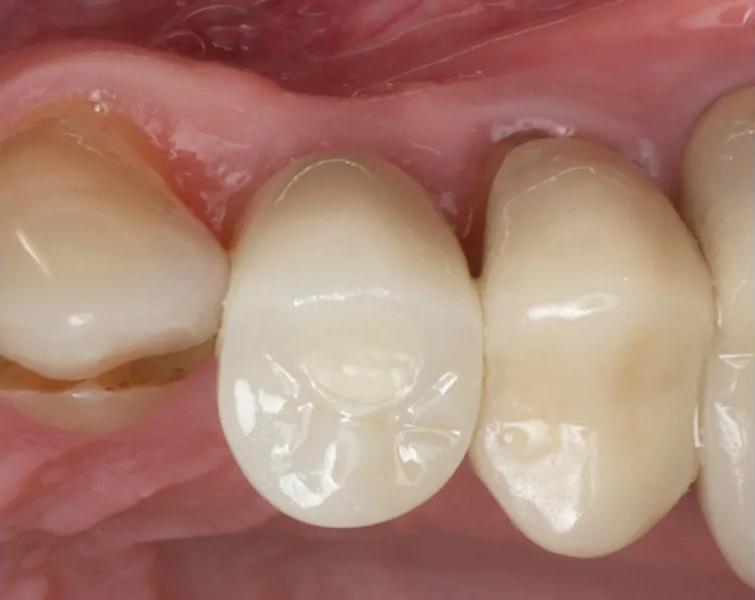
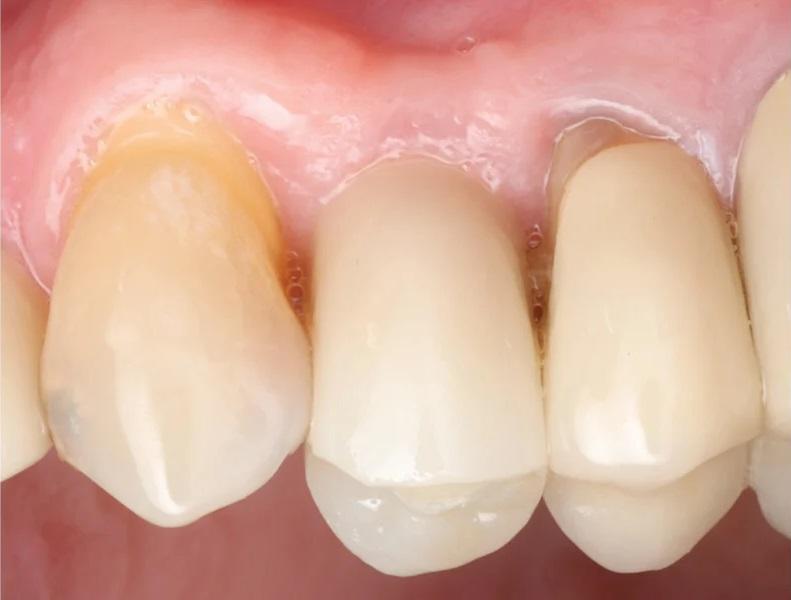
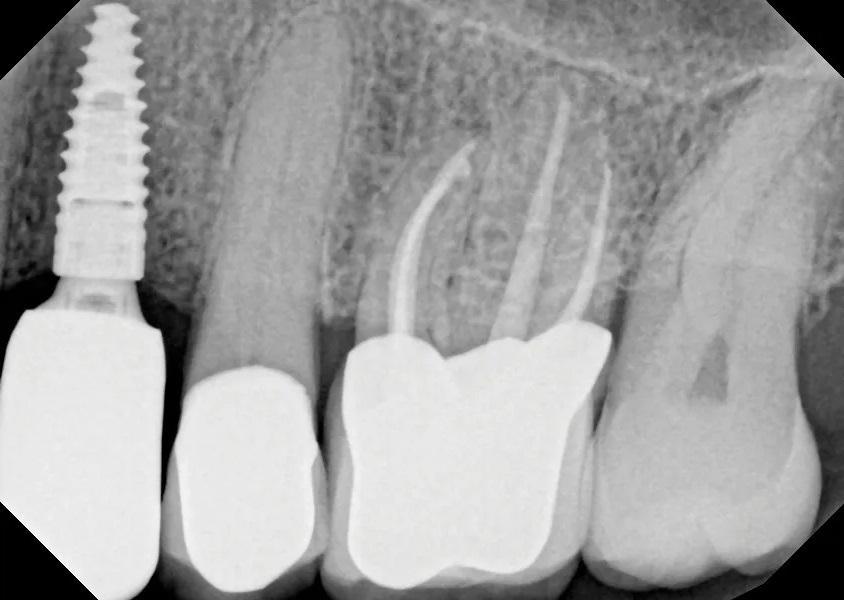
Фото 24. На контрольном осмотре через 16 месяцев: ПА рентгеновский снимок показывает стабильный уровень краевой кости, патологии не выявлено.
Обсуждение
Заживление пародонтальных ран — это высокодинамичный и многофакторный процесс, на который влияет широкий спектр локальных, системных и средовых факторов как на микро-, так и на макроуровне. Он включает скоординированное действие различных типов клеток, биологических медиаторов, цитокинов и компонентов внеклеточного матрикса, работающих через перекрывающиеся фазы заживления. Примечательно, что ранняя фаза играет решающую роль в определении общего результата.
Для поддержки оптимального заживления пародонтальной раны клиницисты должны придерживаться принципов PASS: обеспечение первичной стабильности раны, стимулирование ангиогенеза для адекватного кровоснабжения, создание пространства для репопуляции клеток и поддержание общей стабильности раны. Эти же принципы применимы к клинической цели сохранения оптимальных объемных размеров кости и мягких тканей после удаления зуба. Направленная тканевая регенерация и сохранение альвеолярного гребня — это различные, но взаимодополняющие подходы для повышения предсказуемости процедур регенерации тканей полости рта. НТР основана на принципе избирательной репопуляции клеток, когда барьерная мембрана используется для исключения прорастания десневой соединительной ткани и предотвращения врастания эпителия, позволяя регенеративным клеткам (например, из периодонтальной связки, кости и цемента) первыми заселить участок раны. С другой стороны, САГ фокусируется на сохранении размеров гребня после удаления зуба и имеет убедительные доказательства в этом отношении, тогда как клиническая эффективность используемых биоматериалов (таких как ауто-, алло-, ксенотрансплантаты и аллопласты) показывает лишь умеренные доказательства, в основном из-за неоднородности дизайна исследований и отчетности по материалам. В клинической практике выбор материала должен определяться рядом факторов, включая биологические и механические свойства, потенциал костеобразования, скорость резорбции, хирургические показания, комфорт пациента, реакцию заживления раны, долгосрочную стабильность, удовлетворенность пациента и экономическую эффективность.
Несмотря на многообещающую эффективность этих методик, среди наблюдаемых осложнений — экспозиция мембраны, инфицирование и необходимость дополнительного хирургического вмешательства. Кроме того, при принятии клинических решений с точки зрения, ориентированной на пациента, следует учитывать экономическую эффективность. Определяемая как степень, в которой вмешательство дает благоприятный результат по отношению к его стоимости, подход может быть признан менее экономически эффективным, если он дает минимальную клиническую пользу. Хотя это само по себе не осложнение, плохая экономическая эффективность может повлиять на непрерывность лечения, вводя дополнительные расходы и способствуя неудовлетворенности пациента. Помимо тщательного отбора случаев и скрупулезного планирования лечения, клинический выбор биоматериала может снизить частоту осложнений. Резорбируемый биоматериал, использованный в данном описании случая, состоящий из матрицы коллагена бычьего ахиллова сухожилия в сочетании с биоактивными резорбируемыми кристаллами апатита кальция, предназначен для использования при сохранении альвеолярного гребня. Исследования in vitro коммерчески доступных продуктов для САГ продемонстрировали, что резорбируемый ксеногенно-аллопластический биоматериал обладает высокой биосовместимостью, что подтверждается оценками остеогенного потенциала и целостности каркаса. Более того, рандомизированное контролируемое клиническое исследование с использованием КЛКТ методом разделения полости рта выявило значительно меньшую горизонтальную (1,36 мм) и вертикальную (0,91 мм) потерю кости на участках, обработанных биоматериалом, по сравнению с участками, заживавшими самостоятельно.
Данный биоматериал предназначен для однократного использования во время процедуры аугментации и предназначен для резорбции и замещения тканью хозяина с течением времени, что устраняет необходимость удаления мембраны или вторичных вмешательств. Важно отметить, что критерии отбора пациента для данного случая включали хороший контроль зубного налета, отсутствие системных заболеваний и высокую приверженность пациента лечению и поддерживающей терапии.
Данный случай является новым, поскольку в нем задокументировано успешное использование единого резорбируемого биоматериала для двух показаний к регенеративной пародонтальной терапии. Ограничением данного описания случая является то, что он представляет собой единичный пример и не может быть обобщен из-за своей уникальности и отсутствия включения в более широкую серию случаев.
Заключение
В рамках ограничений данного описания случая комбинированная ксеногенно-аллопластическая пробка оказалась эффективной, удобной в клиническом применении и экономичной альтернативой традиционным методикам САГ, требующим нескольких компонентов. Способность материала поддерживать сохранение гребня, способствовать образованию новой кости и поддерживать стабильность мягких тканей свидетельствует о многообещающем потенциале для упрощенных регенеративных протоколов в рутинной клинической практике. Для подтверждения этих данных и оценки долгосрочных результатов рекомендуются дальнейшие многоцентровые практико-ориентированные рандомизированные клинические исследования.
Авторы:
Diandra S. Luz, DDS
Irina F. Dragan, DDS, DMD, MS, eMBA
В данном описании клинического случая представлено использование единого резорбируемого композитного биоматериала, состоящего из бычьего коллагена и биоактивного апатита кальция, при комбинированном сложном дефекте, подчеркивая регенерацию тканей полости рта. Согласно стандартным процедурам лечения, 68-летний пациент был пролечен в условиях частной практики одним и тем же биоматериалом по двум различным терапевтическим показаниям: сохранение альвеолярного гребня в беззубом участке зуба № 2.4 и направленная тканевая регенерация на медиальной поверхности зуба № 2.5. Никакие другие биоматериалы не использовались при лечении данного комбинированного сложного дефекта. Заживление протекало без осложнений, и пациент был удовлетворен окончательным результатом лечения. Беззубый промежуток № 2.4 в дальнейшем был восстановлен с помощью реставрации с винтовой фиксацией на имплантате. На контрольном осмотре через 16 месяцев клиническая оценка выявила сохраненный объем гребня и стабильную кератинизированную мягкую ткань. Рентгенологический анализ подтвердил стабильный уровень кости вокруг имплантата № 2.4 и положительные рентгенологические изменения, свидетельствующие о регенерации тканей на медиальной поверхности зуба № 2.5, включая восстановление периодонтальной связки. В рамках ограничений данного описания случая, биоматериал продемонстрировал эффективность, удобство клинического применения и экономическую эффективность в качестве однокомпонентного подхода, уменьшая потребность в дополнительных вмешательствах.

Методы сохранения альвеолярного гребня (САГ) направлены на поддержание его объема путем заполнения лунки костным заменителем — аутогенным, аллогенным, ксеногенным трансплантатом или аллопластом — с мембраной или без нее, а также с пластикой мягких тканей для облегчения регенерации тканей полости рта. Хотя САГ имеет убедительные доказательства в сохранении размеров, эффективность биоматериалов оценивается как умеренная из-за ограниченной стандартизации и отчетности. Клиницисты должны взвешивать свойства и такие факторы, как биосовместимость, резорбция, доказательства формирования новой кости, удобство использования, послеоперационный комфорт, экономическая эффективность и предпочтения пациента. Дизайн каркаса также значительно влияет на результаты регенерации. Кроме того, взаимосвязанность пор, размер частиц и пористость влияют на поведение остеобластов, причем каркасы, богатые коллагеном, превосходят высокоминерализованные по показателям костеобразования.
Современная стоматология предлагает несколько вариантов лечения зуба, значительно пораженного пародонтологическим заболеванием, включая удаление с САГ или направленную тканевую регенерацию (НТР). При рассмотрении регенеративных методов восстановление поврежденных пародонтальных тканей так же важно, как и сохранение объема альвеолярного гребня для достижения успешной реабилитации. НТР использует мембраны для предотвращения врастания эпителиальных клеток в дефект и поддержания пространства для регенерации кости. Однако экспозиция мембраны остается частым осложнением, особенно если мембрана нерезорбируемая. Один из подходов к решению этой проблемы — использование резорбируемого ксеногенно-аллопластического биоматериала (OsteoGen Plug, Impladent Ltd.), разработанного для поддержки ключевых принципов регенерации тканей полости рта при одновременном снижении риска коллапса мембраны. Состоящий из резорбируемого апатита кальция и коллагена из бычьего ахиллова сухожилия, биоматериал имитирует органические и неорганические компоненты натуральной кости. Его форма в виде пробки предлагает простую, экономически эффективную альтернативу костным гранулам и мембранным трансплантатам, улучшая удобство клинического применения.
В данном описании клинического случая представлено использование этого резорбируемого каркаса из бычьего коллагена и биоактивного апатита кальция в качестве единственного биоматериала для САГ в беззубом участке зуба № 2.4 и для НТР на медиальной поверхности зуба № 2.5.
Клинический случай
Пациент мужского пола 68 лет был направлен эндодонтистом с диагнозом симптоматический необратимый пульпит с нормальными периапикальными тканями и значительной потерей костной ткани с вовлечением фуркации у первого премоляра верхней челюсти слева (зуб № 2.4). Из-за состояния пародонта была показана реабилитация с помощью имплантационной реставрации. Конусно-лучевая компьютерная томография (КЛКТ) выявила потерю кости с дистальной стороны пораженного зуба, размером 5 мм в ширину и 9 мм в длину соответственно, с вовлечением альвеолярного костного гребня (Фото 1 – Фото 4).
Фото 1. Предоперационный интраоральный передний вид.

Фото 2. Предоперационный интраоральный латеральный вестибулярный вид.

Фото 3. Предоперационный корональный срез КЛКТ первого премоляра верхней челюсти слева.

Фото 4. Предоперационный сагиттальный срез КЛКТ первого премоляра верхней челюсти слева, демонстрирующий область рентгенопрозрачности, вовлекающую более двух третей корня, включая пришеечную область и альвеолярный костный гребень.

Хирургическое удаление и регенеративные процедуры: После всестороннего изучения медицинского и стоматологического анамнеза пациента, клинического обследования и разработки индивидуального плана лечения было получено информированное согласие. За 30 минут до операции пациент получил премедикацию: амоксициллин 500 мг, ацетаминофен 500 мг и ибупрофен 600 мг. Были зафиксированы жизненные показатели и сделан периапикальный (ПА) рентгеновский снимок (Фото 5). Местная анестезия была проведена методом инфильтрации артикаина гидрохлоридом 4% с эпинефрином 1:100 000 (Septocaine, Septodont).
Фото 5. ПА рентгеновский снимок на исходном этапе перед удалением первого премоляра верхней челюсти слева.

Существующая реставрация (№ 2.4) была разделена для получения доступа к фуркации. Оба корня (щечный и небный) были удалены с использованием периотомов, элеваторов и щипцов. Лунка была очищена от грануляционной ткани, которая отправлена на гистопатологический анализ. ПА рентгеновский снимок подтвердил полное удаление корней. Процедура САГ была выполнена с использованием упомянутого выше резорбируемого ксеногенно-аллопластического биоматериала (OsteoGen Plug), который был адаптирован в лунку (Фото 6). ПА рентгеновский снимок подтвердил правильное размещение биоматериала. Участок был ушит швом из политетрафторэтилена (ПТФЭ) (Фото 7 – Фото 10). Пациенту были даны инструкции по гигиене полости рта и послеоперационному уходу.
Фото 6. Пробка из ксеногенно-аллопластического биоматериала была подточена для оптимальной адаптации к лунке.

Фото 7. Удаление первого премоляра верхней челюсти слева. Свежая лунка демонстрирует сохраненный контур мягких тканей.

Фото 8. Вестибулярный лоскут слегка отслоен, видны хороший уровень васкуляризации и немедленное образование кровяного сгустка в лунке.

Фото 9. Пробка из ксеногенно-аллопластического биоматериала помещена в лунку, и наложен матрацный шов из ПТФЭ.

Фото 10. ПА рентгеновский снимок непосредственно после САГ.

На контрольном осмотре через 1 неделю пациент не сообщал о боли или отеке. Шов был удален, и инструкции по гигиене полости рта были повторены.
Через 5 месяцев после удаления были выполнены контрольные КЛКТ и интраоральное сканирование, а также завершено цифровое планирование имплантации (Фото 11).
Фото 11. 3D-позиционирование имплантата при цифровом планировании.

Операция по установке имплантата: Изменений в состоянии здоровья пациента не отмечено. Форма информированного согласия была рассмотрена и подписана. За 30 минут до операции пациент получил премедикацию: амоксициллин 500 мг, ацетаминофен 500 мг и ибупрофен 600 мг. Была проведена местная инфильтрационная анестезия (Septocaine) с вестибулярной и небной сторон. Используя цифровое планирование имплантации на основе КЛКТ через 5 месяцев после удаления, был выполнен серединный гребневой разрез и отслоен полнослойный лоскут для доступа к кости. На нескольких этапах были сделаны ПА рентгеновские снимки, использовалась направляющая штанга для подтверждения глубины и угла, и был установлен конический имплантат на уровне кости диаметром 3,3 мм и длиной 10 мм (Straumann). Лоскуты были репозиционированы для увеличения толщины кератинизированной вестибулярной слизистой (Фото 12 – Фото 16).
Фото 12. Вестибулярный вид здоровых мягких тканей через 5 месяцев после удаления первого премоляра верхней челюсти слева.

Фото 13. Окклюзионный вид сохраненного объема альвеолярного гребня после удаления.

Фото 14. Окклюзионный вид ложа для установки имплантата.

Фото 15. Окклюзионный вид гребня непосредственно после установки имплантата.

Фото 16. Окклюзионный вид шва, демонстрирующий первичное закрытие.

Пациенту были даны инструкции по гигиене полости рта и послеоперационному уходу. Швы были сняты через 1 неделю, и инструкции по гигиене полости рта были повторены.
Раскрытие имплантата: Через шесть месяцев после установки имплантата были выполнены оценка мягких тканей и рентгенография (Фото 17). Была проведена местная инфильтрационная анестезия препаратом Septocaine, выполнен гребневой разрез для обнажения ранее установленного имплантата. Была установлена формировательная головка (Фото 18). ПА рентгеновский снимок подтвердил краевое прилегание абатмента к имплантату (Фото 19). Участок был ушит швом ПТФЭ, и пациенту были даны инструкции по гигиене полости рта и послеоперационному уходу. Контрольный осмотр проведен через 2 недели после раскрытия имплантата, мягкие ткани выглядели здоровыми (Фото 20 и Фото 21).
Фото 17. Окклюзионный вид здоровых мягких тканей и ширины гребня через 6 месяцев после установки имплантата.

Фото 18. Вестибулярный вид непосредственно после раскрытия имплантата, установки абатмента и коррекции вестибулярной мягкой ткани.

Фото 19. ПА рентгеновский снимок, подтверждающий хорошую посадку абатмента на имплантат.

Фото 20. Через две недели после раскрытия имплантата.

Фото 21. Окклюзионный вид ширины гребня через 2 недели после раскрытия имплантата, демонстрирующий улучшения на вестибулярной стороне мягкой ткани.

Окончательная реставрация была установлена на имплантат стоматологом-ортопедом через 4 недели после процедуры раскрытия имплантата.
Результаты
Заживление в данном случае протекало без осложнений, и в течение 5 месяцев после удаления зуба и проведения САГ были отмечены положительные клинические и рентгенологические изменения как в области удаления, так и на медиальной поверхности зуба № 2.5, включая наличие периодонтальной связки, что, возможно, указывает на регенерацию. Сохраненный объем гребня наряду с формированием плотной, хорошо интегрированной кости обеспечили оптимальное основание для установки имплантата. Кроме того, окружающая кератинизированная мягкая ткань показала стабильность и здоровую архитектуру, что способствует предсказуемым эстетическим и функциональным результатам имплантационной реставрации. Эти данные подчеркивают эффективность использованного в данном случае биоматериала.
На контрольном осмотре через 16 месяцев клиническая оценка выявила сохраненный объем гребня и стабильную кератинизированную мягкую ткань (Фото 22 и Фото 23). Рентгенологический анализ подтвердил стабильный уровень кости вокруг имплантата № 2.4 и положительные рентгенологические изменения, свидетельствующие о регенерации тканей на медиальной поверхности зуба № 2.5, включая восстановление периодонтальной связки (Фото 24).
Фото 22 и Фото 23. На контрольном осмотре через 16 месяцев: интраоральный окклюзионный вид (Фото 22) и латеральный вестибулярный вид (Фото 23) демонстрируют реставрацию на имплантате с винтовой фиксацией.


Фото 24. На контрольном осмотре через 16 месяцев: ПА рентгеновский снимок показывает стабильный уровень краевой кости, патологии не выявлено.

Обсуждение
Заживление пародонтальных ран — это высокодинамичный и многофакторный процесс, на который влияет широкий спектр локальных, системных и средовых факторов как на микро-, так и на макроуровне. Он включает скоординированное действие различных типов клеток, биологических медиаторов, цитокинов и компонентов внеклеточного матрикса, работающих через перекрывающиеся фазы заживления. Примечательно, что ранняя фаза играет решающую роль в определении общего результата.
Для поддержки оптимального заживления пародонтальной раны клиницисты должны придерживаться принципов PASS: обеспечение первичной стабильности раны, стимулирование ангиогенеза для адекватного кровоснабжения, создание пространства для репопуляции клеток и поддержание общей стабильности раны. Эти же принципы применимы к клинической цели сохранения оптимальных объемных размеров кости и мягких тканей после удаления зуба. Направленная тканевая регенерация и сохранение альвеолярного гребня — это различные, но взаимодополняющие подходы для повышения предсказуемости процедур регенерации тканей полости рта. НТР основана на принципе избирательной репопуляции клеток, когда барьерная мембрана используется для исключения прорастания десневой соединительной ткани и предотвращения врастания эпителия, позволяя регенеративным клеткам (например, из периодонтальной связки, кости и цемента) первыми заселить участок раны. С другой стороны, САГ фокусируется на сохранении размеров гребня после удаления зуба и имеет убедительные доказательства в этом отношении, тогда как клиническая эффективность используемых биоматериалов (таких как ауто-, алло-, ксенотрансплантаты и аллопласты) показывает лишь умеренные доказательства, в основном из-за неоднородности дизайна исследований и отчетности по материалам. В клинической практике выбор материала должен определяться рядом факторов, включая биологические и механические свойства, потенциал костеобразования, скорость резорбции, хирургические показания, комфорт пациента, реакцию заживления раны, долгосрочную стабильность, удовлетворенность пациента и экономическую эффективность.
Несмотря на многообещающую эффективность этих методик, среди наблюдаемых осложнений — экспозиция мембраны, инфицирование и необходимость дополнительного хирургического вмешательства. Кроме того, при принятии клинических решений с точки зрения, ориентированной на пациента, следует учитывать экономическую эффективность. Определяемая как степень, в которой вмешательство дает благоприятный результат по отношению к его стоимости, подход может быть признан менее экономически эффективным, если он дает минимальную клиническую пользу. Хотя это само по себе не осложнение, плохая экономическая эффективность может повлиять на непрерывность лечения, вводя дополнительные расходы и способствуя неудовлетворенности пациента. Помимо тщательного отбора случаев и скрупулезного планирования лечения, клинический выбор биоматериала может снизить частоту осложнений. Резорбируемый биоматериал, использованный в данном описании случая, состоящий из матрицы коллагена бычьего ахиллова сухожилия в сочетании с биоактивными резорбируемыми кристаллами апатита кальция, предназначен для использования при сохранении альвеолярного гребня. Исследования in vitro коммерчески доступных продуктов для САГ продемонстрировали, что резорбируемый ксеногенно-аллопластический биоматериал обладает высокой биосовместимостью, что подтверждается оценками остеогенного потенциала и целостности каркаса. Более того, рандомизированное контролируемое клиническое исследование с использованием КЛКТ методом разделения полости рта выявило значительно меньшую горизонтальную (1,36 мм) и вертикальную (0,91 мм) потерю кости на участках, обработанных биоматериалом, по сравнению с участками, заживавшими самостоятельно.
Данный биоматериал предназначен для однократного использования во время процедуры аугментации и предназначен для резорбции и замещения тканью хозяина с течением времени, что устраняет необходимость удаления мембраны или вторичных вмешательств. Важно отметить, что критерии отбора пациента для данного случая включали хороший контроль зубного налета, отсутствие системных заболеваний и высокую приверженность пациента лечению и поддерживающей терапии.
Данный случай является новым, поскольку в нем задокументировано успешное использование единого резорбируемого биоматериала для двух показаний к регенеративной пародонтальной терапии. Ограничением данного описания случая является то, что он представляет собой единичный пример и не может быть обобщен из-за своей уникальности и отсутствия включения в более широкую серию случаев.
Заключение
В рамках ограничений данного описания случая комбинированная ксеногенно-аллопластическая пробка оказалась эффективной, удобной в клиническом применении и экономичной альтернативой традиционным методикам САГ, требующим нескольких компонентов. Способность материала поддерживать сохранение гребня, способствовать образованию новой кости и поддерживать стабильность мягких тканей свидетельствует о многообещающем потенциале для упрощенных регенеративных протоколов в рутинной клинической практике. Для подтверждения этих данных и оценки долгосрочных результатов рекомендуются дальнейшие многоцентровые практико-ориентированные рандомизированные клинические исследования.
Авторы:
Diandra S. Luz, DDS
Irina F. Dragan, DDS, DMD, MS, eMBA





























































































































































0 комментариев