Лечение расхождения мягких тканей вокруг имплантата (РМТВИ) может быть довольно сложным для многих лечащих врачей и оставлять серьезные эстетические проблемы для пациентов. В данной статье описывается лечение двух соседних РМТВИ в переднем отделе, где также наблюдался дефект сосочков. В данном случае был использован откинутый в корональном направлении лоскут и соединительнотканный трансплантат (СТТ) с погружным заживлением. Коронки и абатменты с опорой на имплантаты были удалены, и было проведено наращивание мягких тканей с помощью СТТ, который был подшит к щечной стороне места установки имплантатов. Лоскут был выкроен и подшит над имплантатами, которые были погружены с целью закрытия первичным натяжением. Через 3 месяца для увеличения ширины кератинизированной слизистой вокруг имплантатов и наращивания периимплантатного сосочка была проведена комбинированная операция с использованием апикально расположенного лоскута и ротированного лоскута. Через 1 год были получены удовлетворительные клинические и эстетические результаты.
РМТВИ может ухудшить восприятие пациентами имплантологического лечения и, возможно, оказать негативное влияние на качество их жизни. Было выявлено несколько факторов риска возникновения РМТВИ, к которым относятся недостаточное количество кератинизированной слизистой и толщина мягких тканей, буккально расположенные имплантаты, тонкая буккальная кость, расхождения краев или фенестрации костной ткани, а также несколько соседних дентальных имплантатов. В частности, недавнее исследование, проведенное нашими авторами, показало, что каждый миллиметр увеличения расхождения буккальной костной ткани повышает вероятность возникновения РМТВИ примерно на 41%.
Для лечения ПСТД описано несколько подходов, включая использование откинутого в корональном направлении лоскута (ОКНЛ) в сочетании с соединительнотканным трансплантатом (СТТ), туннельные методы (ТУН), свободные десневые трансплантаты, процедуры направленной костной регенерации, хирургический ортопедический подход и вертикальное наращивание мягких тканей с использованием СТТ-платформенного подхода. Целесообразность применения этих подходов во многом зависит от ожиданий и финансовых возможностей пациента, а также от характеристик эстетического осложнения со стороны имплантата, включая высоту коронки с опорой на имплантат, букколингвальное положение имплантата и размер сосочков, но не ограничиваясь ими. Недавно группа авторов представила классификацию РМТВИ, а также рекомендации по их лечению.Четыре основных класса (I, II, III и IV) были определены на основе букколингвального положения коронки/платформы имплантата, с тремя подклассами (a, b и c), которые относятся к высоте сосочков вокруг имплантата. Более сложные случаи включают в себя несколько соседних имплантатов с РМТВИ.
В данной статье описан случай установки двух дентальных имплантатов в передней верхней челюсти с дегисценцией мягких тканей, которые были пролечены с помощью ОКНЛ + СТТ с использованием погружного подхода.
Описание клинического случая и план лечения
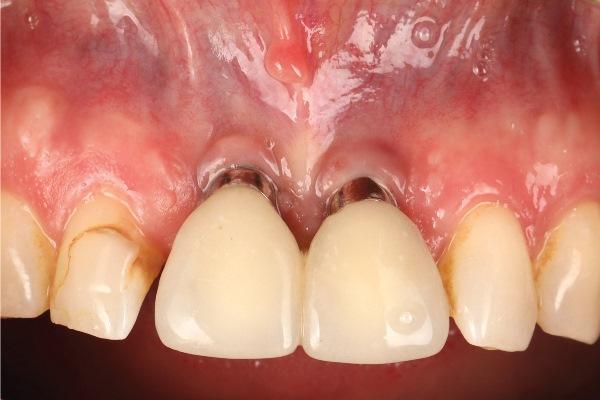
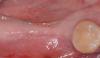
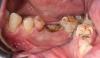
Пациентка, 46 лет, соматически и пародонтологически здоровая, обратилась в клинику пародонтологии Мичиганского университета с жалобами на плохую эстетику улыбки из-за двух дентальных имплантатов (1.1 и 2.1), на которых видны металлические компоненты (фото 1). Пациентка сообщила, что имплантаты были установлены 15-20 лет назад после несчастного случая. Клинический осмотр показал, что глубина зондирования имплантатов не превышает 3 мм (глубина зондирования с вестибулярной стороны 3-2-3 мм для имплантата 1.1 и 2-2-2 мм для имплантата 2.1), кровотечение при зондировании и нагноение отсутствуют, поэтому имплантаты были признаны состоятельными (фото 1 и фото 2). Сосочек между двумя имплантатами был неполноценным с щечной стороны. Имплантаты были установлены буккально, и отмечался значительный недостаток объема мягких тканей.
Фото 1: Вид в момент приема.

Фото 2: Изначальная периапикальная рентгенограмма.

План лечения был составлен и обсужден с пациентом и включал удаление коронок и абатментов с опорой на имплантаты и хирургическое вмешательство с применением ОКНЛ + СТТ с погружным заживлением.
Откинутый в корональном направлении лоскут и соединительнотканный трансплантат с погружным заживлением
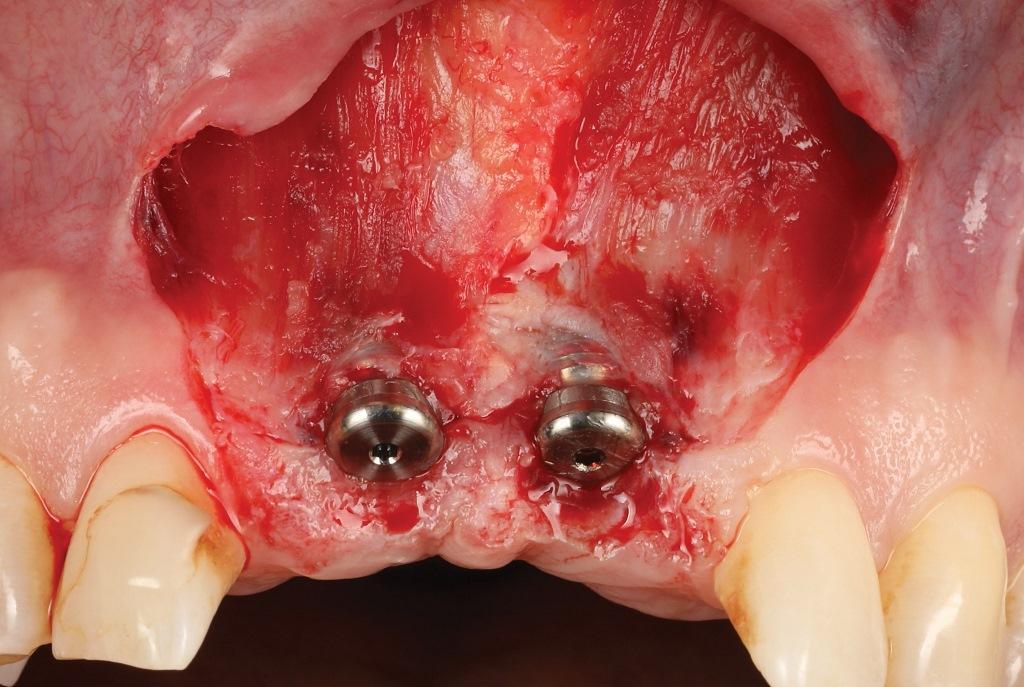
Инструкции по гигиене полости рта были рассмотрены с пациентом и закреплены за 6 недель до посещения с целью хирургического вмешательства. На приеме у хирурга коронки и абатменты с опорой на имплантаты были удалены, и были установлены два покрывных винта. Был выкроен расщепленный ОКНЛ трапециевидной формы (фото 3). Два слегка расходящихся косых разреза были расположены между имплантатами и боковыми резцами. Расщепленный лоскут был поднят, при этом соблюдалась осторожность, чтобы сохранить слой соединительной ткани, прилегающей к поверхности имплантата. Сохранение этого слоя соединительной ткани на корпусе имплантата, лишенного костной ткани с щечной стороны, является важным этапом, который отличает поднятие лоскута на состоятельных имплантатах с РМТВИ от имплантатов с периимплантитом (фото 4).
Фото 3: Откинутый в корональном направлении лоскут после удаления коронок для аугментации мягких тканей.

Фото 4: Поднятие расщепленного лоскута.
После этого лоскут высвобождался глубоким разрезом параллельно кости, а затем поверхностным разрезом лезвием параллельно наружной поверхности слизистой оболочки, пока он не мог пассивно достичь положения, примерно на 2 мм корональнее идеального конечного уровня края мягких тканей. С помощью микроножа были деэпителизированы анатомические сосочки между имплантатами и боковыми резцами, а также межрезцовый сосочек, причем не только c щечной, но и c окклюзионной стороны, чтобы улучшить сосудистое ложе для лоскута.
Свободный десневой трансплантат был взят с неба и затем деэпителизирован вне полости рта для получения плотного и волокнистого СТТ (фото 5). На небный донорский участок накладывалась коллагеновая губка и стабилизировалась швом из политетрафторэтилена (ПТФЭ) 5-0. Поверх коллагеновой губки наносился тонкий слой цианоакрилатного тканевого клея, как описано в работе Tavelli et al. в 2019 году. На поверхность имплантата не наносились химические или механические средства для кондиционирования корня. СТТ стабилизировали простыми прерывистыми швами (7-0 полигликолевая кислота [ПГК], "бабочка") к деэпителизированным анатомическим сосочкам с корональной стороны и надкостнице в апикальной части (фото 6). Затем лоскут был откинут в корональном направлении и ушит простыми прерывистыми швами (6-0 и 7-0 полипропилен) на уровне вертикальных разрезов и на уровне небного края, чтобы полностью закрыть трансплантат и покрывные винты (фото 7).
Фото 5: Соединительнотканный трансплантат, полученный в результате деэпителизации эпителизированного десневого трансплантата.
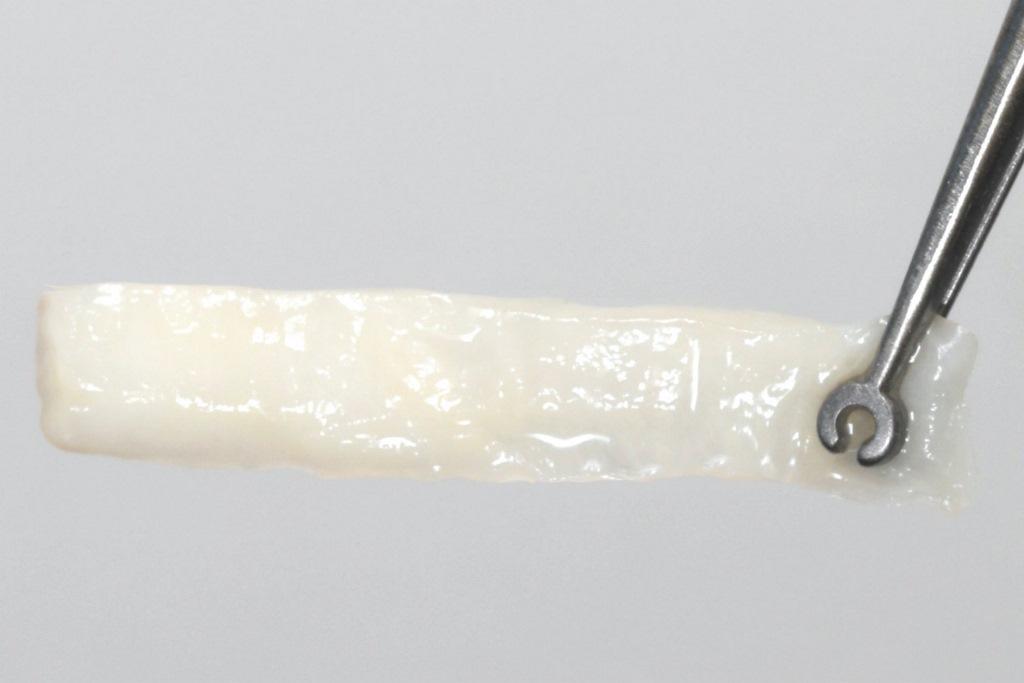
Фото 6: Стабилизация соединительнотканного трансплантата.
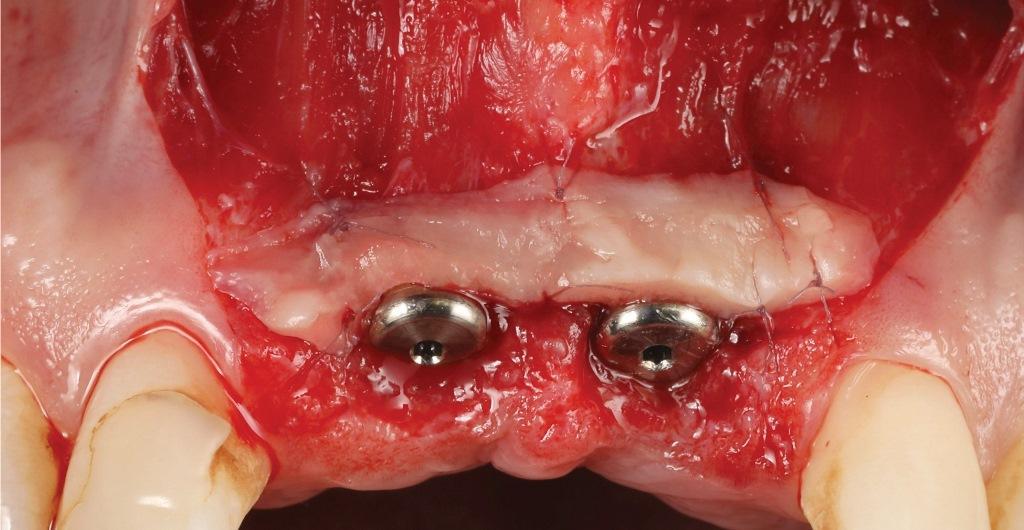
Фото 7: Погружное заживление с закрытием лоскута.
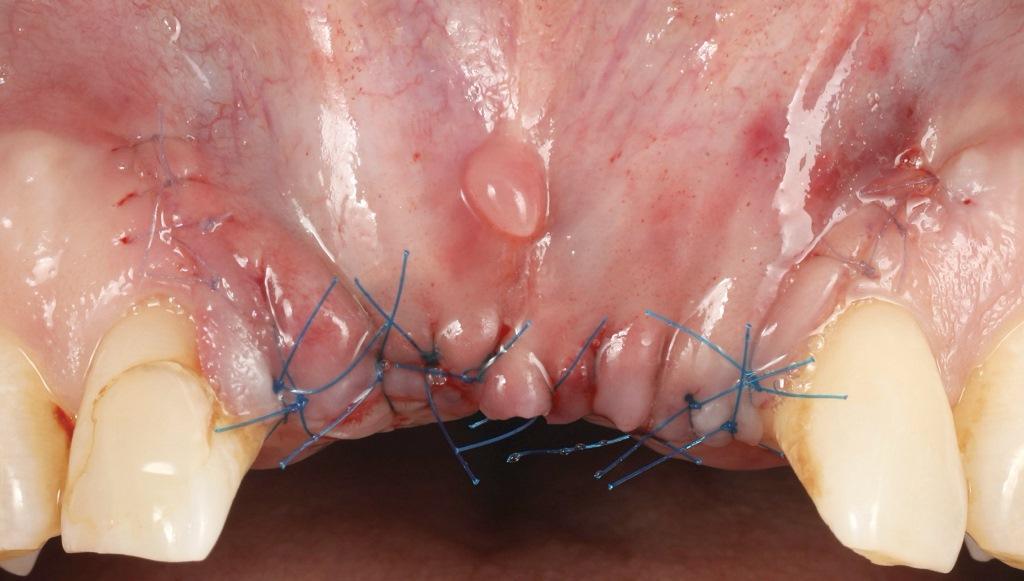
Швы были сняты через 2 недели, и пациентка сообщила об ограниченной степени осложнений в послеоперационном периоде.
Повторное открытие участка и восстановительный этап
Через 3 месяца после погружного заживления на оперированном участке появилась ограниченная кератинизированная слизистая оболочка с щечной стороны (фото 8). Поэтому был выкроен лоскут двумя вертикальными разрезами, начиная с небной стороны двух погруженных имплантатов. Кроме того, часть лоскута в средней части неба была вытянута к небной стороне для получения ротированного лоскута, который был деэпителизирован бором и в итоге свернут для увеличения объема межпроксимальной мягкой ткани между двумя имплантатами (фото 9). Расщепленный лоскут был поднят, при этом мягкие ткани над имплантатами были удалены, чтобы выявить покрывные винты (фото 10). По сравнению с первым хирургическим вмешательством наблюдалось значительное увеличение толщины мягких тканей с щечной стороны имплантатов (фото 11), когда имплантаты были видны через тонкий слой соединительнотканных волокон, прилегающих к поверхностям имплантатов. Покрывные винты были удалены, и были установлены временные титановые абатменты.
Фото 8: Место операции через 3 месяца.
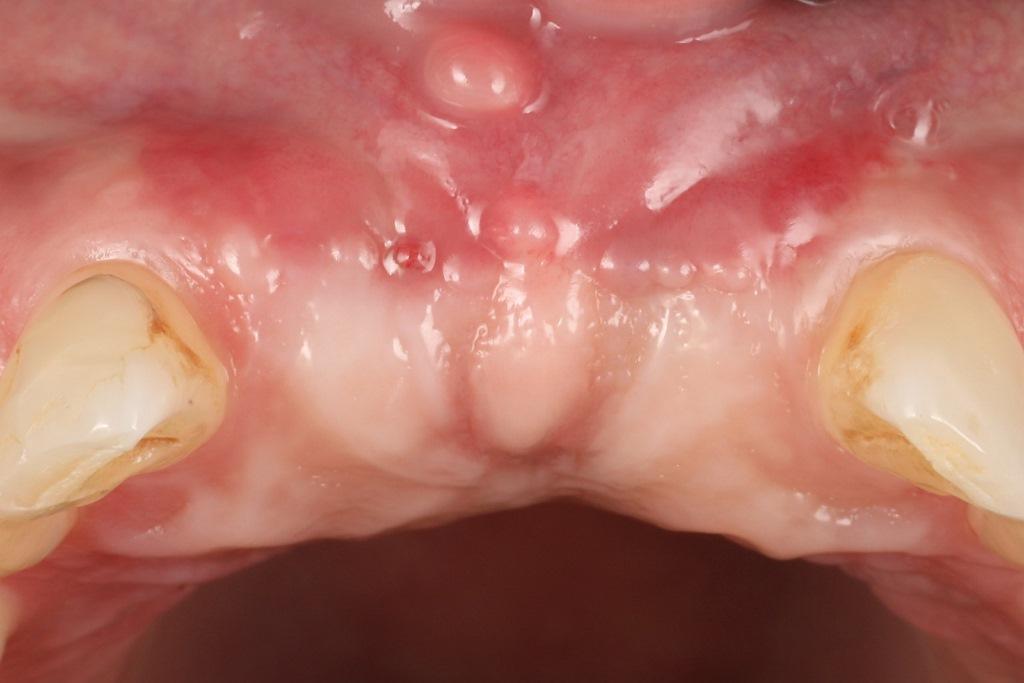
Фото 9: Планирование формы лоскута.
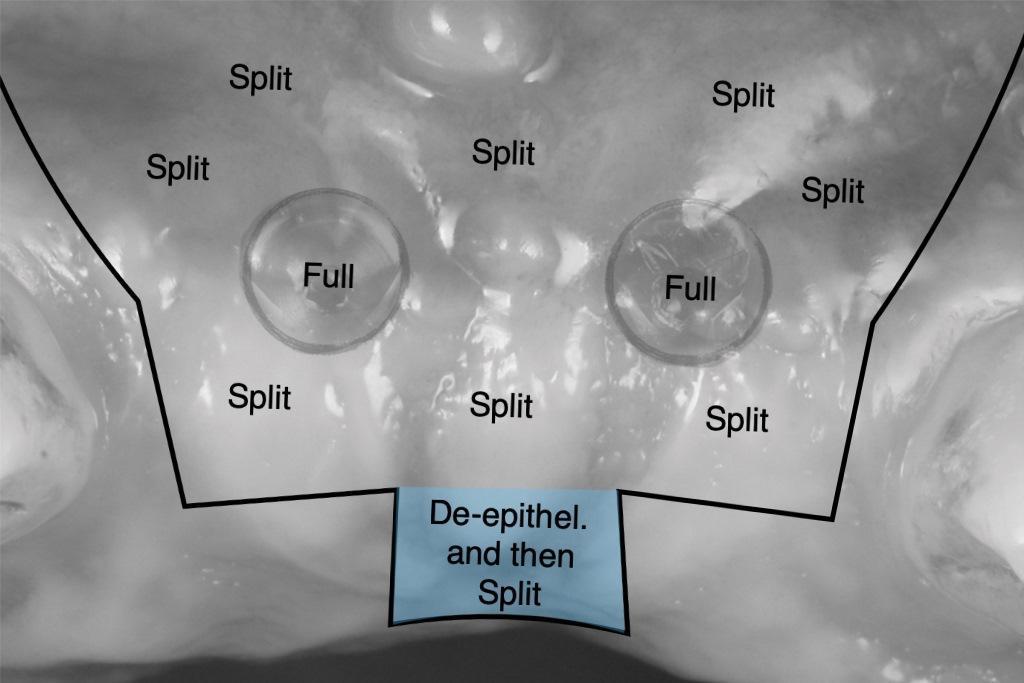
Фото 10: Поднятие лоскута. Обратите внимание, что средняя часть лоскута была деэпителизирована, чтобы его можно было поместить между двумя имплантатами.

Фото 11: Поднятие расщепленного лоскута. Обратите внимание на увеличение толщины мягких тканей со щечных сторон имплантатов.

Лоскут закрывался простыми прерывистыми швами (7-0 ПГК, "бабочка"), при этом средняя часть лоскута складывалась и сворачивалась, чтобы увеличить толщину и высоту межпроксимальных мягких тканей между двумя имплантатами (фото 12). Временные коронки, отпечатанные на 3D-принтере, были адаптированы к лоскуту и установлены (фото 13). Дальнейшая модификация временных коронок проводилась в период от 1 месяца до 3 месяцев, когда были установлены окончательные керамические реставрации.
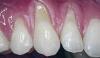
На фото 14 показан конечный результат через 1 год (который можно сравнить с фотографией до лечения на фото 1). На фото с 15 по 18 показаны клинические сравнения результатов на исходном уровне и через 1 год, а на фото 19 и 20 представлена ультрасонографическая характеристика мягких тканей на начальном этапе и через 1 год. Глубина зондирования с вестибулярной стороны через 1 год составила 3-3-3 мм для имплантата 1.1 и 3-2-3 мм для имплантата 2.1. Пациентка осталась очень довольна эстетическими результатами и общим ходом лечения.
Фото 12: Соединение абатментов и ушивание лоскутов.
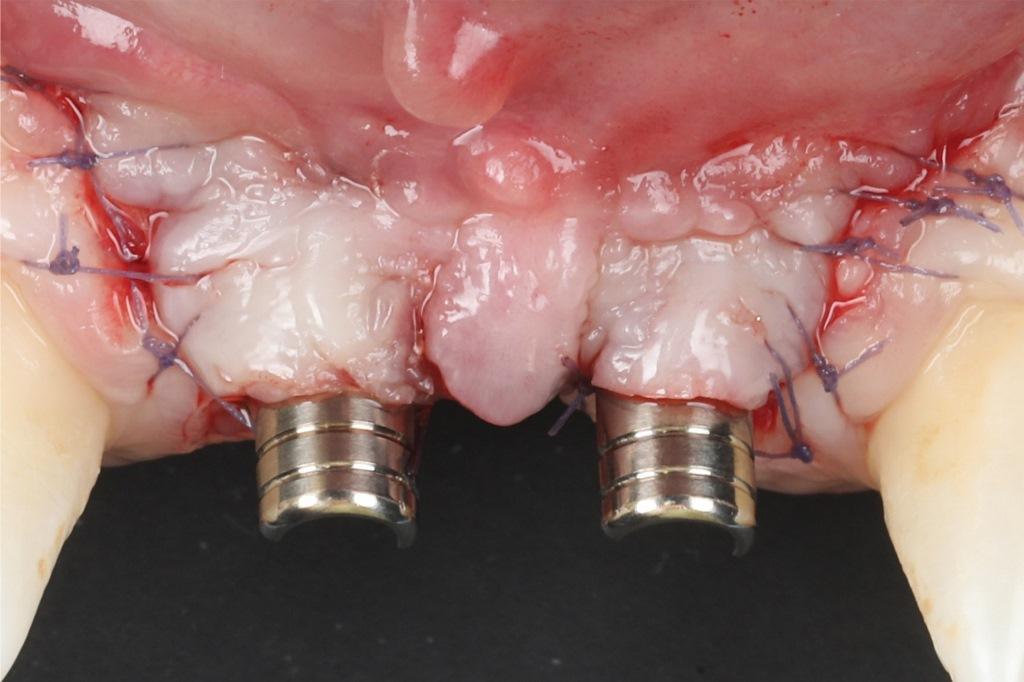
Фото 13: Временные коронки.
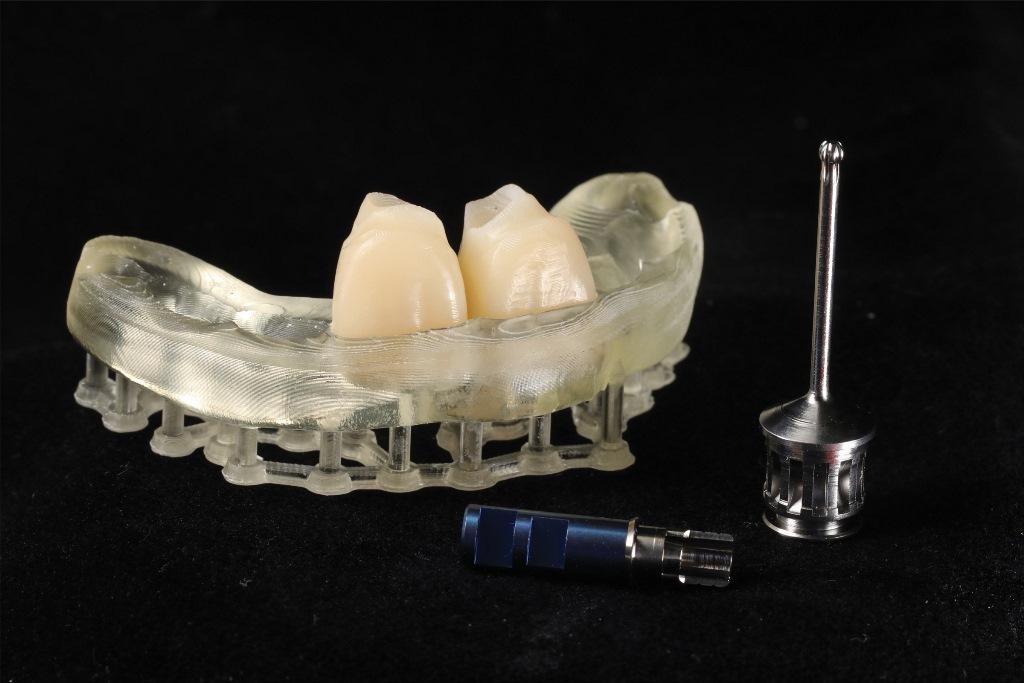
Фото 14: Итоговый результат через 1 год.
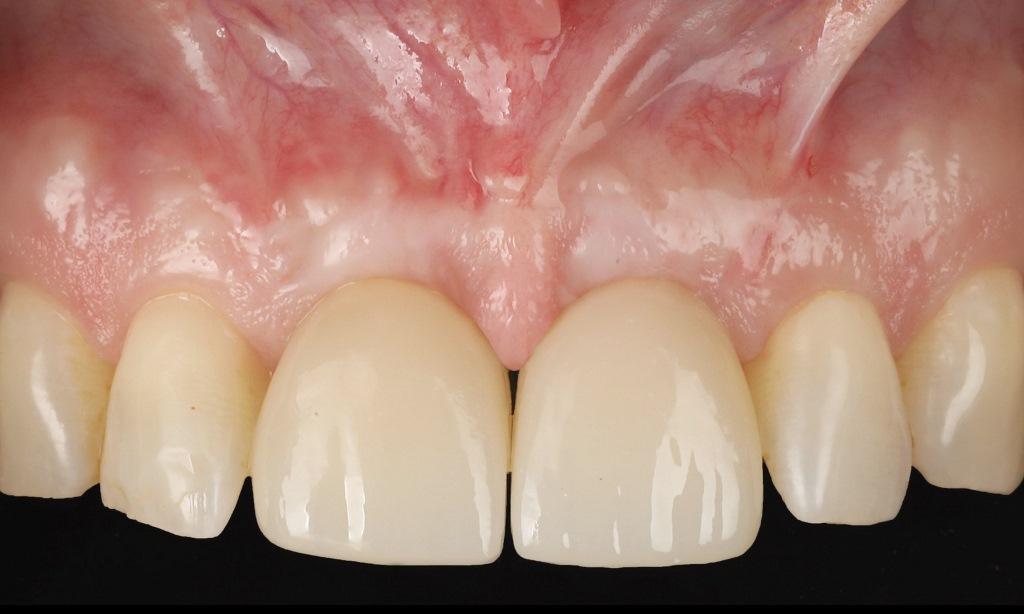
Фото 15: Клиническое сравнение увеличения объема, достигнутого в результате вмешательства: вид с фронтальной стороны.
Фото 15: Исходный этап: фронтальный вид.
Фото 16: Фронтальный вид через 1 год после лечения.
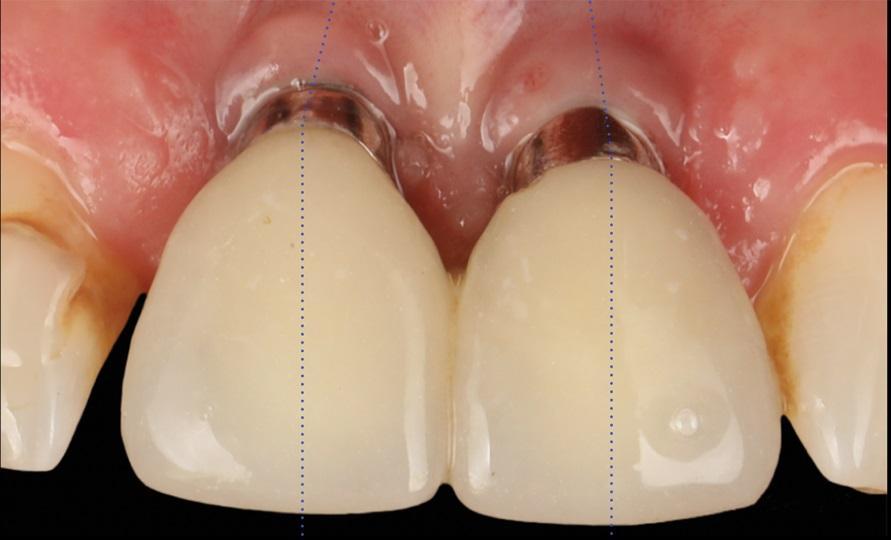
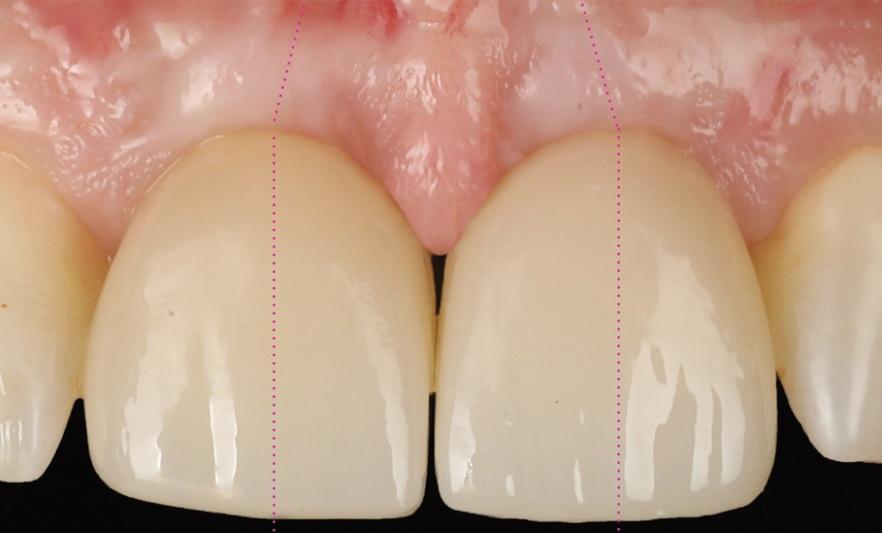
Фото 17: Клиническое сравнение увеличения объема, достигнутого в результате вмешательства: вид с окклюзионной стороны.
Фото 17: Исходный этап: вид с окклюзионной стороны.
Фото 18: Вид с окклюзионной стороны через 1 год после лечения.
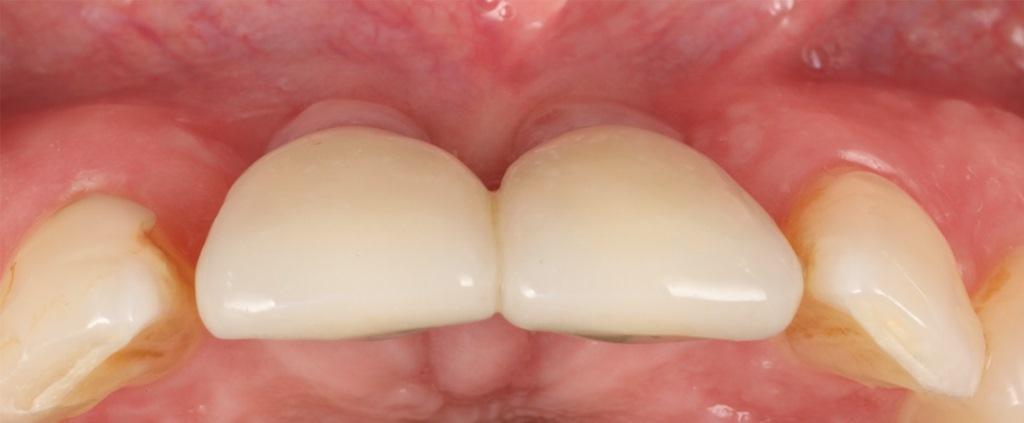
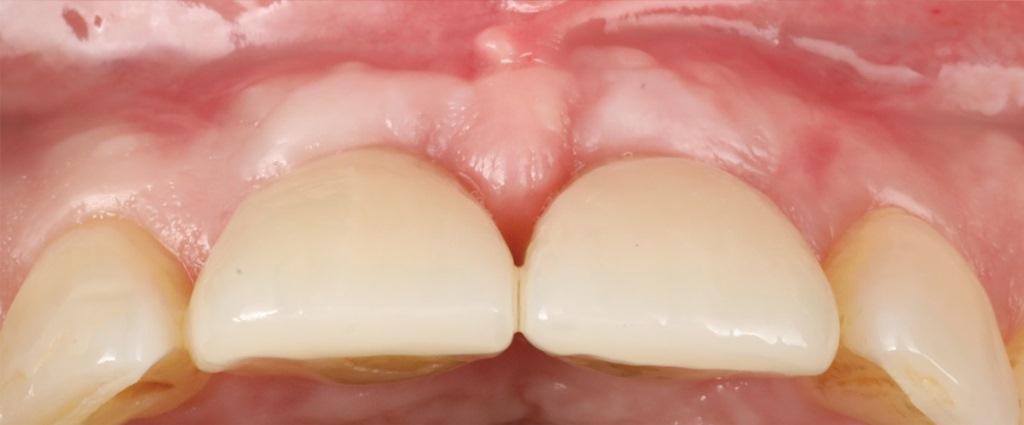
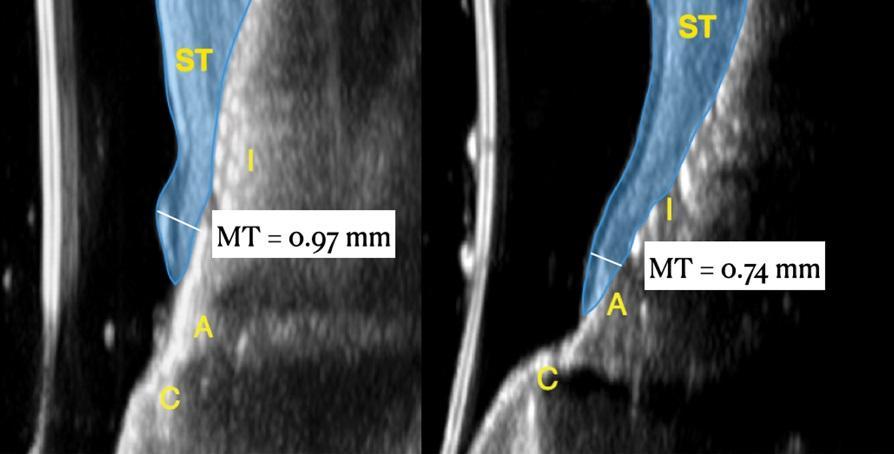
Фото 19: Ультрасонографическое сравнение увеличения объема, достигнутого в результате вмешательства.
Фото 19: Исходный этап.
Фото 20: Через 1 год после лечения. "C" обозначает коронку, "A" - абатмент, "I" - имплантат, а "ST" - мягкие ткани. Мягкие ткани на исходном этапе (фото 19) выделены синим цветом, а мягкие ткани через 1 год наблюдения (фото 20) - фиолетовым. Также показана толщина слизистой оболочки ("МТ") на исходном этапе (фото 19) и через 1 год (фото 20). (На обоих рисунках левая секция - имплантат 1.1 в средней части лица, а правая - имплантат 2.1 в средней части лица).
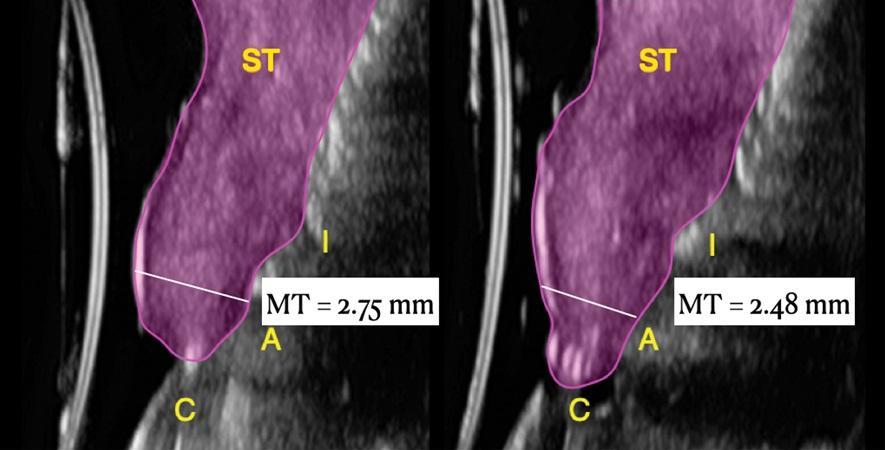
Ультрасонографическая оценка увеличения толщины слизистой оболочки
В предыдущих исследованиях подробно описаны настройки ультразвукового оборудования и процедуры сканирования. Для получения снимков средней зоны лица и межпроксимального пространства на исходном уровне и при наблюдении в течение 1 года использовался имеющийся в продаже ультразвуковой аппарат с миниатюрным датчиком 24 МГц. Датчик был ориентирован перпендикулярно окклюзионной плоскости и параллельно длинной оси имплантата для получения полутоновых изображений в "режиме В". Режим В формирует двумерные полутоновые изображения, яркость которых является результатом возвращенного эхо-сигнала и его силы, которая зависит от акустических свойств твердо- и мягкотканных структур пародонта. Сканы были сохранены в файлах формата DICOM (Digital Imaging and Communications in Medicine) и затем экспортированы в пакет программного обеспечения, где толщина слизистой была измерена на 1,5 мм апикальнее края мягких тканей и составила 0,97 мм и 0,74 мм на правом и левом имплантатах, соответственно. Через 12 месяцев толщина слизистой оболочки составила 2,75 мм и 2,48 мм. Прирост толщины мягких тканей на уровне правого имплантата составил 1,78 мм для правого имплантата и 1,74 мм для левого имплантата.
Обсуждение
Эффективность ОКНЛ + СТТ для закрытия корней в естественных зубах хорошо известна. Тем не менее, когда та же "традиционная" методика была применена к РМТВИ, первые исследования не подтвердили предсказуемость результатов, наблюдаемых на естественных зубах. В пилотной серии случаев Burkhardt et al. получили трапециевидный ОКНЛ + субэпителиальный СТТ (полученный из самых глубоких слоев задней части нёба с помощью одноразовой техники) для лечения РМТВИ. С течением времени наблюдался прогрессирующий рецидив/уменьшение мягких тканей со средним покрытием РМТВИ 75% через 1 месяц и 70% через 3 месяца. По итогам 6-месячного наблюдения средний показатель РМТВИ составил 66%, при этом ни в одном из участков не было отмечено полного закрытия РМТВИ во время последнего посещения. Авторы предположили, что отсутствие периодонтальной связки и общее пониженное кровоснабжение, характерное для тканей вокруг имплантата по сравнению с естественными зубами, могли негативно повлиять на результаты лечения. Anderson и соавт. рандомизировали 13 пациентов: ОКНЛ + субэпителиальный СТТ (взятый из глубоких слоев неба) или ОКНЛ + ацеллюлярный дермальный матрикс (АДМ). Через 6 месяцев авторы сообщили, что среднее закрытие РМТВИ составило 40% для ОКНЛ + субэпителиального СТТ и 28% для ОКНЛ + АДМ. Об ограниченном закрытии рецессии также свидетельствовали эстетические показатели пациентов, которые не показали значительного улучшения через 6 месяцев после лечения.
Другие авторы предлагают для лечения РМТВИ использовать СТТ, взятые либо из самых поверхностных слоев неба, используя технику забора свободного десневого трансплантата с последующим удалением эпителия вне полости рта, либо из верхнечелюстного бугорка. Используемая техника забора мягких тканей неба может повлиять на качество трансплантата: СТТ, полученные в результате деэпителизации эпителизированного небного трансплантата, состоят в основном из собственной пластинки, в то время как СТТ из глубоких слоев неба, полученные с помощью обычных методов забора (например, глубокие ткани неба), содержат большее количество железистой и жировой ткани. Из-за этой несхожести трансплантата СТТ из поверхностных тканей неба существенно отличается от СТТ из глубоких тканей неба, при этом поверхностные СТТ более твердые, стабильные и ими легче управлять. Эти свойства СТТ могут также положительно влиять на кератинизацию вышележащего эпителия. С другой стороны, СТТ, богатый жировой и железистой тканью, как, например, СТТ из глубоких тканей неба, может выступать в качестве барьера и ограничивать диффузию плазмы и васкуляризацию на первом этапе заживления, а также может ухудшать способность трансплантата вызывать кератинизацию вышележащего эпителия. Недавнее рандомизированное контролируемое клиническое исследование, проведенное группой авторов, показало, что при лечении РМТВИ с помощью ОКНЛ + СТТ (полученного из поверхностных тканей неба) средний прирост кератинизированной слизистой оболочки составил 2,57 мм через 1 год. Кроме того, было обнаружено, что ОКНЛ + СТТ дают лучшие клинические результаты, результаты достижения объема и результаты по отзывам пациентов по сравнению с ТУН + СТТ. Через 12 месяцев среднее закрытие РМТВИ с помощью ОКНЛ + СТТ и ТУН + СТТ составило 90,23% и 59,76%, соответственно.
Еще одним важным аспектом является то, что существенная разница между лечением рецессий десны и РМТВИ связана с возможностью удаления супраструктуры в местах установки имплантатов, когда это необходимо. В описанном случае коронки с опорой на имплантаты и абатменты были сняты в день хирургического вмешательства. Основные преимущества удаления супраструктуры имплантата заключаются в улучшении доступа для создания, поднятия и ушивания лоскута, а также в увеличении площади, которая может быть деэпителизирована и обеспечить достаточное питание и кровоснабжение откинутого в корональном направлении лоскута. Авторы считают, что это ключевой аспект лечения РМТВИ.
В описанном клиническом случае имплантаты были расположены немного буккально, а буккальная кость в средней части лица отсутствовала. Несмотря на то, что уровень буккальной кости (расхождение буккальной кости) является показателем риска РМТВИ, лечение имплантатов с РМТВИ, не имеющих буккальной кости, должно проводиться только с помощью пересадки мягких тканей, а не с помощью наращивания кости.Недавнее исследование Quirynen et al. показало, что ограничения латеральной костной аугментации диктуются размерами костной пластинки пациента. Другими словами, при лечении имплантатов с РМТВИ с буккальным смещением вероятность успешной костной аугментации костной ткани ограничена. Аугментация мягких тканей для лечения РМТВИ зарекомендовала себя как эффективный подход со стабильными результатами с течением времени, как описано в двух 5-летних сериях клинических случаев. Действительно, увеличение толщины мягких тканей — еще один важный результат лечения РМТВИ, который способствует стабильности края мягких тканей с течением времени.
В данной статье описано использование неионизирующей высокочастотной ультрасонографии в режиме реального времени для оценки увеличения толщины мягких тканей и анатомии структур вокруг имплантата до лечения и в течение 1 года наблюдения. Надежность и воспроизводимость этой технологии была продемонстрирована в нескольких клинических исследованиях, в которых ультразвук также использовался для оценки перфузии тканей после процедуры трансплантации и уровня кровотока в здоровых и больных местах имплантации. Ультрасонография позволила наблюдать значительное увеличение толщины слизистой оболочки через 1 год: исходная толщина мягких тканей (измеренная на 1,5 мм апикальнее края мягких тканей) составила 0,97 мм и 0,74 мм на правом и левом дентальных имплантатах соответственно, а конечная толщина слизистой оболочки составила 2,75 мм и 2,48 мм на правом и левом дентальных имплантатах соответственно. Многочисленные данные подтверждают ключевую роль увеличенной толщины десны в стабильности края мягких тканей в естественном зубном ряду, и разумно предположить, что эта концепция также может быть применима в местах установки имплантатов. Преимущества изменения фенотипа мягких тканей в виде увеличения толщины кератинизированной слизистой оболочки и слизистой оболочки также включают в себя результаты по отзывам пациентов и параметры, связанные со здоровьем имплантатов.
Наконец, лечение РМТВИ в значительной степени зависит от желаний, ожиданий и финансовых возможностей пациента. Поэтому решение о снятии коронки должно обсуждаться с пациентом до хирургического вмешательства. Тем не менее, лечащим врачам следует помнить, что некоторые виды РМТВИ, например, случаи, характеризующиеся более длинной коронкой с розовой керамикой или без нее в самой апикальной области, или случаи с плоской или отрицательной архитектурой сосочков, могут быть устранены только в том случае, если пациент готов заменить коронку.
Заключение
Расхождение мягких тканей вокруг имплантата в эстетической зоне — довольно распространенное явление. Правильная диагностика и грамотное планирование лечения имеют решающее значение для лечения эстетических осложнений имплантатов. В данной статье представлен случай расхождения мягких тканей вокруг имплантата при использовании откинутого в корональном направлении лоскута и соединительнотканного трансплантата с погружным заживлением. Через год после лечения было отмечено полное устранение дефекта, изменение фенотипа мягких тканей вокруг имплантата и удовлетворительные эстетические результаты и результаты по отзывам пациентов.
Авторы:
Lorenzo Tavelli, DDS, MS, PhD
Giovanni Zucchelli, DDS, PhD
Hom-Lay Wang, DDS, MSD, PhD
Shayan Barootchi, DMD, MS
Лечение расхождения мягких тканей вокруг имплантата (РМТВИ) может быть довольно сложным для многих лечащих врачей и оставлять серьезные эстетические проблемы для пациентов. В данной статье описывается лечение двух соседних РМТВИ в переднем отделе, где также наблюдался дефект сосочков. В данном случае был использован откинутый в корональном направлении лоскут и соединительнотканный трансплантат (СТТ) с погружным заживлением. Коронки и абатменты с опорой на имплантаты были удалены, и было проведено наращивание мягких тканей с помощью СТТ, который был подшит к щечной стороне места установки имплантатов. Лоскут был выкроен и подшит над имплантатами, которые были погружены с целью закрытия первичным натяжением. Через 3 месяца для увеличения ширины кератинизированной слизистой вокруг имплантатов и наращивания периимплантатного сосочка была проведена комбинированная операция с использованием апикально расположенного лоскута и ротированного лоскута. Через 1 год были получены удовлетворительные клинические и эстетические результаты.

РМТВИ может ухудшить восприятие пациентами имплантологического лечения и, возможно, оказать негативное влияние на качество их жизни. Было выявлено несколько факторов риска возникновения РМТВИ, к которым относятся недостаточное количество кератинизированной слизистой и толщина мягких тканей, буккально расположенные имплантаты, тонкая буккальная кость, расхождения краев или фенестрации костной ткани, а также несколько соседних дентальных имплантатов. В частности, недавнее исследование, проведенное нашими авторами, показало, что каждый миллиметр увеличения расхождения буккальной костной ткани повышает вероятность возникновения РМТВИ примерно на 41%.
Для лечения ПСТД описано несколько подходов, включая использование откинутого в корональном направлении лоскута (ОКНЛ) в сочетании с соединительнотканным трансплантатом (СТТ), туннельные методы (ТУН), свободные десневые трансплантаты, процедуры направленной костной регенерации, хирургический ортопедический подход и вертикальное наращивание мягких тканей с использованием СТТ-платформенного подхода. Целесообразность применения этих подходов во многом зависит от ожиданий и финансовых возможностей пациента, а также от характеристик эстетического осложнения со стороны имплантата, включая высоту коронки с опорой на имплантат, букколингвальное положение имплантата и размер сосочков, но не ограничиваясь ими. Недавно группа авторов представила классификацию РМТВИ, а также рекомендации по их лечению.Четыре основных класса (I, II, III и IV) были определены на основе букколингвального положения коронки/платформы имплантата, с тремя подклассами (a, b и c), которые относятся к высоте сосочков вокруг имплантата. Более сложные случаи включают в себя несколько соседних имплантатов с РМТВИ.
В данной статье описан случай установки двух дентальных имплантатов в передней верхней челюсти с дегисценцией мягких тканей, которые были пролечены с помощью ОКНЛ + СТТ с использованием погружного подхода.
Описание клинического случая и план лечения
Пациентка, 46 лет, соматически и пародонтологически здоровая, обратилась в клинику пародонтологии Мичиганского университета с жалобами на плохую эстетику улыбки из-за двух дентальных имплантатов (1.1 и 2.1), на которых видны металлические компоненты (фото 1). Пациентка сообщила, что имплантаты были установлены 15-20 лет назад после несчастного случая. Клинический осмотр показал, что глубина зондирования имплантатов не превышает 3 мм (глубина зондирования с вестибулярной стороны 3-2-3 мм для имплантата 1.1 и 2-2-2 мм для имплантата 2.1), кровотечение при зондировании и нагноение отсутствуют, поэтому имплантаты были признаны состоятельными (фото 1 и фото 2). Сосочек между двумя имплантатами был неполноценным с щечной стороны. Имплантаты были установлены буккально, и отмечался значительный недостаток объема мягких тканей.
Фото 1: Вид в момент приема.

Фото 2: Изначальная периапикальная рентгенограмма.

План лечения был составлен и обсужден с пациентом и включал удаление коронок и абатментов с опорой на имплантаты и хирургическое вмешательство с применением ОКНЛ + СТТ с погружным заживлением.
Откинутый в корональном направлении лоскут и соединительнотканный трансплантат с погружным заживлением
Инструкции по гигиене полости рта были рассмотрены с пациентом и закреплены за 6 недель до посещения с целью хирургического вмешательства. На приеме у хирурга коронки и абатменты с опорой на имплантаты были удалены, и были установлены два покрывных винта. Был выкроен расщепленный ОКНЛ трапециевидной формы (фото 3). Два слегка расходящихся косых разреза были расположены между имплантатами и боковыми резцами. Расщепленный лоскут был поднят, при этом соблюдалась осторожность, чтобы сохранить слой соединительной ткани, прилегающей к поверхности имплантата. Сохранение этого слоя соединительной ткани на корпусе имплантата, лишенного костной ткани с щечной стороны, является важным этапом, который отличает поднятие лоскута на состоятельных имплантатах с РМТВИ от имплантатов с периимплантитом (фото 4).
Фото 3: Откинутый в корональном направлении лоскут после удаления коронок для аугментации мягких тканей.

Фото 4: Поднятие расщепленного лоскута.

После этого лоскут высвобождался глубоким разрезом параллельно кости, а затем поверхностным разрезом лезвием параллельно наружной поверхности слизистой оболочки, пока он не мог пассивно достичь положения, примерно на 2 мм корональнее идеального конечного уровня края мягких тканей. С помощью микроножа были деэпителизированы анатомические сосочки между имплантатами и боковыми резцами, а также межрезцовый сосочек, причем не только c щечной, но и c окклюзионной стороны, чтобы улучшить сосудистое ложе для лоскута.
Свободный десневой трансплантат был взят с неба и затем деэпителизирован вне полости рта для получения плотного и волокнистого СТТ (фото 5). На небный донорский участок накладывалась коллагеновая губка и стабилизировалась швом из политетрафторэтилена (ПТФЭ) 5-0. Поверх коллагеновой губки наносился тонкий слой цианоакрилатного тканевого клея, как описано в работе Tavelli et al. в 2019 году. На поверхность имплантата не наносились химические или механические средства для кондиционирования корня. СТТ стабилизировали простыми прерывистыми швами (7-0 полигликолевая кислота [ПГК], "бабочка") к деэпителизированным анатомическим сосочкам с корональной стороны и надкостнице в апикальной части (фото 6). Затем лоскут был откинут в корональном направлении и ушит простыми прерывистыми швами (6-0 и 7-0 полипропилен) на уровне вертикальных разрезов и на уровне небного края, чтобы полностью закрыть трансплантат и покрывные винты (фото 7).
Фото 5: Соединительнотканный трансплантат, полученный в результате деэпителизации эпителизированного десневого трансплантата.

Фото 6: Стабилизация соединительнотканного трансплантата.

Фото 7: Погружное заживление с закрытием лоскута.

Швы были сняты через 2 недели, и пациентка сообщила об ограниченной степени осложнений в послеоперационном периоде.
Повторное открытие участка и восстановительный этап
Через 3 месяца после погружного заживления на оперированном участке появилась ограниченная кератинизированная слизистая оболочка с щечной стороны (фото 8). Поэтому был выкроен лоскут двумя вертикальными разрезами, начиная с небной стороны двух погруженных имплантатов. Кроме того, часть лоскута в средней части неба была вытянута к небной стороне для получения ротированного лоскута, который был деэпителизирован бором и в итоге свернут для увеличения объема межпроксимальной мягкой ткани между двумя имплантатами (фото 9). Расщепленный лоскут был поднят, при этом мягкие ткани над имплантатами были удалены, чтобы выявить покрывные винты (фото 10). По сравнению с первым хирургическим вмешательством наблюдалось значительное увеличение толщины мягких тканей с щечной стороны имплантатов (фото 11), когда имплантаты были видны через тонкий слой соединительнотканных волокон, прилегающих к поверхностям имплантатов. Покрывные винты были удалены, и были установлены временные титановые абатменты.
Фото 8: Место операции через 3 месяца.

Фото 9: Планирование формы лоскута.

Фото 10: Поднятие лоскута. Обратите внимание, что средняя часть лоскута была деэпителизирована, чтобы его можно было поместить между двумя имплантатами.

Фото 11: Поднятие расщепленного лоскута. Обратите внимание на увеличение толщины мягких тканей со щечных сторон имплантатов.

Лоскут закрывался простыми прерывистыми швами (7-0 ПГК, "бабочка"), при этом средняя часть лоскута складывалась и сворачивалась, чтобы увеличить толщину и высоту межпроксимальных мягких тканей между двумя имплантатами (фото 12). Временные коронки, отпечатанные на 3D-принтере, были адаптированы к лоскуту и установлены (фото 13). Дальнейшая модификация временных коронок проводилась в период от 1 месяца до 3 месяцев, когда были установлены окончательные керамические реставрации.
На фото 14 показан конечный результат через 1 год (который можно сравнить с фотографией до лечения на фото 1). На фото с 15 по 18 показаны клинические сравнения результатов на исходном уровне и через 1 год, а на фото 19 и 20 представлена ультрасонографическая характеристика мягких тканей на начальном этапе и через 1 год. Глубина зондирования с вестибулярной стороны через 1 год составила 3-3-3 мм для имплантата 1.1 и 3-2-3 мм для имплантата 2.1. Пациентка осталась очень довольна эстетическими результатами и общим ходом лечения.
Фото 12: Соединение абатментов и ушивание лоскутов.

Фото 13: Временные коронки.

Фото 14: Итоговый результат через 1 год.

Фото 15: Клиническое сравнение увеличения объема, достигнутого в результате вмешательства: вид с фронтальной стороны.
Фото 15: Исходный этап: фронтальный вид.
Фото 16: Фронтальный вид через 1 год после лечения.


Фото 17: Клиническое сравнение увеличения объема, достигнутого в результате вмешательства: вид с окклюзионной стороны.
Фото 17: Исходный этап: вид с окклюзионной стороны.
Фото 18: Вид с окклюзионной стороны через 1 год после лечения.


Фото 19: Ультрасонографическое сравнение увеличения объема, достигнутого в результате вмешательства.
Фото 19: Исходный этап.
Фото 20: Через 1 год после лечения. "C" обозначает коронку, "A" - абатмент, "I" - имплантат, а "ST" - мягкие ткани. Мягкие ткани на исходном этапе (фото 19) выделены синим цветом, а мягкие ткани через 1 год наблюдения (фото 20) - фиолетовым. Также показана толщина слизистой оболочки ("МТ") на исходном этапе (фото 19) и через 1 год (фото 20). (На обоих рисунках левая секция - имплантат 1.1 в средней части лица, а правая - имплантат 2.1 в средней части лица).


Ультрасонографическая оценка увеличения толщины слизистой оболочки
В предыдущих исследованиях подробно описаны настройки ультразвукового оборудования и процедуры сканирования. Для получения снимков средней зоны лица и межпроксимального пространства на исходном уровне и при наблюдении в течение 1 года использовался имеющийся в продаже ультразвуковой аппарат с миниатюрным датчиком 24 МГц. Датчик был ориентирован перпендикулярно окклюзионной плоскости и параллельно длинной оси имплантата для получения полутоновых изображений в "режиме В". Режим В формирует двумерные полутоновые изображения, яркость которых является результатом возвращенного эхо-сигнала и его силы, которая зависит от акустических свойств твердо- и мягкотканных структур пародонта. Сканы были сохранены в файлах формата DICOM (Digital Imaging and Communications in Medicine) и затем экспортированы в пакет программного обеспечения, где толщина слизистой была измерена на 1,5 мм апикальнее края мягких тканей и составила 0,97 мм и 0,74 мм на правом и левом имплантатах, соответственно. Через 12 месяцев толщина слизистой оболочки составила 2,75 мм и 2,48 мм. Прирост толщины мягких тканей на уровне правого имплантата составил 1,78 мм для правого имплантата и 1,74 мм для левого имплантата.
Обсуждение
Эффективность ОКНЛ + СТТ для закрытия корней в естественных зубах хорошо известна. Тем не менее, когда та же "традиционная" методика была применена к РМТВИ, первые исследования не подтвердили предсказуемость результатов, наблюдаемых на естественных зубах. В пилотной серии случаев Burkhardt et al. получили трапециевидный ОКНЛ + субэпителиальный СТТ (полученный из самых глубоких слоев задней части нёба с помощью одноразовой техники) для лечения РМТВИ. С течением времени наблюдался прогрессирующий рецидив/уменьшение мягких тканей со средним покрытием РМТВИ 75% через 1 месяц и 70% через 3 месяца. По итогам 6-месячного наблюдения средний показатель РМТВИ составил 66%, при этом ни в одном из участков не было отмечено полного закрытия РМТВИ во время последнего посещения. Авторы предположили, что отсутствие периодонтальной связки и общее пониженное кровоснабжение, характерное для тканей вокруг имплантата по сравнению с естественными зубами, могли негативно повлиять на результаты лечения. Anderson и соавт. рандомизировали 13 пациентов: ОКНЛ + субэпителиальный СТТ (взятый из глубоких слоев неба) или ОКНЛ + ацеллюлярный дермальный матрикс (АДМ). Через 6 месяцев авторы сообщили, что среднее закрытие РМТВИ составило 40% для ОКНЛ + субэпителиального СТТ и 28% для ОКНЛ + АДМ. Об ограниченном закрытии рецессии также свидетельствовали эстетические показатели пациентов, которые не показали значительного улучшения через 6 месяцев после лечения.
Другие авторы предлагают для лечения РМТВИ использовать СТТ, взятые либо из самых поверхностных слоев неба, используя технику забора свободного десневого трансплантата с последующим удалением эпителия вне полости рта, либо из верхнечелюстного бугорка. Используемая техника забора мягких тканей неба может повлиять на качество трансплантата: СТТ, полученные в результате деэпителизации эпителизированного небного трансплантата, состоят в основном из собственной пластинки, в то время как СТТ из глубоких слоев неба, полученные с помощью обычных методов забора (например, глубокие ткани неба), содержат большее количество железистой и жировой ткани. Из-за этой несхожести трансплантата СТТ из поверхностных тканей неба существенно отличается от СТТ из глубоких тканей неба, при этом поверхностные СТТ более твердые, стабильные и ими легче управлять. Эти свойства СТТ могут также положительно влиять на кератинизацию вышележащего эпителия. С другой стороны, СТТ, богатый жировой и железистой тканью, как, например, СТТ из глубоких тканей неба, может выступать в качестве барьера и ограничивать диффузию плазмы и васкуляризацию на первом этапе заживления, а также может ухудшать способность трансплантата вызывать кератинизацию вышележащего эпителия. Недавнее рандомизированное контролируемое клиническое исследование, проведенное группой авторов, показало, что при лечении РМТВИ с помощью ОКНЛ + СТТ (полученного из поверхностных тканей неба) средний прирост кератинизированной слизистой оболочки составил 2,57 мм через 1 год. Кроме того, было обнаружено, что ОКНЛ + СТТ дают лучшие клинические результаты, результаты достижения объема и результаты по отзывам пациентов по сравнению с ТУН + СТТ. Через 12 месяцев среднее закрытие РМТВИ с помощью ОКНЛ + СТТ и ТУН + СТТ составило 90,23% и 59,76%, соответственно.
Еще одним важным аспектом является то, что существенная разница между лечением рецессий десны и РМТВИ связана с возможностью удаления супраструктуры в местах установки имплантатов, когда это необходимо. В описанном случае коронки с опорой на имплантаты и абатменты были сняты в день хирургического вмешательства. Основные преимущества удаления супраструктуры имплантата заключаются в улучшении доступа для создания, поднятия и ушивания лоскута, а также в увеличении площади, которая может быть деэпителизирована и обеспечить достаточное питание и кровоснабжение откинутого в корональном направлении лоскута. Авторы считают, что это ключевой аспект лечения РМТВИ.
В описанном клиническом случае имплантаты были расположены немного буккально, а буккальная кость в средней части лица отсутствовала. Несмотря на то, что уровень буккальной кости (расхождение буккальной кости) является показателем риска РМТВИ, лечение имплантатов с РМТВИ, не имеющих буккальной кости, должно проводиться только с помощью пересадки мягких тканей, а не с помощью наращивания кости.Недавнее исследование Quirynen et al. показало, что ограничения латеральной костной аугментации диктуются размерами костной пластинки пациента. Другими словами, при лечении имплантатов с РМТВИ с буккальным смещением вероятность успешной костной аугментации костной ткани ограничена. Аугментация мягких тканей для лечения РМТВИ зарекомендовала себя как эффективный подход со стабильными результатами с течением времени, как описано в двух 5-летних сериях клинических случаев. Действительно, увеличение толщины мягких тканей — еще один важный результат лечения РМТВИ, который способствует стабильности края мягких тканей с течением времени.
В данной статье описано использование неионизирующей высокочастотной ультрасонографии в режиме реального времени для оценки увеличения толщины мягких тканей и анатомии структур вокруг имплантата до лечения и в течение 1 года наблюдения. Надежность и воспроизводимость этой технологии была продемонстрирована в нескольких клинических исследованиях, в которых ультразвук также использовался для оценки перфузии тканей после процедуры трансплантации и уровня кровотока в здоровых и больных местах имплантации. Ультрасонография позволила наблюдать значительное увеличение толщины слизистой оболочки через 1 год: исходная толщина мягких тканей (измеренная на 1,5 мм апикальнее края мягких тканей) составила 0,97 мм и 0,74 мм на правом и левом дентальных имплантатах соответственно, а конечная толщина слизистой оболочки составила 2,75 мм и 2,48 мм на правом и левом дентальных имплантатах соответственно. Многочисленные данные подтверждают ключевую роль увеличенной толщины десны в стабильности края мягких тканей в естественном зубном ряду, и разумно предположить, что эта концепция также может быть применима в местах установки имплантатов. Преимущества изменения фенотипа мягких тканей в виде увеличения толщины кератинизированной слизистой оболочки и слизистой оболочки также включают в себя результаты по отзывам пациентов и параметры, связанные со здоровьем имплантатов.
Наконец, лечение РМТВИ в значительной степени зависит от желаний, ожиданий и финансовых возможностей пациента. Поэтому решение о снятии коронки должно обсуждаться с пациентом до хирургического вмешательства. Тем не менее, лечащим врачам следует помнить, что некоторые виды РМТВИ, например, случаи, характеризующиеся более длинной коронкой с розовой керамикой или без нее в самой апикальной области, или случаи с плоской или отрицательной архитектурой сосочков, могут быть устранены только в том случае, если пациент готов заменить коронку.
Заключение
Расхождение мягких тканей вокруг имплантата в эстетической зоне — довольно распространенное явление. Правильная диагностика и грамотное планирование лечения имеют решающее значение для лечения эстетических осложнений имплантатов. В данной статье представлен случай расхождения мягких тканей вокруг имплантата при использовании откинутого в корональном направлении лоскута и соединительнотканного трансплантата с погружным заживлением. Через год после лечения было отмечено полное устранение дефекта, изменение фенотипа мягких тканей вокруг имплантата и удовлетворительные эстетические результаты и результаты по отзывам пациентов.
Авторы:
Lorenzo Tavelli, DDS, MS, PhD
Giovanni Zucchelli, DDS, PhD
Hom-Lay Wang, DDS, MSD, PhD
Shayan Barootchi, DMD, MS





























































































































































0 комментариев