За последние годы проблема контрафакта лекарственных препаратов в России достигла такого уровня, что вынудила правительство к принятию кардинальных мер. С 1-го января 2020 года все организации, имеющие лицензии на фармацевтическую и медицинскую деятельность, будут обязаны передавать данные в Федеральную государственную информационную систему «Мониторинг движения лекарственных препаратов» (ФГИС МДЛП или ИС «Честный знак»). Для этого всем пользователям необходимо будет внедрить специальный электронный документооборот. Что ждать от данного нововведения клиникам, производителям и компаниям-дистрибьюторам? Очередных проблем и поборов или, все-таки на этот раз, есть шанс не только упорядочить свою работу с ЛП, но и даже получить прибыль. Попробуем разобраться.

Мониторинг движения лекарственных препаратов (далее ФГИС МДЛП или ИС МДЛП) – является частью общенациональной системы маркировки и отслеживания продукции под названием «Честный знак» по направлению «Лекарственные препараты». Специальный цифровой код (Data Matrix, штрих-код) гарантирует подлинность и качество товара. Основная задача данной системы – повышение уровня безопасности потребителей, борьба с контрафактом и некачественными аналогами.
Причины внедрения ИС МДЛП
По данным Минпромторга, только за 2018 год в обороте было выявлено свыше 6 миллионов единиц контрафактной продукции. Эта проблема наиболее серьезно отражается на конечных потребителях, которые за свои же собственные деньги рискуют здоровьем, и, зачастую, жизнью. Что касается производителей лекарственных препаратов и клиник, то здесь контрафакт грозит не только серьезными репутационными и финансовыми убытками, но и возможной уголовной ответственностью для должностных лиц.

Наличие цифровой маркировки позволяет получить полную информацию о товаре: название предприятия-изготовителя, место, дату и время производства и продажи, срок годности, артикул и номер стандарта. Данные хранятся в государственной информационной системе. Маркировка направлена на снижение распространения всех видов нелегальной продукции: контрафакта, фальсификата, контрабанды и т.д.
История принятия закона
Решение о создании федеральной государственной информационной системы мониторинга движения лекарственных препаратов от производителя до конечного потребителя с использованием маркировки принято 4 февраля 2015 г. на совещании Президента РФ с членами правительства. 20 февраля 2015 г. было подписано поручение, на основании которого Министерству Здравоохранения РФ поручалось обеспечить разработку и поэтапное внедрение системы. 30.11.2015 г. издан приказ №866 «Об утверждении концепции создания федеральной государственной информационной системы мониторинга движения лекарственных препаратов от производителя до конечного потребителя с использованием маркировки», утвердивший общую концепцию создания системы, ее цели и задачи, основные требования, а также перечень функциональных возможностей и сервисов.
Сроки внедрения и ответственный оператор
Внедрение информационной системы «Честный знак» (далее – ИС «Честный знак») планируется проводить поэтапно до 2024 года. Предполагается, что, начиная с этой даты, все виды товаров, производимых и/или реализуемых на территории РФ, должны иметь индивидуальную цифровую маркировку (штрих-код), позволяющий отследить их происхождение, логистику и использование в России.
1 января 2020 года стартует запуск информационной системы мониторинга движения лекарственных препаратов. Система МДЛП создана для защиты потребителей всех уровней от нелегальных лекарственных средств и призвана предоставить гражданам и организациям возможность оперативной проверки их легальности. Внедрение системы мониторинга движения лекарственных препаратов позволит получать детальные сведения о перемещении упаковки препарата, а также информацию, которая препятствует ее нелегальному обращению (например, при наличии данных о том, что лекарство было ранее продано или выведено из обращения по какой-либо причине).
Разработчиком и оператором системы назначена Федеральная налоговая служба (ФНС). На официальном сайте ведомства создан специализированный раздел, посвященный системе маркировки лекарственных препаратов. Дополнительно подробная информация о ходе реализации проекта публикуется на сайте Росздравнадзора. Кроме этого участниками со стороны государства, помимо Минздрава и ФНС, являются министерство финансов Российской Федерации, министерство промышленности и торговли и Федеральная таможенная служба.
Кто обязан использовать ФГИС МДЛП?
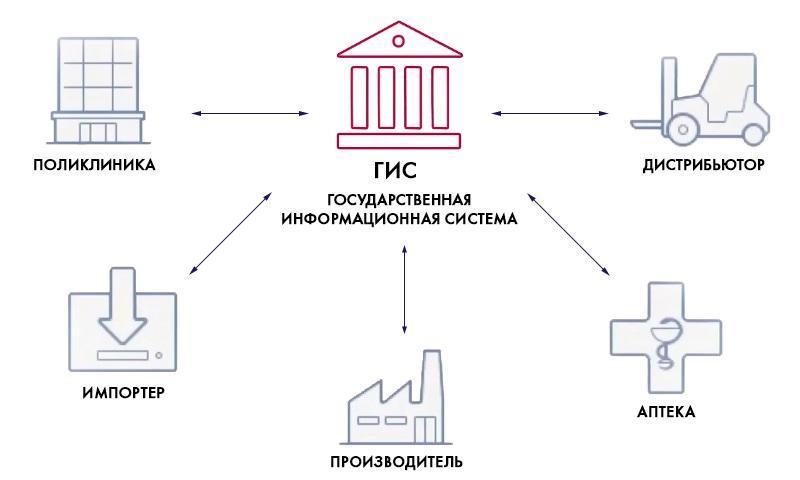
Непосредственными пользователями системы станут все участники рынка обращения лекарственных препаратов (ЛП):
- российские производители ЛП;
- иностранные держатели регистрационных удостоверений ЛП и их представительства;
- организации оптовой и розничной торговли ЛП (аптеки);
- медицинские организации (МО), в т.ч. и стоматологические клиники.

Что будет, если проигнорировать данное нововведение?
Как и любое другое законодательное решение, введение системы МДЛП требует его исполнения. Однако на практике, особенно если следование букве закона на начальном этапе требует материальных расходов, многие продолжают работать по старинке, не обращая внимания на изменения условий. Так к чему нужно быть готовым руководителям клиник, игнорирующим систему МДЛП?
Согласно статье 6.34 КоАП РФ:
Несвоевременное внесение данных в систему МДЛП либо внесение в нее недостоверных данных влечет наложение административного штрафа
- на должностных лиц в размере от 5 тысяч до 10 тысяч рублей;
- на юридических лиц - от 50 тысяч до 100 тысяч рублей.
Примечание. За административные правонарушения, предусмотренные настоящей статьей, лица, осуществляющие предпринимательскую деятельность без образования юридического лица (ИП), несут административную ответственность как юридические лица.
*Статья 6.34 вступает в силу с 1 января 2020 года
Что касается частных врачей, работающих как ИП, то согласно ст. 323-ФЗ, индивидуальный предприниматель с медицинской лицензией законодательно приравнивается к статусу медицинской организации. Таким образом, на него в полной мере распространяются все требования законов, касающихся медицинской деятельности.
К 1 января 2020 года все участники рынка медицинских и фармацевтических услуг обязаны быть зарегистрированы в системе и обладать для работы в ней всей необходимой техникой и программами.
В противном случае компании лишаются возможности приобретать лекарственные препараты и автоматически попадают на штрафы. Зуботехнические лаборатории с медицинской лицензией так же должны выполнять данное требование, т.к. по закону они относятся к медицинским организациям, а значит обязаны регистрироваться в системе МДЛП. Проверить уклонистов от исполнения закона будет просто: в базу вводят номер из реестра медицинских лицензий и смотрят, есть ли регистрация в системе МДЛП. Если нет - штраф придет автоматом.
Как повлияет внедрение системы мониторинга движения лекарственных средств на ее участников (клиники, производители, дистрибьюторы)?
Клиники
С наступлением нового года всем медицинским организациям, работающим на территории РФ, придется передавать информацию о каждой поставке ЛП от поставщика, их перемещении между отделениями клиники, отпуске препаратов для медицинского применения, уничтожении или выводе их из оборота. Если во время приемки препарата информация со штрих-кода (маркировка) на упаковке и в системе мониторинга не совпадет, лекарство необходимо будет вернуть поставщику. Закупать и применять ЛП, данные о которых не внесены в систему, запрещается.
Перемещение препаратов должно быть отражено в системе в течение 5 рабочих дней. На данный момент есть неподтвержденная информация о том, что после запуска системы в эксплуатацию срок может быть сокращен до 1 рабочего дня.
Для работы в системе клиникам необходимо подготовиться: закупить нужное оборудование (сканеры), выделить ПК, бесперебойно подключенный к Интернет, установить программу для работы с системой мониторинга, а также обучить работе с системой ответственных лиц.
Что касается производителей и дистрибьюторов, то их ожидают куда более серьезные затраты. Это отнюдь не дешевое оборудование по нанесению маркировки препаратов, а также формирование дополнительных отделов сотрудников и оснащения рабочих мест.
Сотрудники редакции «Клуба стоматологов» задали этот вопрос разным представителям стоматологического рынка и получили довольно неожиданные ответы. Общее настроение участников опроса можно охарактеризовать, скорее, как пессимистичное. Итак, тема опроса: как повлияет внедрение системы мониторинга движения лекарственных средств на ее участников? И полученные нами отзывы о ИС МДЛП:
- Мария Таскина, директор и главный врач клиники «Ваш стоматолог» (г. Севастополь)
Плюсов введения системы не вижу. Ответственные руководители всегда старались купить оригинальную продукцию, а приобрести подделку подешевле все равно можно будет при желании.
С нелегальными препаратами я сама не сталкивалась, т.к. мы тщательно выбираем поставщиков. А вот предложения купить китайские подделки материалов поступают регулярно. По этой причине не приобретаю никаких материалов на выставках, только у проверенных поставщиков.
На мой взгляд, внедряемая государством система мониторинга приведёт к удорожанию препаратов, и, как следствие, удорожанию услуг и усложнению работы. Проблем она не решит- всегда будут желающие купить дешевле, а спрос, как известно, рождает предложение. ЕГАИС ведь не избавил нас от контрафактного алкоголя. Как торговали паленкой из под полы, так и торгуют.
Тем не менее, мы не собираемся игнорировать законодательство и систему контроля уже начали внедрять: купили ключи и зарегистрировались.
- Ольга Агальцова, руководитель стоматологической клиники "Идеалдент" (г. Таруса)
Я думаю, что кроме разовых затрат на покупку оборудования, получения ЭЦП и выделения дополнительной функции старшей медсестре, внедрение системы контроля больше никак не отразится на работе нашей небольшой клиники. На первом этапе предполагаю также сложности в закупке лекарственных средств, так как система вводится одномоментно по всей стране, и, скорее всего, будут накладки и перебои с поставками. Кроме того, оборудование может сломаться, программа – зависнуть, а техподдержка будет перегружена. Но в конечном итоге, все «утрясется», как утряслось внедрение онлайн касс, например, или номенклатурного прейскуранта.
Случаев поставок нелегальных препаратов у нас не было. Несмотря на то, что в стоматологии лекарственных средств не так уж и много, мы отслеживаем списки отозванных или недоброкачественных лекарств - Минздрав Калужской области облегчает нам задачу и регулярно делает рассылку этих списков.
Что касается возможности использования различных схем обхода данной системы, то, на мой взгляд, в каких-то масштабных проектах, крупных аптечных сетях и складах, возможно и есть шанс придумать и реализовывать какие-либо серые схемы. Хотя сразу оговорюсь: я в таких делах не эксперт, это просто предположение. Ожидаю, что нас, мелких потребителей, контролировать будут достаточно жестко (уже идут предупреждения и напоминания о внедрении системы из контролирующих органов), несмотря на то, что мы не занимаемся реализацией лекарственных препаратов.
Внедрять систему МДЛП в своей клинике конечно же мы планируем, хотя мне не верится, что с 1 января она заработает без перебоев. Цены на услуги будем повышать в плановом порядке.
- Мария Ардинцева, заместитель директора "Дент Арт" (г. Армавир)
Безусловно, внедрение системы МДЛП для клиники приведет к увеличению зарплатного фонда (минимально (!) от 5000 рублей в месяц) и затрат на оборудование дополнительного рабочего пространства (минимально от 50 000 рублей единовременно: на дополнительный стационарный компьютер (порядка 30-40 000 руб. с хорошими характеристиками), изготовление УКЭП (1100 руб.) на защищенном носителе (1200 руб.), приобретение Криптопро с бессрочной лицензией (2700 руб. ) и сканера поступления ЛП (пока под вопросом – от 3000 руб. ). И это в том случае, если не понадобится ещё и спецоценка дополнительного рабочего места. Но можно взглянуть на эту ситуацию и с другой стороны: если раньше кому-то из сотрудников приходилось отслеживать данные из информационных писем РЗН с целью выявления отзыва МИ и ЛС из обращения, то теперь это действие будет производиться автоматически путём сканирования при поступлении ЛП от поставщика. Таким образом, задача, которая решалась в организациях времене- и энергозатратным способом – упрощается и автоматизируется.
К сожалению, я уверена, что на первоначальном этапе система не заработает корректно. По опыту применения он-лайн кассы могу предположить, что технические заминки на местах (при отлаженной работе «Честного знака») будут возникать ещё в течение как минимум двух лет. Именно поэтому сегодня важно сделать «запасы» ЛП без маркировки и с большим сроком годности. В своей клинике мы начали работу по внедрению системы МДЛП, однако процедура регистрации на портале «Честный знак» говорит о затруднениях в работе всего нововведения. Сделав всё необходимое, мы пока не можем в установленные сроки получить подтверждение регистрации. Надеемся, что повторные запросы в службу тех поддержки позволят оказаться в реестре зарегистрированных организаций до 01.01.2020г. и избежать первоначальных штрафов.
Тем не менее среди участников опроса все-таки нашлись и сторонники системы.
- Сергей Кузнецов, президент РОО «Стоматологи столицы», совладелец и руководитель сети клиник ГК «Центр эстетической стоматологии», доктором медицинских наук, профессором (г. Москва)
Лично я вижу от внедрения системы только плюсы! Чем больше контроля со стороны государства, особенно в такой сфере как фармацевтика, тем лучше! Конечно, контрафакт сохранится, но его количество сократиться в разы. Что касается сбоев в работе системы на первоначальном этапе, то они у нас в стране возможны всегда и во всём!
Дистрибьютор ЛП
- Ольга Машкина, директор департамента продаж компании "Рокада Мед" (г. Казань)
Допускаю, что внедрение системы контроля способствует прекращению нелегального оборота ЛС на рынке России, который негативно влияет на здоровье пациентов и юридическую безопасность клиник. В компании «Рокада Мед» поставка ЛС осуществляется напрямую от изготовителя, что полностью исключает нелегальную продукцию. Минусом является повышение стоимости ЛС и соответственно услуг клиник из-за затрат на внедрение системы на всех этапах прохождения ЛС. Сегодня государство заинтересовано навести порядок и ликвидировать контрафакт, поэтому мы рассчитываем, что 90% оборота будут составлять маркированные ЛС. Клиники и торгующие компании, которые не внедрят систему, окажутся на "черном ранке". На начальном этапе возможны проблемы с работой системы, поэтому мы, как компания-импортер, создали большой запас ЛС для обеспечения спроса на переходный период. К внедрению ИС «Честный знак» наша компания полностью готова. Система протестирована, но реальные поставки еще не проводились в связи с отсутствием маркированных ЛС, зарегистрированных в системе.
Есть ли выгоды от внедрения ИС МДЛП для участников медицинского рынка?
Предполагается, что внедрение системы МДЛП и маркировка позволит бизнесу повысить производительность, усовершенствовать логистические схемы, нарастить долю рынка и в конечном счете увеличить выручку:
- За счет снижения процента контрафакта легальные производители смогут увеличить объемы производства на 5-50% в зависимости от товарной группы.
- Бизнес сможет перевести производство на Индустрию 4.0, на работу по принципу Just-in-Time. Получая в режиме онлайн данные о движении продукции, он будет оптимально планировать производство, снижать запасы и повышать оборачиваемость продукции.
- Подключение к оператору электронного документооборота (если в ЭДО ранее не работали).
- Производители смогут экономить на логистике: при внедрении полного прослеживания получение производителем или логистической компанией актуального статистического материала о географии, интенсивности, сезонности продаж позволит перестроить логистические схемы, оптимизировать поставки и складские запасы.
- Наладится учет. Сейчас многие предприниматели не имеют собственных данных об остатках и кодах товаров на складах. Без правильного учета невозможно считать прибыль или планировать закупки, поэтому автоматизация поможет предпринимателям навести порядок в своем бизнесе.
- Переход на электронный документооборот. ЭДО радикально сокращает объем бумажных документов, которыми до сих пор активно обмениваются между собой российские компании и снизит издержки бизнеса и повысит производительность труда.
Что касается клиник, то самая главная и неоспоримая для них выгода – это хорошая репутация и полная уверенность в том, что используемые ЛП являются легальными, а значит не нанесут ущерб здоровью пациента. Кроме этого, систематизируется документооборот, появиться возможность максимально оптимизировать поставки и контроль за складскими запасами.
Как организована работа системы мониторинга движения лекарственных препаратов?
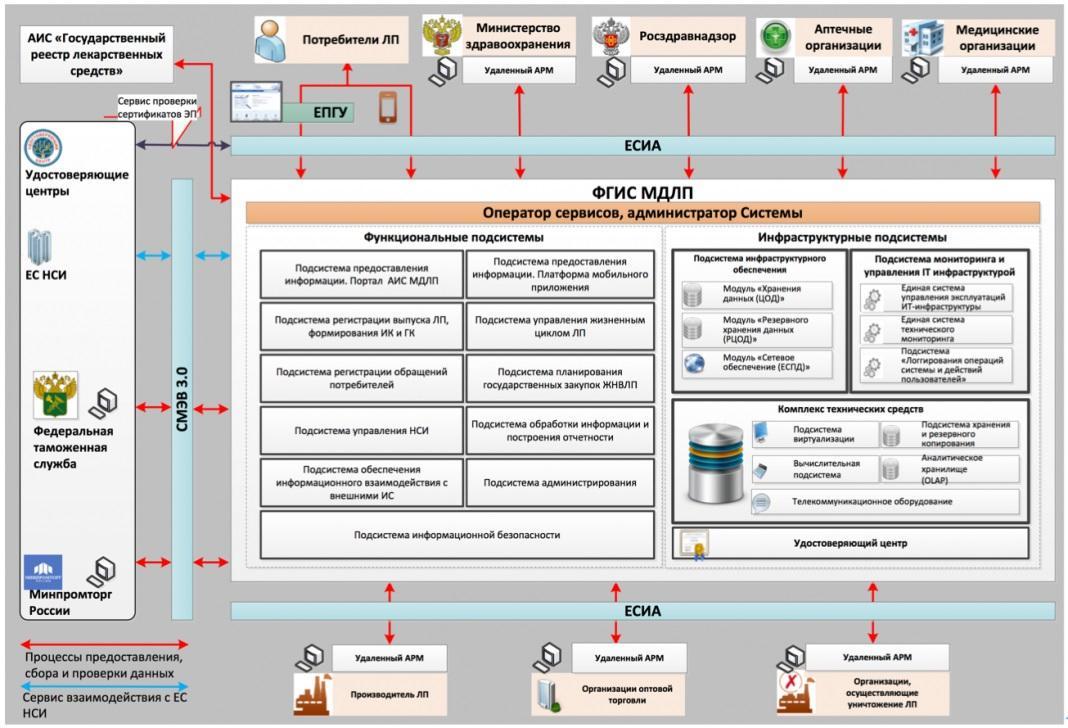
Простые вопросы о системе МДЛП, ответы на которые должен знать руководитель клиники.
1. Какие препараты должны быть занесены в систему мониторинга?
Все препараты медицинского назначения, которые зарегистрированы в РФ именно как лекарственные средства. Проверить препарат можно по государственному реестру лекарственных средств.
2. Кто обязан наносить маркировку?
Это делает производитель или поставщик ЛП.
3. Каким образом проводится проверка подлинности препаратов в условиях клиники?
Проверку подлинности лекарственных средств при получении их от поставщика проводят путем сканирования маркировки (штрих-кода) специальным сканером, подключенным к системе учета ЛП через компьютер. При приемке препарата от поставщика ответственный сотрудник обязан отсканировать код на упаковке и либо принять препарат на баланс в клинику, либо забраковать его, если система покажет несоответствие информации на упаковке и в системе.
4. Что нужно сделать руководителю клиники для использования ИС МДЛС (пошаговая инструкция):
- Создать рабочее место, оснащенное персональным компьютером, бесперебойно подключенным к Интернет, и устройством считывания индивидуальной маркировки (сканером).
- Установить на рабочем месте сертификат ключа ЭЦП (электронной цифровой подписи*) – специальной программы, обеспечивающей работу с электронной подписью и защиту информации.
- Открыть информационный ресурс «Маркировка лекарственных средств» по адресу: https://mdlp.crpt.ru/ и пройти проверку настройки ЭЦП и программ, обеспечивающих защиту информации. На этом же ресурсе необходимо заполнить заявление на регистрацию в системе. Бланк заявления появится автоматически при первом входе в «Личный кабинет».
- Дождаться получения подтверждения о регистрации на электронную почту, указанную в заявлении.
- Вновь войти с помощью ЭЦП на информационный ресурс «Маркировка лекарственных средств» по адресу https://mdlp.crpt.ru/ и зарегистрироваться как пользователь системы.
Как получить электронную цифровую подпись (ЭЦП)?
В соответствии с положениями Федерального закона от 6 апреля 2011 г.№ 63-ФЗ «Об электронной подписи» средства электронной подписи и квалифицированные сертификаты ключей проверки электронных подписей выдаются аккредитованными удостоверяющими центрами. Для получения электронной подписи необходимо обратиться в такой центр по месту нахождения организации. Ст. 5 № 63-ФЗ определяет следующие виды электронной подписи: простая электронная подпись и усиленная электронная подпись. Различаются усиленная неквалифицированная электронная подпись и усиленная квалифицированная электронная подпись. Таким образом, перед обращением в удостоверяющий центр для получения электронной подписи, заявителю следует определить вид электронной подписи, который необходим для осуществления различных правоотношений в электронном виде. Для работы с ФГИС МДЛП рекомендуется усиленная электронная подпись.
Выбор сканера: модели, отличия, цены
В данной статье мы приведем примеры наиболее популярных и уже проверенных моделей, но, ни в коем случае, не будем утверждать, что они идеальны. Право выбора всегда остается за самими пользователями.
Штрих-коды DataMatrix, которые с 1 января следующего года будут наноситься на упаковки всех ЛП, представляют собой двумерный матричный код. Для распознавания такого вида кодировки нужен специальный 2D сканер штрих-кода. Другая, более простая линейная модель (1D) не сможет распознать установленный код. Конечно, двумерные сканеры стоят дороже линейных, но, как правило, такие приборы считывают как двумерные (2D), так и линейные (1D) кодировки. Для предотвращения фальсификата идентификатор на упаковках лекарственных препаратов будет отличаться особой сложностью для сканирования. Это и картонные пачки, и блистерные упаковки с блестящим и матовым покрытием. Сканер для считывания таких маленьких, иногда трудночитаемых штрих-кодов должен быть высокочувствительным.
- 2D сканер Datalogic QuickScan QD2430 USB
«+» - сканер для маркировки проверенный на работоспособность, рекомендован к использованию ИС «Честный знак». Это ручной проводной сканер с технологией image-сканирования. Легко подключается к компьютеру за счет USB-разъема. Сканирует двумерные и линейные штрих-коды с любых поверхностей. Распознает коды на расстоянии до 35 см, выдерживает множественные падения.
«-» - пока не обнаружено.
Цена - от 5 200 руб.

- 2D сканер Honeywell 1450g
«+» - сканер для маркировки проверенный «Честным знаком». Устройство имеет высокую производительность, быстро и безошибочно сканирует даже поврежденные DataMatrix. Это проводной сканер с технологией image-сканирования. Подключается с помощью USB, RS232, RS485. Сканирует двумерные и линейные штрих-коды с экранов, мониторов, этикеток и других поверхностей. Распознает коды на расстоянии до 55 см. Сканирует 1D и 2D штрих-коды, имеет высокую производительность, ударопрочен, работает с ЕГАИС и Маркировкой.
«-» - не обнаружено.
Цена – от 4 000 руб.

- Zebra (Motorola) DS2208
«+» - недорогой качественный сканер для маркировки. Продукт рекомендован «Честным знаком» и имеет модуль сканирования Motorolla. Быстрое и точное сканирование элементов на различных поверхностях. Подключается к компьютеру за счет USB-разъема. Сканирует двумерные и линейные 1D и 2D штрих-коды под любым углом наклона. Распознает коды на расстоянии до 36,8 см. Ударопрочен.
«-» - не обнаружено.
Цена – от 4 500 руб.

- АТОЛ SB 2108 2D
Недорогой сканер от АТОЛ. Легко справляется с поврежденными штрихкодами, считывает штрихкоды с любых поверхностей. Успешное считывание подтверждается звуковой и визуальной индикацией. Подключается через USB-интерфейс. Для начала работы нужно подключить сканер к компьютеру, драйвер установится сам. Имеет удобную рукоятку и малый вес — всего 125 г. Низкая цена.
«-» - не обнаружено.
Цена – от 3 800 руб.

- Ручной сканер 2D штрих-кодов VMC BurstScan Lite v2
«+» - рекомендован оператором ИС Маркировки «Честный ЗНАК». Представляет собой ручной фотосканер двумерных штрих-кодов, оптимизированный для работы со штрих-кодами маркировки (Data Matrix) и акцизных марок ЕГАИС. Считывает широко распространённые линейные (1D) и двумерные (2D) штрих-коды, в том числе с экранов мобильных телефонов. Работает на подставке с активацией по событию появления объекта в поле зрения. Хорошо считывает мятые, поцарапанные, затертые, низкоконтрастные штрих-коды. Сравнительно невысокая стоимость.
«-» - нет информации об ударопрочности, возможно требует аккуратного обращения.
Цена – от 3 900 руб.

CRM, готовые к работе с ФГИС МДЛП на данный момент
Решение от 1С
1С:МДЛП - облачное приложение для организаций с небольшим оборотом лекарств без ведения автоматизированного складского учета.
Решение от Клуба стоматологов

StomX – программа для стоматологических клиник (расписание, амбулаторные карты, отчеты, CRM и многое другое). Взаимодействие с ИС МДЛП поддерживает и приемку и выбытие лекарственных препаратов с поддержкой и без сканера штрихкодов, а также регистратора выбытия. (перейти на сайт программы).
Решение от Первый БИТ
БИТ.Управление медицинским центром — программа для управления клиникой на базе 1С. Регистратура. Аналитика и финансы. Медицинский учет и ЭМК. Склад. Маркетинг и СRM, МДЛП;
БИТ.Стоматология — программа для управления стоматологической клиникой на базе 1С. Регистратура. Аналитика и финансы. Медицинский учет и Зубная карта. Склад. Маркетинг и СRM, МДЛП.
Бизнес-процесс по приёму и выбытию лекарственного препарата в медицинском учреждении на примере Национального медико-хирургического Центра имени Н.И. Пирогова
Обновления
12 декабря 2019г.
Госдума приняла закон, который переносит на полгода срок вступления в силу положений законодательства об обязательной маркировке лекарственных средств. Вместо 1 января обязательная маркировка стартует 1 июля 2020 года.
10 января 2020г.
Правительство РФ установило особенности внедрения системы цифровой маркировки и прослеживания лекарств. С учетом успешного опыта по запуску маркировки препаратов группы 7ВЗН с 1 октября 2019 г., 31 декабря 2019 г. было подписано Постановление Правительства РФ №1954 определяющее оптимальный режим подготовки всех участников оборота к дате обязательной маркировки всех препаратов.
Основные этапы подключения к системе:
- С 1 января до 29 февраля 2020 г. включительно все участники оборота лекарств обязаны зарегистрироваться в системе маркировки.
- До 15 февраля 2020 г. – медицинские учреждения (больницы, поликлиники, иные учреждения, имеющие лицензию на медицинскую деятельность), которые еще не подали заявку Оператору системы на получение регистратора выбытия (устройство фиксации факта выбытия препарата) – должны это сделать.
- До 1 мая 2020 г. участники оборота лекарств (производители и импортеры) должны подать заявку на получение регистратора эмиссии.
- С 1 июля 2020 г. наступает запрет на производство и импорт немаркированных лекарств, передача сведений об обороте маркированных лекарств в систему маркировки обязательна для всех участников оборота. Продажа немаркированных лекарств, поступивших в оборот до 1 июля 2020 г., разрешается до окончания срока их годности.
За последние годы проблема контрафакта лекарственных препаратов в России достигла такого уровня, что вынудила правительство к принятию кардинальных мер. С 1-го января 2020 года все организации, имеющие лицензии на фармацевтическую и медицинскую деятельность, будут обязаны передавать данные в Федеральную государственную информационную систему «Мониторинг движения лекарственных препаратов» (ФГИС МДЛП или ИС «Честный знак»). Для этого всем пользователям необходимо будет внедрить специальный электронный документооборот. Что ждать от данного нововведения клиникам, производителям и компаниям-дистрибьюторам? Очередных проблем и поборов или, все-таки на этот раз, есть шанс не только упорядочить свою работу с ЛП, но и даже получить прибыль. Попробуем разобраться.

Мониторинг движения лекарственных препаратов (далее ФГИС МДЛП или ИС МДЛП) – является частью общенациональной системы маркировки и отслеживания продукции под названием «Честный знак» по направлению «Лекарственные препараты». Специальный цифровой код (Data Matrix, штрих-код) гарантирует подлинность и качество товара. Основная задача данной системы – повышение уровня безопасности потребителей, борьба с контрафактом и некачественными аналогами.
Причины внедрения ИС МДЛП
По данным Минпромторга, только за 2018 год в обороте было выявлено свыше 6 миллионов единиц контрафактной продукции. Эта проблема наиболее серьезно отражается на конечных потребителях, которые за свои же собственные деньги рискуют здоровьем, и, зачастую, жизнью. Что касается производителей лекарственных препаратов и клиник, то здесь контрафакт грозит не только серьезными репутационными и финансовыми убытками, но и возможной уголовной ответственностью для должностных лиц.

Наличие цифровой маркировки позволяет получить полную информацию о товаре: название предприятия-изготовителя, место, дату и время производства и продажи, срок годности, артикул и номер стандарта. Данные хранятся в государственной информационной системе. Маркировка направлена на снижение распространения всех видов нелегальной продукции: контрафакта, фальсификата, контрабанды и т.д.
История принятия закона
Решение о создании федеральной государственной информационной системы мониторинга движения лекарственных препаратов от производителя до конечного потребителя с использованием маркировки принято 4 февраля 2015 г. на совещании Президента РФ с членами правительства. 20 февраля 2015 г. было подписано поручение, на основании которого Министерству Здравоохранения РФ поручалось обеспечить разработку и поэтапное внедрение системы. 30.11.2015 г. издан приказ №866 «Об утверждении концепции создания федеральной государственной информационной системы мониторинга движения лекарственных препаратов от производителя до конечного потребителя с использованием маркировки», утвердивший общую концепцию создания системы, ее цели и задачи, основные требования, а также перечень функциональных возможностей и сервисов.
Сроки внедрения и ответственный оператор
Внедрение информационной системы «Честный знак» (далее – ИС «Честный знак») планируется проводить поэтапно до 2024 года. Предполагается, что, начиная с этой даты, все виды товаров, производимых и/или реализуемых на территории РФ, должны иметь индивидуальную цифровую маркировку (штрих-код), позволяющий отследить их происхождение, логистику и использование в России.
1 января 2020 года стартует запуск информационной системы мониторинга движения лекарственных препаратов. Система МДЛП создана для защиты потребителей всех уровней от нелегальных лекарственных средств и призвана предоставить гражданам и организациям возможность оперативной проверки их легальности. Внедрение системы мониторинга движения лекарственных препаратов позволит получать детальные сведения о перемещении упаковки препарата, а также информацию, которая препятствует ее нелегальному обращению (например, при наличии данных о том, что лекарство было ранее продано или выведено из обращения по какой-либо причине).

Разработчиком и оператором системы назначена Федеральная налоговая служба (ФНС). На официальном сайте ведомства создан специализированный раздел, посвященный системе маркировки лекарственных препаратов. Дополнительно подробная информация о ходе реализации проекта публикуется на сайте Росздравнадзора. Кроме этого участниками со стороны государства, помимо Минздрава и ФНС, являются министерство финансов Российской Федерации, министерство промышленности и торговли и Федеральная таможенная служба.
Кто обязан использовать ФГИС МДЛП?
Непосредственными пользователями системы станут все участники рынка обращения лекарственных препаратов (ЛП):
- российские производители ЛП;
- иностранные держатели регистрационных удостоверений ЛП и их представительства;
- организации оптовой и розничной торговли ЛП (аптеки);
- медицинские организации (МО), в т.ч. и стоматологические клиники.

Что будет, если проигнорировать данное нововведение?
Как и любое другое законодательное решение, введение системы МДЛП требует его исполнения. Однако на практике, особенно если следование букве закона на начальном этапе требует материальных расходов, многие продолжают работать по старинке, не обращая внимания на изменения условий. Так к чему нужно быть готовым руководителям клиник, игнорирующим систему МДЛП?
Согласно статье 6.34 КоАП РФ:
Несвоевременное внесение данных в систему МДЛП либо внесение в нее недостоверных данных влечет наложение административного штрафа
- на должностных лиц в размере от 5 тысяч до 10 тысяч рублей;
- на юридических лиц - от 50 тысяч до 100 тысяч рублей.
Примечание. За административные правонарушения, предусмотренные настоящей статьей, лица, осуществляющие предпринимательскую деятельность без образования юридического лица (ИП), несут административную ответственность как юридические лица.
*Статья 6.34 вступает в силу с 1 января 2020 года
Что касается частных врачей, работающих как ИП, то согласно ст. 323-ФЗ, индивидуальный предприниматель с медицинской лицензией законодательно приравнивается к статусу медицинской организации. Таким образом, на него в полной мере распространяются все требования законов, касающихся медицинской деятельности.
К 1 января 2020 года все участники рынка медицинских и фармацевтических услуг обязаны быть зарегистрированы в системе и обладать для работы в ней всей необходимой техникой и программами.
В противном случае компании лишаются возможности приобретать лекарственные препараты и автоматически попадают на штрафы. Зуботехнические лаборатории с медицинской лицензией так же должны выполнять данное требование, т.к. по закону они относятся к медицинским организациям, а значит обязаны регистрироваться в системе МДЛП. Проверить уклонистов от исполнения закона будет просто: в базу вводят номер из реестра медицинских лицензий и смотрят, есть ли регистрация в системе МДЛП. Если нет - штраф придет автоматом.
Как повлияет внедрение системы мониторинга движения лекарственных средств на ее участников (клиники, производители, дистрибьюторы)?
Клиники
С наступлением нового года всем медицинским организациям, работающим на территории РФ, придется передавать информацию о каждой поставке ЛП от поставщика, их перемещении между отделениями клиники, отпуске препаратов для медицинского применения, уничтожении или выводе их из оборота. Если во время приемки препарата информация со штрих-кода (маркировка) на упаковке и в системе мониторинга не совпадет, лекарство необходимо будет вернуть поставщику. Закупать и применять ЛП, данные о которых не внесены в систему, запрещается.
Перемещение препаратов должно быть отражено в системе в течение 5 рабочих дней. На данный момент есть неподтвержденная информация о том, что после запуска системы в эксплуатацию срок может быть сокращен до 1 рабочего дня.
Для работы в системе клиникам необходимо подготовиться: закупить нужное оборудование (сканеры), выделить ПК, бесперебойно подключенный к Интернет, установить программу для работы с системой мониторинга, а также обучить работе с системой ответственных лиц.
Что касается производителей и дистрибьюторов, то их ожидают куда более серьезные затраты. Это отнюдь не дешевое оборудование по нанесению маркировки препаратов, а также формирование дополнительных отделов сотрудников и оснащения рабочих мест.
Сотрудники редакции «Клуба стоматологов» задали этот вопрос разным представителям стоматологического рынка и получили довольно неожиданные ответы. Общее настроение участников опроса можно охарактеризовать, скорее, как пессимистичное. Итак, тема опроса: как повлияет внедрение системы мониторинга движения лекарственных средств на ее участников? И полученные нами отзывы о ИС МДЛП:
- Мария Таскина, директор и главный врач клиники «Ваш стоматолог» (г. Севастополь)
Плюсов введения системы не вижу. Ответственные руководители всегда старались купить оригинальную продукцию, а приобрести подделку подешевле все равно можно будет при желании.
С нелегальными препаратами я сама не сталкивалась, т.к. мы тщательно выбираем поставщиков. А вот предложения купить китайские подделки материалов поступают регулярно. По этой причине не приобретаю никаких материалов на выставках, только у проверенных поставщиков.
На мой взгляд, внедряемая государством система мониторинга приведёт к удорожанию препаратов, и, как следствие, удорожанию услуг и усложнению работы. Проблем она не решит- всегда будут желающие купить дешевле, а спрос, как известно, рождает предложение. ЕГАИС ведь не избавил нас от контрафактного алкоголя. Как торговали паленкой из под полы, так и торгуют.
Тем не менее, мы не собираемся игнорировать законодательство и систему контроля уже начали внедрять: купили ключи и зарегистрировались.
- Ольга Агальцова, руководитель стоматологической клиники "Идеалдент" (г. Таруса)
Я думаю, что кроме разовых затрат на покупку оборудования, получения ЭЦП и выделения дополнительной функции старшей медсестре, внедрение системы контроля больше никак не отразится на работе нашей небольшой клиники. На первом этапе предполагаю также сложности в закупке лекарственных средств, так как система вводится одномоментно по всей стране, и, скорее всего, будут накладки и перебои с поставками. Кроме того, оборудование может сломаться, программа – зависнуть, а техподдержка будет перегружена. Но в конечном итоге, все «утрясется», как утряслось внедрение онлайн касс, например, или номенклатурного прейскуранта.
Случаев поставок нелегальных препаратов у нас не было. Несмотря на то, что в стоматологии лекарственных средств не так уж и много, мы отслеживаем списки отозванных или недоброкачественных лекарств - Минздрав Калужской области облегчает нам задачу и регулярно делает рассылку этих списков.
Что касается возможности использования различных схем обхода данной системы, то, на мой взгляд, в каких-то масштабных проектах, крупных аптечных сетях и складах, возможно и есть шанс придумать и реализовывать какие-либо серые схемы. Хотя сразу оговорюсь: я в таких делах не эксперт, это просто предположение. Ожидаю, что нас, мелких потребителей, контролировать будут достаточно жестко (уже идут предупреждения и напоминания о внедрении системы из контролирующих органов), несмотря на то, что мы не занимаемся реализацией лекарственных препаратов.
Внедрять систему МДЛП в своей клинике конечно же мы планируем, хотя мне не верится, что с 1 января она заработает без перебоев. Цены на услуги будем повышать в плановом порядке.
- Мария Ардинцева, заместитель директора "Дент Арт" (г. Армавир)
Безусловно, внедрение системы МДЛП для клиники приведет к увеличению зарплатного фонда (минимально (!) от 5000 рублей в месяц) и затрат на оборудование дополнительного рабочего пространства (минимально от 50 000 рублей единовременно: на дополнительный стационарный компьютер (порядка 30-40 000 руб. с хорошими характеристиками), изготовление УКЭП (1100 руб.) на защищенном носителе (1200 руб.), приобретение Криптопро с бессрочной лицензией (2700 руб. ) и сканера поступления ЛП (пока под вопросом – от 3000 руб. ). И это в том случае, если не понадобится ещё и спецоценка дополнительного рабочего места. Но можно взглянуть на эту ситуацию и с другой стороны: если раньше кому-то из сотрудников приходилось отслеживать данные из информационных писем РЗН с целью выявления отзыва МИ и ЛС из обращения, то теперь это действие будет производиться автоматически путём сканирования при поступлении ЛП от поставщика. Таким образом, задача, которая решалась в организациях времене- и энергозатратным способом – упрощается и автоматизируется.
К сожалению, я уверена, что на первоначальном этапе система не заработает корректно. По опыту применения он-лайн кассы могу предположить, что технические заминки на местах (при отлаженной работе «Честного знака») будут возникать ещё в течение как минимум двух лет. Именно поэтому сегодня важно сделать «запасы» ЛП без маркировки и с большим сроком годности. В своей клинике мы начали работу по внедрению системы МДЛП, однако процедура регистрации на портале «Честный знак» говорит о затруднениях в работе всего нововведения. Сделав всё необходимое, мы пока не можем в установленные сроки получить подтверждение регистрации. Надеемся, что повторные запросы в службу тех поддержки позволят оказаться в реестре зарегистрированных организаций до 01.01.2020г. и избежать первоначальных штрафов.
Тем не менее среди участников опроса все-таки нашлись и сторонники системы.
- Сергей Кузнецов, президент РОО «Стоматологи столицы», совладелец и руководитель сети клиник ГК «Центр эстетической стоматологии», доктором медицинских наук, профессором (г. Москва)
Лично я вижу от внедрения системы только плюсы! Чем больше контроля со стороны государства, особенно в такой сфере как фармацевтика, тем лучше! Конечно, контрафакт сохранится, но его количество сократиться в разы. Что касается сбоев в работе системы на первоначальном этапе, то они у нас в стране возможны всегда и во всём!
Дистрибьютор ЛП
- Ольга Машкина, директор департамента продаж компании "Рокада Мед" (г. Казань)
Допускаю, что внедрение системы контроля способствует прекращению нелегального оборота ЛС на рынке России, который негативно влияет на здоровье пациентов и юридическую безопасность клиник. В компании «Рокада Мед» поставка ЛС осуществляется напрямую от изготовителя, что полностью исключает нелегальную продукцию. Минусом является повышение стоимости ЛС и соответственно услуг клиник из-за затрат на внедрение системы на всех этапах прохождения ЛС. Сегодня государство заинтересовано навести порядок и ликвидировать контрафакт, поэтому мы рассчитываем, что 90% оборота будут составлять маркированные ЛС. Клиники и торгующие компании, которые не внедрят систему, окажутся на "черном ранке". На начальном этапе возможны проблемы с работой системы, поэтому мы, как компания-импортер, создали большой запас ЛС для обеспечения спроса на переходный период. К внедрению ИС «Честный знак» наша компания полностью готова. Система протестирована, но реальные поставки еще не проводились в связи с отсутствием маркированных ЛС, зарегистрированных в системе.
Есть ли выгоды от внедрения ИС МДЛП для участников медицинского рынка?
Предполагается, что внедрение системы МДЛП и маркировка позволит бизнесу повысить производительность, усовершенствовать логистические схемы, нарастить долю рынка и в конечном счете увеличить выручку:
- За счет снижения процента контрафакта легальные производители смогут увеличить объемы производства на 5-50% в зависимости от товарной группы.
- Бизнес сможет перевести производство на Индустрию 4.0, на работу по принципу Just-in-Time. Получая в режиме онлайн данные о движении продукции, он будет оптимально планировать производство, снижать запасы и повышать оборачиваемость продукции.
- Подключение к оператору электронного документооборота (если в ЭДО ранее не работали).
- Производители смогут экономить на логистике: при внедрении полного прослеживания получение производителем или логистической компанией актуального статистического материала о географии, интенсивности, сезонности продаж позволит перестроить логистические схемы, оптимизировать поставки и складские запасы.
- Наладится учет. Сейчас многие предприниматели не имеют собственных данных об остатках и кодах товаров на складах. Без правильного учета невозможно считать прибыль или планировать закупки, поэтому автоматизация поможет предпринимателям навести порядок в своем бизнесе.
- Переход на электронный документооборот. ЭДО радикально сокращает объем бумажных документов, которыми до сих пор активно обмениваются между собой российские компании и снизит издержки бизнеса и повысит производительность труда.
Что касается клиник, то самая главная и неоспоримая для них выгода – это хорошая репутация и полная уверенность в том, что используемые ЛП являются легальными, а значит не нанесут ущерб здоровью пациента. Кроме этого, систематизируется документооборот, появиться возможность максимально оптимизировать поставки и контроль за складскими запасами.
Как организована работа системы мониторинга движения лекарственных препаратов?

Простые вопросы о системе МДЛП, ответы на которые должен знать руководитель клиники.
1. Какие препараты должны быть занесены в систему мониторинга?
Все препараты медицинского назначения, которые зарегистрированы в РФ именно как лекарственные средства. Проверить препарат можно по государственному реестру лекарственных средств.
2. Кто обязан наносить маркировку?
Это делает производитель или поставщик ЛП.
3. Каким образом проводится проверка подлинности препаратов в условиях клиники?
Проверку подлинности лекарственных средств при получении их от поставщика проводят путем сканирования маркировки (штрих-кода) специальным сканером, подключенным к системе учета ЛП через компьютер. При приемке препарата от поставщика ответственный сотрудник обязан отсканировать код на упаковке и либо принять препарат на баланс в клинику, либо забраковать его, если система покажет несоответствие информации на упаковке и в системе.
4. Что нужно сделать руководителю клиники для использования ИС МДЛС (пошаговая инструкция):
- Создать рабочее место, оснащенное персональным компьютером, бесперебойно подключенным к Интернет, и устройством считывания индивидуальной маркировки (сканером).
- Установить на рабочем месте сертификат ключа ЭЦП (электронной цифровой подписи*) – специальной программы, обеспечивающей работу с электронной подписью и защиту информации.
- Открыть информационный ресурс «Маркировка лекарственных средств» по адресу: https://mdlp.crpt.ru/ и пройти проверку настройки ЭЦП и программ, обеспечивающих защиту информации. На этом же ресурсе необходимо заполнить заявление на регистрацию в системе. Бланк заявления появится автоматически при первом входе в «Личный кабинет».
- Дождаться получения подтверждения о регистрации на электронную почту, указанную в заявлении.
- Вновь войти с помощью ЭЦП на информационный ресурс «Маркировка лекарственных средств» по адресу https://mdlp.crpt.ru/ и зарегистрироваться как пользователь системы.
Как получить электронную цифровую подпись (ЭЦП)?
В соответствии с положениями Федерального закона от 6 апреля 2011 г.№ 63-ФЗ «Об электронной подписи» средства электронной подписи и квалифицированные сертификаты ключей проверки электронных подписей выдаются аккредитованными удостоверяющими центрами. Для получения электронной подписи необходимо обратиться в такой центр по месту нахождения организации. Ст. 5 № 63-ФЗ определяет следующие виды электронной подписи: простая электронная подпись и усиленная электронная подпись. Различаются усиленная неквалифицированная электронная подпись и усиленная квалифицированная электронная подпись. Таким образом, перед обращением в удостоверяющий центр для получения электронной подписи, заявителю следует определить вид электронной подписи, который необходим для осуществления различных правоотношений в электронном виде. Для работы с ФГИС МДЛП рекомендуется усиленная электронная подпись.
Выбор сканера: модели, отличия, цены
В данной статье мы приведем примеры наиболее популярных и уже проверенных моделей, но, ни в коем случае, не будем утверждать, что они идеальны. Право выбора всегда остается за самими пользователями.
Штрих-коды DataMatrix, которые с 1 января следующего года будут наноситься на упаковки всех ЛП, представляют собой двумерный матричный код. Для распознавания такого вида кодировки нужен специальный 2D сканер штрих-кода. Другая, более простая линейная модель (1D) не сможет распознать установленный код. Конечно, двумерные сканеры стоят дороже линейных, но, как правило, такие приборы считывают как двумерные (2D), так и линейные (1D) кодировки. Для предотвращения фальсификата идентификатор на упаковках лекарственных препаратов будет отличаться особой сложностью для сканирования. Это и картонные пачки, и блистерные упаковки с блестящим и матовым покрытием. Сканер для считывания таких маленьких, иногда трудночитаемых штрих-кодов должен быть высокочувствительным.
- 2D сканер Datalogic QuickScan QD2430 USB
«+» - сканер для маркировки проверенный на работоспособность, рекомендован к использованию ИС «Честный знак». Это ручной проводной сканер с технологией image-сканирования. Легко подключается к компьютеру за счет USB-разъема. Сканирует двумерные и линейные штрих-коды с любых поверхностей. Распознает коды на расстоянии до 35 см, выдерживает множественные падения.
«-» - пока не обнаружено.
Цена - от 5 200 руб.

- 2D сканер Honeywell 1450g
«+» - сканер для маркировки проверенный «Честным знаком». Устройство имеет высокую производительность, быстро и безошибочно сканирует даже поврежденные DataMatrix. Это проводной сканер с технологией image-сканирования. Подключается с помощью USB, RS232, RS485. Сканирует двумерные и линейные штрих-коды с экранов, мониторов, этикеток и других поверхностей. Распознает коды на расстоянии до 55 см. Сканирует 1D и 2D штрих-коды, имеет высокую производительность, ударопрочен, работает с ЕГАИС и Маркировкой.
«-» - не обнаружено.
Цена – от 4 000 руб.

- Zebra (Motorola) DS2208
«+» - недорогой качественный сканер для маркировки. Продукт рекомендован «Честным знаком» и имеет модуль сканирования Motorolla. Быстрое и точное сканирование элементов на различных поверхностях. Подключается к компьютеру за счет USB-разъема. Сканирует двумерные и линейные 1D и 2D штрих-коды под любым углом наклона. Распознает коды на расстоянии до 36,8 см. Ударопрочен.
«-» - не обнаружено.
Цена – от 4 500 руб.

- АТОЛ SB 2108 2D
Недорогой сканер от АТОЛ. Легко справляется с поврежденными штрихкодами, считывает штрихкоды с любых поверхностей. Успешное считывание подтверждается звуковой и визуальной индикацией. Подключается через USB-интерфейс. Для начала работы нужно подключить сканер к компьютеру, драйвер установится сам. Имеет удобную рукоятку и малый вес — всего 125 г. Низкая цена.
«-» - не обнаружено.
Цена – от 3 800 руб.

- Ручной сканер 2D штрих-кодов VMC BurstScan Lite v2
«+» - рекомендован оператором ИС Маркировки «Честный ЗНАК». Представляет собой ручной фотосканер двумерных штрих-кодов, оптимизированный для работы со штрих-кодами маркировки (Data Matrix) и акцизных марок ЕГАИС. Считывает широко распространённые линейные (1D) и двумерные (2D) штрих-коды, в том числе с экранов мобильных телефонов. Работает на подставке с активацией по событию появления объекта в поле зрения. Хорошо считывает мятые, поцарапанные, затертые, низкоконтрастные штрих-коды. Сравнительно невысокая стоимость.
«-» - нет информации об ударопрочности, возможно требует аккуратного обращения.
Цена – от 3 900 руб.

CRM, готовые к работе с ФГИС МДЛП на данный момент
Решение от 1С
1С:МДЛП - облачное приложение для организаций с небольшим оборотом лекарств без ведения автоматизированного складского учета.
Решение от Клуба стоматологов

StomX – программа для стоматологических клиник (расписание, амбулаторные карты, отчеты, CRM и многое другое). Взаимодействие с ИС МДЛП поддерживает и приемку и выбытие лекарственных препаратов с поддержкой и без сканера штрихкодов, а также регистратора выбытия. (перейти на сайт программы).
Решение от Первый БИТ
БИТ.Управление медицинским центром — программа для управления клиникой на базе 1С. Регистратура. Аналитика и финансы. Медицинский учет и ЭМК. Склад. Маркетинг и СRM, МДЛП;
БИТ.Стоматология — программа для управления стоматологической клиникой на базе 1С. Регистратура. Аналитика и финансы. Медицинский учет и Зубная карта. Склад. Маркетинг и СRM, МДЛП.
Бизнес-процесс по приёму и выбытию лекарственного препарата в медицинском учреждении на примере Национального медико-хирургического Центра имени Н.И. Пирогова
Обновления
12 декабря 2019г.
Госдума приняла закон, который переносит на полгода срок вступления в силу положений законодательства об обязательной маркировке лекарственных средств. Вместо 1 января обязательная маркировка стартует 1 июля 2020 года.
10 января 2020г.
Правительство РФ установило особенности внедрения системы цифровой маркировки и прослеживания лекарств. С учетом успешного опыта по запуску маркировки препаратов группы 7ВЗН с 1 октября 2019 г., 31 декабря 2019 г. было подписано Постановление Правительства РФ №1954 определяющее оптимальный режим подготовки всех участников оборота к дате обязательной маркировки всех препаратов.
Основные этапы подключения к системе:
- С 1 января до 29 февраля 2020 г. включительно все участники оборота лекарств обязаны зарегистрироваться в системе маркировки.
- До 15 февраля 2020 г. – медицинские учреждения (больницы, поликлиники, иные учреждения, имеющие лицензию на медицинскую деятельность), которые еще не подали заявку Оператору системы на получение регистратора выбытия (устройство фиксации факта выбытия препарата) – должны это сделать.
- До 1 мая 2020 г. участники оборота лекарств (производители и импортеры) должны подать заявку на получение регистратора эмиссии.
- С 1 июля 2020 г. наступает запрет на производство и импорт немаркированных лекарств, передача сведений об обороте маркированных лекарств в систему маркировки обязательна для всех участников оборота. Продажа немаркированных лекарств, поступивших в оборот до 1 июля 2020 г., разрешается до окончания срока их годности.






























































































































































1 комментарий
Мы это уже проходили. И называлось это "Знак качества"