В 2017 году во всем мире было установлено около 5 миллионов имплантатов, при этом распространенность самой процедуры имплантации возрастает в среднем на 14% каждый год. На Международной стоматологической выставке, проходившей в начале 2019 года в Кельне (Германия), было представлено более 200 стендов, посвященных тематике имплантации, что только подтверждает стремительное развитие отрасли. При этом, несмотря на такую возрастающую популярность имплантации как одного из вариантов стоматологической реабилитации, до сих пор не все врачи понимают, как обеспечить надежное долговременное функционирование интраоссальной конструкции, которое непосредственно влияет на успешность лечения в целом. Ведь планирование, установка и нагрузка имплантата – это составляющие немедленного результата, в то время как последующее обеспечение «работы» имплантата в условиях здоровых окружающих тканей являются аспектами более гигиеническими, нежели инвазивными. В данной статье будут описаны особенности тканей периимплантатной области, и то, как данные аспекты влияют на последующее «обслуживание» внутрикостной опоры гигиентистом. Также будут приведены отдельные аспекты лечения перимукозита и периимплантита.
Анатомические особенности периимплантатных тканей
Несмотря на сходства периимплантатных тканей с тканями пародонта вокруг собственного зуба, между этими двумя комплексами имеются значительные структурные отличия относительно взаимодействия с окружающими структурами и механизмов формирования биологического прикрепления. Периимплантатная область сформирована зоной окружающих мягких тканей/слизистой, которая формируется в период заживления, и зоной окружающих твердых тканей/кости, которая тесно прилегает к титановой поверхности, обеспечивая стабильность интраоссальной конструкции. Сегмент слизистой, обращенный к зоне интерфейса соединения имплантата-абатмента, часто именуется биологической шириной, и состоит из двух связанных составляющих: корональной части, включающей тонкий слой некератинизированного эпителия и бороздковый эпителий; и апикальной части, состоящей из соединительной ткани, которая непосредственно контактирует с областью имплантата/абатмента, формируя слой толщиной в 1-2 мм. Механизм соединения эпителиальных компонентов с поверхностью титановой конструкции остаётся предметом изучения и дискуссий, однако все, что нужно помнить врачу – это то, что данный тип соединения является очень тонким и хрупким. Понимание основной разницы между комплексами пародонтальных и периимплантатных тканей имеет крайне важное значение для клинициста, поскольку именно из-за разницы структуры данных составляющий в дальнейшем будут отличаться и паттерны деструкций этих тканей при пародонтите и периимплантите. Пучки соединяющих волокон в структуре пародонта характеризуются множественным механизмом поддержки, питания и чувствительности, в то время как пучки волокон вокруг имплантата такими характеристиками, к сожалению, не обладают. Это следует учитывать, как во время диагностики периимплантатной области, так и во время ее гигиенической очистки. Степень инвазии любого инструмента, работающего в непосредственной близости к имплантату должна быть минимальна, дабы не нарушить и без того хрупкий механизм адгезии периимплантатной слизистой.
Этиология и микробиология инфекционных поражений периимплантатных тканей
Пародонтальные поражения являются полиэтиологическими по своей природе, при этом было доказано, что поражения периимплантатных тканей подвержены действию аналогических факторов риска. С биологической точки зрения, первичным этиологическим фактором развития инфекционных поражений периимплантатных тканей является наличие зрелой бактериальной биопленки (налета). Постоянный контакт с микробами негативно влияет на состояние периимплантатной слизистой, в том числе и на ее «замыкающую» способность вокруг интерфейса имплантата/абатмента. Tomasi и коллеги установили, что бактерии, контаминирующие поверхность имплантата, формируют в разных случаях очень отличающиеся по структуре микробиомы, профиль которых не зависит от исходного пародонтального микробиома человека. Известно, что микробиом полости рта представляет собой сложную экосистему, которая включает около 700 видов микроорганизмов. При этом в норме данный комплекс бактерий находиться в специфическом состоянии баланса с преобладанием комменсалов и симбионтов. При нарушении данного баланса, которое наступает в ходе воспалительной реакции, начинается развитие периимплантатных патологий, ассоциированных с разными комплексами бактерий. Так, например, в состоянии дисбиоза возрастает количество ключевых патогенов по типу Porphyromonas gingivalis, что, в свою очередь, нарушает баланс между комменсалами и симбионтами. Таким образом формируется провоспалительна дисбиотическая экосистема, которая является характерной для периимплантитных поражений. Наличие же правильно «сбалансированной» биопленки в полости рта является характерной чертой здорового состояния полости рта.
Снятие зубных отложений может происходить посредством ручных или механических инструментов, что обеспечивает профилактику развития дисбиотического состояния ротовой полости. В ходе очистки проблемных областей всегда следует учитывать особенности биологии периимплантатных тканей, ведь при неправильном выполнении гигиенической чистки могут возникнуть осложнения уже имеющихся патологических состояний. Поэтому первое, что должен помнить гигиенист – это то, что уход за периимплантатной областью должен быть максимально аккуратными и атравматичным, а также следовать разработанным для этой цели специальным протоколам.
Обработка области дентального имплантата
Независимо от используемого метода обработки имплантатов, ручными инструментами или же посредством каких-либо аппаратов, он должен обеспечивать механическую очистку отложений без нарушения целостности поверхности интраосальной конструкции или же интерфейса соединения имплантата/абатмента. Современные инструменты для гигиенической очистки имплантатов изготовляются из пластика (ненаполненных смол), графита (наполненных смол), золота, титана, или же характеризуются наличием титановой рабочей поверхности. Такие инструменты можно приобрести в наборе-комплекте или же по одному в зависимости от потребностей. В ходе исследований с применением профилометрического лазера и сканирующей электронной микроскопии (СЭМ) было доказано, что инструменты, изготовленные из титана в наименьшей степени, повреждают рельеф поверхности, установленной инфраоссальной опоры. Кроме того, при очистке имплантата титановыми инструментами отмечается наименьшее количество резидуальных частиц в окружающих периимплантатных тканях по сравнению с использованием пластиковых или графитовых скайлеров. Некоторые производители титановых инструментов, используемых для ухода за имплантатами, представили на рынке вариации инструментов с более тонкими рабочими головками, которые при этом характеризуются повышенной прочностью на растяжение для более эффективной очистки зубных отложений или остатков цемента.
Насадки для механической очистки поверхности интраоссальных опор (магнитострикционные или же пьезохиругические) в основном являются металлическими с разным дизайном рабочих головок. Однако вопрос, касающийся возможности повреждения рельефа поверхности имплантата такими насадками до сих пор остается до конца нерешенным. Кроме того, логично, что чем ниже амплитуда вибраций, которые применяются в ходе очистки, тем меньше возможность альтерации инфраоссальной конструкции и интерфейса ее соединения с абатментом.
Воздухоабразивная очистка низкоабразивными порошками по типу глицина или эритритола считается одним из наиболее безопасных методов гигиенического ухода за имплантатами, обеспечивающим эффективное снятие поддесневых и наддесневых отложений. Кроме того, такое вмешательство является максимально комфортным для пациента и достаточно аргументированным с точки зрения временных и финансовых затрат. Leung и соавторы провели эксперимент, в котором титановые диски с SLA поверхностью инокулировали зубным налетом и анаэробно инкубированными микроорганизмами в течение 21 дня, позволяя биопленке полностью созреть и перекрыть все поверхности исследуемых дисков. Далее исследователи очищали поверхность дисков глициновым порошком и смогли добиться статистически значимой деконтаминации. Полученные результаты совпадают с теми, которые ранее были получены Cobb и коллегами, которые доказали большую эффективность глицинового порошка по сравнению с бикарбонатным при воздухоабразивной обработке поверхностей имплантатов и других биоматериалов.
Petersilka и коллеги применяли метод световой микроскопии для оценки повреждения десневого эпителия. В ходе эксперимента исследователи на гистологическом уровне регистрировали степень поражения десен сразу же после ручной обработки поверхности имплантата механическими инструментами и глициновым порошком, после чего сравнивали эти данные с теми, которые были верифицированы через 1 и 14 дней после вмешательства. Таким образом, было доказано, что при воздухоабразивной очистке глицином уровень эрозии мягких тканей были минимальным, в то время как ручная обработка спровоцировала эрозивные поражения окружающей слизистой средней и тяжелой степени. Однако уже через 14 дней после механической очистки окружающие ткани достигали своего исходного интактного состояния.
Также необходимо учитывать, что на сегодняшнее время на рынке представлено значительное количество разных модификаций поверхностей имплантатов и разных дизайнов протезов и абатментов (циркониевых, золотых, керамических), следовательно, подход к очистке каждого из них следует учета определенных особенностей. Но как бы там ни было, врач должен признать, что какой-либо инструмент он бы не использовал, все они провоцируют определенные поражение поверхности имплантата при очистке, вопрос только в том, насколько данное повреждение является значительным. Для выбора того или иного протокола гигиенического ухода за имплантатом врач должен учитывать влияние множества факторов, в том числе и особенностей биологии периимплантатных тканей, стараясь свести процесс вмешательства к минимально инвазивному.
Индикаторы риска
При осмотре пациентов с компрометированным состоянием пародонтологического статуса крайне важно обеспечить оценку и компенсацию всех потенциальных факторов риска, учитывая, что, по сути, лечения пародонтита как отдельной патологии нет. Грубо говоря, врач должен «откорректировать» все состояния, которые могут быть связаны с пародонтальным поражением и, таким образом, уменьшить риск его развития или прогрессирования. Heitz-Mayfield и Salvi сформулировали последующие факторы риска, ассоциированные с периимплантатной инфекцией: перимукозит, накопление зубного налета, курение и облучение.
Непрерывное лечение периимплантатных нарушений является крайне важным для обеспечения успешного длительного функционирования имплантатов. Так, например, лечение перимукозита способствует ограничению прогрессирования патологии для предотвращения развития стадии периимплантита. Пациенты же, которые своевременно не являются на профессиональную гигиену ротовой полости каждые 3-6 месяцев, в 48% случаев характеризуются признаками развития перимукозита, что было установлено в ходе наблюдений на протяжении 9-14 лет.
Несколько систематических обзоров указали на составляющую пародонтита в анамнезе как существенный фактор повышенного риска развития биологических осложнений, ассоциированных с дентальными имплантатами. Более того, пациенты, ранее болеющие агрессивной формой пародонтита, характеризуются очень высоким риском потери интраоссальных опор в целом. Использование коронок с цементной фиксацией на имплантатах также повышает риск развития периимплантатных нарушений из-за возможного негативного влияния остатков цемента на окружающие твердые и мягкие ткани. Даже несмотря на все попытки тщательно вычистить цемент вокруг супраконструкций, исследователям удавалось идентифицировать его остатки разного размера в окружающих тканях. Периимплантатные осложнения также могут быть связаны с дефицитом окружающих тканей по типу недостаточной кератинизации или объема слизистой в целом. Дентальные имплантаты с дефицитом окружающей слизистой характеризуются худшими параметрами функционирования, повышенным риском потери костной ткани и значительной предрасположенностью к развитию рецессий.
Лечение периимплантатных нарушений
Логично, что большая распространенность использования имплантатов связана с повышением частоты развития ассоциированных периимплантатных осложнений. Воспалительные реакции со стороны окружающих тканей могут быть вызваны длительным действием бактериальной биопленки, дефектом составляющих элементов (перелом имплантата, несоответствующее соединением имплантата и абатмента), другими патологиями ротовой полости по типу периферической гигантоклеточной гранулемы. Наиболее современное определение периимплантатных нарушений было сформулировано в ходе Всемирного Семинара, посвященного вопросам классификации пародонтальных и периимплантатных болезней, состоявшегося в 2017 году. Так, здоровые периимплантатные ткани характеризуются розовым цветом, отсутствием отека, определенной жесткостью тканей, отсутствием кровотечения при зондировании и отсутствием признаков потери костной ткани после заживления. В условиях перимукозита и периимплантита ткани вокруг титановой опоры стают красными и отекают, а их консистенция стает рыхлой. При перимукозите отмечается линейное или точечное кровотечение при зондировании, которое не сопровождается признаками потери окружающей костной ткани. Периимплантит характеризуется же профузным выделением крови или гноя при зондировании и значительным увеличением параметров самой глубины зондирования. При этом также отмечается ассоциированная потеря костной ткани, прогрессирующая по сравнению с показателями в первый год функционирования имплантата. Наличие налета и признаков кровотечения при зондировании обосновывают необходимость проведения механической очистки области имплантации и полировки поверхности титановой опоры. Если кровотечение при зондировании ассоциировано с потерей костной ткани менее чем на 2 мм, тогда можно обойтись только механической очисткой и приемом антибиотиков, если же потеря кости превысила 2 мм, необходимо обеспечить доступ к проблемного имплантату, проведение резективных и/или же регенераторных вмешательств, в отдельных случаях может понадобиться эксплантация.
Перимукозит
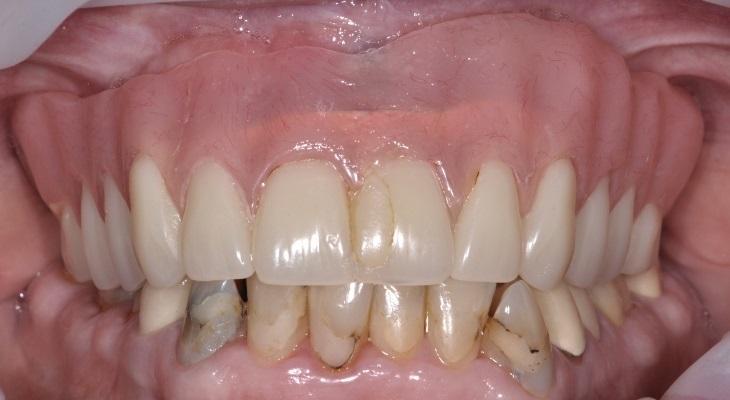
Основная цель лечения перимукозита состоит в устранении воспалительного процесса. Терапия данного нарушения предусматривает реализацию двухстороннего подхода. С одной стороны, врач должен оценить возможности пациента самостоятельно чистить проблемную область, и при необходимости проконсультировать его о других альтернативных подходах эффективного удаления зубного налета (фото 1 - 2).
Фото 1. Вид пациента до лечения.
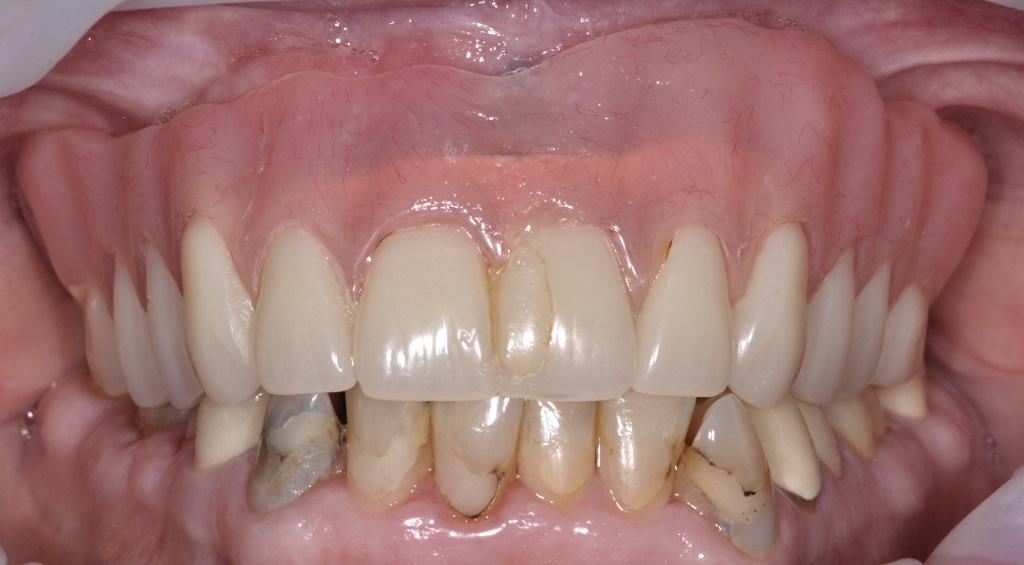
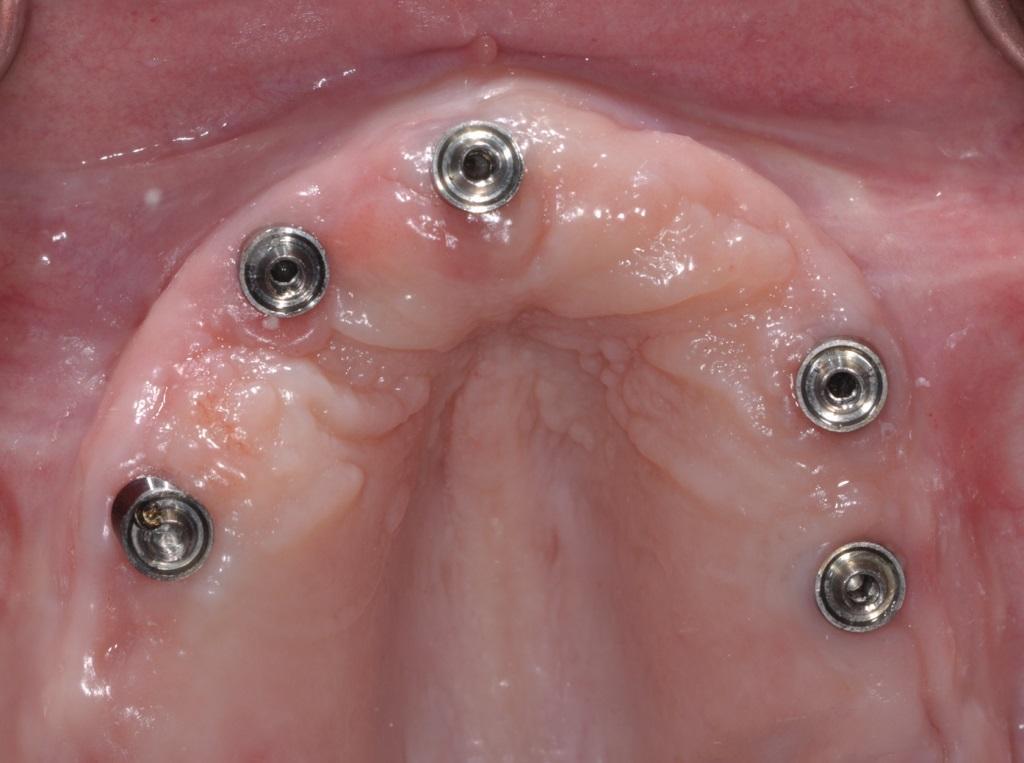
Фото 2. Вид после снятия протеза: присутствуют признаки перимукозита.
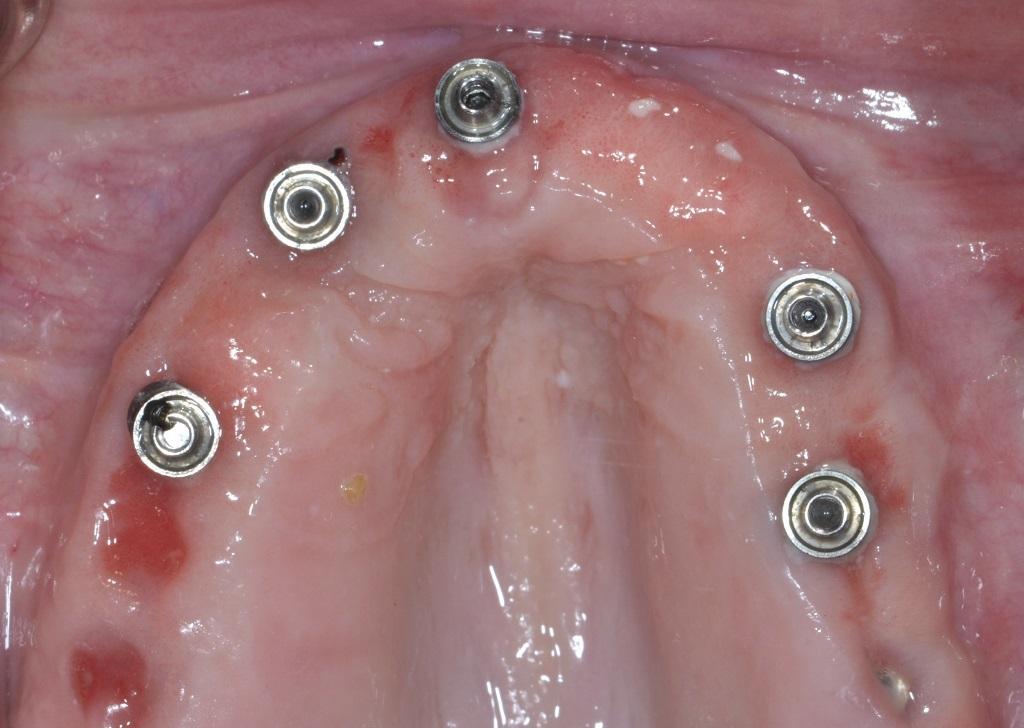
С другой стороны, врач также должен провести тщательную механическую чистку периимплантатной области и обеспечить последующий мониторинг за состоянием проблемной области. Для того, чтобы продемонстрировать пациенту наличие зубного налета стоматолог может использовать специальные красители. Такой метод также позволяет в значительной мере мотивировать пациента к дальнейшему более тщательному уходу за областью имплантата. Нехирургическое лечение периимплантатных нарушений предусматривает механическое снятие зубных отложений и контроль за их состоянием в ходе мониторинга. Для удаления биопленки могут использовать ручные кюретки, звуковые и ультразвуковые насадки и воздухоабразивные приспособления. Применение в подобных случаях антибиотиков местно или системно позволяет добиться лишь минимального эффекта. В ходе лечения перимукозита крайне важно оценить реакцию тканей на проводимую терапию (фото 3 - 4).
Фото 3. Нехирургическое лечение проблемных участков и модификация дизайна протеза для обеспечения лучших условий с целью проведения гигиенических мероприятий.
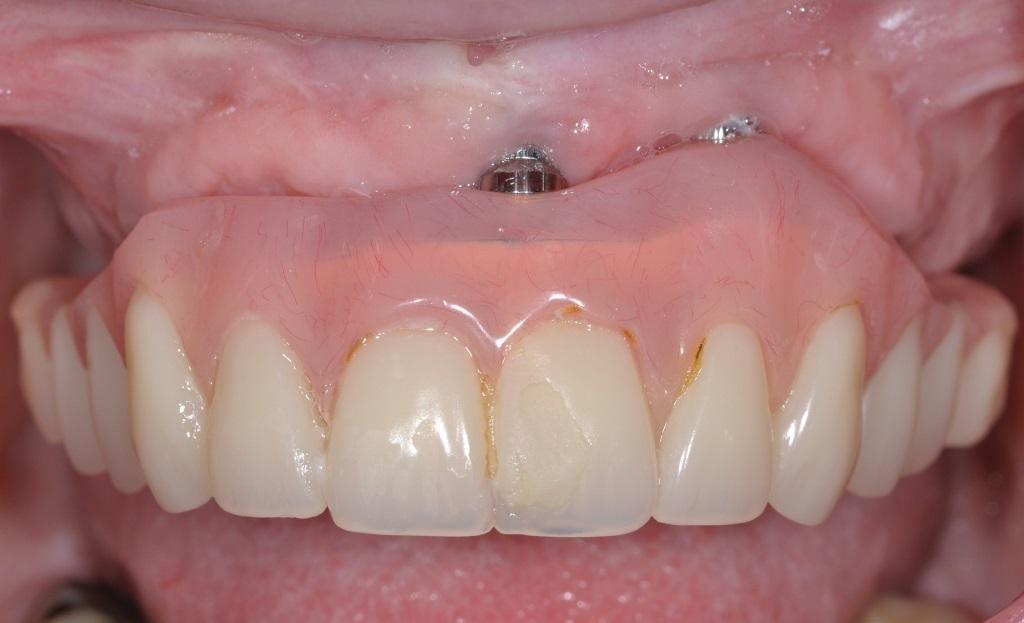
Фото 4. Вид через 4 недели после лечения: здоровое состояние периимплантатных тканей.
Если лечение не обеспечивает ожидаемых результатов, тогда нужно оценить точность посадки и дизайн используемых супраконструкций, а также проверить периимплантатные ткани на наличие остатков фиксирующего цемента.
Периимплантит
После постановки диагноза периимплантита (фото 5 - 6) необходимо провести исходную оценку пораженного имплантата для того, чтобы выбрать наиболее подходящий алгоритм лечения. Несмотря на то, что нехирургическое лечение периимплантита не всегда является успешным, данный метод всегда должен предшествовать хирургической альтернативе.
Фото 5. Признаки наличия пародонтальных карманов, выделение гноя и кровотечение во время диагностики конструкции на имплантате.
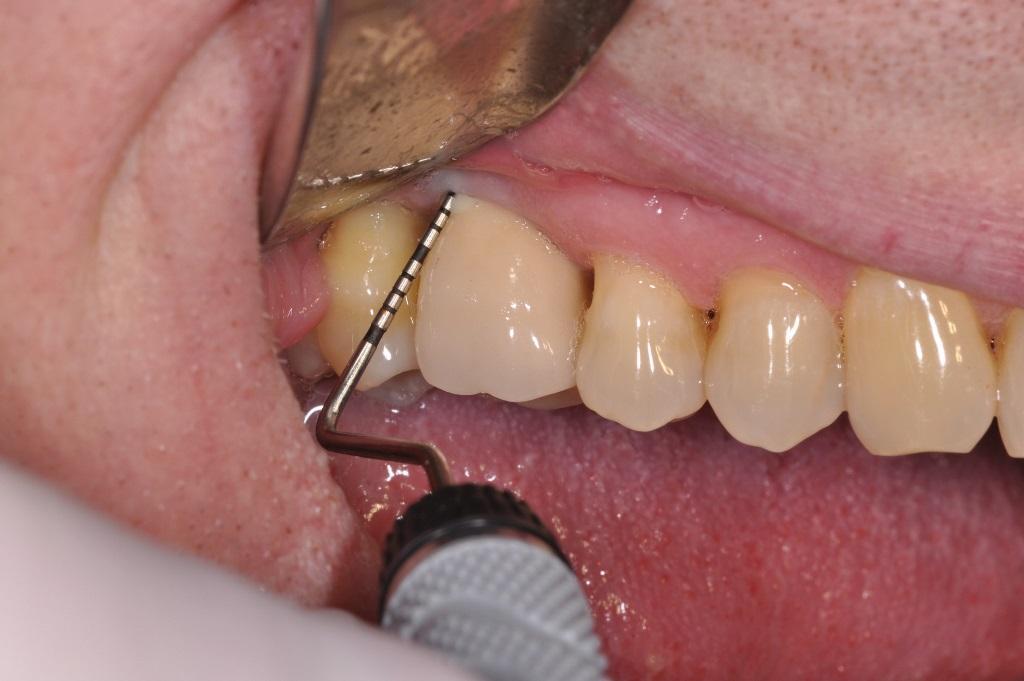
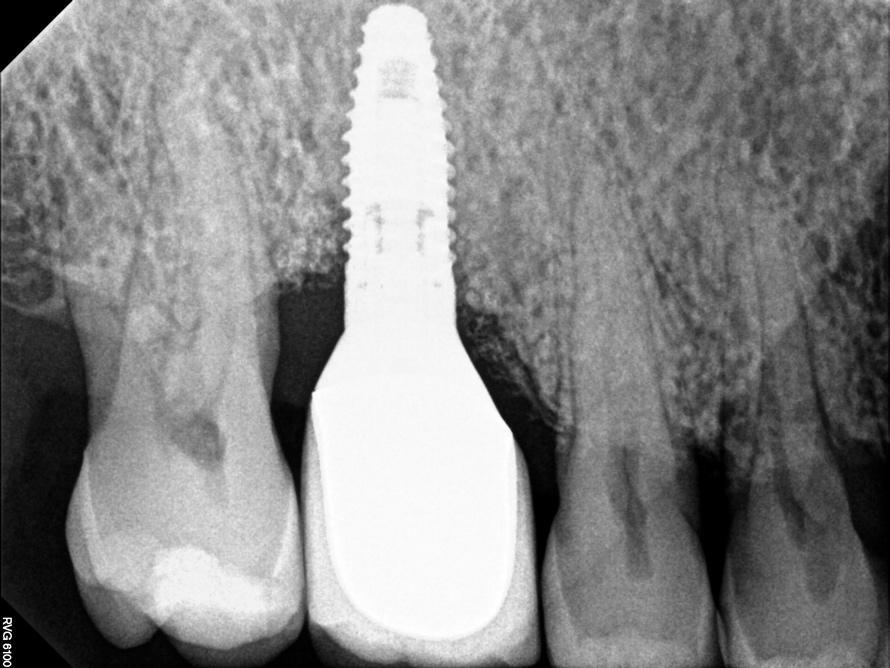
Фото 6. Признаки потери костной ткани вокруг имплантата подтверждают диагноз периимплантита.
Цель хирургического лечения периимплантатных поражений состоит в деконтаминации поверхности пораженного имплантата. И хотя в данное время известно несколько протоколов такой контаминации, однако ни один из них не является заметно более успешным по сравнению с другими. После очистки поверхности имплантата в каждом отдельном клиническом случае могут выполнять и дополнительные хирургические вмешательства по типу формирующих, резективных или же регенеративных, выбор которых зависит от положения имплантата и конфигурации имеющегося периимплантатного дефекта (фото 7). Результаты недавнего мета-анализа подтвердили, что в результате хирургического лечения периимплантита возможно добиться средней редукции зондирования в периимплантатной области на 2-3 мм. Данные других исследований указывают на то, что процедура имплантопластики является более эффективной, чем процедура формирования лоскута с целью обеспечения доступа (фото 8). Использование костных заменителей, в свою очередь, способствует дополнительному заполнению костных дефектов на 2 мм в процессе реализации регенеративного протокола вмешательства, который, однако, противопоказан для курильщиков.
Фото 7. Формирование доступа с сепарацией лоскута.
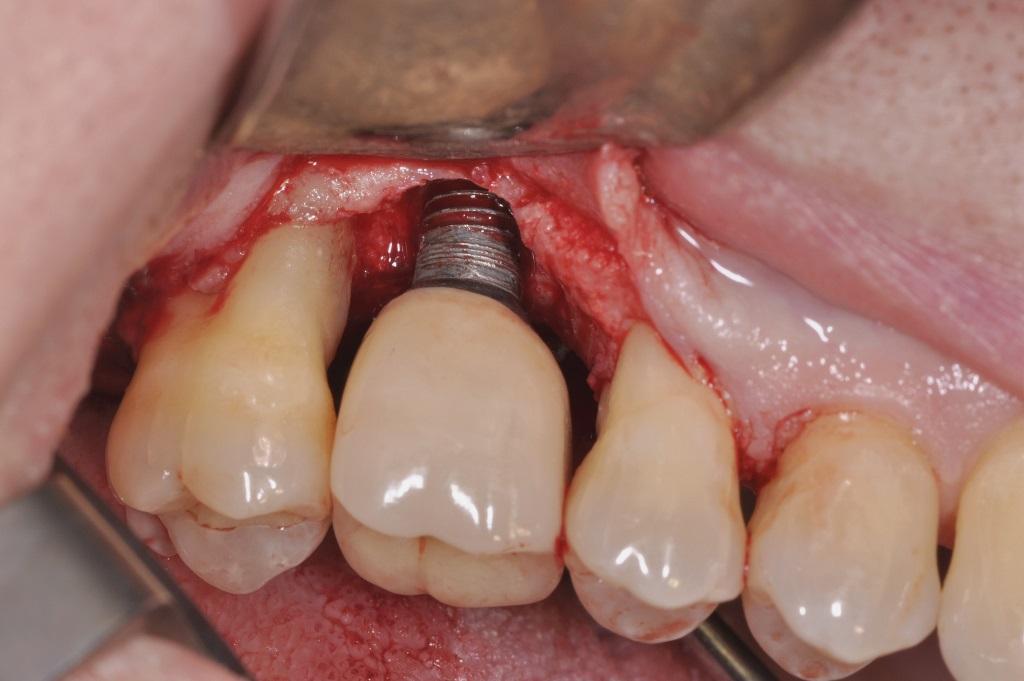
Фото 8. Проведение остэктомии и модификации поверхности имплантата.
Дефицит окружающих периимплантатных тканей
Параметры окружающих мягких тканей также играют важную роль в обеспечении успешного функционирования имплантата. Дефицит кератинизированной слизистой или же объема мягких тканей в целом формирует условия, способствующие развитию периимплантита. Толщина окружающей имплантат слизистой в 2 мм и более чем 2 мм кератинизированных десен являются адекватными параметрами для поддержки адекватного состояния дентального имплантата. Мягкотканная аугментация области имплантации позволяет добиться формирования более благоприятных биологических условий для длительного функционирования интраоссальной опоры.
Обслуживание дентальных имплантатов после лечения периимплантатных патологий
После лечения периимплантатных нарушений крайне важно обеспечить индивидуализированный мониторинг за пациентом, который бы предполагал купирование всех возможных факторов риска. Имплантаты, которые ранее уже подлежали лечению посредством хирургических и нехирургических подходов, должны находиться под тщательным наблюдением в ходе контрольных визитов пациента. Результаты недавнего систематического обзора указывают на то, что имплантаты, которые ранее были пролечены по поводу периимплантита, и в дальнейшем находятся под тщательным врачебным мониторингом, характеризуются более стабильными клиническими параметрами функционирования и выраженной стабильностью окружающей костной ткани. При этом параметры успешности и выживания имплантатов после проведенного лечения зависят от исходной потери окружающей костного ткани и конфигурации сформировавшегося костного дефекта. Если же после лечения периимплантита имплантат «брошен на произвол судьбы», то есть не находится под каким-либо мониторингом, то это значит только одно – его область рано или поздно снова будет поражена периимплантитом. Частота развития периимплантита у пациентов с ранее зарегистрированными фактами данного нарушения в анамнезе почти в 6 раз превышает аналогичный показатель у пациентов без наличия каких-либо предварительных периимплантатных поражений. Пациенты, которые отказались от контрольных визитов, почти в 15 раз чаще повторно страдают от периимплантита, чем те, которые четко следовали протоколу мониторинга (30% против 2,4%). Эффективность мониторинга за состоянием имплантатов снижается вследствие действия таких факторов как наличие пародонтита в анамнезе, тяжелая форма исходного поражения и курение.
Заключение
Для того чтобы обеспечить своевременную диагностику имплантат-ассоциированных поражений, и эффективность проводимых всех терапевтических манипуляций с ними связанных, любой врач-стоматолог должен быть в полной мере ознакомлен с фундаментальными принципами дизайна имплантата и абатмента, а также особенностями их функционирования и взаимодействия с окружающими тканями. Протоколы продолжительного мониторинга за состоянием имплантатов предусматривают проведение профессиональной очистки зубного налета с поверхности интраоссальной опоры, поддержку высокого гигиенического уровня ротовой полости в целом, а также тщательную оценку состояния окружающих мягких и твердых тканей, от которых в принципе и зависят все параметры успешности и выживания инфраоссальных титановых конструкций.
Авторы:
Penny Hatzimanolakis, Dipl. DH, BDSc, MSc
Ioannis Tsourounakis, DDS, MSc, Cert. Perio
Anastasia Kelekis-Cholakis, DMD, Dipl. Perio
В 2017 году во всем мире было установлено около 5 миллионов имплантатов, при этом распространенность самой процедуры имплантации возрастает в среднем на 14% каждый год. На Международной стоматологической выставке, проходившей в начале 2019 года в Кельне (Германия), было представлено более 200 стендов, посвященных тематике имплантации, что только подтверждает стремительное развитие отрасли. При этом, несмотря на такую возрастающую популярность имплантации как одного из вариантов стоматологической реабилитации, до сих пор не все врачи понимают, как обеспечить надежное долговременное функционирование интраоссальной конструкции, которое непосредственно влияет на успешность лечения в целом. Ведь планирование, установка и нагрузка имплантата – это составляющие немедленного результата, в то время как последующее обеспечение «работы» имплантата в условиях здоровых окружающих тканей являются аспектами более гигиеническими, нежели инвазивными. В данной статье будут описаны особенности тканей периимплантатной области, и то, как данные аспекты влияют на последующее «обслуживание» внутрикостной опоры гигиентистом. Также будут приведены отдельные аспекты лечения перимукозита и периимплантита.

Анатомические особенности периимплантатных тканей
Несмотря на сходства периимплантатных тканей с тканями пародонта вокруг собственного зуба, между этими двумя комплексами имеются значительные структурные отличия относительно взаимодействия с окружающими структурами и механизмов формирования биологического прикрепления. Периимплантатная область сформирована зоной окружающих мягких тканей/слизистой, которая формируется в период заживления, и зоной окружающих твердых тканей/кости, которая тесно прилегает к титановой поверхности, обеспечивая стабильность интраоссальной конструкции. Сегмент слизистой, обращенный к зоне интерфейса соединения имплантата-абатмента, часто именуется биологической шириной, и состоит из двух связанных составляющих: корональной части, включающей тонкий слой некератинизированного эпителия и бороздковый эпителий; и апикальной части, состоящей из соединительной ткани, которая непосредственно контактирует с областью имплантата/абатмента, формируя слой толщиной в 1-2 мм. Механизм соединения эпителиальных компонентов с поверхностью титановой конструкции остаётся предметом изучения и дискуссий, однако все, что нужно помнить врачу – это то, что данный тип соединения является очень тонким и хрупким. Понимание основной разницы между комплексами пародонтальных и периимплантатных тканей имеет крайне важное значение для клинициста, поскольку именно из-за разницы структуры данных составляющий в дальнейшем будут отличаться и паттерны деструкций этих тканей при пародонтите и периимплантите. Пучки соединяющих волокон в структуре пародонта характеризуются множественным механизмом поддержки, питания и чувствительности, в то время как пучки волокон вокруг имплантата такими характеристиками, к сожалению, не обладают. Это следует учитывать, как во время диагностики периимплантатной области, так и во время ее гигиенической очистки. Степень инвазии любого инструмента, работающего в непосредственной близости к имплантату должна быть минимальна, дабы не нарушить и без того хрупкий механизм адгезии периимплантатной слизистой.
Этиология и микробиология инфекционных поражений периимплантатных тканей
Пародонтальные поражения являются полиэтиологическими по своей природе, при этом было доказано, что поражения периимплантатных тканей подвержены действию аналогических факторов риска. С биологической точки зрения, первичным этиологическим фактором развития инфекционных поражений периимплантатных тканей является наличие зрелой бактериальной биопленки (налета). Постоянный контакт с микробами негативно влияет на состояние периимплантатной слизистой, в том числе и на ее «замыкающую» способность вокруг интерфейса имплантата/абатмента. Tomasi и коллеги установили, что бактерии, контаминирующие поверхность имплантата, формируют в разных случаях очень отличающиеся по структуре микробиомы, профиль которых не зависит от исходного пародонтального микробиома человека. Известно, что микробиом полости рта представляет собой сложную экосистему, которая включает около 700 видов микроорганизмов. При этом в норме данный комплекс бактерий находиться в специфическом состоянии баланса с преобладанием комменсалов и симбионтов. При нарушении данного баланса, которое наступает в ходе воспалительной реакции, начинается развитие периимплантатных патологий, ассоциированных с разными комплексами бактерий. Так, например, в состоянии дисбиоза возрастает количество ключевых патогенов по типу Porphyromonas gingivalis, что, в свою очередь, нарушает баланс между комменсалами и симбионтами. Таким образом формируется провоспалительна дисбиотическая экосистема, которая является характерной для периимплантитных поражений. Наличие же правильно «сбалансированной» биопленки в полости рта является характерной чертой здорового состояния полости рта.
Снятие зубных отложений может происходить посредством ручных или механических инструментов, что обеспечивает профилактику развития дисбиотического состояния ротовой полости. В ходе очистки проблемных областей всегда следует учитывать особенности биологии периимплантатных тканей, ведь при неправильном выполнении гигиенической чистки могут возникнуть осложнения уже имеющихся патологических состояний. Поэтому первое, что должен помнить гигиенист – это то, что уход за периимплантатной областью должен быть максимально аккуратными и атравматичным, а также следовать разработанным для этой цели специальным протоколам.
Обработка области дентального имплантата
Независимо от используемого метода обработки имплантатов, ручными инструментами или же посредством каких-либо аппаратов, он должен обеспечивать механическую очистку отложений без нарушения целостности поверхности интраосальной конструкции или же интерфейса соединения имплантата/абатмента. Современные инструменты для гигиенической очистки имплантатов изготовляются из пластика (ненаполненных смол), графита (наполненных смол), золота, титана, или же характеризуются наличием титановой рабочей поверхности. Такие инструменты можно приобрести в наборе-комплекте или же по одному в зависимости от потребностей. В ходе исследований с применением профилометрического лазера и сканирующей электронной микроскопии (СЭМ) было доказано, что инструменты, изготовленные из титана в наименьшей степени, повреждают рельеф поверхности, установленной инфраоссальной опоры. Кроме того, при очистке имплантата титановыми инструментами отмечается наименьшее количество резидуальных частиц в окружающих периимплантатных тканях по сравнению с использованием пластиковых или графитовых скайлеров. Некоторые производители титановых инструментов, используемых для ухода за имплантатами, представили на рынке вариации инструментов с более тонкими рабочими головками, которые при этом характеризуются повышенной прочностью на растяжение для более эффективной очистки зубных отложений или остатков цемента.
Насадки для механической очистки поверхности интраоссальных опор (магнитострикционные или же пьезохиругические) в основном являются металлическими с разным дизайном рабочих головок. Однако вопрос, касающийся возможности повреждения рельефа поверхности имплантата такими насадками до сих пор остается до конца нерешенным. Кроме того, логично, что чем ниже амплитуда вибраций, которые применяются в ходе очистки, тем меньше возможность альтерации инфраоссальной конструкции и интерфейса ее соединения с абатментом.
Воздухоабразивная очистка низкоабразивными порошками по типу глицина или эритритола считается одним из наиболее безопасных методов гигиенического ухода за имплантатами, обеспечивающим эффективное снятие поддесневых и наддесневых отложений. Кроме того, такое вмешательство является максимально комфортным для пациента и достаточно аргументированным с точки зрения временных и финансовых затрат. Leung и соавторы провели эксперимент, в котором титановые диски с SLA поверхностью инокулировали зубным налетом и анаэробно инкубированными микроорганизмами в течение 21 дня, позволяя биопленке полностью созреть и перекрыть все поверхности исследуемых дисков. Далее исследователи очищали поверхность дисков глициновым порошком и смогли добиться статистически значимой деконтаминации. Полученные результаты совпадают с теми, которые ранее были получены Cobb и коллегами, которые доказали большую эффективность глицинового порошка по сравнению с бикарбонатным при воздухоабразивной обработке поверхностей имплантатов и других биоматериалов.
Petersilka и коллеги применяли метод световой микроскопии для оценки повреждения десневого эпителия. В ходе эксперимента исследователи на гистологическом уровне регистрировали степень поражения десен сразу же после ручной обработки поверхности имплантата механическими инструментами и глициновым порошком, после чего сравнивали эти данные с теми, которые были верифицированы через 1 и 14 дней после вмешательства. Таким образом, было доказано, что при воздухоабразивной очистке глицином уровень эрозии мягких тканей были минимальным, в то время как ручная обработка спровоцировала эрозивные поражения окружающей слизистой средней и тяжелой степени. Однако уже через 14 дней после механической очистки окружающие ткани достигали своего исходного интактного состояния.
Также необходимо учитывать, что на сегодняшнее время на рынке представлено значительное количество разных модификаций поверхностей имплантатов и разных дизайнов протезов и абатментов (циркониевых, золотых, керамических), следовательно, подход к очистке каждого из них следует учета определенных особенностей. Но как бы там ни было, врач должен признать, что какой-либо инструмент он бы не использовал, все они провоцируют определенные поражение поверхности имплантата при очистке, вопрос только в том, насколько данное повреждение является значительным. Для выбора того или иного протокола гигиенического ухода за имплантатом врач должен учитывать влияние множества факторов, в том числе и особенностей биологии периимплантатных тканей, стараясь свести процесс вмешательства к минимально инвазивному.
Индикаторы риска
При осмотре пациентов с компрометированным состоянием пародонтологического статуса крайне важно обеспечить оценку и компенсацию всех потенциальных факторов риска, учитывая, что, по сути, лечения пародонтита как отдельной патологии нет. Грубо говоря, врач должен «откорректировать» все состояния, которые могут быть связаны с пародонтальным поражением и, таким образом, уменьшить риск его развития или прогрессирования. Heitz-Mayfield и Salvi сформулировали последующие факторы риска, ассоциированные с периимплантатной инфекцией: перимукозит, накопление зубного налета, курение и облучение.
Непрерывное лечение периимплантатных нарушений является крайне важным для обеспечения успешного длительного функционирования имплантатов. Так, например, лечение перимукозита способствует ограничению прогрессирования патологии для предотвращения развития стадии периимплантита. Пациенты же, которые своевременно не являются на профессиональную гигиену ротовой полости каждые 3-6 месяцев, в 48% случаев характеризуются признаками развития перимукозита, что было установлено в ходе наблюдений на протяжении 9-14 лет.
Несколько систематических обзоров указали на составляющую пародонтита в анамнезе как существенный фактор повышенного риска развития биологических осложнений, ассоциированных с дентальными имплантатами. Более того, пациенты, ранее болеющие агрессивной формой пародонтита, характеризуются очень высоким риском потери интраоссальных опор в целом. Использование коронок с цементной фиксацией на имплантатах также повышает риск развития периимплантатных нарушений из-за возможного негативного влияния остатков цемента на окружающие твердые и мягкие ткани. Даже несмотря на все попытки тщательно вычистить цемент вокруг супраконструкций, исследователям удавалось идентифицировать его остатки разного размера в окружающих тканях. Периимплантатные осложнения также могут быть связаны с дефицитом окружающих тканей по типу недостаточной кератинизации или объема слизистой в целом. Дентальные имплантаты с дефицитом окружающей слизистой характеризуются худшими параметрами функционирования, повышенным риском потери костной ткани и значительной предрасположенностью к развитию рецессий.
Лечение периимплантатных нарушений
Логично, что большая распространенность использования имплантатов связана с повышением частоты развития ассоциированных периимплантатных осложнений. Воспалительные реакции со стороны окружающих тканей могут быть вызваны длительным действием бактериальной биопленки, дефектом составляющих элементов (перелом имплантата, несоответствующее соединением имплантата и абатмента), другими патологиями ротовой полости по типу периферической гигантоклеточной гранулемы. Наиболее современное определение периимплантатных нарушений было сформулировано в ходе Всемирного Семинара, посвященного вопросам классификации пародонтальных и периимплантатных болезней, состоявшегося в 2017 году. Так, здоровые периимплантатные ткани характеризуются розовым цветом, отсутствием отека, определенной жесткостью тканей, отсутствием кровотечения при зондировании и отсутствием признаков потери костной ткани после заживления. В условиях перимукозита и периимплантита ткани вокруг титановой опоры стают красными и отекают, а их консистенция стает рыхлой. При перимукозите отмечается линейное или точечное кровотечение при зондировании, которое не сопровождается признаками потери окружающей костной ткани. Периимплантит характеризуется же профузным выделением крови или гноя при зондировании и значительным увеличением параметров самой глубины зондирования. При этом также отмечается ассоциированная потеря костной ткани, прогрессирующая по сравнению с показателями в первый год функционирования имплантата. Наличие налета и признаков кровотечения при зондировании обосновывают необходимость проведения механической очистки области имплантации и полировки поверхности титановой опоры. Если кровотечение при зондировании ассоциировано с потерей костной ткани менее чем на 2 мм, тогда можно обойтись только механической очисткой и приемом антибиотиков, если же потеря кости превысила 2 мм, необходимо обеспечить доступ к проблемного имплантату, проведение резективных и/или же регенераторных вмешательств, в отдельных случаях может понадобиться эксплантация.
Перимукозит
Основная цель лечения перимукозита состоит в устранении воспалительного процесса. Терапия данного нарушения предусматривает реализацию двухстороннего подхода. С одной стороны, врач должен оценить возможности пациента самостоятельно чистить проблемную область, и при необходимости проконсультировать его о других альтернативных подходах эффективного удаления зубного налета (фото 1 - 2).
Фото 1. Вид пациента до лечения.

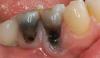
Фото 2. Вид после снятия протеза: присутствуют признаки перимукозита.

С другой стороны, врач также должен провести тщательную механическую чистку периимплантатной области и обеспечить последующий мониторинг за состоянием проблемной области. Для того, чтобы продемонстрировать пациенту наличие зубного налета стоматолог может использовать специальные красители. Такой метод также позволяет в значительной мере мотивировать пациента к дальнейшему более тщательному уходу за областью имплантата. Нехирургическое лечение периимплантатных нарушений предусматривает механическое снятие зубных отложений и контроль за их состоянием в ходе мониторинга. Для удаления биопленки могут использовать ручные кюретки, звуковые и ультразвуковые насадки и воздухоабразивные приспособления. Применение в подобных случаях антибиотиков местно или системно позволяет добиться лишь минимального эффекта. В ходе лечения перимукозита крайне важно оценить реакцию тканей на проводимую терапию (фото 3 - 4).
Фото 3. Нехирургическое лечение проблемных участков и модификация дизайна протеза для обеспечения лучших условий с целью проведения гигиенических мероприятий.

Фото 4. Вид через 4 недели после лечения: здоровое состояние периимплантатных тканей.

Если лечение не обеспечивает ожидаемых результатов, тогда нужно оценить точность посадки и дизайн используемых супраконструкций, а также проверить периимплантатные ткани на наличие остатков фиксирующего цемента.
Периимплантит
После постановки диагноза периимплантита (фото 5 - 6) необходимо провести исходную оценку пораженного имплантата для того, чтобы выбрать наиболее подходящий алгоритм лечения. Несмотря на то, что нехирургическое лечение периимплантита не всегда является успешным, данный метод всегда должен предшествовать хирургической альтернативе.
Фото 5. Признаки наличия пародонтальных карманов, выделение гноя и кровотечение во время диагностики конструкции на имплантате.

Фото 6. Признаки потери костной ткани вокруг имплантата подтверждают диагноз периимплантита.

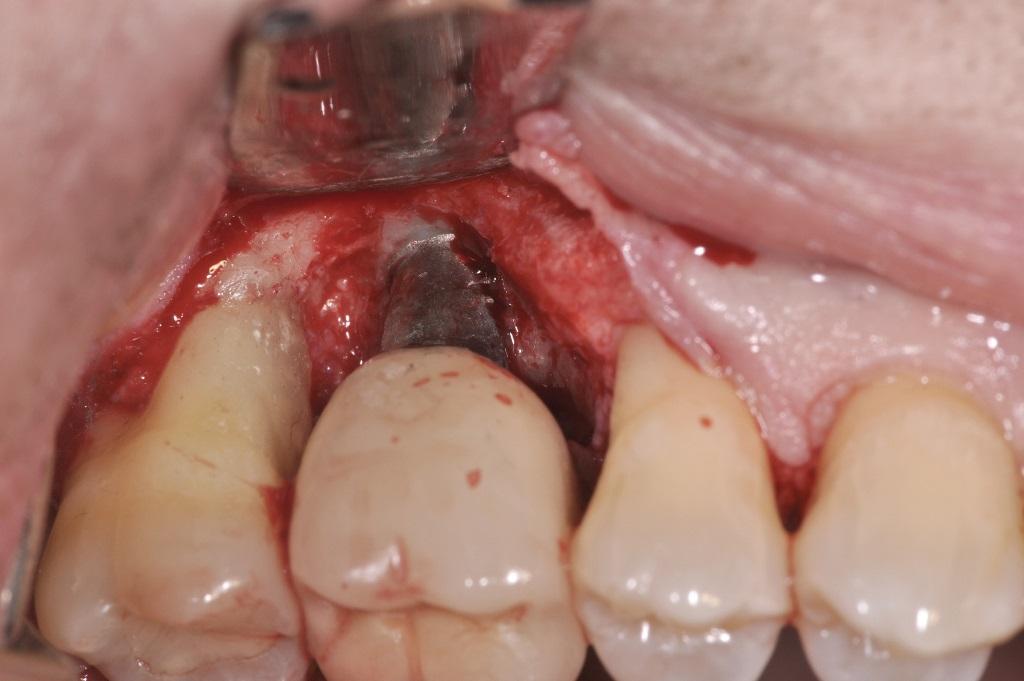
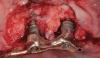
Цель хирургического лечения периимплантатных поражений состоит в деконтаминации поверхности пораженного имплантата. И хотя в данное время известно несколько протоколов такой контаминации, однако ни один из них не является заметно более успешным по сравнению с другими. После очистки поверхности имплантата в каждом отдельном клиническом случае могут выполнять и дополнительные хирургические вмешательства по типу формирующих, резективных или же регенеративных, выбор которых зависит от положения имплантата и конфигурации имеющегося периимплантатного дефекта (фото 7). Результаты недавнего мета-анализа подтвердили, что в результате хирургического лечения периимплантита возможно добиться средней редукции зондирования в периимплантатной области на 2-3 мм. Данные других исследований указывают на то, что процедура имплантопластики является более эффективной, чем процедура формирования лоскута с целью обеспечения доступа (фото 8). Использование костных заменителей, в свою очередь, способствует дополнительному заполнению костных дефектов на 2 мм в процессе реализации регенеративного протокола вмешательства, который, однако, противопоказан для курильщиков.
Фото 7. Формирование доступа с сепарацией лоскута.

Фото 8. Проведение остэктомии и модификации поверхности имплантата.

Дефицит окружающих периимплантатных тканей
Параметры окружающих мягких тканей также играют важную роль в обеспечении успешного функционирования имплантата. Дефицит кератинизированной слизистой или же объема мягких тканей в целом формирует условия, способствующие развитию периимплантита. Толщина окружающей имплантат слизистой в 2 мм и более чем 2 мм кератинизированных десен являются адекватными параметрами для поддержки адекватного состояния дентального имплантата. Мягкотканная аугментация области имплантации позволяет добиться формирования более благоприятных биологических условий для длительного функционирования интраоссальной опоры.
Обслуживание дентальных имплантатов после лечения периимплантатных патологий
После лечения периимплантатных нарушений крайне важно обеспечить индивидуализированный мониторинг за пациентом, который бы предполагал купирование всех возможных факторов риска. Имплантаты, которые ранее уже подлежали лечению посредством хирургических и нехирургических подходов, должны находиться под тщательным наблюдением в ходе контрольных визитов пациента. Результаты недавнего систематического обзора указывают на то, что имплантаты, которые ранее были пролечены по поводу периимплантита, и в дальнейшем находятся под тщательным врачебным мониторингом, характеризуются более стабильными клиническими параметрами функционирования и выраженной стабильностью окружающей костной ткани. При этом параметры успешности и выживания имплантатов после проведенного лечения зависят от исходной потери окружающей костного ткани и конфигурации сформировавшегося костного дефекта. Если же после лечения периимплантита имплантат «брошен на произвол судьбы», то есть не находится под каким-либо мониторингом, то это значит только одно – его область рано или поздно снова будет поражена периимплантитом. Частота развития периимплантита у пациентов с ранее зарегистрированными фактами данного нарушения в анамнезе почти в 6 раз превышает аналогичный показатель у пациентов без наличия каких-либо предварительных периимплантатных поражений. Пациенты, которые отказались от контрольных визитов, почти в 15 раз чаще повторно страдают от периимплантита, чем те, которые четко следовали протоколу мониторинга (30% против 2,4%). Эффективность мониторинга за состоянием имплантатов снижается вследствие действия таких факторов как наличие пародонтита в анамнезе, тяжелая форма исходного поражения и курение.
Заключение
Для того чтобы обеспечить своевременную диагностику имплантат-ассоциированных поражений, и эффективность проводимых всех терапевтических манипуляций с ними связанных, любой врач-стоматолог должен быть в полной мере ознакомлен с фундаментальными принципами дизайна имплантата и абатмента, а также особенностями их функционирования и взаимодействия с окружающими тканями. Протоколы продолжительного мониторинга за состоянием имплантатов предусматривают проведение профессиональной очистки зубного налета с поверхности интраоссальной опоры, поддержку высокого гигиенического уровня ротовой полости в целом, а также тщательную оценку состояния окружающих мягких и твердых тканей, от которых в принципе и зависят все параметры успешности и выживания инфраоссальных титановых конструкций.
Авторы:
Penny Hatzimanolakis, Dipl. DH, BDSc, MSc
Ioannis Tsourounakis, DDS, MSc, Cert. Perio
Anastasia Kelekis-Cholakis, DMD, Dipl. Perio






























































































































































0 комментариев