Болезни пародонта – это обобщающий термин, используемый для описания инфекционного воспалительного процесса, который может поражать один структурный элемент или комплекс составных элементов пародонта. Структуры, поддерживающие зуб, представлены альвеолярной костью, периодонтальной связкой и цементом корня. Заболевания пародонта в основном спровоцированы действием зубного налета или микробной биопленкой, представляющей собой гетерогенную структуру из патогенных микроорганизмов. Более 500 видов микроорганизмов считаются потенциальными этиологическими агентами, провоцирующими поражение тканей пародонта. Кроме них, вирусы и грибки тоже играют не последнюю роль в патогенетическом процессе. При возникновении и прогрессировании заболевания патогенные микроорганизмы колонизируют область десен, окружающую зуб, а вследствие их воздействия на ткани начинает формироваться пародонтальный карман. В глубоких пародонтальных карманах можно найти до 109 разновидностей бактерий, но несмотря на потенциал многих патогенов, которые ассоциируются с заболеваниями пародонта, лишь небольшое их количество связано с активной фазой заболевания.
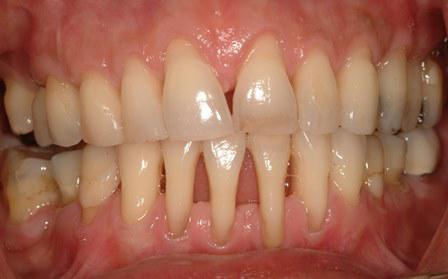
Антибиотики
Системная антибиотикотерапия должна рассматриваться как один из приемлемых вариантов лечения пациентов с пародонтитом. Данный подход актуален для пациентов, резистентных к обычной терапии заболевания, или у которых наблюдаются следующие проблемы со здоровьем: наличие абсцесса, компромиссное или ослабленное состояние иммунитета, неконтролируемый сахарный диабет, присутствие признаков и симптомов системных поражений, лихорадки и лимфаденопатии. Выбор наиболее подходящего системного антибиотика должен основываться на результатах культивирования микроорганизмов и тестирования их чувствительности к определенному препарату. Таким образом, удается узнать, во-первых, какие микроорганизмы присутствуют в области поражения, и, во-вторых, подобрать наиболее эффективный и действующий агент. Но следует помнить, что системная антибиотикотерапия не должна быть единственным методом лечения, а лишь представлять собой сегмент комплексного подхода обследования, диагностики и разработки адекватной системной терапии. Антибиотикотерапия, как и какой-либо другой метод лечения, имеет свои преимущества и недостатки. Поскольку прием данных препаратов является довольно таки известным методом лечения, пациенты, как правило, понимают основные ключевые моменты данного лечения, и без проблем соглашаются на предложенный алгоритм курса медикаментов. Но вместе с тем, пациенты часто могут путать официальные основные наименования лекарств, забывать дозу, время или даже сам факт их приема, нарушая тем самым эффект их действия. Системные антибиотики могут вызывать побочные эффекты и нарушения функционирования желудочно-кишечной системы в форме диареи или абдоминальных спазмов. Другие возможные негативные влияния препаратов связаны с аллергическими реакциями и возникновением резистентности бактерий к антибиотикам при их длительном и неконтролируемом приеме. Бактериальная резистентность является серьезной проблемой в медицине, поскольку она формирует ряд других научно-клинических дилемм относительно терапевтического соотношения риска лечения против потенциальной пользы от приема антибиотиков.
Системные антибиотики достигают тканей пародонта путем транссудации из сыворотки крови, после чего проходят через соединительный эпителий и выстилку десневого кармана, чтобы попасть в область десневой борозды. Эффективная концентрация антибиотика при достижении им десневой борозды во время курсового приема отличается от таковой в любой другой системе тканей или органе с признаками инфицирования, что связано со специфической структурой пародонта. Существует ряд уже хорошо апробированных схем приема антибиотиков для лечения заболеваний пародонта, которые, как правило, используются в сочетании с механическим удалением над- и поддесневых отложений и бактериального налета. Данный подход в комплексе с эффективной домашней гигиеной полости рта направлен на снижение бактериальной нагрузки в области тканей десны выше и ниже маргинальной границы. Некоторые врачи обычно назначают схемы антибиотикотерапии для лечения и управления заболеваниями пародонта на основе амоксициллина (375 мг) и метронидазола (500 мг) при приеме препаратов 3 раза в день в течение 7 дней в сочетании с проведением скейлинга ротовой полости и полной очисткой области корней в первые 48 часов. Такой подход помогает достичь уменьшения глубины карманов и снизить уровень кровотечения, что было обнаружено при сравнении результатов лечения в исследуемой и контрольной группах. Альтернативная схема лечения предусматривает прием азитромицина (500 мг) в течение 3 дней до проведения процедуры полного удаления зубного камня и очистки поверхности корней, чтобы уменьшить количество бактерий красного комплекса и снизить показатели гингивального индекса. При отсутствии возможностей проведения посева культуры бактерий и определения их чувствительности к антибиотикам, можно пользоваться эмпирическим принципом назначения препаратов для лечения пародонтита. Обоснованные варианты лечения включают в себя комбинацию амоксициллина и метронидазола (250 мг - 500 мг каждого) с приемом препаратов 3 раза в день в течение 8 дней, или комбинацию метронидазола и ципрофлоксацина (500 мг) в течение 8 дней по 2 раза в сутки.
Местная антибиотикотерапия является альтернативным адъюватным вариантом лечения, который также может применятся в ходе лечения поражений пародонта. Суть процедуры состоит в доставке антибиотика непосредственно в пародонтальный карман – то есть прямо в место колонизации патогенных бактерий, при этом концентрация антибиотика в области поражения по сравнению с системным приемом заметно увеличивается. Другим преимуществом является отсутствие потенциальных нарушений расстройств желудочно-кишечного тракта и аллергических реакций. Первым антибиотиком, используемым для местного лечения, был Actisite (пародонтальный тетрациклин). Он состоял из нерезорбируемых, пропитанных тетрациклином, волокон, которые помещались непосредственно в пародонтальный карман и оставались там в течение 10 дней – вплоть до следующего визита к стоматологу. Со временем проходило усовершенствование препаратов и методов их доставки в область пародонтального поражения. Таким образом, был разработан Atridox (Denmat), который является первым резорбируемым антибиотиком местного действия, состоящим из гелевой формы доксициклина. Данный препарат вводится в карман с помощью шприца, и при контакте со слюной – затвердевает, приобретая восковую консистенцию. Таким образом, антибиотик может выделятся из затвердевшей фазы на протяжении 21 дня. Arestin (Orapharma) также является представителем местных рассасывающихся препаратов антибактериального действия, который состоит из гранул миноциклина в форме порошка. Поставляется он в виде ампул, заряженных в шприц. Порошок вводится непосредственно в пародонтальный карман, высокий уровень его терапевтического действия продолжается в течении 14 дней, а сам препарат остается в кармане на протяжении 28 суток. Исследования доказали, что использование антибиотиков местного действия вместе с процедурой полного удаления зубного камня и очисткой поверхности корней позволяет добиться клинически эффективных результатов: наблюдается уменьшение глубины карманов и частичное восстановление нарушенного биологического прикрепления.
Противомикробные ополаскиватели полости рта
Противомикробные полоскания являются хорошо известными и приемлемыми процедурами, эффективно дополняющими комплексное лечение воспаления тканей десен. Примерами аргументированного их использования являются ситуации, когда пациент не в состоянии обеспечить оптимальный уход за полостью рта с помощью обычных гигиенических средств в домашних условиях, например, в послеоперационный период. Чтобы правильно выбрать ротовой ополаскиватель, который бы эффективно справлялся с воспалением десен и в то же время с профилактикой зубного налета, нужно узнать имеет ли он Сертификат одобрения Американской стоматологической ассоциацией. Если да, то данный продукт прошел через ряд клинических, биологических и лабораторных испытаний, которые доказали его противовоспалительную и антибактериальную эффективность. Однако, следует понимать, что данная оценка является рекомендательной, но никак не директивной в отношении препарата. Единственными ополаскивателями, доступными на рынке с соответствующей оценкой Ассоциации, являются представители с фенольными составляющими, по типу Listerine и других аналогичных версий. Золотым стандартом среди антимикробных ополаскивателей также считается хлоргексидин глюконат (0,12%), который в США отпускается лишь по рецепту и известен под коммерческими названиями Peridex и PerioGuard (Colgate-Palmolive). Хлоргексидин является наиболее эффективным антимикробным ополаскивателем, снижающим число бактерий и обеспечивающим эффективное лечение гингивита. Препарат более эффективен в отношении грамположительных бактерий и дрожжей, и менее эффективен в борьбе с грам-отрицательными патогенами. Его обычно назначают в послеоперационный период для снижения бактериальной нагрузки в период заживления. Хлоргексидин имеет высокую субстантивность, что обеспечивает его пролонгированное действие. Некоторые побочные эффекты, связанные с использованием хлоргексидина, включают потенциальное окрашивание зубов и спинки языка; изменение вкусовых восприятий; риск возможного образования наддесневого камня, формирование признаков мукозита и десквамации эпителия. Другими противомикробными ополаскивателями, доступными для широких масс, но менее часто рекомендованными специалистами, являются производные четвертичного аммония, такие как Cepacol (Reckitt Benckiser). Продукты на основе сангвинарина, по типу Viadent, больше широко не доступны на рынке. Продукты на основе оксигенатов, как пероксид водорода, рекомендуется чаще использовать в форме пасты. Они владеют противовоспалительными свойствами, благодаря которым уменьшаются признаки кровотечения. Последнее является важным критическим показателем для оценки воспаления пародонта. Однако данные представители имеют лишь небольшое влияние на уровень бактериальной контаминации, а в последнее время все чаще высказывается мнение об их возможном канцерогенном потенциале. Триклозан является еще одним антимикробным агентом, поставляющимся в форме зубных паст и ополаскивателей. Тем не менее, согласно данных исследований, он тоже демонстрирует минимальное влияние на микробную флору полости рта, а безопасность его использования до сих пор находится под вопросом.
Противовоспалительные агенты
Мы должны помнить, что заболевания пародонта имеют инфекционную природу, а воспалительные явления являются иммунным ответом организма на микробную контаминацию. В воспаленных тканях процесс размножения патогенных бактерий происходит быстрее, что приводит к прогрессированию патологических и разрушительных эффектов воспалительного процесса, посредством активации клеток иммунной системы организма (макрофагов и их предшественников, моноцитов, лимфоцитов, и полиморфноядерных лейкоцитов, таких как нейтрофилы). Компоненты микробной структуры, по типу липополисахарида, который находится в стенках клеток грамотрицательных анаэробных микроорганизмов, активируют макрофаги для продуцирования и секретирования провоспалительных цитокинов, таких как интерлейкин-1 (IL-1) и фактор некроза опухолей-альфа (TNF-alpha). Интерлейкин-1 стимулирует резорбцию кости, а также способствует высвобождению PGE2 клетками фибробластов, которые являются основными и наиболее распространенными типами клеток соединительной ткани. Фибробласты синтезируют коллаген – основной структурный белок соединительной ткани, который является также основным компонентом волокон десны и кости. Данные клетки и клетки воспалительной реакции (нейтрофилы и макрофаги) синтезируют матриксные металлопротеиназы (ММР), которые представляют собой ферменты или белки, участвующие в ряде биологических реакций. Например, ММР-1 и ММР-8 являются ферментами, которые принимают участие в деградации коллагена, что значительно ослабляет структуру пародонта. Активация иммунной системы по своей сути является защитной реакцией организма – ответом на бактериальную инвазию, однако в ходе механизма реализации иммунного ответа происходит разрушение тканей самого организма-хозяина. Данный феномен связан с высвобождением цитокинов, провоспалительных медиаторов и ММР, поскольку данные агенты действуют не только локально на ткани пародонта, но попадая в кровоток могут вызвать и нежелательные системные эффекты.
ММР являются группой протеолитических ферментов, обнаруженных в тканях пародонта, которые в своем составе имеют коллагеназу и желатиназу. Функция данных ферментов состоит в ремоделировании внеклеточного матрикса. Поскольку исследователями было обнаружено, что доксициклин имеет антиколлагенлитические свойства, они предложили использовать его в качестве модуляторного агента для лечения пародонтита. Субантимикробные дозы доксициклина (20 мг дважды в день) являются эффективными для ингибирования активности коллагеназы, и в то же время никак не влияют на фактор антимикробной резистентности при его использовании в сочетании с полным удалением зубного камня и очисткой поверхности корней. Такой подход обеспечивает максимальный эффект для восстановления биологического прикрепления тканей и снижения глубины пародонтальных карманов.
Пероральные лекарственные средства
Нестероидные противовоспалительные препараты (НПВП) также были изучены в качестве ингибиторов реакции организма хозяина при лечении заболеваний пародонта. Механизм их действия состоит в предотвращении продукции простагландинов. Простагландин Е2 (PGE2) напрямую ассоциирован с процессами воспаления и резорбции костной ткани, что подтверждено его верификацией в пораженных пародонтальных участках. В ходе изучения различных НПВП (флурбипрофен, ибупрофен, кеторолак, напроксен, аспирин), которые вводились системно или локально, было обнаружено, что при их сочетании с процедурой полного удаления зубного камня и очисткой поверхности корней, удавалось сохранить имеющуюся высоту альвеолярного гребня, предупреждая его резорбцию. Бисфосфонаты представляют собой класс препаратов, ингибирующих резорбцию альвеолярной кости, которые также были использованы в качестве хост-модулирующих агентов при лечении заболеваний пародонта. Исследования показали, что бисфосфонаты при использовании в сочетании с полной очисткой полости рта, обеспечивают снижение глубины пародонтальных карманов и уровня кровотечения во время зондирования, а также улучшают восстановление биологического прикрепления и обеспечивают сохранение высоты альвеолярного гребня. Однако, несмотря на потенциальные преимущества бисфосфонатов, исследования показали, что длительное применение и высокие дозы препаратов инициируют остеонекроз челюстей. Очевидно, что для аргументированных выводов необходимо проведение дальнейших более детализированных исследований, которые помогут определить соотношение потенциальной пользы препаратов и относительного риска осложнений в процессе лечения пародонтита.
Хост-модулирующая терапия
Локальное применение хост-модулирующих агентов, таких как эмалевые матриксные протеины, костные морфогенетические белки и тромбоцитарные факторы роста, может быть довольно эффективным в ходе комплексного лечения пародонтита. Эмалевые матриксные протеины доступны в форме препарата Emdogain (Straumann) и успешно используются в ходе восстановления пародонтальных дефектов. Данные белки играют роль модуляторов заживления, стимулируя регенерацию всех пародонтальных компонентов поддерживающего аппарата зуба. Костные морфогенетические белки способствуют модуляции и дифференциации мезенхимальных клеток в клетки-предшественники костной ткани. Они действуют в качестве каркаса, на который может наращиваться новая костная ткань, и часто используются при направленной костной регенерации во время аугментации альвеолярного гребня. Наконец, тромбоцитарные факторы роста усиливают хемотаксис нейтрофилов и моноцитов, стимулируют пролиферацию фибробластов, а соответственно и синтез внеклеточного матрикса, а также повышают уровень дифференциации мезенхимальных клеток-предшественников, фибробластов и эндотелиальных клеток. Именно тромбоцитарные факторы роста наиболее часто используется при хирургических вмешательствах на тканях пародонта с целью ускорения их регенерации.
Выводы
Новые знания относительно хост-бактериальных взаимодействий и иммунных реакций организма, которые провоцируют поражение тканей пародонта, станут полезными для разработки более новых и эффективных концепций лечения пародонтита с использованием системных и местных антибиотиков, антимикробных ополаскивателей и принципов хост-модулирующей терапии. Результаты дальнейших исследований могут пролить свет на вспомогательную адьювантную терапию, которая может быть использована для коррекции алгоритмов лечения с целью достижения наиболее успешного эффекта комплексной терапии поражений поддерживающего аппарата зуба.
Автор: Alison Glascoe, DDS, MS
Болезни пародонта – это обобщающий термин, используемый для описания инфекционного воспалительного процесса, который может поражать один структурный элемент или комплекс составных элементов пародонта. Структуры, поддерживающие зуб, представлены альвеолярной костью, периодонтальной связкой и цементом корня. Заболевания пародонта в основном спровоцированы действием зубного налета или микробной биопленкой, представляющей собой гетерогенную структуру из патогенных микроорганизмов. Более 500 видов микроорганизмов считаются потенциальными этиологическими агентами, провоцирующими поражение тканей пародонта. Кроме них, вирусы и грибки тоже играют не последнюю роль в патогенетическом процессе. При возникновении и прогрессировании заболевания патогенные микроорганизмы колонизируют область десен, окружающую зуб, а вследствие их воздействия на ткани начинает формироваться пародонтальный карман. В глубоких пародонтальных карманах можно найти до 109 разновидностей бактерий, но несмотря на потенциал многих патогенов, которые ассоциируются с заболеваниями пародонта, лишь небольшое их количество связано с активной фазой заболевания.

Антибиотики
Системная антибиотикотерапия должна рассматриваться как один из приемлемых вариантов лечения пациентов с пародонтитом. Данный подход актуален для пациентов, резистентных к обычной терапии заболевания, или у которых наблюдаются следующие проблемы со здоровьем: наличие абсцесса, компромиссное или ослабленное состояние иммунитета, неконтролируемый сахарный диабет, присутствие признаков и симптомов системных поражений, лихорадки и лимфаденопатии. Выбор наиболее подходящего системного антибиотика должен основываться на результатах культивирования микроорганизмов и тестирования их чувствительности к определенному препарату. Таким образом, удается узнать, во-первых, какие микроорганизмы присутствуют в области поражения, и, во-вторых, подобрать наиболее эффективный и действующий агент. Но следует помнить, что системная антибиотикотерапия не должна быть единственным методом лечения, а лишь представлять собой сегмент комплексного подхода обследования, диагностики и разработки адекватной системной терапии. Антибиотикотерапия, как и какой-либо другой метод лечения, имеет свои преимущества и недостатки. Поскольку прием данных препаратов является довольно таки известным методом лечения, пациенты, как правило, понимают основные ключевые моменты данного лечения, и без проблем соглашаются на предложенный алгоритм курса медикаментов. Но вместе с тем, пациенты часто могут путать официальные основные наименования лекарств, забывать дозу, время или даже сам факт их приема, нарушая тем самым эффект их действия. Системные антибиотики могут вызывать побочные эффекты и нарушения функционирования желудочно-кишечной системы в форме диареи или абдоминальных спазмов. Другие возможные негативные влияния препаратов связаны с аллергическими реакциями и возникновением резистентности бактерий к антибиотикам при их длительном и неконтролируемом приеме. Бактериальная резистентность является серьезной проблемой в медицине, поскольку она формирует ряд других научно-клинических дилемм относительно терапевтического соотношения риска лечения против потенциальной пользы от приема антибиотиков.
Системные антибиотики достигают тканей пародонта путем транссудации из сыворотки крови, после чего проходят через соединительный эпителий и выстилку десневого кармана, чтобы попасть в область десневой борозды. Эффективная концентрация антибиотика при достижении им десневой борозды во время курсового приема отличается от таковой в любой другой системе тканей или органе с признаками инфицирования, что связано со специфической структурой пародонта. Существует ряд уже хорошо апробированных схем приема антибиотиков для лечения заболеваний пародонта, которые, как правило, используются в сочетании с механическим удалением над- и поддесневых отложений и бактериального налета. Данный подход в комплексе с эффективной домашней гигиеной полости рта направлен на снижение бактериальной нагрузки в области тканей десны выше и ниже маргинальной границы. Некоторые врачи обычно назначают схемы антибиотикотерапии для лечения и управления заболеваниями пародонта на основе амоксициллина (375 мг) и метронидазола (500 мг) при приеме препаратов 3 раза в день в течение 7 дней в сочетании с проведением скейлинга ротовой полости и полной очисткой области корней в первые 48 часов. Такой подход помогает достичь уменьшения глубины карманов и снизить уровень кровотечения, что было обнаружено при сравнении результатов лечения в исследуемой и контрольной группах. Альтернативная схема лечения предусматривает прием азитромицина (500 мг) в течение 3 дней до проведения процедуры полного удаления зубного камня и очистки поверхности корней, чтобы уменьшить количество бактерий красного комплекса и снизить показатели гингивального индекса. При отсутствии возможностей проведения посева культуры бактерий и определения их чувствительности к антибиотикам, можно пользоваться эмпирическим принципом назначения препаратов для лечения пародонтита. Обоснованные варианты лечения включают в себя комбинацию амоксициллина и метронидазола (250 мг - 500 мг каждого) с приемом препаратов 3 раза в день в течение 8 дней, или комбинацию метронидазола и ципрофлоксацина (500 мг) в течение 8 дней по 2 раза в сутки.
Местная антибиотикотерапия является альтернативным адъюватным вариантом лечения, который также может применятся в ходе лечения поражений пародонта. Суть процедуры состоит в доставке антибиотика непосредственно в пародонтальный карман – то есть прямо в место колонизации патогенных бактерий, при этом концентрация антибиотика в области поражения по сравнению с системным приемом заметно увеличивается. Другим преимуществом является отсутствие потенциальных нарушений расстройств желудочно-кишечного тракта и аллергических реакций. Первым антибиотиком, используемым для местного лечения, был Actisite (пародонтальный тетрациклин). Он состоял из нерезорбируемых, пропитанных тетрациклином, волокон, которые помещались непосредственно в пародонтальный карман и оставались там в течение 10 дней – вплоть до следующего визита к стоматологу. Со временем проходило усовершенствование препаратов и методов их доставки в область пародонтального поражения. Таким образом, был разработан Atridox (Denmat), который является первым резорбируемым антибиотиком местного действия, состоящим из гелевой формы доксициклина. Данный препарат вводится в карман с помощью шприца, и при контакте со слюной – затвердевает, приобретая восковую консистенцию. Таким образом, антибиотик может выделятся из затвердевшей фазы на протяжении 21 дня. Arestin (Orapharma) также является представителем местных рассасывающихся препаратов антибактериального действия, который состоит из гранул миноциклина в форме порошка. Поставляется он в виде ампул, заряженных в шприц. Порошок вводится непосредственно в пародонтальный карман, высокий уровень его терапевтического действия продолжается в течении 14 дней, а сам препарат остается в кармане на протяжении 28 суток. Исследования доказали, что использование антибиотиков местного действия вместе с процедурой полного удаления зубного камня и очисткой поверхности корней позволяет добиться клинически эффективных результатов: наблюдается уменьшение глубины карманов и частичное восстановление нарушенного биологического прикрепления.
Противомикробные ополаскиватели полости рта
Противомикробные полоскания являются хорошо известными и приемлемыми процедурами, эффективно дополняющими комплексное лечение воспаления тканей десен. Примерами аргументированного их использования являются ситуации, когда пациент не в состоянии обеспечить оптимальный уход за полостью рта с помощью обычных гигиенических средств в домашних условиях, например, в послеоперационный период. Чтобы правильно выбрать ротовой ополаскиватель, который бы эффективно справлялся с воспалением десен и в то же время с профилактикой зубного налета, нужно узнать имеет ли он Сертификат одобрения Американской стоматологической ассоциацией. Если да, то данный продукт прошел через ряд клинических, биологических и лабораторных испытаний, которые доказали его противовоспалительную и антибактериальную эффективность. Однако, следует понимать, что данная оценка является рекомендательной, но никак не директивной в отношении препарата. Единственными ополаскивателями, доступными на рынке с соответствующей оценкой Ассоциации, являются представители с фенольными составляющими, по типу Listerine и других аналогичных версий. Золотым стандартом среди антимикробных ополаскивателей также считается хлоргексидин глюконат (0,12%), который в США отпускается лишь по рецепту и известен под коммерческими названиями Peridex и PerioGuard (Colgate-Palmolive). Хлоргексидин является наиболее эффективным антимикробным ополаскивателем, снижающим число бактерий и обеспечивающим эффективное лечение гингивита. Препарат более эффективен в отношении грамположительных бактерий и дрожжей, и менее эффективен в борьбе с грам-отрицательными патогенами. Его обычно назначают в послеоперационный период для снижения бактериальной нагрузки в период заживления. Хлоргексидин имеет высокую субстантивность, что обеспечивает его пролонгированное действие. Некоторые побочные эффекты, связанные с использованием хлоргексидина, включают потенциальное окрашивание зубов и спинки языка; изменение вкусовых восприятий; риск возможного образования наддесневого камня, формирование признаков мукозита и десквамации эпителия. Другими противомикробными ополаскивателями, доступными для широких масс, но менее часто рекомендованными специалистами, являются производные четвертичного аммония, такие как Cepacol (Reckitt Benckiser). Продукты на основе сангвинарина, по типу Viadent, больше широко не доступны на рынке. Продукты на основе оксигенатов, как пероксид водорода, рекомендуется чаще использовать в форме пасты. Они владеют противовоспалительными свойствами, благодаря которым уменьшаются признаки кровотечения. Последнее является важным критическим показателем для оценки воспаления пародонта. Однако данные представители имеют лишь небольшое влияние на уровень бактериальной контаминации, а в последнее время все чаще высказывается мнение об их возможном канцерогенном потенциале. Триклозан является еще одним антимикробным агентом, поставляющимся в форме зубных паст и ополаскивателей. Тем не менее, согласно данных исследований, он тоже демонстрирует минимальное влияние на микробную флору полости рта, а безопасность его использования до сих пор находится под вопросом.
Противовоспалительные агенты
Мы должны помнить, что заболевания пародонта имеют инфекционную природу, а воспалительные явления являются иммунным ответом организма на микробную контаминацию. В воспаленных тканях процесс размножения патогенных бактерий происходит быстрее, что приводит к прогрессированию патологических и разрушительных эффектов воспалительного процесса, посредством активации клеток иммунной системы организма (макрофагов и их предшественников, моноцитов, лимфоцитов, и полиморфноядерных лейкоцитов, таких как нейтрофилы). Компоненты микробной структуры, по типу липополисахарида, который находится в стенках клеток грамотрицательных анаэробных микроорганизмов, активируют макрофаги для продуцирования и секретирования провоспалительных цитокинов, таких как интерлейкин-1 (IL-1) и фактор некроза опухолей-альфа (TNF-alpha). Интерлейкин-1 стимулирует резорбцию кости, а также способствует высвобождению PGE2 клетками фибробластов, которые являются основными и наиболее распространенными типами клеток соединительной ткани. Фибробласты синтезируют коллаген – основной структурный белок соединительной ткани, который является также основным компонентом волокон десны и кости. Данные клетки и клетки воспалительной реакции (нейтрофилы и макрофаги) синтезируют матриксные металлопротеиназы (ММР), которые представляют собой ферменты или белки, участвующие в ряде биологических реакций. Например, ММР-1 и ММР-8 являются ферментами, которые принимают участие в деградации коллагена, что значительно ослабляет структуру пародонта. Активация иммунной системы по своей сути является защитной реакцией организма – ответом на бактериальную инвазию, однако в ходе механизма реализации иммунного ответа происходит разрушение тканей самого организма-хозяина. Данный феномен связан с высвобождением цитокинов, провоспалительных медиаторов и ММР, поскольку данные агенты действуют не только локально на ткани пародонта, но попадая в кровоток могут вызвать и нежелательные системные эффекты.
ММР являются группой протеолитических ферментов, обнаруженных в тканях пародонта, которые в своем составе имеют коллагеназу и желатиназу. Функция данных ферментов состоит в ремоделировании внеклеточного матрикса. Поскольку исследователями было обнаружено, что доксициклин имеет антиколлагенлитические свойства, они предложили использовать его в качестве модуляторного агента для лечения пародонтита. Субантимикробные дозы доксициклина (20 мг дважды в день) являются эффективными для ингибирования активности коллагеназы, и в то же время никак не влияют на фактор антимикробной резистентности при его использовании в сочетании с полным удалением зубного камня и очисткой поверхности корней. Такой подход обеспечивает максимальный эффект для восстановления биологического прикрепления тканей и снижения глубины пародонтальных карманов.
Пероральные лекарственные средства
Нестероидные противовоспалительные препараты (НПВП) также были изучены в качестве ингибиторов реакции организма хозяина при лечении заболеваний пародонта. Механизм их действия состоит в предотвращении продукции простагландинов. Простагландин Е2 (PGE2) напрямую ассоциирован с процессами воспаления и резорбции костной ткани, что подтверждено его верификацией в пораженных пародонтальных участках. В ходе изучения различных НПВП (флурбипрофен, ибупрофен, кеторолак, напроксен, аспирин), которые вводились системно или локально, было обнаружено, что при их сочетании с процедурой полного удаления зубного камня и очисткой поверхности корней, удавалось сохранить имеющуюся высоту альвеолярного гребня, предупреждая его резорбцию. Бисфосфонаты представляют собой класс препаратов, ингибирующих резорбцию альвеолярной кости, которые также были использованы в качестве хост-модулирующих агентов при лечении заболеваний пародонта. Исследования показали, что бисфосфонаты при использовании в сочетании с полной очисткой полости рта, обеспечивают снижение глубины пародонтальных карманов и уровня кровотечения во время зондирования, а также улучшают восстановление биологического прикрепления и обеспечивают сохранение высоты альвеолярного гребня. Однако, несмотря на потенциальные преимущества бисфосфонатов, исследования показали, что длительное применение и высокие дозы препаратов инициируют остеонекроз челюстей. Очевидно, что для аргументированных выводов необходимо проведение дальнейших более детализированных исследований, которые помогут определить соотношение потенциальной пользы препаратов и относительного риска осложнений в процессе лечения пародонтита.
Хост-модулирующая терапия
Локальное применение хост-модулирующих агентов, таких как эмалевые матриксные протеины, костные морфогенетические белки и тромбоцитарные факторы роста, может быть довольно эффективным в ходе комплексного лечения пародонтита. Эмалевые матриксные протеины доступны в форме препарата Emdogain (Straumann) и успешно используются в ходе восстановления пародонтальных дефектов. Данные белки играют роль модуляторов заживления, стимулируя регенерацию всех пародонтальных компонентов поддерживающего аппарата зуба. Костные морфогенетические белки способствуют модуляции и дифференциации мезенхимальных клеток в клетки-предшественники костной ткани. Они действуют в качестве каркаса, на который может наращиваться новая костная ткань, и часто используются при направленной костной регенерации во время аугментации альвеолярного гребня. Наконец, тромбоцитарные факторы роста усиливают хемотаксис нейтрофилов и моноцитов, стимулируют пролиферацию фибробластов, а соответственно и синтез внеклеточного матрикса, а также повышают уровень дифференциации мезенхимальных клеток-предшественников, фибробластов и эндотелиальных клеток. Именно тромбоцитарные факторы роста наиболее часто используется при хирургических вмешательствах на тканях пародонта с целью ускорения их регенерации.
Выводы
Новые знания относительно хост-бактериальных взаимодействий и иммунных реакций организма, которые провоцируют поражение тканей пародонта, станут полезными для разработки более новых и эффективных концепций лечения пародонтита с использованием системных и местных антибиотиков, антимикробных ополаскивателей и принципов хост-модулирующей терапии. Результаты дальнейших исследований могут пролить свет на вспомогательную адьювантную терапию, которая может быть использована для коррекции алгоритмов лечения с целью достижения наиболее успешного эффекта комплексной терапии поражений поддерживающего аппарата зуба.
Автор: Alison Glascoe, DDS, MS































































































































































0 комментариев